2. 浙江天元生物药业公司;
3. 浙江大学医学院附属第一医院
在人用H5N1禽流感疫苗研究的第一部分中证实, 从国外引进的R1194和R1203两株毒种为减毒株, 符合目前国际用于制造人用H5N1亚型禽流感疫苗的标准。并按照我国对研制疫苗的要求, 设计3种生产疫苗的纯化工艺, 制造疫苗, 对制成的疫苗进行全面检定, 选取其中较好株毒种生产的疫苗, 用于人用禽流感疫苗临床前动物免疫的研究。
1 材料与方法 1.1 材料(1)毒种: H5N1禽流感毒种R1194株和R1203株(英国国家生物制品检定所和美国疾病控制中心); (2)生产疫苗胚蛋:来源于封闭式房舍内饲养的健康鸡群; (3)滤器和滤膜(美国Millipore公司); (4)β -丙内脂(美国Sigma公司), 用于灭活病毒; (5) Triton N101(美国Aldrich公司), 用于裂解病毒; (6)脱氧胆酸钠(上海伯奥生物科技公司进口分装), 用于裂解病毒; (7)凝胶柱(瑞典安发玛西亚生物技术公司), 型号: PB G 300/950;(8)凝胶Sephrose -4FF (瑞典安发玛西亚生物技术公司); (9)超声波细胞粉碎机(宁波新芝公司); (10)区带离心机(日本日立公司); (11)电泳仪(美国伯乐公司)。
1.2 方法(1)总蛋白测定:采用Lowry法; (2)卵清蛋白测定:采用对流免疫电泳法; (3)细菌内毒素测定:鲎试验定量法; (4)病毒液浓缩:先用15 000 r/min连续离心澄清, 再超滤膜浓缩40~50倍; (5)病毒灭活验证试验:标本接种胚蛋, 培养后, 再盲传一代, 血凝应阴性; (6)蔗糖梯度密度离心:待纯化的病毒液30 000 r/min梯度离心3 h, 收集病毒峰, 用磷酸盐缓冲液(PBS)进行超滤清洗, 去除蔗糖; (7)电子显微镜观察:由浙江医学科学院电镜室协助拍摄。
2 结果 2.1 生产工艺的设计普通流感疫苗已有60年的生产历史, 工艺比较成熟, 根据生产流感疫苗的经验, 设计了3种禽流感疫苗的生产工艺:(1)全病毒疫苗:毒种接种鸡胚经培养、收液、超滤浓缩、β-丙内脂灭活、层析、区带离心等纯化程序, 病毒未经裂解处理。(2)裂解-1疫苗:程序相似, 中间增加用裂解剂Triton N101和脱氧胆酸钠, 裂解病毒的处理。(3)裂解-2疫苗:仅用裂解剂Triton N101裂解病毒的处理。
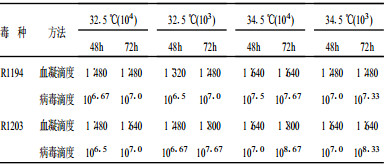
2.2 主要技术参数(表 1)| 表 1 不同滴度和不同温度及时间接种培养效果比较 |
比较2毒种的不同滴度接种蛋胚, 经不同温度和不同时间培养结果表明, 接种剂量为104 EID50/ml (0.2ml), 培养温度34.5 ℃, 培养时间3d较好。
2.3 病毒灭活采用1:4 000β-丙内脂, 4 ℃, 作用24 h, 经病毒灭活验证试验证明, 对R1194或R1203毒株均可灭活。
2.4 病毒裂解经采用Triton N101和脱氧胆酸钠, 在超声波的作用下, 对R1194或R1203毒株均可裂解。
2.5 电镜观察(图 1)
|
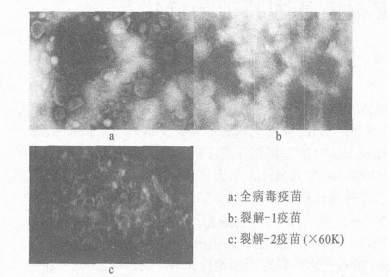
图 1 3种工艺生产的禽流感疫苗的电镜结果 |
从图 1可见, 3种工艺生产的疫苗形态完全不同, 全病毒疫苗的病毒形态比较完整, 裂解-1疫苗对病毒的裂解比较细, 已看不见完整的病毒及碎片, 裂解-2疫苗均为不完整的病毒及病毒碎片。
2.6 疫苗的SDS-PA GE的电泳结果(图 2)
|
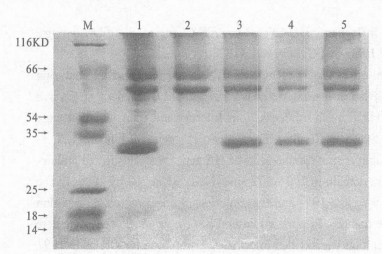
M :mark; 1 :全病毒苗; 2 :裂解-1疫苗; 3~5 :裂解-2疫苗 图 2 3种生产工艺疫苗的SDS -PAGE电泳结果 |
从图 2可见, 全病毒疫苗和裂解-2疫苗的形态相似, 而裂解-1疫苗, 在32 KD左右的条带已缺失。
2.7 疫苗的核酸扩增(图 3)
|
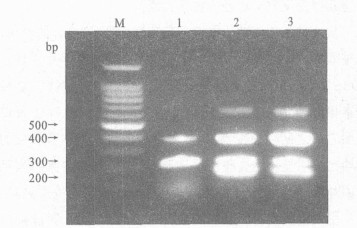
M :mark; 1 :裂解-1疫苗; 2 :裂解-2疫苗; 3 :全病毒苗 图 3 H5 N1禽流感病毒引物扩增3种疫苗的电泳结果 |
用国家流感中心提供确诊H5N1禽流感病毒的引物, 扩增3种疫苗的电泳。
从图 3可见, 3种疫苗在378 bp处均有明显的条带, 证明裂解后的疫苗还能扩增到禽流感病毒的基因片段。
2.8 浓缩和纯化通过对血凝素含量的测定, 了解浓缩和纯化每一环节对抗原活性成分的影响, 确立最佳方法和条件, 达到优化的目的, 并制订相应的参数, 建立稳定的浓缩纯化工艺。
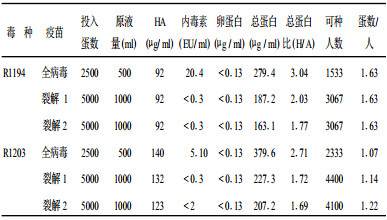
2.9 原液的检定及产出比(表 2)| 表 2 疫苗原液检定结果及产出比 |
对浓缩和纯化后的疫苗原液进行全面检定, 并计算出投入鸡蛋数与疫苗产出比。从表 2可知, 制备的3种疫苗原液, 主要指标均明显优于国家标准, 投入的鸡胚量与疫苗产出比(按每人15 mg 2针30μg计算) R1194毒种制的疫苗每人份需1.63个蛋, 而R1203毒种制的疫苗仅需1.07~122个蛋。因而下一步的研究, 用R1203株制成的疫苗进行动物接种, 以比较3种不同工艺生产疫苗的免疫效果。
3 讨论自1937年流感病毒在鸡胚中获得培养成功, 使鸡胚可用于大量生产流感疫苗, 直至今日, 世界各国提供的流感疫苗, 绝大部分是用鸡胚生产的灭活疫苗。本研究获得的R1194和R1203禽流感毒株, 也为鸡胚适应株, 故采用鸡胚培养病毒。由于无致病菌(SPF)鸡蛋缺少且价格昂贵, 无法满足疫苗生产的巨量需求, 因而目前我国规定, 制备疫苗毒种必须用SPF鸡蛋, 而生产疫苗可用封闭饲养健康鸡群的蛋, 由于本研究的工艺设计中有甲醛防腐(也能杀死99.999 %病毒, 即从108/ml降至103/ml左右)和β -丙内脂再灭活, 用封闭饲养健康鸡群的蛋, 安全有保障。
为了防止儿童接种流感全病毒疫苗引起的发热反应, 将病毒进行裂解, 制成裂解疫苗取得很好的效果, 可以在儿童中接种。一般认为, 裂解疫苗的免疫效果不如全病毒疫苗。但由于裂解病毒的方法各不相同, 目前国际上研制的禽流感疫苗, 有全病毒的〔1, 2〕也有裂解的〔3, 4〕。故本研究设计了有全病毒和不同裂解程度的3种生产工艺, 以比较它们的免疫效果。希望获得免疫效果较好的禽流感疫苗。
从3种工艺疫苗的电镜形态观察, 达到原设计的要求, 即完整病毒; 病毒裂解很细和不完整病毒或病毒碎片3种。从SDS -PA GE电泳的条带来分析, 全病毒疫苗与裂解-2疫苗基本相似, 裂解-3疫苗未见32 KD左右的条带(M1蛋白), 表明它们之间存在差别, 但3种疫苗的血凝素和核蛋白的条带均比较明显。经核酸扩增试验, 均能扩增到禽流感病毒的基因片段, 提示H5N1的核酸扩增可用于疫苗的鉴别试验。
引发流感疫苗副反应的成分主要有内毒素、卵清蛋白和其他杂蛋白。因而疫苗质量的好坏主要取决以下4项指标, 即内毒素、卵清蛋白、总氮、总氮与血凝素之比。国家标准〔5〕规定内毒素不高于200 EU/ml (本实验为 < 2 EU/ml), 卵清蛋白不高于2μg/ml (本实验为 < 0.125μg/ml), 总氮不高于600μg/ml (本实验为 < 100μg/ml, 因配成30μg/ml疫苗, 原液还要稀释4倍), 总氮与血凝素之比不高于6(本实验为2左右)。比较可见, 本研究设计生产的禽流感疫苗可达到进口普通流感疫苗质量。
(参加本项工作的还有:谢荣辉, 赵芝雅, 金美珍, 丁云龙, 李枫, 黎丹, 袁勇等)
| [1] | John J, Treanor MD, James D, et al. Safety and immunogenicity of an inactivated subvirion influenza A (H5N1) vaccine[J]. N Engl J Med, 2006, 354(13) : 1343–1351. DOI:10.1056/NEJMoa055778 |
| [2] | Lin J, Zhang J, Dong X, et al. Safety and immunogenicity of an inac2 tivated adjuvanted whole-virion influenza A (H5N1) vaccine: a phase Ⅰ randomised controlled trial[J]. Lancet, 2006, 368(9540) : 991–997. DOI:10.1016/S0140-6736(06)69294-5 |
| [3] | Bresson JL, Perronne C, Launay O, et al. Safety and immunogenici2 ty of an inactivated split-virion ifluenza A/Vietnam/1194/2004(H5N1) vaccine: phase Ⅰ randomised trial[J]. Lancet, 2006, 367(9523) : 1657–1664. DOI:10.1016/S0140-6736(06)68656-X |
| [4] | 英国葛兰素史克.禽流感疫苗临床试验成功[EB/OL].http://info.pharmacy.hc360.com/2006/04/07101739167.shtml. |
| [5] | 国家药典委员会.流行性感冒疫苗制造及检定规程[S].中国药典三部.北京:化学工业出版社, 2005:19-23. |
 2007, Vol. 23
2007, Vol. 23