2. 贵阳医学院病理生理学教研室
地方性砷中毒是严重危害人类身体健康的一种疾病。贵州省是我国地方性砷中毒重病区之一, 目前仍然存在众多的砷中毒病区和砷中毒病患者。迄今为止, 砷毒性作用的机制尚未完全阐明。在有关砷中毒的酶学研究中发现, 砷中毒时并不是体内所有酶的活性都受到抑制, 有些酶的活性反而升高, 相关酶活性变化的研究结果也并不一致〔1-4〕。砷进入机体后, 主要经血液进入肝脏, 并主要分布于肝脏线粒体〔2〕。因此, 研究砷中毒时与肝细胞及肝细胞线粒体受损相关的酶显得甚为重要。此外, 在慢性砷中毒时, 血液中多种生物学指标的改变可能早于临床表现, 因此, 探讨血液生化指标, 对于临床慢性砷中毒的早期诊断也具有积极的意义。本文以大鼠为研究对象, 探讨慢性砷中毒时大鼠肝脏线粒体相关酶及肝脏损伤相关血清酶活性的改变, 以便为进一步揭示砷对机体的毒性作用机制并为选择有意义的慢性砷中毒早期诊断酶学指标提供有价值的资料。
1 材料与方法 1.1 试剂及物品脲酶(英国默克公司); 瓜氨酸, 氨基甲酰二锂磷酸盐(美国Fluka公司); 其余均为国产分析纯试剂。
1.2 实验动物分组及处理1~2月龄Wistar大鼠48只, 雌雄各半。随机分为2组:实验组28只, 饮用含75 mg/ L三氧化二砷(As2O3)的蒸馏水, 常规大鼠饲料喂养。对照组20只, 饮用蒸馏水, 以同样的饲料喂养。2组均于染毒前、染毒3个月及6个月时测定大鼠毛砷含量。染毒3个月时, 随机抽取实验组及对照组大鼠各10只, 股动脉放血处死; 6个月时, 处死全部动物, 取肝脏及血液进行检查。
1.3 毛砷含量测定采用二乙氨基二硫代甲酸银法〔5〕。
1.4 大鼠线粒体制备取大鼠肝2 g。采用差速离心法制备〔6〕。按考马斯亮蓝法〔7〕, 以牛血清白蛋白为标准, 定量线粒体蛋白。
1.5 线粒体酶活性测定细胞色素C氧化酶(COX)活性测定及线粒体ATP酶活性测定参照文献〔8〕进行, COX比活力=K ×min/ mg线粒体蛋白。ATP酶活性单位以μmol/ (mg pro·min)表示。
1.6 大鼠血清酶活性测定鸟氨酸氨基甲酰转移酶(OCT)测定, 血清谷氨酸脱氢酶(GDH)活性测定及血清精氨酸酶(Arginase)活性测定参照文献〔9〕进行。OCT活力国际单位为:每升血清每分钟在37 ℃时, 由OCT的作用产生1μmol瓜氨酸定为一个国际单位。谷氨酸脱氢酶活性(毫国际单位GDH=△吸光度×2 ×0.5 ×1 000。精氨酸酶单位=鸟氨酸的微克数×0.505。血清腺苷脱氨酸(ADA)活力测定参照文献〔10〕进行, 其活力单位指1 ml血清使腺苷产生1μg氨氮为一个活力单位。血清谷胱甘肽硫转酶(GST)活力测定参照文献〔11〕进行, 一个GST酶单位活性, 相当于在37 ℃条件下1 min催化1μmol CDNB与GSH结合的能力。
1.7 统计分析应用SPSS 11.0软件进行分析。毛砷含量呈偏态分布, 结果以G±SG表示。结果均采用t检验进行差异的统计学检验。
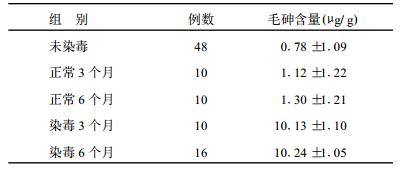
2 结果 2.1 大鼠毛砷含量测定(表 1)| 表 1 各组大鼠毛砷含量测定结果比较(G+SG) |
在饲养过程中, 由于大鼠死亡, 在染毒6个月时, 大鼠数量为16只。砷染毒3个月后大鼠毛砷含量即显著升高, 与实验前及正常对照组相比, 差异有统计学意义(P < 0.01), 同时染毒3个月与6个月时毛砷含量相当, 说明大鼠砷染毒后, 已处于稳定的砷中毒状态。
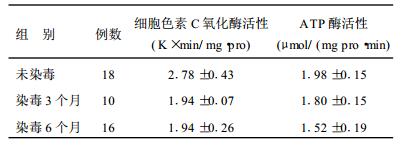
2.2 大鼠肝脏线粒体酶活性变化(表 2)| 表 2 各组大鼠肝脏线粒体酶活性变化(x±s) |
与正常对照组比较, 大鼠染毒3个月后其肝脏线粒体COX活力显著降低(P < 0.01), 而染毒3个月及6个月组酶活性则差异无统计学意义(P > 0.05)。表明砷中毒时, 大鼠肝脏线粒体细胞色素C氧化酶活性已较早并持续地受到抑制。同时染毒3个月及6个月组大鼠肝脏线粒体ATP酶活力均显著降低(P < 0.01), 而染毒6个月组则较染毒3个月组的酶活性进一步下降(P < 0.01)。说明砷不仅抑制肝脏线粒体ATP酶的活性, 而且其抑制作用可随着中毒时间的延长而加重。
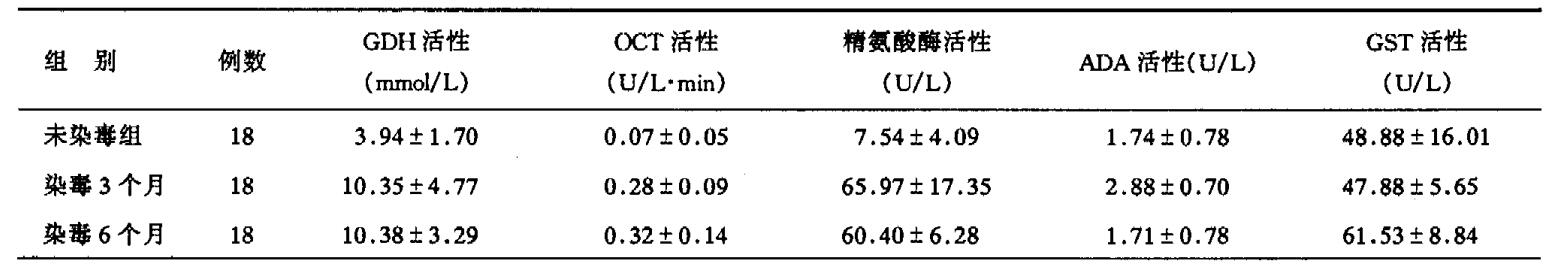
2.3 大鼠血清酶活性变化(表 3)| 表 3 各组大鼠血清酶活性变化(x±s) |
砷中毒3个月及6个月大鼠血清谷氨酸脱氢酶及鸟氨酸氨基甲酰转移酶活力均有显著升高(P < 0.01), 由于这2种酶位于线粒体基质内, 砷中毒时其活性升高, 表明砷中毒不仅可能使大鼠肝细胞受损, 而且也使线粒体受到损伤, 致使酶释放到血液中; 染毒3个月及6个月组大鼠血清精氨酸酶活力显著升高, 与正常对照组比较差异有统计学意义(P < 0.01), 而染毒6个月组酶活性较染毒3个月组有降低倾向, 但差异无统计学意义(P > 0.05)。与正常对照组比较, 染毒3个月时血清腺苷脱氨酶活性显著升高(P < 0.01), 而染毒6个月时其酶活力恢复到正常对照组水平(P > 0.05)。表明砷中毒时, 血清腺苷脱氨酶活性变化可能只在急性和亚急性期的血清酶学指标才有一定意义。染毒3个月时血清谷胱甘肽硫转酶活性仍无明显改变(P > 0.1), 染毒6个月时才出现该酶活力的显著升高(P < 0.01), 可能该酶对早期诊断意义不大。
3 讨论本研究采用饮水加三氧化二砷复制慢性砷中毒大鼠模型, 辅以毛砷含量检测观察大鼠的砷中毒状况。钟复光等〔5〕对燃煤型砷中毒病区砷毒接触者发砷含量的研究结果表明, 发砷含量对慢性砷中毒诊断有重要意义。本文测定结果表明, 染毒组大鼠毛砷含量与对照组及染毒前大鼠比较明显升高, 说明实验动物已经处于严重的砷中毒状态。
本文研究结果表明, 砷可显著抑制肝脏线粒体细胞色素C氧化酶及ATP酶的活性。这2种酶的活性受到抑制, 必然引起氧化磷酸化过程受阻, 能量产生障碍, 导致线粒体功能的损害, 严重影响机体细胞功能〔12〕。这可能是慢性砷中毒时, 砷毒性作用的重要机制之一。本实验研究还发现, 砷中毒大鼠血清GDH及OCT活性均显著升高。由于这2种酶均定位于肝脏线粒体基质, 是肝脏线粒体的特异性酶类。其血清酶活性增高, 反映了砷中毒不仅可使肝细胞, 而且可使其线粒体受到严重损伤, 以至酶自线粒体和细胞内渗出到血液中增加其活性。精氨酸酶、ADA及GST都是存在于肝细胞的特异酶类。血清精氨酸酶及GST活性升高, 可能是肝细胞受损后肝细胞内酶释出到血清中引起。ADA属于一种巯基酶, 每个分子至少含2个活性巯基〔13〕。大鼠染毒3个月时血清ADA活性升高, 其原因可能是因为肝细胞膜受到砷中毒的影响而通透性增高, 使ADA泄漏到血液中所致。而随着砷中毒时间的延长, 体内积蓄的砷可能与肝细胞内和血液中的部分ADA的活性巯基结合, 而抑制其活性, 这可能是其血清中酶活性回降的原因之一。
本实验共检测了5个血清酶在大鼠持续砷中毒时的酶活性变化, 从寻找慢性砷中毒早期诊断酶学指标的角度看, 血清谷氨酸脱氢酶、精氨酸酶在大鼠砷中毒期间一直升高, 其活性变化持续的时间较久, 可能更适宜作为一种临床诊断的参考指标。
| [1] | 李艳红, 王晓君. 砷的毒性[J]. 国外医学:医学地理分册, 1996, 17(1) : 7–10. |
| [2] | 朱建华, 王翔朴. 砷在砷中毒性肝脏内的亚细胞水平分布[J]. 中国现代医学杂志, 1997, 7(2) : 40–436. |
| [3] | 刘泰, 王国荃, 肖碧玉, 等. 氟砷联合作用对肝肾损伤的研究[J]. 地方病学通报, 1997, 16(4) : 292–295. |
| [4] | 荀黎红, 吴丛雅. 地方性砷中毒与人体多系统损害的研究进展[J]. 国外医学医学地理分册, 1998, 19(4) : 145–148, 156. |
| [5] | 钟复光, 单可人, 何燕, 等. 燃煤型慢性砷中毒接触者发砷含量的比较研究[J]. 中国公共卫生, 1999, 15(3) : 261–263. |
| [6] | 汪谦. 现代医学实验方法[M]. 北京: 人民卫生出版社, 1997: 335-342. |
| [7] | 张龙翔. 生化实验方法和技术[M].2版. 北京: 高等教育出版社, 1997: 138. |
| [8] | 方学军, 迟彦邦, 李靖. 胆道梗阻再通后肝线粒体呼吸酶活力的变化[J]. 第一军医大学学报, 1997, 17(3) : 201–202. |
| [9] | 王继贵. 临床生化检验[M]. 长沙: 湖南科学技术出版社, 1981: 239-277. |
| [10] | 刘信荣, 孙文献, 郑德成, 等. 腺苷脱氨酶活力测定方法探讨[J]. 中华医学检验杂志, 1998, 11(5) : 266–268. |
| [11] | 张振中, 刘利娥, 刘洁, 等. 谷胱甘肽-S转移酶的测定及其临床应用[J]. 河南医科大学学报, 1995, 30(4) : 419–421. |
| [12] | 沈同, 王镜岩. 生物化学[M].2版. 北京: 高等教育出版社, 1998: 56-73. |
| [13] | Abd Ellah MR, Nishimori K, Goryo M, et al. Serum adenosine deaminase activity in bovine liver diseases[J]. J Vet Med Sci, 2004, 66(11) : 1421–1422. DOI:10.1292/jvms.66.1421 |
 2007, Vol. 23
2007, Vol. 23