兴奋性氨基酸(EAA)引起的兴奋毒性是糖尿病视网膜病变〔1〕、青光眼、视网膜变性等疾病的视网膜神经元损伤及死亡的主要机制之一。体内研究表明, 视网膜的兴奋毒性主要由N-甲基-D-天冬氨酸(N-methyl-D-aspartate, NMDA)受体介导〔2〕。牛磺酸(Taurine)是视网膜含量最丰富的游离氨基酸, 近年来发现, 牛磺酸可以保护培养的小脑颗粒细胞对抗兴奋毒性损伤〔3〕。本实验通过在大鼠玻璃体内注射NMDA制备视网膜兴奋毒性损伤模型, 观察牛磺酸对NMDA诱导的视网膜组织结构及超微结构损伤的保护作用。
1 材料与方法 1.1 实验动物及视网膜NMDA兴奋毒性损伤动物模型的建立成年雄性Sprague-Dawley大鼠20只, 体质量200~250 g (第三军医大学野战外科研究所实验动物中心), 实验动物质量合格证号:SCXK (军)2002008。大鼠腹腔注射速眠新注射液0.1 ml/100 g (长春军需大学兽医研究所)麻醉, 5%托品酰胺散瞳, 1%利多卡因进行角膜表面麻醉, 用微量注射器从颞上方巩膜距角膜缘外3 mm处进针, 见针尖到达玻璃体中后部后, 缓慢注入5 μl 4 mmo l/L的NMDA〔2〕。洁霉素滴眼预防感染。眼瞎大鼠弃去。
1.2 实验分组20只大鼠按随机数字表法分为4组:(1)正常对照组; (2) NMDA组; (3) NMDA+牛磺酸干预组; (4)磷酸盐缓冲液(PBS)对照组; 每组5只大鼠。正常对照组不进行任何处理; NMDA组为上述模型组; 牛磺酸干预组于眼内注射NMDA前1 h及其后每天腹腔注射牛磺酸(25 mg/kg〔4〕), 共注射3 d; PBS对照组于玻璃体内注射5 μl 0.1 mol/L PBS。玻璃体注射后第4 d观察指标变化。NMDA、牛磺酸(美国Sigma公司), 用无菌0.1 mol/L PBS稀释。
1.3 视网膜组织病理学观察及视网膜厚度测量腹腔注射2 ml/100 g 0.3%戊巴比妥钠处死大鼠, 迅速摘取右眼, 去除前节、晶状体及玻璃体, 将眼杯用10%福尔马林固定, 常规石蜡包埋, 经视乳头切片(5 Lm), 苏木精-伊红(HE)染色, 观察视网膜组织结构并照相, LEICA Q WIN图像分析软件于距视乳头中心1.5 mm处双侧测量视网膜全层及视见网膜内层(包括内核层、内网状层、节细胞层和神经纤维层)厚度, 每只眼球取6张切片, 每组5只大鼠结果求平均值。
1.4 视网膜超微结构观察按前法处死大鼠, 摘取左眼, 将眼杯迅速置于4℃预冷的3%戊二醛固定, 常规1%锇酸固定, 系列丙酮脱水, 环氧树脂浸透包埋, 经光镜定位后行超薄切片, 于TENCAI10 PHILIPS透射电镜下观察视网膜各层细胞的超微结构。
1.5 统计分析采用SPSS统计软件处理, 组间比较用单因素方差分析。
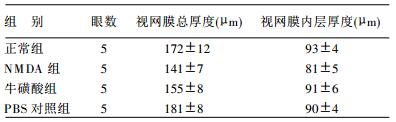
2 结果 2.1 视网膜组织病理结构改变及视网膜厚度测量(表 1)| 表 1 各组视网膜总厚度及视网膜内层厚度测量结果( x±s) |
HE染色及视网膜厚度测量结果显示, 玻璃体内注射NMDA后第4 d, 与未注射眼视网膜相比, 视网膜总厚度变薄(P < 0.001), 尤以视网膜内层厚度变薄明显(P < 0.001), 节细胞数有减少, 而视网膜内、外段及外核层改变不明显。牛磺酸干预使视网膜总厚度(P=0.017)及内网状层厚度(P=0.001)较模型组增厚, 节细胞的丢失减少。表明牛磺酸干预可有效保护NMDA兴奋毒性对视网膜组织病理结构改变。
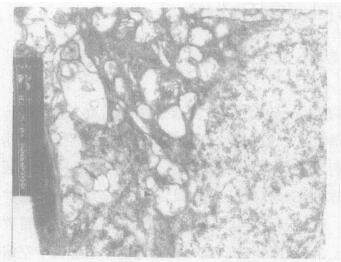
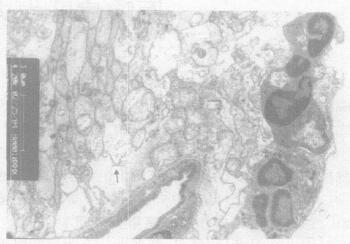
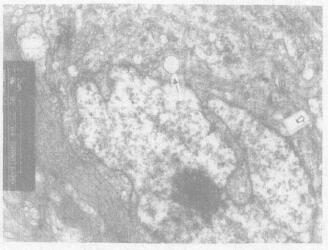
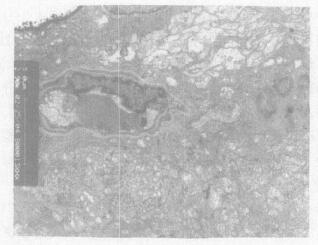
2.2 玻璃体注射NMDA及牛磺酸干预对视网膜超微结构的影响透射电镜观察发现, 玻璃体注射NMDA后第4 d, 视网膜内核层细胞及节细胞超微结构发生改变。镜下可见, NMDA组:视细胞胞体无明显病变, 色素上皮细胞及盘膜正常, 内核层神经元线粒体中、重度肿胀, 嵴消失甚至空泡样变, 内质网严重扩张(图 1), 节细胞部分轴突明显肿胀, 视神经纤维明显肿胀甚至解体(图 2), 整个内核层神经元及节细胞表现为变性改变。牛磺酸干预组:内核层细胞有轻度线粒体肿胀及内质网扩张, 节细胞超微结构正常, 仅部分节细胞见轻度线粒体肿胀和内质网扩张(图 3), 视神经纤维层轴突肿胀不明显(图 4), 牛磺酸组超微结构改变较NMDA组明显减轻。
|
图 1 NMDA组的内核层细胞(×7000) |
|
图 2 NMDA组视神经纤维层(×4200) |
|
图 3 牛磺酸干预组的节细胞(×7000) |
|
图 4 牛磺酸干预组视神经纤维层(×2900) |
3 讨论
目前认为EAA引起的兴奋毒性是糖尿病视网膜病变、青光眼、视网膜缺氧等的视网膜神经元死亡的主要机制之一。研究表明〔2〕, 视网膜内层神经元的兴奋毒性损伤主要由对NMDA受体的过度刺激引起, NMDA受体的各亚单位在视网膜主要见于内网状层的突触后神经元, 即无足细胞和节细胞〔5〕。Lam等〔6〕用玻璃体内注射NMDA的大鼠模型发现, 注射18 h后内核层和节细胞层出现大量细胞凋亡。腹腔注射NMDA受体拮抗剂-MK-801能有效预防NMDA对视网膜细胞的损伤〔7〕。
将NMDA受体拮抗剂用于预防视网膜兴奋毒性是一种值得探索的方向, 但由于NMDA受体同时介导许多正常的生理功能, 其拮抗剂用于人体可能对中枢神经系统产生多种副作用, 使其临床应用受到限制〔8〕。牛磺酸是一种正常存在于人体多种组织的游离氨基酸, 目前公认牛磺酸是一个调节及降低神经细胞内Ca2+水平的强有力因子〔9〕。有研究提示, 牛磺酸可通过防止或降低谷氨酸诱导的胞内Ca2+水平的升高而保护培养的大脑神经元〔3〕。我们研究发现, 牛横酸可保护大鼠糖尿病视网膜病变的组织结构及超微结构损伤〔10〕。本实验发现, 牛磺酸在体内可拮抗NMDA兴奋毒性对视网膜组织结构及超微结构的损伤。由于目前未发现较高剂量的牛磺酸摄入对人体有负面影响, 提示将其用于预防EAA兴奋毒性引起的视网膜神经元损伤可能有较好的临床应用前景。
| [1] | Kowluru RA, Engerman RL, Case GL, et al. Retinal glutamate in diabetes and effect of antioxidants[J]. Neurochem Int, 2001, 38(5) : 385–390. DOI:10.1016/S0197-0186(00)00112-1 |
| [2] | Moncaster JA, Walsh DT, Gentleman SM, et al. Ergothioneine treatment protects neurons against N-methyl-D-aspartate excito-toxicity in vivo rat retinal model[J]. Neurosci Let, 2002, 328(1) : 55–59. DOI:10.1016/S0304-3940(02)00427-5 |
| [3] | Chen WQ, Jin H, Nuyen M. Role of taurine in regulation of intracellular calcium level and neuroprotective functon in cultured neurons[J]. J Neurosci Res, 2001, 66(4) : 612–619. DOI:10.1002/(ISSN)1097-4547 |
| [4] | 许红霞, 糜漫天, 徐朝霞. 牛磺酸对大鼠视网膜谷氨酸兴奋毒性的防护作用研究[J]. 营养学报, 2005, 7(2) : 114–118. |
| [5] | Fletcher EL, Hack I, Branstatter JH, et al. Synaptic localization of NMDA receptor subunit in the rat retina[J]. J Comp Neurol, 2000, 420 : 98–112. DOI:10.1002/(ISSN)1096-9861 |
| [6] | Lam TT, Ablen AS, Kwong JMK, et al. N-methyl-D-aspart ate (NMDA)-induced apoptosis in rat retina[J]. Invest Ophthalmol Vis Sci, 1999, 40 : 2391–397. |
| [7] | Sun Q, Ooi VE, Chan SO. N-emthyl-D-aspart ate-induced excitotoxicity in adult rat retina is antagonized by single systemic injection of MK-801[J]. Exp Brain Res, 2001, 138(1) : 37–45. DOI:10.1007/s002210100688 |
| [8] | Ikonomidou C, Turski L. Why did NMDA receptor antagonists fail clinical trials for stroke and traumat ic brain injury?[J]. Lancet Neurol, 20021, 1(6) : 383–386. |
| [9] | Foos TM, Wu JY. The role of taurine in the central nervous system and the modulation of intracellular calcium homeost asis[J]. Neurochem Res, 2002, 7(1-2) : 21–26. |
| [10] | 徐朝霞, 糜漫天, 许红霞. 牛磺酸对早期糖尿病大鼠视网膜超微结构的影响[J]. 中国公共卫生, 2004, 20(5) : 554–556. |
 2007, Vol. 23
2007, Vol. 23