氚是天然存在的氢的放射性同位素,广泛存在于环境中。氚又是重要的人工放射性核素,核爆炸和核动力推生产都能够产生大量的氚,可能对环境产生较大的影响。故许多国家相继开展了对环境氚含量及所致剂量的研究工作,本文就此作一简要介绍。
一 方法学概述环境样品的氚含量一般是很低的,仅为10-2~10-1Bq·-1,因此,对于氚的检测要求有特殊低水平测量装置,并需预先对样品进行浓缩和纯化处理,近20年来广泛使用的液体闪烁测量技术,使氚核素溶解或悬浮于闪烁液中,与闪烁液密切接触,几何条件接近4π,探测灵敏度较高,操作简单。
在样品制备方面,水样常用电解浓缩方法,使水中氚富集[1],用蒸馏方法除去水中杂质,也可将水样直接加到闪烁液内进行测量[2]。
近10多年来使用较多的地缘真空蒸馏方法,可避免高温常压蒸馏过程中产生的同位素效应,减少误差[1],食物样品常用低温蒸馏方法收集食物游离水氚,然后用燃烧—氧化方法把食物组织的有机结合氚转变成氚化水,用液体闪烁法测量[1]。空中空气样品常用硅胶吸附法或冷凝法采集[1], 用蒸馏法提取硅胶极富吸附的氚化水, 或把硅胶直接投入闪烁液中进行测量。
二 环境氚含量及分布环境氚来源于天然存在的氚和人工产生的氚。天然氚由宇宙射线与大气中的氮、氧相互作用产生,人工氚主要由核爆炸核工业产生,氚在环境中大部分转化为氚化水,参与天然水的循环,最终权基于海洋里。在各种环境中氚的储存量百分比为;海洋65%,陆地表面和生物圈27%,大气7.2%[4]。
环境氚的天气天然浓度很小,空气氚浓度约为1.2×10-4Bq·m-3,水氚浓度10-2~10Bq·-1。在各种水中水,雨水氚浓度最高, 地下水最低, 氚浓度大小顺序为:雨水>河水>湖水>海水>地下水。五十年代以后大规模核武器试验产生的氚对全球环境造成了严重污染,使全球水体中的氚浓度提高了1~2个数量级,个别地区甚至增加了5个数量级以上[5],大气水蒸汽和雨水氚浓度从1954年期逐年增高。1963年达到高峰,然后逐年下降,到70年代后期注意趋于平稳。河水、海水、地下水也呈现相应的变化趋势。
核工业排放氚对全球影响全球环境的影响目前还不太大,但可是局部地区的环境氚浓度增加。目前环境中的氚主要是天然氚和核爆炸残留氚,氚浓度在10-1~101Bq·-1之间。
1. 空气氚和雨水氚
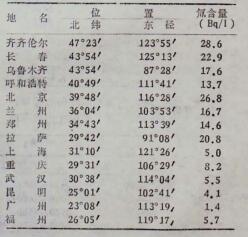
大气水蒸汽和雨水氚的氚在不同纬度带浓度不同,北半球氚浓度高,南半球氚浓度低,而在北半球,氚浓度随纬度降低呈下降趋势。在同一纬度上,沿海地区氚浓度比内路地区低[6]。我国降水氚浓度北部地区较高,南部地区较低,最低值在广东、福建沿海一带(表 1)。
|
|
表 1 1978年5月我国部分地区降水氚含量 |
大气水蒸汽和雨水氚浓度随季节有明显的变化,冬春季氚浓度较高,夏秋季较低,但在赤道附近季节变化不明显。这可能由不同季节的空气水分和降雨量差异所致,冬春季降水少,空气湿度小,被雨水冲洗稀释和沉降的氚较少,空气中氚浓度较高;反之,氚浓度较低。
2. 地表水氚浓度
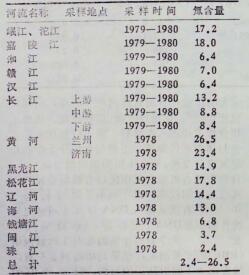
地表水氚浓度受降水和局部人工污染的影响,有明显的季节变化,丰水器氚浓度低,枯水期氚浓度较高。我国长江、黄河水氚浓度均自西向东递减,而且都高于当地的降水。长江上游支流氚浓度比下游干流氚浓度较高,而黄河水氚浓度自西向东下降较少。松花江、辽河、海河、钱塘江、闽江、珠江等河水氚浓度则按地理位置由北向南逐渐减少(表 2)。
|
|
表 2 1978-1980年我国河水氚浓度(Bq/l) |
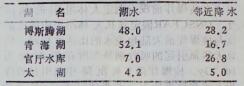
湖水氚浓度一湖泊类型不同而有差异,内流湖高,外流湖低。这是由主要由于内流湖的补给和排泄周期较长,湖水氚浓度受早些时候核爆炸引起的环境高氚水平影响,而外流湖的补给和排泄周期较短,湖水氚浓度反映近几年邻近地区降水氚平均水平(表 3)。
|
|
表 3 1978年5月我国几个湖水氚含量(Bq/l) |
地下水氚浓度取决于第一面水联系的程度,联系密切者氚浓度较高,一般深井水氚浓度比浅井水低,浅井水氚浓度比地面水低。饮用水氚浓度则依水源类型不同而有差异。表 4列出了我国部分地区和世界一些国家的饮用水氚浓度,各地饮用水氚浓度均比地面水氚浓度低。
|
|
表 4 饮用水流含量(Bq/l) |
3.食物氚含量
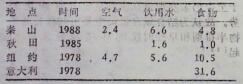
食物氚可分为游离水氚和可机结合氚。从美国、日本等几个国家的研究结果看,游离水氚浓度与当地引用水氚浓度相接近,结合氚含量比游离水氚高(表 5)。二者比值取决于游离水氚与结合氚的转换速率、环境水氚浓度的涨落和食物中氚的浓集情况,由于至今认为发现氚在生态系统中有浓集趋势,故认为结合氚含量高主要由其较长的生物半排期和早些时候的环境高氚水平引起[12]。
|
|
表 5 食物氚含量 |
环境氚对人体所致剂量取决于产生和排放到环境的氚量、氮在环境里的物理扩散和生态行为,以及氚在人体内的代谢过程、人体组织内的游离水氛和结合氮活度等因素。由于在核爆炸前没有测定人体组织的氚活度,UNSCFAR假定氚在人体组织中的氚活度与核爆炸前大陆地表水的比活度相同,估算天然氚引起的剂量在所有组织均为10-8Gy。核爆炸落下灰沉降中氚引起的待积有效剂量当量为:北半球51μSv, 南半球14μSv,全球41μSv,集体待积有效剂量当星为2.4×10-5manSv。根据吸入途经(包括皮肤吸收)和食入途径氚进入人体的相对摄入量,剂量负担可分为7%来自吸入和皮肤吸收,93%来自食入[4]。
核工业排放氚所致的待积有效剂量当量因各种核设施不同的排放途径而相差很大。1980~1984年间各类反应堆排放到大气和水环境引起的区域人群集体待积有效剂量当量中,大气排放为0.15manSv(TBq)-1, 其中吸入1.5×10-3manSv·(TBq)-1, 食入途经所致剂量比吸入途径约髙6倍,平均归一化集体待积有效剂量当量为0.67manSv (GWa)-1。水排放假设以河水为饮用水源,引起的集体待积有效剂量当量为0.03manSv (GWa)-1。每单位排放量向水环境排放的氚比向大气排放的氚约低20倍(表 6) [7]。
|
|
表 6 1980-1984年各国反应堆氚平均排放量及局部和区域集体待积有效剂量当量 |
不同环境介质中氚所致待积有效剂量当量因各国居民的饮水、膳食习惯不同而有差异。组约居民所受氚待积有效剂量当量中,来自食物的占50%,饮用水占23%,食物是组约居民氚剂量的主要来源。日本秋田居民饮用水所致氚剂量比食物大。我国浙江秦山核电厂周围居民经饮用水和食物摄入是氚剂量的主要来源,空气氚所致剂量只占17%(表 7)。
|
|
表 7 居民氚待积有效剂量当量(×10-8Sv/y) |
氚是氢的放射性同位素,物理半衰期12,3年,生物半排期10~450天,氚衰变产生纯β粒子,平均能量5.7keV,最大能量18.6keV。尽管氚粒子的能量小,在组织内的射程短,但在微米体积的组织内可以把它的大部分能量传递给分子,在这些地方形成大的比能,在细胞核内产生电离,引起细胞死亡[8]。氚通过呼吸、皮肤吸收、饮用水和食物途径进入人体后,除了以氚化水形式参与体内水代谢外,还能与有机分子中的稳定氢进行交换,形成牢固的组织结合氚[9]。食物中的有机结合氚也能以有机结合氚的形式参与组织代谢,其生物半排期可长达一年[10]。有机氚掺入DNA分子中可通过转换作用引起DNA单键断裂,导致基因突变[11]。一些学者对于氚的相对生物效应值(RBE)的实验研究,结果均增高到3左右,故提出为了辐射防护的目的,目前使用的RBE为1似乎不够慎重,今后更恰当的“应用的”RBE可能提高到3[8, 13]。
氚又是重要的人工放射性核素,核反应堆运行、爆料后处理厂生产等核工业生产都能够产生和排放氚[14],同时氚在农业、医学、水文等方面有着广泛的用途,这些都可能引起氚对环境的污染和对人体造成危害。特别是作为未来能源的聚变反应堆的发展,领非将有更多的氚进入人类环境[15],到本世纪末核动力堆生产产生的氚量可能超过天然本底产生和核武器试验残留的氚量[9]。氚对环境和人类健康的影影值得重视,因而对环境氚含量的研究及所致剂量的估标逐渐成为国际性的项目[6, 16],并且已经取得了一些有意义的结果,这对于研究氚在环境中的分布、转移及人工产生氚对环境的影响,估算公众剂量可提供必要的依据。
我国核电站建设刚开始起步,核电站建成运行以后产生和排放的氚对环境和人群健康的影响研究在辐射防护领域中占有相当重要的位置,这对于保护人群健康、促进核能发展都具有重要的意义。
| [1] |
NCRP. Report No. 47. Tritium measurements techniqucs. Washington: NCRP. 1976.
|
| [2] |
Iwakura. T., et al.A Iow-background liquid scintillation counter for measuring low-level tritium. Behaviovr of tritium in the environment, Vienna: IAEA. 1979: 162-171.
|
| [3] |
姜金岭, 等.硅胶吸附法测定空气中氚.辐射防护监测技术汇编.北京: 中囯科学院原子能研究所. 1978 : 115.
|
| [4] |
UNSCEAR.Ionizing radiation: Sources and biological effects.Ncwrork: United Nations. 1982.
|
| [5] |
Libby, M.F, Tritium in the Physical and biological sciences. Vienna; IAEA. 1962: 5.
|
| [6] |
Suess H.E. Tritium Geophysics as an international reseach Project[J]. Science, 1969, 1405-1410. |
| [7] |
UNSCEAI. Annex B exporures from the nuclear Power Productiont 36th Session of UNSCEAR.Vienna: United Nations. 1988.
|
| [8] |
Dobson, R.L. Application of the dose limitation system for radion Protection Practical implication. IAEA-SR36/23. Vienna: IAEA. 1979 : 593.
|
| [9] |
NCRP. Report No.62. Tritium in the environment. Washington: NGRP. 1979.
|
| [10] |
Etnier E.L., et al. Matabolism of organically bound tritium in man[J]. Radia. Res, 1984, 100: 487-502. DOI:10.2307/3576412 |
| [11] |
Matsudaira H., et al. Induction of cell killing mutation and oncogenic transformation allowing exposure to trhtiated water in cultured mammalian cells[J]. Radia. Prot. Dosit, 1986, 16(1-2): 145-150. DOI:10.1093/oxfordjournals.rpd.a079733 |
| [12] |
Shunchi hisamatsu, et al. Fallout H-3 ingestion in Akita, Japan.Health Phrs. 1987; 53 (3) : 287-293.
|
| [13] |
周湘艳, 等. 氘相对生物效应的实验研究及遗传危害的估计[J]. 中华放射医学与防护杂志, 1988, 8(6): 369-274. |
| [14] |
Lurkx F., et al. Tritium relases from nuclear Power Plants and nuclear fuel reprocessing Plants Radia[J]. Prot. Dosi, 1986, 16(1-2): 31-36. DOI:10.1093/oxfordjournals.rpd.a079708 |
| [15] |
Feinegen L.E., et al. Radiation Problcui in fusion energy Production[J]. Radhat. Environ. Biophys, 1980, 18: 157-133. DOI:10.1007/BF01323596 |
| [16] |
Soldat, J.K., et al, Werid-wide Population doses Jrom tritium releases from nuclear facilitids. EUR9065. Luxembourg: CEC. 1984: 575-584.
|