2. 中山大学肿瘤防治中心放疗科, 广东 广州 510060;
3. 华南恶性肿瘤防治全国重点实验室, 广东 广州 510060
2. Department of Radiation Oncology, Sun Yat-sen University Cancer Center, Guangzhou 510060 China;
3. State Key Laboratory of Oncology in South China, Guangzhou 510060 China
据世界卫生组织国际癌症研究中心发布的Globocan 2020数据[1]显示,全球前列腺癌发病率居男性恶性肿瘤第2位,死亡率居第5位,是中老年男性泌尿系统最常见的一种恶性肿瘤。前列腺癌的治疗手段包括手术切除、内分泌治疗、放射治疗等。放射治疗作为前列腺癌根治性治疗手段之一,高剂量的调强放射治疗技术已成为根治性放疗的金标准[2-3]。在放疗实施过程中,治疗师可以通过CBCT清晰准确的观察到患者靶区及危及器官的变化。膀胱和直肠的解剖学位置紧挨前列腺,是前列腺癌放疗的重要危及器官,随着放射治疗处方剂量的增加,其毒副反应也会增加[4],会发生严重的放射性直肠损伤和放射性膀胱炎,如腹泻、里急后重、直肠出血、尿频、尿急、尿痛等,严重影响患者的生活质量。因此,膀胱和肠道准备成为前列腺癌放疗成功的关键,在临床上备受关注。但在患者每日的治疗实施过程中仍会出现膀胱充盈较少或较多、肠道胀气、肠道有粪便的情况,影响患者成功治疗的因素和不同膀胱和肠道准备的情况对放疗精准实施的影响暂无研究。本研究通过CBCT观察前列腺癌患者每日膀胱和肠道的准备情况,分析影响患者成功治疗的因素,记录分次间摆位误差,并记录患者出现的副反应情况,为临床前列腺癌放疗中膀胱和肠道准备提供参考。
1 材料与方法 1.1 临床资料研究对象为回顾性选取中山大学肿瘤防治中心放疗科2023年4月—2023年9月前列腺癌患者38例。年龄49~80岁,中位年龄67岁,身体质量指数(body mass index,BMI)为16.8~30.4,中位BMI为24.7。患者在瑞典医科达VersaHD直线加速器行容积调强放射治疗,放疗处方剂量为5600~8000 cGy,处方分次为25~35次,常规剂量分割。患者纳入标准:①组织病理学诊断或临床诊断标准确诊为前列腺癌,影像学证实未见明显远处转移;②治疗前无膀胱炎和尿道炎,可自主充盈膀胱;③无沟通障碍。患者排除标准:①合并其他部位恶性肿瘤;②治疗中后期需重新设计放疗计划;③因自身原因终止放疗;④仅使用真空袋进行体位固定。已获得临床伦理批号:SL-B2023-710-01。
1.2 模拟定位前膀胱和肠道准备在体位固定至少1周前先对患者进行宣教和饮食管理,告知患者放射治疗的利弊和主要步骤、治疗总次数、注意事项、一周一次的复诊频率等事项,增加患者的积极配合程度和对放疗过程的了解,尤其是膀胱和肠道的准备。因个体化差异,患者可通过练习膀胱排空后饮水,掌握饮水量和时间,了解膀胱充盈程度。且需排空肠道,整个治疗期间,患者应特别注意饮食,避免进食易产气的食物,多走动和按摩腹部,同时可用陈皮水、益生菌、二甲硅油、开塞露等辅助药物来促进肠道排气排便。
1.3 体位固定、CT模拟定位和放疗计划复位验证固定装置均采用个体化俯卧板 + 真空袋联合固定,患者双手上举俯卧于真空袋上。在PHILIPS大孔径螺旋CT模拟定位机(brillianceTM big bore CT)获取CT定位图像。要求膀胱充盈程度250~350 mL和精囊腺以下层面直肠最大直径 ≤ 3 cm,扫描范围从第3腰椎下缘至坐骨结节下3 cm。扫描完成后将CT定位图像发送至Monaco计划系统,由主治医生和物理师进行肿瘤靶区勾画和计划设计,待计划确认后,把包含完整靶区结构的放疗计划和计划CT图像导入Mosaiq放疗系统,进行复位验证,确定治疗中心点位置,并进行标记。
1.4 采集图像和获取数据首次治疗前将计划CT图像传至VersaHD直线加速器X线容积成像XVI系统中,勾画配准框,选择灰度配准。治疗前先行CBCT扫描,与计划CT图像进行配准。观察患者准备情况,使用XVI系统的距离测量工具,分别在CBCT图像和计划CT图像上,根据膀胱径线测量膀胱体积[5]和测量精囊腺以下层面的直肠最大直径,计算CBCT扫描与CT模拟定位的膀胱体积比R和直肠最大直径比r。根据研究[6-7]和临床工作经验划分为:R < 0.9或R > 1.1为膀胱充盈较少或较多,0.9 ≤ R ≤ 1.1为膀胱充盈适中;r ≤ 1为直肠准备良好,r > 1为直肠准备不充分。若靶区和直肠自动灰度配准结果不符合临床需求[8],则需治疗师手动调整摆位误差。将移床值传至加速器进行治疗,分别记录移床值和自动灰度配准的摆位误差值。配准结果由主治医生审核无误。若患者准备严重不足,则停止治疗,待准备充分后再行CBCT扫描。通过查询患者每周复诊的病历信息,记录患者膀胱和肠道的副反应情况。每位患者成功治疗频率为患者处方分次相对于CBCT扫描次数的比例。治疗师调整的误差值为满足临床需求的移床值与自动灰度配准摆位误差的差值。
1.5 统计学方法采用Excel和SPSS17.0统计学软件进行数据处理和分析。患者成功治疗频率与副反应情况作Spearman相关性分析,相关系数用r表示(r为正值,正相关;r为负值,负相关)。采用Shapiro-Wilk方法对数据进行正态性检验。若数据符合正态分布使用t检验,用均值
38例患者处方分次为25~35次,总处方分次为1062次,治疗前CBCT扫描次数为25~40次,扫描总次数为1155次,计算患者成功治疗频率为(92.14 ± 5.25)%,范围为75.76%~100%。38例患者有93次膀胱和肠道准备严重不足,不能满足临床需求,其中45次是膀胱充盈过少,占48.4%,R < 0.7;28次是肠道胀气,占30.1%,r = (1.37 ± 0.17);6次是肠道粪便,占6.5%;7次是肠道胀气和粪便,占7.5%;7次是膀胱和肠道准备均严重不足,占7.5%。
2.2 患者副反应情况统计患者放疗副反应的情况,结果显示18例患者直至放疗结束身体均无明显不适,20例患者在放疗(15.9 ± 6.2)次后出现排便次数和夜尿次数稍增多、尿频、尿急等反应。对患者副反应情况与成功治疗频率作相关性分析,结果显示二者成负相关(r = −0.393,P = 0.015)。
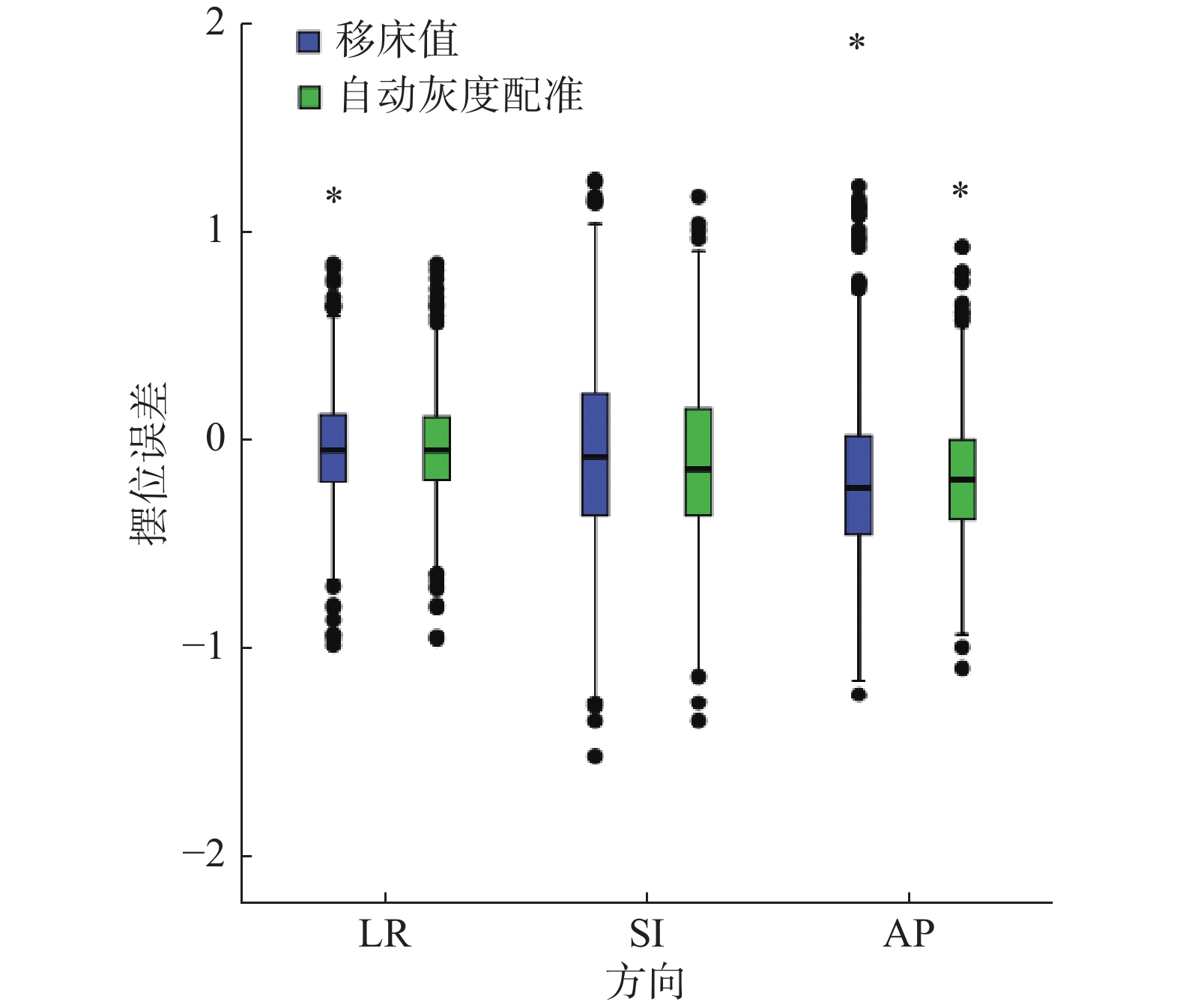
2.3 38例患者摆位误差值的比较 2.3.1 满足临床需求的移床值和自动灰度配准摆位误差的比较38例患者治疗前满足临床需求的移床值和自动灰度配准的摆位误差均不符合正态分布,二者进行非参数秩和检验,差异在LR、SI、AP方向均具有统计学意义(P < 0.05),见表1。数据分布见图1。
|
|
表 1 移床值和自动灰度配准摆位误差比较 Table 1 Comparison of the setup errors of bed shift and automatic grayscale registration |
|
图 1 移床值和自动灰度配准摆位误差的分布 Figure 1 Distribution of the setup errors of bed-shift and automatic grayscale registration |
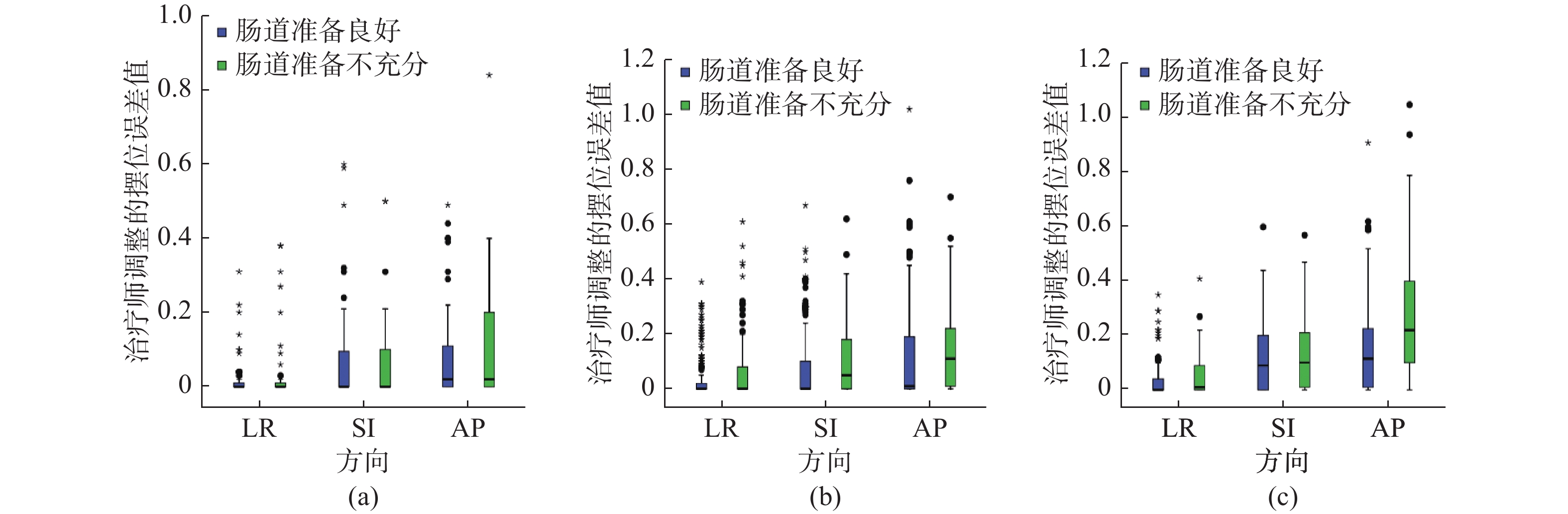
对不同膀胱和肠道准备情况下治疗师调整的误差值进行交互效应分析,结果显示膀胱的主效应在SI(F = 12.080,P < 0.001)、AP(F = 34.740,P < 0.001)方向上差异有统计学意义,直肠的主效应在LR(F = 9.296,P = 0.002)、SI(F = 5.308,P = 0.021)、AP(F = 30.568,P < 0.001)方向上差异有统计学意义,膀胱和直肠的交互效应在AP(F = 3.221,P = 0.040)方向上差异有统计学意义。其中,膀胱充盈较多的患者,肠道准备在LR、SI、AP方向上治疗师调整的误差值比较差异无统计学意义(P > 0.05);膀胱充盈适中和较少的患者,二者比较差异均有统计学意义(P < 0.05),见表2。数据分布见图2。
|
|
表 2 不同膀胱和肠道准备情况下治疗师调整的误差值 Table 2 Radiotherapist-adjusted setup errors under different bladder and bowel preparation conditions |
|
图 2 治疗师调整摆位误差值的分布 Figure 2 Distribution of radiotherapist-adjusted setup errors 注:(a)膀胱充盈较多,(b)膀胱充盈适中,(c)膀胱充盈较少。 |
前列腺靶区及危及器官的剂量受膀胱和直肠充盈程度的影响较大[9-11]。有研究发现,未进行膀胱和肠道准备的患者膀胱体积最大变化高达98%,直肠体积最大变化高达96%[12]。因此,从CT模拟定位到放疗实施,保持膀胱和肠道状态的一致性至关重要。Rowe等[13]亦指出在模拟定位前和整个治疗过程中应对前列腺癌患者的饮食、肠道和膀胱准备进行指导,实现膀胱和肠道的可重复性。不少国内外研究者提出保证膀胱和肠道一致性的方法,如定时定量饮水、膀胱灌注、直肠植入水凝胶、高纤维饮食、每日微灌肠等[14-17],但因操作复杂,或患者依从性不高、肾功能不佳、不良饮食和生活习惯、身体代谢情况、排汗量等因素影响,仍会出现治疗时实际准备情况不能满足临床要求,进而导致靶区“脱靶”或直肠部分过多进入高剂量区的情况。Jotwani等[18]建议先排空肠道和膀胱,并在治疗前1 h喝250 mL水,结果发现在治疗后期膀胱和直肠剂量变化可达9.83%和8.92%。李婷等[19]研究发现在前列腺癌患者放疗实施过程中,膀胱和直肠体积平均每天减少3.59 mL和0.37 mL。因此,治疗前借助CBCT扫描来判断膀胱和肠道状态,对于避免治疗中后期发生严重的副反应,影响后续放疗的顺利实施和降低患者的生活质量尤为重要。若扫描后观察患者准备状态不佳,则要求患者暂停治疗,待准备充分后再行CBCT扫描。
本研究通过CBCT对38例患者每日膀胱和肠道的准备情况进行分析,发现仅4例患者每日准备全部满足临床需求,余34例患者存在不能成功治疗的情况,共93次,需重新准备。患者成功治疗的频率为(92.14 ± 5.25)%,其中膀胱充盈过少是影响患者成功治疗的主要因素,肠道胀气次之,分别为48.4%和30.1%。肠道胀气使直肠直径明显增大,可达CT模拟定位时的1.37倍,需进行饮食调整和使用辅助药物来促进排气。
根据美国放射肿瘤协会RTOG急性放射损伤分级标准统计患者的副反应情况,发现18例患者无急性放射性损伤(0级),20例患者出现1~2级损伤,0例患者出现3级及以上损伤,副反应情况较Linney等[20]统计结果轻。且副反应与成功治疗频率成负相关r = -0.393。可见,患者准备越充分,成功治疗频率就越高,副反应发生机率就越低。
曾自力等[21]指出摆位误差会对靶区和危及器官产生影响。对满足临床需求的移床值和自动灰度配准的摆位误差进行差异性比较,发现二者在LR、SI、AP方向均有差异(P < 0.05),且移床值(−0.05~−0.23) cm大于自动灰度配准的摆位误差(−0.05~−0.19) cm,“−”代表治疗床移动方向。可见,治疗师对前列腺癌患者进行CBCT配准时,应根据临床需求来调整摆位误差,与董晓庆等[22]研究结果有差异。刘豪佳等[23]亦指出实际工作中需人工确认或微调。进一步对不同膀胱和肠道准备情况下治疗师调整的误差值进行分析,发现膀胱和肠道准备的主效应均显著,交互效应在AP方向亦显著,说明膀胱和肠道的准备情况对治疗师调整的误差值有交互影响。其中,膀胱充盈较多时,肠道准备良好与准备不充分的患者治疗师调整的误差值无差异,调整了(0.00~0.02)cm,说明当患者膀胱充盈比CT模拟定位多时,肠道准备情况对前列腺体内位置变化无影响,治疗师调整的误差值较小;膀胱充盈适中和较少时,肠道准备良好调整的误差值分别为(0.00~0.01) cm和(0.00~0.12) cm,肠道准备不充分分别为(0.00~0.11) cm和(0.01~0.22) cm,二者有差异,说明膀胱充盈适中和较少时,肠道准备情况对治疗师调整的误差值有影响,即对前列腺体内位置变化有影响,且准备越不充分,位置变化就越大。
综上所述,膀胱充盈过少和肠道胀气是影响前列腺癌患者放射治疗的主要因素,治疗前应严格做好膀胱和肠道准备,提高治疗成功率,减轻放疗副反应。同时应加强放射治疗师的专业知识水平,CBCT配准时根据临床需求来调整摆位误差。为了避免出现较严重的放射性直肠损伤,治疗时应特别关注危及器官的保护,建议患者治疗时膀胱充盈程度稍多于CT模拟定位时,肠道准备对前列腺体内位置变化无影响,治疗师调整的误差值较小。但不可过度充盈膀胱,以免改变患者体位和影响放疗疗效。
| [1] |
Sung H, Ferlay J, Siegel RL, et al. Global cancer statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA Cancer J Clin, 2021, 71(3): 209-249. DOI:10.3322/caac.21660 |
| [2] |
Kuban DA, Tucker SL, Dong L, et al. Long-term results of the M. D. Anderson randomized dose-escalation trial for prostate cancer[J]. Int J Radiat Oncol Biol Phys, 2008, 70(1): 67-74. DOI:10.1016/j.ijrobp.2007.06.054 |
| [3] |
Yao LH, Shou JZ, Wang SL, et al. Long-term outcomes of moderately hypofractionated radiotherapy (67.5 Gy in 25 fractions) for prostate cancer confined to the pelvis: a single center retrospective analysis[J]. Radiat Oncol, 2020, 15(1): 231. DOI:10.1186/s13014-020-01679-0 |
| [4] |
王慧, 谢瑞霖, 秦庆伟, 等. T1b-4N0-1M0期前列腺癌高剂量及常规剂量放疗疗效及安全性对比Meta分析[J]. 中华放射肿瘤学杂志, 2019, 28(7): 514-517. Wang H, Xie RL, Qin QW, et al. Efficacy and safety of high-dose versus conventional-dose conventionally fractionated external beam radiotherapy for stage T1b-4N0-1M0 prostate cancer: a meta-analysis[J]. Chin J Radiat Oncol, 2019, 28(7): 514-517. DOI:10.3760/cma.j.issn.1004-4221.2019.07.008 |
| [5] |
林玉菊, 陈建鑫, 袁岩成, 等. 基于DRR图像的膀胱径线与体积相关性研究[J]. 医疗装备, 2018, 31(1): 1-2. Lin YJ, Chen JX, Yuan YC, et al. Investigate the correlation of volume and radial direction distance of bladder for cervical cancer in digitally reconstructed radiography[J]. Med Equip, 2018, 31(1): 1-2. DOI:10.3969/j.issn.1002-2376.2018.01.001 |
| [6] |
Chang JS, Yoon HI, Cha HJ, et al. Bladder filling variations during concurrent chemotherapy and pelvic radiotherapy in rectal cancer patients: early experience of bladder volume assessment using ultrasound scanner[J]. Radiat Oncol J, 2013, 31(1): 41-47. DOI:10.3857/roj.2013.31.1.41 |
| [7] |
姜晓勃, 钟庆初, 黄群峰, 等. 盆腔肿瘤放疗中膀胱充盈一致性初步研究[J]. 中华放射肿瘤学杂志, 2016, 25(6): 598-601. Jiang XB, Zhong QC, Huang QF, et al. Consistency of bladder filling during radiotherapy for pelvic tumor: a preliminary study[J]. Chin J Radiat Oncol, 2016, 25(6): 598-601. DOI:10.3760/cma.j.issn.1004-4221.2016.06.012 |
| [8] |
中国医师协会放射肿瘤治疗医师分会, 中华医学会放射肿瘤治疗学分会, 中国抗癌协会肿瘤放射治疗专业委员会. 中国前列腺癌放射治疗指南(2020年版)[J]. 中华肿瘤防治杂志, 2021, 28(5): 323-337. Radiooncologist Branch of Chinese Medical Doctor Association, Radiation Oncology Therapy Branch of the Chinese Medical Society, Cancer Radiotherapy Professional Committee of China Anti-Cancer Association. Radiotherapy guidelines for prostate cancer in China (2020ed)[J]. Chin J Radiat Oncol, 2021, 28(5): 323-337. DOI:10.16073/j.cnki.cjcpt.2021.05.01 |
| [9] |
应文敏, 廖绍光, 傅志超, 等. 前列腺癌调强放疗中直肠充盈状态对靶区及危及器官的影响[J]. 临床肿瘤学杂志, 2016, 21(9): 810-813. Ying WM, Liao SG, Fu ZC, et al. Impacts of rectum filling status on dosimetric parameters of target volume and organ at risk in intensity-modulated radiotherapy for prostate cancer[J]. Chin Clin Oncol, 2016, 21(9): 810-813. |
| [10] |
李明, 林海磊, 修霞, 等. 膀胱直肠管理对前列腺癌靶区及OAR剂量影响[J]. 中华放射肿瘤学杂志, 2015, 24(6): 644-648. Li M, Lin HL, Xiu X, et al. Effects of bladder and rectum management on dose distributions of target and organs at risk in intensity-modulated radiotherapy for prostate cancer[J]. Chin J Radiat Oncol, 2015, 24(6): 644-648. DOI:10.3760/cma.j.issn.1004-4221.2015.06.009 |
| [11] |
李克新, 鞠永健, 曹丽媛, 等. 前列腺癌患者定位与调强放疗时膀胱充盈程度不一致对剂量学参数的影响[J]. 中华放射医学与防护杂志, 2019, 39(3): 192-196. Li KX, Ju YJ, Cao LY, et al. The dosimetric effect of inconsistency of bladder filling states between CT simulation and IMRT treatment for prostate cancer patients[J]. Chin J Radiol Med Prot, 2019, 39(3): 192-196. DOI:10.3760/cma.j.issn.0254-5098.2019.03.006 |
| [12] |
Heng SP, Low SH, Sivamany K. The influence of the bowel and bladder preparation protocol for radiotherapy of prostate cancer using kilo-voltage cone beam CT: our experience[J]. Indian J Cancer, 2015, 52(4): 639-644. DOI:10.4103/0019-509X.178386 |
| [13] |
Rowe LS, Mandia JJ, Salerno KE, et al. Bowel and bladder reproducibility in image guided radiation therapy for prostate cancer: results of a patterns of practice survey[J]. Adv Radiat Oncol, 2022, 7(5): 100902. DOI:10.1016/j.adro.2022.100902 |
| [14] |
伍嘉颖, 陆世培, 李存啸, 等. 盆腔肿瘤放疗执行前膀胱充盈一致性研究[J]. 中华放射肿瘤学杂志, 2021, 30(1): 61-65. Wu JY, Lu SP, Li CX, et al. Study on the bladder filling consistency of pelvic tumors prior to the radiotherapy[J]. Chin J Radiat Oncol, 2021, 30(1): 61-65. DOI:10.3760/cma.j.cn113030-20190624-00245 |
| [15] |
钟嘉健, 丘敏敏, 邓永锦, 等. 两种膀胱充盈方式在宫颈癌术后调强放疗中的对比[J]. 中华肿瘤防治杂志, 2021, 28(12): 944-948. Zhong JJ, Qiu MM, Deng YJ, et al. Comparison of two methods of bladder filling in postoperative IMRT for cervical cancer[J]. Chin J Cancer Prev Treat, 2021, 28(12): 944-948. DOI:10.16073/j.cnki.cjcpt.2021.12.11 |
| [16] |
杨烨, 侯彦杰, 薛少军, 等. 前列腺癌放疗患者植入水凝胶后对直肠保护作用的Meta分析[J]. 中华放射医学与防护杂志, 2021, 41(6): 436-443. Yang Y, Hou YJ, Xue SJ, et al. The protective effects of hydrogel implantation in prostate cancer patients for radiotherapy: a Meta-analysis[J]. Chin J Radiol Med Prot, 2021, 41(6): 436-443. DOI:10.3760/cma.j.issn.0254-5098.2021.06.007 |
| [17] |
Yahya S, Zarkar A, Southgate E, et al. Which bowel preparation is best? Comparison of a high-fibre diet leaflet, daily microenema and no preparation in prostate cancer patients treated with radical radiotherapy to assess the effect on planned target volume shifts due to rectal distension[J]. Br J Radiol, 2013, 86(1031): 20130457. DOI:10.1259/bjr.20130457 |
| [18] |
Jotwani A, Surendran J, Chilukuri S, et al. Rectum and bladder dose variations during prostate IGRT: an evaluation of bowel and bladder preparation protocol[J]. Int J Radiat Oncol Biol Phys, 2012, 84(3S): S395. DOI:10.1016/j.ijrobp.2012.07.1042 |
| [19] |
李婷, 郭雨军, 杨鑫, 等. 肠道膀胱准备下前列腺癌精准放疗膀胱直肠变化分析[J]. 中华放射肿瘤学杂志, 2023, 32(2): 124-130. Li T, Guo YJ, Yang X, et al. Analysis of the rectum and bladder changes in prostate precise radiotherapy under the bowel and bladder preparation[J]. Chin J Radiat Oncol, 2023, 32(2): 124-130. DOI:10.3760/cma.j.cn113030-20220701-00229 |
| [20] |
Linney H, Barrett S. Stereotactic body radiation therapy for patients with early-stage prostate cancer[J]. Anticancer Res, 2018, 38(3): 1231-1240. DOI:10.21873/anticanres.12344 |
| [21] |
曾自力, 林锋, 谭勇. 摆位误差对直肠癌术后调强放射治疗剂量学影响的研究[J]. 中国辐射卫生, 2021, 30(4): 517-523,528. Zeng ZL, Lin F, Tan Y. Dosimetric effects study of set-up error in postoperative intensity modulated radiotherapy of rectal cancer[J]. Chin J Radiol Health, 2021, 30(4): 517-523,528. DOI:10.13491/j.issn.1004-714X.2021.04.025 |
| [22] |
董晓庆, 胡杰, 陆春花, 等. 前列腺癌图像引导放射治疗精准度评估[J]. 中国医学物理学杂志, 2016, 33(7): 658-663. Dong XQ, Hu J, Lu CH, et al. Accuracy assessment of image-guided radiotherapy for prostate cancer[J]. Chin J Med Phys, 2016, 33(7): 658-663. DOI:10.3969/j.issn.1005-202X.2016.07.003 |
| [23] |
刘豪佳, 王慧涛, 徐红卫, 等. X射线容积成像系统配准方式对中下段食管癌放疗体位验证的影响[J]. 中国辐射卫生, 2023, 32(1): 52-57. Liu HJ, Wang HT, Xu HW, et al. Effects of X-ray volume imaging registration methods on position verification for radiotherapy in treatment of middle/lower-segment esophageal cancer[J]. Chin J Radiol Health, 2023, 32(1): 52-57. DOI:10.13491/j.issn.1004-714X.2023.01.011 |




