2. 军事科学院军事医学研究院辐射医学研究所, 北京市放射生物学重点实验室, 北京 100850;
3. 泰山学院化学化工学院, 山东 泰安 271021;
4. 军事科学院军事医学研究院毒物药物研究所, 北京 100850;
5. 河北大学生命科学学院, 河北 保定 071002
2. Institute of Radiation Medicine, Academy of Military Medicine, Academy of Military Sciences, Beijing Key Laboratory of Radiobiology, Beijing 100850 China;
3. School of Chemistry and Chemical Engineering, Taishan University, Taian 271021 China;
4. Institute of Pharmacology and Toxicology, Academy of Military Medical Sciences, Academy of Military Sciences, Beijing 100850 China;
5. College of Life Sciences, Hebei University, Baoding 071002 China
铀是长寿命放射性重金属,铀污染对环境及人类健康将带来严重威胁[1-2]。人们一直致力于铀污染处理的研究,但至今没有特别好的措施。近年来,杯芳烃[3-5]作为较新的铀吸附化合物备受瞩目。研究发现[6-7],多种杯芳烃衍生物如磺酸基衍生物对铀酰离子有良好的螯合作用,能与之形成稳定配合物。其中杯[6]芳烃的化学结构更利于和铀酰离子结合[8],且将杯芳烃衍生物与材料结合在铀矿废水吸附[9]或皮肤洗消[4,10]上也已有应用。在污染场景的复杂情况下大量的水源往往难得或及时应用。水剂洗消剂有回收困难,二次污染的难题,若能将化合物与载体结合,则有助益于解决上述的问题。纤维素是一种较高利用率的高分子材料[11],棉纤维是一种对皮肤没有刺激的天然纤维素,且纤维素上的羟基易于反应。本研究将4-磺酸杯[6]芳烃与棉纤维进行化学接枝,完成表征后,探究其在硝酸铀酰溶液中的吸附效果和在污染皮肤的洗消效果,初步验证合成材料用于铀的吸附和洗消的可行性。
1 材料与方法 1.1 试剂与仪器 1.1.1 试剂对叔丁基苯酚、吡啶、N,N-二甲基甲酰胺(DMF)和二甲基亚砜(DMSO)、丙酮、30%过氧化氢溶液、硝酸购自国药集团化学试剂有限公司;氯化铝、α-溴异丁酰溴(BIBB)、甲基丙烯酸缩水甘油酯(GMA)、2,2'-联吡啶(Bpy)、溴化铜(CuBr)和溴化亚铜(CuBr2)购自麦克林;甲苯购自西陇化学试剂有限公司;无水二氯甲烷(DCM)购自北京伊诺凯科技有限公司,三乙醇胺购自安耐吉科技有限公司;六水合硝酸铀酰购自北京化工厂;J-22抗干扰型铀荧光增强剂购自北京地质研究院。所有化学试剂为分析级,且在没有进一步纯化的情况下使用。
1.1.2 仪器微波消解仪购自北京盈安美诚科学仪器有限公司;TP-6 透皮扩散仪购自天津市精拓仪器科技有限公司;恒温振荡器购自江苏太仓市实验设备厂;WGJ-Ⅲ型微量铀分析仪购自杭州大吉光电仪器公司;Nicolet IS 50型红外光谱仪,Sigma500 场发射扫描电子显微镜,SCIENTIFIC ESCALAB Xi + X射线光电子能谱仪。
1.2 4-磺酸杯[6]芳烃的合成根据文献[12-14],如图1a所示,以对叔丁基苯酚为原料,在碱性条件下合成对叔丁基杯[6]芳烃;于甲苯中用氯化铝去除化合物中叔丁基,再于浓硫酸中反应得到4-磺酸杯[6]芳烃。

|
图 1 4-磺酸杯[6]芳烃棉纤维合成的技术路线 Figure 1 Synthesis of 4-sulfonylcalix[6]arene-modified cotton |
合成的技术路线如图1b,具体方法如下。
1.3.1 溴化棉纤维首先将棉纤维和30 mL DCM加入圆底烧瓶,容器置于冰水浴中,再将10 mL BIBB加进烧瓶中,然后缓慢加入1 mL吡啶。加完所有试剂后,容器密封并置于磁力搅拌器中,在室温中反应混合搅拌(24 h,150 r/min),冷凝回流。反应完成后,将产物取出,用丙酮和去离子水反复冲洗,最后自然晾干,得到溴化棉纤维(Cotton-Br)。
1.3.2 聚甲基丙烯酸缩水甘油酯棉纤维(Cotton-PGMA)取Cotton-Br置于容器中,加入5 mL去离子水,10 mL DMF,15 mL GMA,0.5 g Bpy,0.12 g CuBr2和0.23 g CuBr,使用真空泵抽出瓶内空气,在N2氛围下反应(45℃,2.5 h,150 r/min)。反应完毕后的产物依次用四氢呋喃、丙酮和去离子水洗涤,自然晾干,得到聚甲基丙烯酸缩水甘油酯棉纤维(Cotton-PGMA)。
1.3.3 4-磺酸杯[6]芳烃棉纤维(Cotton S-C[6]a)3 g 4-磺酸杯[6]芳烃,100 mL 三乙醇胺,100 mL DMSO于烧瓶中搅拌(30℃,24 h),然后加入Cotton-PGMA继续搅拌(150 r/min,50℃,96 h)。冷却后,去离子水洗涤,自然晾干。最后得到成品4-磺酸杯[6]芳烃棉纤维(Cotton S-C[6]a)。
1.4 模拟铀污染皮肤使用电动剃毛刀去除巴马猪背部皮肤表面毛发,刀去除皮下脂肪,流水洗净,皮肤表面擦干,切割为2 cm × 2 cm大小的样品,于-20℃冰箱中备用。冷冻皮肤样品于室温中自然解冻;将制备样品固定在Franz扩散池的供体池和接受池之间,在供体池中加入50 uL 1 mmol/L的硝酸铀酰溶液,接受池充满0.9%生理盐水,置于水浴锅中污染(32℃,2 h)。
1.5 4-磺酸杯[6]芳烃对铀的吸附条件探索使用硝酸或氢氧化钠调节硝酸铀酰溶液的pH,称取定量的4-磺酸杯[6]芳烃棉纤维 投入5 mL 0.05 mmol/L的硝酸铀酰溶液的锥形瓶中,将锥形瓶置于恒温振荡器,25℃,80 rpm振荡一定时间,后将棉纤维取出,检测溶液中剩余铀酰离子含量。采用吸附率(adsorption rate,Ads.)评价吸附效果。
| $ {\rm{Adsorption}}\%=\frac{{{{C}}}_{0}-{{{C}}}_{{{e}}}}{{{C}}_{0}} $ | (1) |
分别制备20 mg棉纤维和4-磺酸杯[6]芳烃棉纤维湿润样品(pH 4.0,含液量 ≥ 4.0),在污染皮肤表面孵用样品进行去污20 min。采用去污效率(decontamination efficiency,DE)评价去污效果。
| $ 去污效率(\mathrm{D}\mathrm{E})=\frac{皮肤消解液中铀含量({\mu }{{\rm{g}}})}{污染物铀含量({\mu }{{\rm{g}}})}\times 100\mathrm{\%} $ | (2) |
首先在烧瓶中加入5 mL 0.05 mmol/L硝酸铀酰(pH=4),分别加入20 mg棉纤维和4-磺酸杯[6]芳烃棉纤维。将烧瓶置于恒温振荡器中(25℃,20 min,80 rpm)中,收集剩余液体。吸附量用吸附百分比(%)和吸附容量(qe)表示,由以下公式1)及以下计算:
| $ {{{q}}}_{{{e}}}=\frac{{V}({{{C}}}_{0}-{{{C}}}_{{{e}}})}{{{m}}} $ | (3) |
C0和Ce是吸附前后溶液中铀的浓度(ug/mL),V(L)代表液体的体积,m(g)是吸附剂的用量,qe是吸附剂上吸附的铀含量。
1.7 铀含量测定取一份样品于微波消解罐中,加入4 mL硝酸,2 mL过氧化氢溶液,于微波消解仪中消解,冷却后调节pH并定容至25 mL。取待测样稀释至适当浓度于石英比色皿中,使用微量铀分析仪分别测试稀释后的样品;稀释后的样品与抗干扰型铀荧光增强剂、稀释后的样品与抗干扰型铀荧光增强剂与铀标准液。最后得到待测液中铀酰离子浓度。
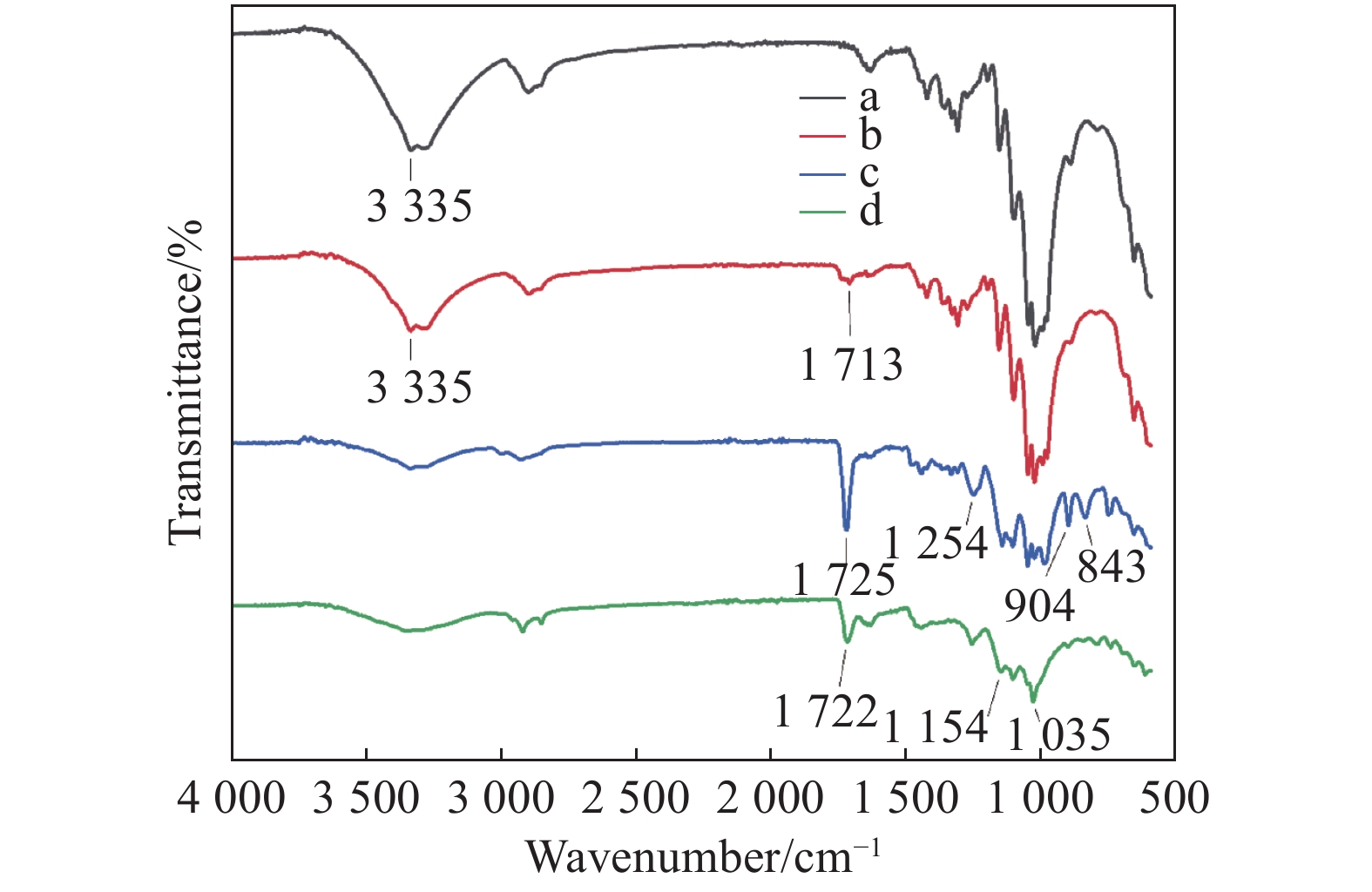
2 结 果 2.1 接枝4-磺酸杯[6]芳烃的棉纤维及其表征 2.1.1 红外光谱如图2所示,在3335 cm−1处出现较宽的峰为棉纤维羟基特征峰;溴化以后,在1713,1725,1722 cm−1处出现−C=O−基团的伸缩振动峰,提示BIBB已经成功在棉纤维表面引入。位于1149 cm−1和1254 cm−1处的峰为GMA分子中−C−O−基团的对称和非对称振动峰,以及位于904 cm−1和842 cm−1的特征峰,说明GMA成功引入。908 cm−1和842 cm−1处环氧基团的特征峰均消失,说明PGMA棉纤维中的环氧基团发生了反应,在1155 cm−1和1035 cm−1附近为磺酸盐中S−O的反对伸缩振动峰,说明材料中磺酸基团的引入。
|
图 2 4-磺酸杯[6]芳烃接枝棉纤维的红外光谱 Figure 2 FT-IR spectra of 4-sulfonylcalix[6]arene-modified cotton 注:(a) 棉纤维;(b) 溴化棉纤维;(c)聚甲基丙烯酸缩水甘油酯棉纤维;(d)4-磺酸杯[6]棉纤维。 |
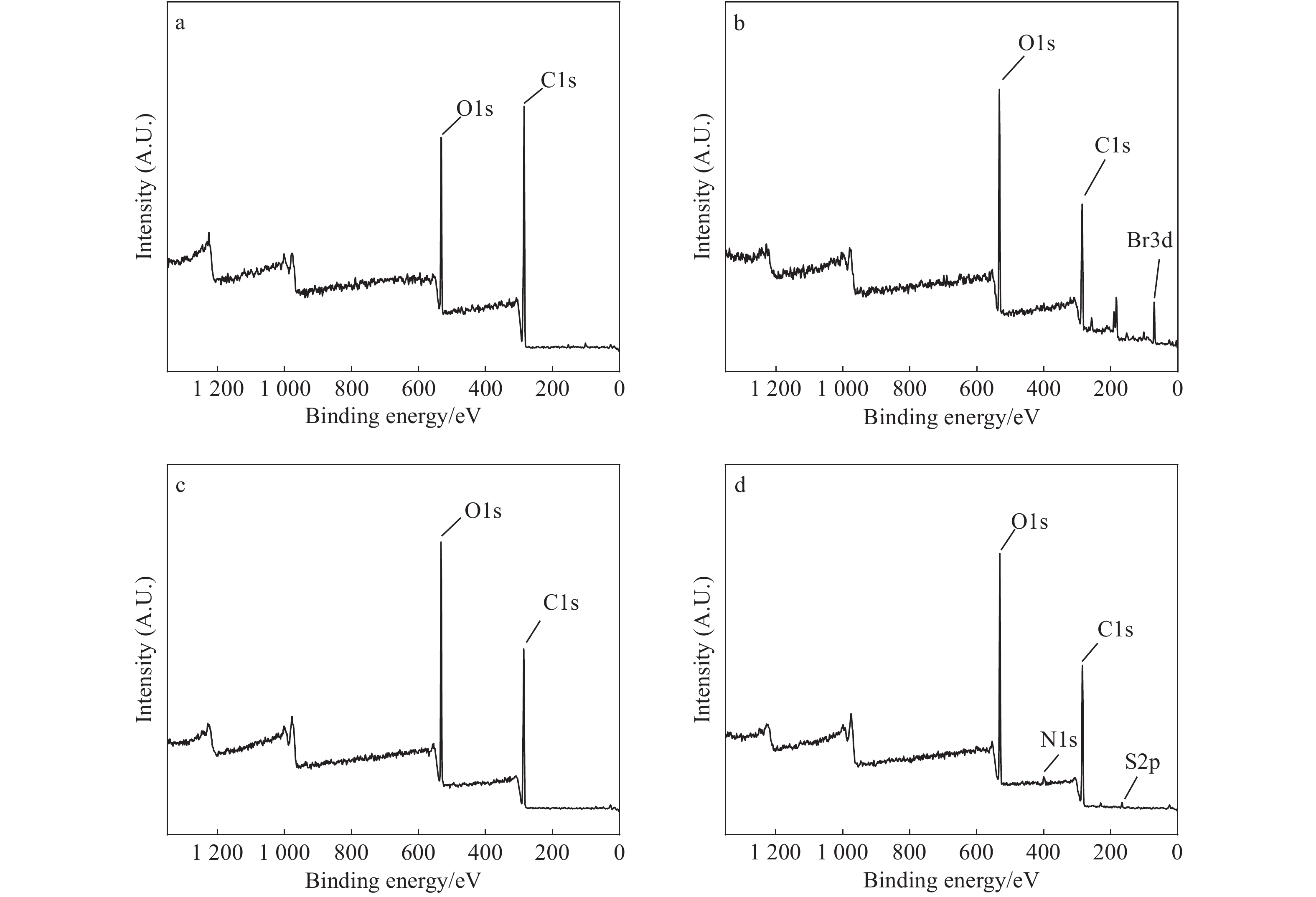
图3a为棉纤维的XPS全谱图,可以清晰的看见C1s和O1s的峰,为棉纤维中纤维素成分的峰;图3b为溴化棉纤维的XPS全谱图,除C1s和O1s的峰外,还出现了Br3d的峰,提示材料表面溴元素的加入。图3c中XPS图中以C1s和O1s的峰为主,因为GMA中主要元素组成是C,O。图3d中,在XPS全谱图中出现了新的峰N1s和S2p,表明材料表面硫元素和氮元素的加入。
|
图 3 4-磺酸杯[6]芳烃接枝棉纤维的X射线电子能谱 Figure 3 XPS spectra of 4-sulfonylcalix[6]arene-modified cotton 注:(a) 棉纤维;(b) 溴化棉纤维;(c)聚甲基丙烯酸缩水甘油酯棉纤维;(d)4-磺酸杯[6]棉纤维。 |
图4a为棉纤维的SEM图,可看出材料表面光滑平整,质地均匀,呈微螺旋扁带状,为典型棉纤维SEM图;图4b为Cotton-Br的SEM图,溴化以后其形态没有明显改变,但其表面多了些许倒刺。图4c可见,反应后棉纤维体积粗糙,体积较之前增加。图4d扫描电镜图可见,材料表面粗糙感相对降低,表面依旧凹凸不平,提示材料表面发生了反应。

|
图 4 4-磺酸杯[6]芳烃接枝棉纤维的扫描电镜图 Figure 4 SEM of 4-sulfonylcalix[6]arene-modified cotton 注:(a) 棉纤维;(b) 溴化棉纤维;(c)聚甲基丙烯酸缩水甘油酯棉纤维;(d)4-磺酸杯[6]棉纤维。 |
pH值的变化会对金属离子沉淀和表面官能团电离产生影响。本部分在不同的pH(pH 1~pH 8)条件下研究了其对4-磺酸杯[6]芳烃(Cotton S-C[6]a)吸附铀的影响,探寻吸附的最佳pH值。如图5a所示,随着pH从pH 1到pH 4的升高,吸附率增加并在pH 4时达到最大值,pH 5后吸附率略有下降。pH较低时,溶液中大量存在的H + 与金属离子会发生竞争吸附,同时溶液中大量存在的H + ,衍生物中的磺酸基团质子化,增加基团对金属阳离子的静电斥力,减少了吸附位点,随着pH升高,基团上的氢键容易丢失,呈电负性,增强了官能团与金属阳离子之间的结合能力和反应几率,吸附率增大。因此在pH由酸到中性时,Cotton S-C[6]a吸附率逐渐升高;pH由中性变碱时,Cotton S-C[6]a吸附率反而下降,这是由于溶液中的金属离子发生水解,形成UO2(OH)2沉淀,不利于对金属离子的吸附作用。

|
图 5 4-磺酸杯[6]芳烃棉纤维吸附铀的影响因素 Figure 5 Factors influencing uranium adsorption by 4-sulfonylcalix[6]arene-modified cotton 注:(a)pH的影响(吸附剂用量=10 mg,铀浓度=5 × 10−5 mol L−1,时间=30 min,液体量=5 mL);(b)吸附剂用量的影响(pH= 4,铀浓度=5 × 10−5 mol L−1,时间=30 min,液体量=5 mL);(c)吸附时间的影响(吸附剂用量=10 mg,铀浓度=5 × 10−5 mol L−1,液体量=5 mL,pH= 4)。 |
不同用量的4-磺酸杯[6]芳烃棉纤维对铀的吸附能力,如图5b所示。吸附用量自15 mg/5 mL时吸附率趋于平缓,吸附用量为30 mg/5 mL时约达82%。吸附率随吸附剂浓度的增加而呈现增加趋势。当吸附剂用量较少时,由于驱动力较低,金属离子的吸收率也较低[15];吸附剂用量的增加,相应地也增加了吸附活性位点和空穴,铀酰离子与Cotton S-C[6]a的结合增多,吸附率上升;用量进一步增加时,吸附已经趋于平衡状态,铀酰离子结合时受阻。但由于棉纤维的亲水性好,也表现出了一定的吸附能力;吸附剂用量增加,可结合位点增加,吸附率上升。
2.2.3 吸附时间的影响影响化学和生物现象的最重要因素是时间。本部分探究了吸附时间对4-磺酸杯[6]芳烃棉纤维吸附铀的影响,以确定其最佳吸附时间。如图5c所示,当接触时间从5~120 min,吸附率从75.5%增加到87%,20 min内可达到84%。吸附开始时吸附迅速,可能是因为吸附剂刚接触到金属离子时,结合位点多,可快速吸附,故在吸附5 min后就可达75.5%;接触时间延长后,结合位点接近饱和,空穴位点减少,吸附率的变化不明显。
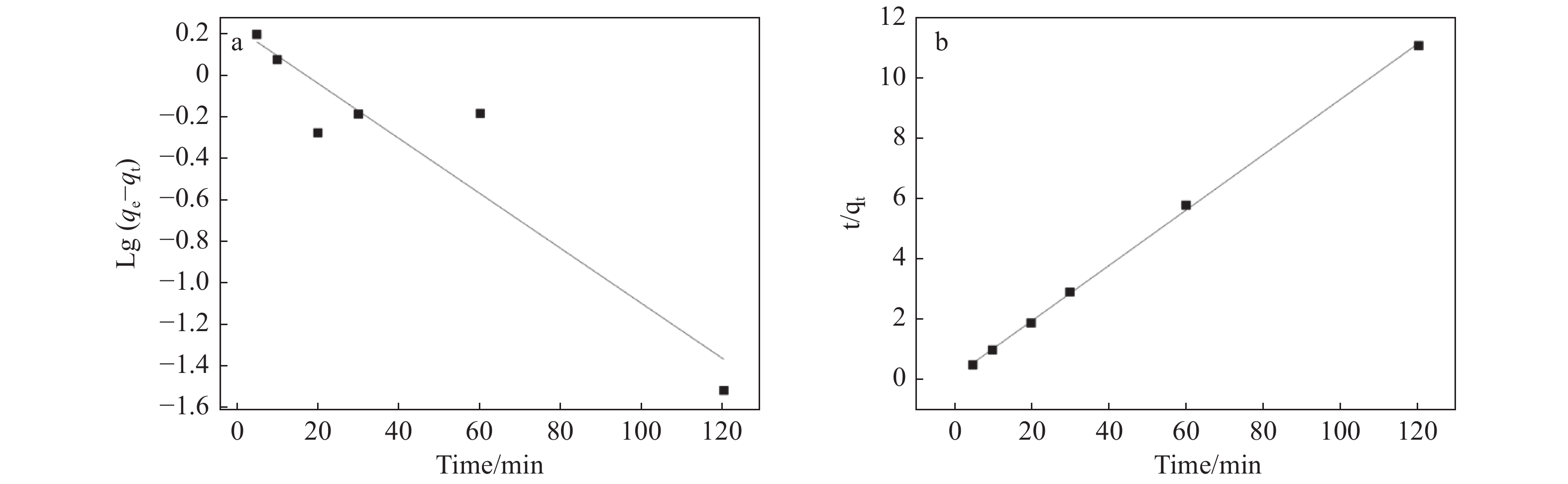
2.2.4 吸附动力学利用吸附动力学描述4-磺酸杯[6]芳烃棉纤维对六价铀的吸附速率和吸附的平衡时间。采用伪一级和伪二级动力学模型对吸附过程进行了模拟,以探究4-磺酸杯[6]芳烃棉纤维的吸附动力学。图6a,b分别显示了lg(qe−qt)与t,t/qt的关系,计算结果列于表1中。
|
图 6 4-磺酸杯[6]芳烃棉纤维吸附铀的动力学模型 Figure 6 Kinetic models of uranium adsorption by 4-sulfonylcalix[6]arene-modified cotton 注:(a)伪一级动力学模型;(b)伪二级动力学模型。 |
|
|
表 1 4-磺酸杯[6]芳烃棉纤维吸附铀 Table 1 Kinetic models of uranium adsorption by 4-sulfonylcalix[6]arene-modified cotton |
伪一级动力学模型以下式计算:
| $ \mathrm{lg}\left({q}_{e}-{q}_{t}\right)=\mathrm{l}\mathrm{g}{{q}}_{e}-\frac{k1}{2.303}t $ | (4) |
伪二级动力学模型以下式计算:
| $ \frac{t}{{q}_{t}}=\frac{1}{{k}_{2}{q}_{t}^{2}} + \frac{t}{{q}_{e}} $ | (5) |
其中k1是伪一级吸附速率常数,min−1,k2是二级吸附速率常数,mg−1 min−1,qe和qt是平衡吸附容量和时间t的吸附容量,mg g−1。如图6所示,吸附剂的伪二阶模型的相关系数优于伪一级模型的相关系数,故伪二阶模型可以较好地描述吸附过程。根据方程(4)计算的4-磺酸杯[6]芳烃棉纤维的qe理论值为11.10 mg g−1,与实验结果(10.89 mg g−1)几乎相同。结果表明,吸附过程主要以化学吸附或表面络合为主。
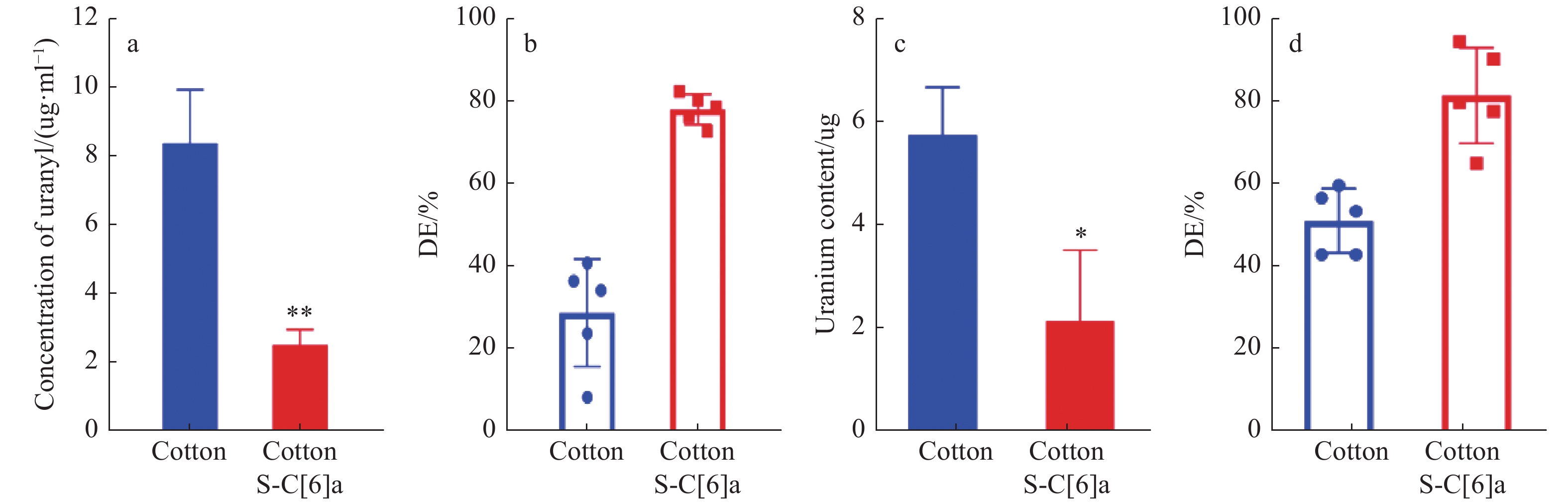
2.3 4-磺酸杯[6]芳烃棉纤维对铀的吸附 2.3.1 溶 液我们前期的实验结果表明,4-磺酸杯[6]芳烃棉纤维吸附铀的最适条件为pH= 4 ,作用时间为20 min。使用棉纤维和4-磺酸杯[6]芳烃棉纤维吸附铀的结果如图7a,b所示,吸附后溶液中的铀酰离子浓度分别为(8.42±1.54)和(2.56±0.44) ug/mL;2种棉纤维对铀的吸附率分别为29.23%±12.98%和78.46%±3.68%。
|
图 7 棉纤维和4-磺酸杯[6]芳烃棉纤维的吸附效果 (n=5) Figure 7 Adsorption efficiency of cotton and 4-sulfonylcalix[6]arene-modified cotton (n = 5) 注:(a )吸附后溶液中铀酰离子浓度;(b) 溶液铀去除率;(c)吸附后皮肤消解液中铀含量;(d)皮肤铀污染的去除率;* P < 0.01 * * P < 0.0001。 |
使用棉纤维和4-磺酸杯[6]芳烃棉纤维孵用于污染后皮肤的吸附效果如图7c,d所示,孵用后皮肤消解液中铀含量为(5.77 ± 0.92) ug和(2.17 ± 1.37) ug;孵用后的铀去除率分别为51.47% ± 7.8%和81.72% ± 11.55%。
3 讨 论杯芳烃的溶解性差,用于洗消多有受限,但通过引入特定的基团可改善杯芳烃的物理性质和吸附特性。引入带负电的基团如磺化后的杯芳烃[16-17],其羧基可提供静电和氢键相互作用位点,从而对阳离子客体产生强亲和力。磺酸基的加入不仅为杯芳烃增加水溶性,也增加了其应用场景[18]。在本实验中,4-磺酸杯[6]芳烃棉纤维对铀的吸附表现出良好的效果。影响杯[6]磺酸棉纤维吸附的因素主要为pH、吸附剂用量、时间。pH对铀吸附的影响很大[7],对于不同材料其最适pH也不尽相同[19-22]。本研究中4-磺酸杯[6]芳烃棉纤维吸附铀的最适pH为4,符合皮肤用湿巾3.5~8.5的标准。结果中pH的影响与之前一些研究[23]非常吻合,即吸附速率随着溶液的碱性增加而趋于下降。本实验中最佳吸附时间约为20 min;最佳吸附剂用量为20 mg,吸附的量随着吸附剂用量上升呈剂量效应关系,作用迅速高效。4-磺酸杯[6]芳烃棉纤维对溶液中铀酰离子的吸附和硝酸铀酰污染的皮肤去污效果显著,且制备简便,有广泛的应用前景,如含铀废水的吸附与皮肤铀污染的应急处理。
本研究将棉纤维材料通过化学接枝的方式与杯芳烃衍生物结合,以期借助其本身材料柔和舒适性,融合杯芳烃衍生物对铀的吸附有效性,在最适条件下安全有效的应用于铀污染去除。本研究仍有一些不足之处,如没能更加接近的模拟皮肤表面污染状态,如战争中这类应用场景并非单纯的铀污染,可能混合有多种核素,化学毒物污染等情况。本研究涉及的只是完整皮肤,未测试在受伤皮肤上铀污染的去污效果。
| [1] |
Berard P, Michel X, Menetrier F, et al. Medical management of a cutaneous contamination[J]. Health Phys, 2010, 99(4): 572-576. DOI:10.1097/HP.0b013e3181d94ec1 |
| [2] |
López R, Díaz Sylvester PL, Ubios AM, et al. Percutaneous toxicity of uranyl nitrate: its effect in terms of exposure area and time[J]. Health Phys, 2000, 78(4): 434-437. DOI:10.1097/00004032-200004000-00007 |
| [3] |
Spagnul A, Bouvier-Capely C, Phan G, et al. Ex vivo decrease in uranium diffusion through intact and excoriated pig ear skin by a calixarene nanoemulsion[J]. Eur J Pharm Biopharm, 2011, 79(2): 258-267. DOI:10.1016/j.ejpb.2011.05.004 |
| [4] |
Phan G, Semili N, Bouvier-Capely C, et al. Calixarene cleansing formulation for uranium skin contamination[J]. Health Phys, 2013, 105(4): 382-389. DOI:10.1097/HP.0b013e318298e8d3 |
| [5] |
周文华, 尹晶晶, 高洁, 等. 体内铀毒性及其新型促排剂研究进展[J]. 中国辐射卫生, 2022, 31(3): 379-385. Zhou WH, Yin JJ, Gao J, et al. Research advances in toxicity of uranium in vivo and its new chelators[J]. Chin J Radiol Health, 2022, 31(3): 379-385. DOI:10.13491/j.issn.1004-714X.2022.03.023 |
| [6] |
Salmon L, Thuéry P, Ephritikhine M. Uranium(IV) complexes of calix[n]arenes (n = 4, 6 and 8)[J]. Chem Commun, 2006(8): 856-858. DOI:10.1039/b516438a |
| [7] |
Bauer A, Jäschke A, Schöne S, et al. Uranium(VI) Complexes with a Calix[4]arene-based 8-hydroxyquinoline ligand: thermodynamic and structural characterization based on calorimetry, spectroscopy, and liquid-liquid extraction[J]. ChemistryOpen, 2018, 7(6): 467-474. DOI:10.1002/open.201800085 |
| [8] |
Shinkai S. Molecular recognition of calixarene-based host molecules[J]. J Incl Phenom Molecul Recogn Chem, 1989, 7(2): 193-201. DOI:10.1007/BF01060721 |
| [9] |
Schmeide K, Heise KH, Bernhard G, et al. Uranium(VI) separation from aqueous solution by calix[6]arene modified textiles[J]. J Radioanal Nucl Chem, 2004, 261(1): 61-67. DOI:10.1023/b:Jrnc.0000030935.11840.52 |
| [10] |
Grivès S, Phan G, Bouvier-Capely C, et al. Compared in vivo efficiency of nanoemulsions unloaded and loaded with calixarene and soapy water in the treatment of superficial wounds contaminated by uranium[J]. Chem Biol Interact, 2017, 267: 33-39. DOI:10.1016/j.cbi.2016.11.030 |
| [11] |
Zhang LT, Sun YF, Wang YB, et al. Easy-cleaning surfaces functionalized with an interface-binding recombinant lipase[J]. Colloids Surf B:Biointerfaces, 2019, 184: 110433. DOI:10.1016/j.colsurfb.2019.110433 |
| [12] |
Gutsche CD, Dhawan B, No K, et al. Additions and Corrections - Calixarenes. 4. The synthesis, characterization, and properties of calixarenes from p-tert-Butylphenol[J]. J Am Chem Soc, 2004, 106(6): 1891-1891. DOI:10.1021/ja00318a600 |
| [13] |
Bocchi V, Foina D, Pochini A, et al. Synthesis, 1H NMR, 13C NMR spectra and conformational preference of open chain ligands on lipophilic macrocycles[J]. Tetrahedron, 1982, 38(3): 373-378. DOI:10.1016/0040-4020(82)80176-2 |
| [14] |
Shinkai S, Mori S, Koreishi H, et al. Hexasulfonated calix[6]arene derivatives: a new class of catalysts, surfactants, and host molecules[J]. J Am Chem Soc, 1986, 108(9): 2409-2016. DOI:10.1021/ja00269a045 |
| [15] |
Sana S, Roostaazad R, Yaghmaei S. Biosorption of uranium (VI) from aqueous solution by pretreated Aspergillus niger using sodium hydroxide[J]. Iran J Chem Chem Eng, 2015, 34(1): 65-74. |
| [16] |
Perret F, Lazar AN, Coleman AW. Biochemistry of the para-sulfonato-calix[n]arenes[J]. Chem Commun, 2006(23): 2425-2438. DOI:10.1039/b600720c |
| [17] |
Shinkai S, Mori S, Tsubaki T, et al. New water-soluble host molecules derived from calix[6]arene[J]. Tetrahedron Lett, 1984, 25(46): 5315-5318. DOI:10.1016/S0040-4039(01)81592-6 |
| [18] |
Ahmad M, Yang K, Li LX, et al. Modified tubular carbon nanofibers for adsorption of Uranium(VI) from water[J]. ACS Appl Nano Mater, 2020, 3(7): 6394-6405. DOI:10.1021/acsanm.0c00837 |
| [19] |
Anirudhan TS, Lekshmi GS, Shainy F. Synthesis and characterization of amidoxime modified chitosan/bentonite composite for the adsorptive removal and recovery of uranium from seawater[J]. J Colloid Interface Sci, 2019, 534: 248-261. DOI:10.1016/j.jcis.2018.09.009 |
| [20] |
Liu HJ, Wang X, Li YJ, et al. Efficient uranium(VI) adsorbing bioinspired nano-sized hydroxyapatite composites: synthesis, tuning, and adsorption mechanism[J]. Environ Sci Pollut Res Int, 2023, 30(7): 18156-18167. DOI:10.1007/s11356-022-23492-w |
| [21] |
Xuan K, Wang J, Gong ZH, et al. Hydroxyapatite modified ZIF-67 composite with abundant binding groups for the highly efficient and selective elimination of uranium (VI) from wastewater[J]. J Hazard Mater, 2022, 426: 127834. DOI:10.1016/j.jhazmat.2021.127834 |
| [22] |
Huynh J, Palacio R, Safizadeh F, et al. Adsorption of Uranium over NH2-functionalized ordered silica in aqueous solutions[J]. ACS Appl Mater Interfaces, 2017, 9(18): 15672-15684. DOI:10.1021/acsami.6b16158 |
| [23] |
Gok C, Aytas S. Biosorption of uranium(VI) from aqueous solution using calcium alginate beads[J]. J Hazard Mater, 2009, 168(1): 369-375. DOI:10.1016/j.jhazmat.2009.02.063 |




