颅内占位性病变是一组良性或恶性、原发或转移性病变[1]。转移性肿瘤是成人最常见的颅内肿瘤,通常预后较差[2]。HIV/AIDS患者、骨髓移植患者等免疫缺陷患者颅内占位性病变发生风险相关较高,而热带地区和发展中国家患者可能因中枢神经系统囊尾蚴病和结核感染而导致颅内占位性病变[3-5]。因此,颅内占位性病变精准诊断和鉴别诊断对于明确患者病因、制定治疗方案、改善预后、提高生活质量均具有重要意义[6]。
常规磁共振成像(MRI)技术可以清晰展示人体的解剖学位置,已成为诊断颅内疑似病变的主要手段[7]。弥散加权成像(DWI)、磁敏感加权成像(SWI)、灌注加权成像(PWI)等技术发展极大提升了MRI技术的诊断准确性,但由于特异性欠佳,诸多颅内占位性病变的诊断仍是一大挑战[8]。作为一种新型MRI技术,磁共振波谱成像(MRS)通过比较不同代谢产物的相对表达水平,推断神经元细胞密度和完整性、细胞膜翻转、感兴趣区域的可能坏死以及可能存在的病理变化等关键信息[9]。与常规MRI、CT、血管造影术等可提供组织结构形态特征的影像学技术不同,MRS可提供神经元细胞密度和完整性、细胞壁增殖或退化、能量代谢、脑组织或肿瘤组织坏死性转变等非解剖学信息[10],在中风、癫痫、多发性硬化、痴呆、头部损伤等常见神经系统疾病鉴别中发挥了越来越重要的作用[11]。本研究主要评价MRS用于颅内占位性病变的诊断价值。
1 对象与方法 1.1 研究对象以2019—2022年在因颅内占位性疾病在新疆医科大学第一附属医院影像中心核磁共振室接受常规MRI后行MRS检查的病例作为研究对象,回顾性收集患者人口学特征。病例纳入标准:(1)患者因颅内占位性疾病就诊。(2)病例行常规MRI后接受MRS检查。(3)患者病历资料完整。(4)签署知情同意书,同意参与此研究。病例排除标准:(1)无颅内占位性病变。(2)未在常规MRI后接受MRS检查。(3)病历资料缺如。(4)不同意签署知情同意书。本研究获得新疆医科大学第一附属医院伦理委员会审批通过,患者均知情同意。
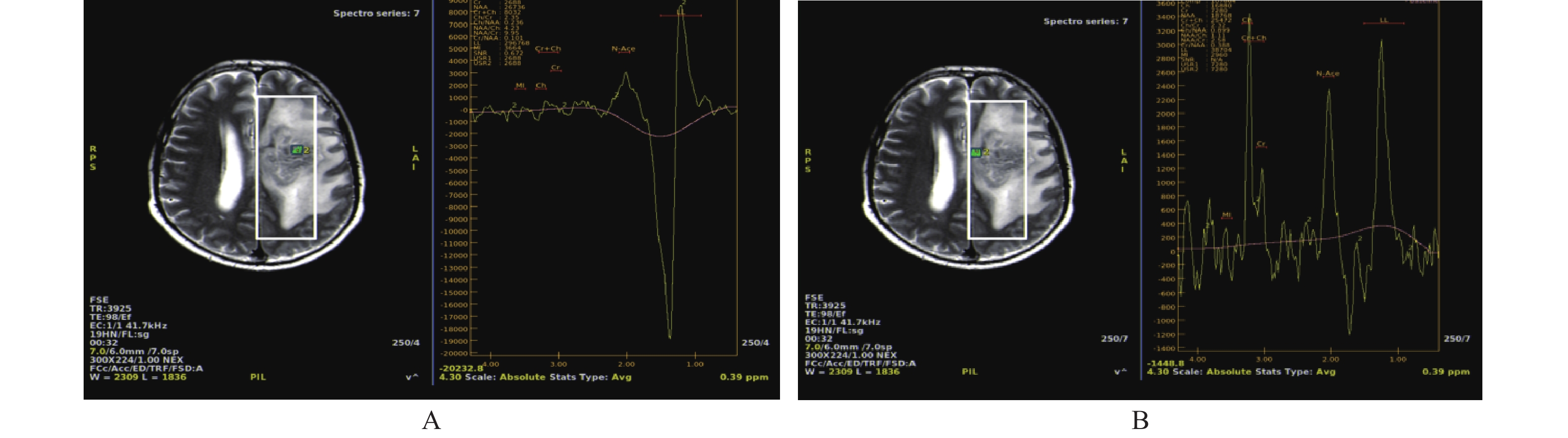
1.2 头颅MRS检查选择T2加权图像或钆增强T1加权轴图像进行体元定位,采用频率选择水抑制的双自旋回波定位技术获取水抑制单体元波谱图像。采用GE 3.0T磁共振成像仪进行常规头颅常规MRI和MRS检查,应用短回波时间为 31 ms、中等回波时间为144 ms的自动波谱序列进行MRS检查;根据病变大小,将2~8 mL的体元置于病变内。全部MRI和MRS检查均由同一组人完成,且由工作经验超过15年的同一位高年资神经影像学专家阅片;收集图像存储与传输系统(PACS)中的历史图像和报告用于分析影像和波谱特征(图1)。
|
图 1 头颅MRS图像 Figure 1 Brain MRS images 注:A左侧放射冠区占病变区域Cho峰升高、NAA峰降低,可见粗大乳酸峰;B 左侧额叶囊实性病灶Cho峰升高,NAA峰降低。 |
采用Microsoft Excel 2019建立数据库,应用SPSS 21.0软件进行统计学分析。组间率的比较采用χ2检验,P < 0.05为差异有统计学意义。
2 结 果 2.1 人口学特征共有126例符合纳入和排除标准的颅内占位性病变患者纳入本研究,其中男性64例(50.79%)、女性62例(49.21%);患者年龄最小6岁、最大89岁,平均(46.21±19.80)岁。
2.2 MRI检测结果如果影像学专家有1种以上鉴别诊断,即使存在2种明确鉴别诊断,也定义为非单一诊断。图2为根据患者临床病史及单独MRI检查作出的诊断结果,仅根据MRI检查难以得出单一确诊。

|
图 2 头颅MRI诊断颅内占位性病变结果 Figure 2 Intracranial space-occupying lesions diagnosed by brain MRI |
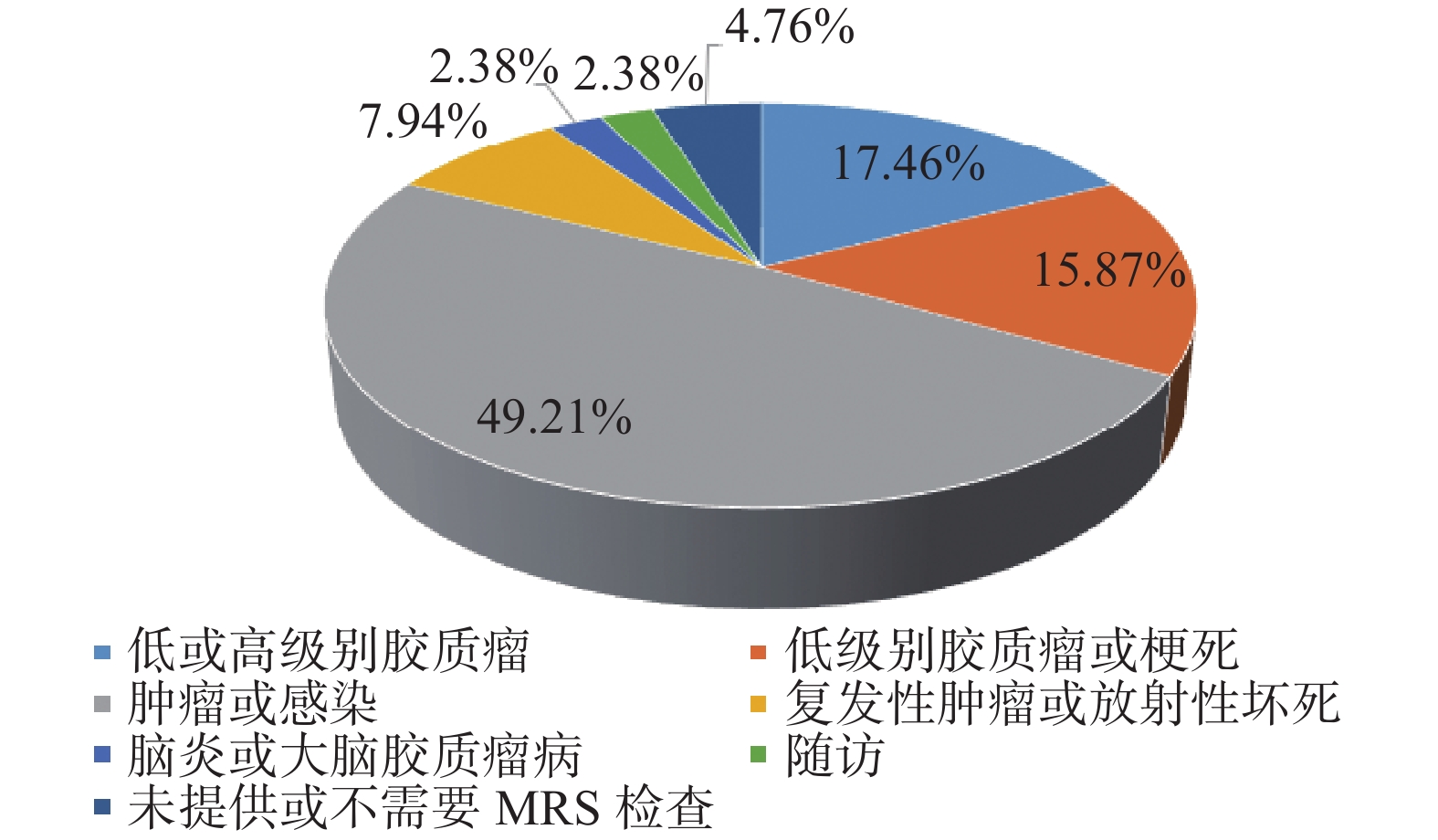
本研究中头颅MRS检查适应证见图3。头颅MRS检查最主要用于鉴别肿瘤和感染,其中96.77%用于鉴别结核瘤和多形性胶质母细胞瘤,另1例是鉴别HIV感染者原发性中枢神经系统淋巴瘤和弓形虫病。结核瘤是该组病例中最常见的感染性颅内占位性病变。值得注意的是,MRI单用或联用MRS均为检出颅内化脓性脓肿。
|
图 3 头颅MRS诊断颅内占位性病变适应证 Figure 3 Indications for brain MRS for diagnosis of intracranial space-occupying lesions |
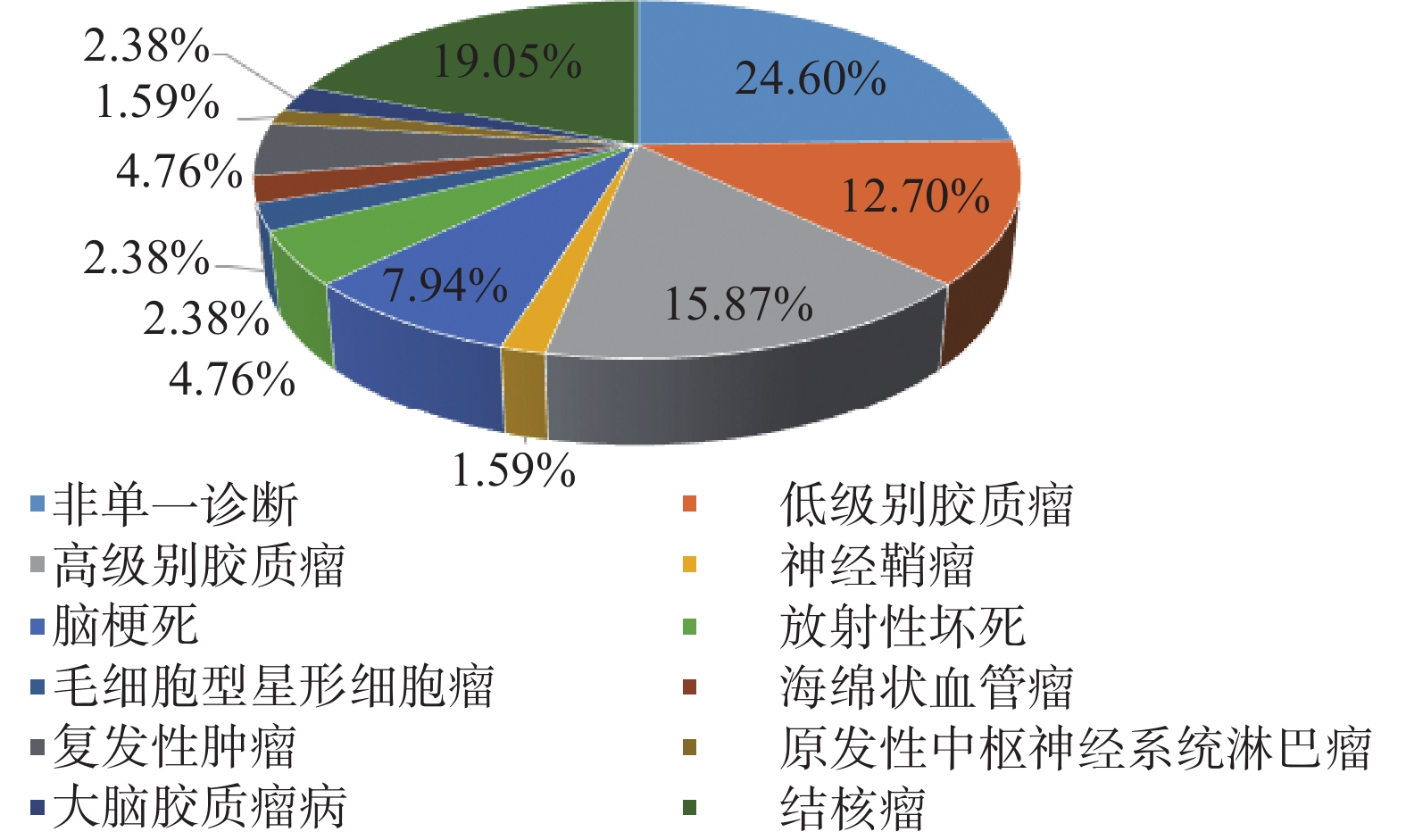
图4为MRI联用MRS诊断颅内占位性病变结果。如果存在1种以上鉴别诊断,定义为非单一诊断。MRI联用MRS诊断的最常见两种颅内占位性病变为结核瘤(19.05%)和高级别胶质瘤(15.87%)。单用MRI,影像学专家仅能对23.81%的颅内占位性病变患者作出影像学确诊;而联用MRI和MRS,影像学专家可对75.40%颅内占位性病变患者作出影像学确诊,提高了2.17倍(χ2 = 67.07,P < 0.01)。联用MRI和MRS较单用MRI提升了70例患者(55.67%)颅内占位性病变影像学诊断准确性;此外,联用MRI和MRS较单用MRI显著提升了影像学专家诊断高级别胶质瘤、低级别胶质瘤、脑梗死、结核瘤、复发性肿瘤和放射性坏死的准确性( P < 0.01)。
|
图 4 头颅MRI联用MRS诊断颅内占位性病变结果 Figure 4 Intracranial space-occupying lesions diagnosed by a combination of brain MRI and MRS |
MRS是利用MRI化学位移原理分析生物组织中代谢产物和分子成分的一种新型MRI功能显像技术,是目前唯一一种无创性观察活体组织代谢及生化变化的技术[12]。既往临床研究显示,MRS用于肝脏疾病[13-15]、前列腺癌诊断价值较高[16-18];此外,MRS对颅内感染[19]、癫痫[20]、脑胶质瘤[21]等脑部疾病均具有较高诊断效能。
基于常规MRI技术,有经验的神经影像学专家可以根据患者年龄、临床表现、病变位置、钙化灶、囊肿形成、对比度增强等影像学特征及临床资料对70%~90%的脑部病变作出准确判断;但如果仅仅根据这些特征,对其余10%~30%的脑部病变则难以鉴别缺血性病变、轴内和轴外脑瘤、高和低级别肿瘤、肿瘤性和非肿瘤性病灶等[22]。与常规MRI、CT、血管造影术等影像学技术不同,MRS可提供神经元细胞密度和完整性、细胞壁增殖或退化、能量代谢、脑组织或肿瘤组织坏死性转变等信息[10]。
本研究发现,MRI联用MRS较单用MRI提高颅内占位性病变影像学确诊率提高了2.17倍(P < 0.01),且联用MRI和MRS较单用MRI显著提升了影像学专家诊断高级别胶质瘤、低级别胶质瘤、脑梗死、结核瘤、复发性肿瘤和放射性坏死的准确性( P < 0.01)。多数接受脑MRS检查的颅内占位性病变患者年龄在41~50岁;而接受脑MRI检查的患者中,MRS主要用于鉴别结核瘤和高级别胶质瘤,两种疾病均以环状增强病灶为主要影像学特征。本研究发现,脑MRS检查的4种主要适应证包括鉴别低和高级别胶质瘤、鉴别颅内肿瘤和感染、鉴别低级别胶质瘤和脑梗死、鉴别复发性肿瘤和放射性坏死;MRI联用MRS较单用MRI提升了对4种适应证的影像学诊断效能,但差异无统计学意义,可能与样本量较小有关。本研究存在如下不足:(1)本研究为单中心回顾性研究。(2)样本量相对较小。(3)未纳入组织病理学证据。
综上所述,本研究结果表明,MRS联用MRI可以较MRI单用提高对颅内占位性病变的影像学诊断效能,适合作为颅内占位性病变的一种无创诊断工具,且有助于影像学专家鉴别低和高级别胶质瘤、高级别胶质瘤和结核瘤以及复发性肿瘤和放射性坏死。
| [1] |
Faraj CA, Snyder RI, McCutcheon IE. Intracranial emergencies in neurosurgical oncology: pathophysiology and clinical management[J]. Emerg Cancer Care, 2022, 1: 13. DOI:10.1186/s44201-022-00013-6 |
| [2] |
van den Bent MJ, Geurts M, French PJ, et al. Primary brain tumours in adults[J]. Lancet, 2023, 402(10412): 1564-1579. DOI:10.1016/S0140-6736(23)01054-1 |
| [3] |
Anon. Focusing on brain tumours and brain metastasis[J]. Nat Rev Cancer, 2020, 20(1): 1. DOI:10.1038/s41568-019-0232-7 |
| [4] |
Nguyen I, Urbanczyk K, Mtui E, et al. Intracranial CNS infections: A literature review and radiology case studies[J]. Semin Ultrasound CT MR, 2020, 41(1): 106-120. DOI:10.1053/j.sult.2019.09.003 |
| [5] |
Walker MD, Zunt JR. Neuroparasitic infections: cestodes, trematodes, and protozoans[J]. Semin Neurol, 2005, 25(3): 262-277. DOI:10.1055/s-2005-917663 |
| [6] |
Nassiri F, Chakravarthy A, Feng SR, et al. Detection and discrimination of intracranial tumors using plasma cell-free DNA methylomes[J]. Nat Med, 2020, 26(7): 1044-1047. DOI:10.1038/s41591-020-0932-2 |
| [7] |
Traboulsee A, Li DKB. Conventional MR imaging[J]. Neuroimaging Clin N Am, 2008, 18(4): 651-673. DOI:10.1016/j.nic.2008.07.001 |
| [8] |
Fink JR, Muzi M, Peck M, et al. Multimodality brain tumor imaging: MR imaging, PET, and PET/MR imaging[J]. J Nucl Med, 2015, 56(10): 1554-1561. DOI:10.2967/jnumed.113.131516 |
| [9] |
Manias KA, Peet A. What is MR spectroscopy?[J]. Arch Dis Child Educ Pract Ed, 2018, 103(4): 213-216. DOI:10.1136/archdischild-2017-312839 |
| [10] |
Tognarelli JM, Dawood M, Shariff MIF, et al. Magnetic resonance spectroscopy: Principles and techniques: Lessons for clinicians[J]. J Clin Exp Hepatol, 2015, 5(4): 320-328. DOI:10.1016/j.jceh.2015.10.006 |
| [11] |
Tran T, Ross B, Lin A. Magnetic resonance spectroscopy in neurological diagnosis[J]. Neurol Clin, 2009, 27(1): 21-60. DOI:10.1016/j.ncl.2008.09.007 |
| [12] |
Rhodes CJ. Magnetic resonance spectroscopy[J]. Sci Prog, 2017, 100(3): 241-292. DOI:10.3184/003685017X14993478654307 |
| [13] |
柏圣还. 探讨磁共振波谱成像在肝硬化诊断与分期中的价值[J]. 中外医疗, 2016, 35(8): 185-186. Bai SH. Study on value of magnetic resonance spectrum imaging in diagnosis and staging of cirrhosis[J]. China Foreign Med Treat, 2016, 35(8): 185-186. DOI:10.16662/j.cnki.1674-0742.2016.08.185 |
| [14] |
陈惠, 冷桂香, 谢春. 磁共振波谱成像对脂肪肝诊断的价值研究[J]. 当代医学, 2017, 23(35): 85-86. Chen H, Leng GX, Xie C. Value of magnetic resonance spectroscopy for diagnosis of fatty liver[J]. Contemp Med, 2017, 23(35): 85-86. DOI:10.3969/j.issn.1009-4393.2017.35.035 |
| [15] |
刘小玲, 阮君, 朱敬松. 磁共振波谱成像检测肝内脂肪浸润水平诊断非酒精性脂肪肝的价值[J]. 肝脏, 2021, 26(3): 305-308. Liu XL, Ruan J, Zhu JS. Value analysis of intrahepatic fat infiltration level detected by magnetic resonance spectroscopy in diagnosis of nonalcoholic fatty liver disease[J]. Chin Hepatol, 2021, 26(3): 305-308. DOI:10.3969/j.issn.1008-1704.2021.03.025 |
| [16] |
郭瑾. 磁共振波谱成像对前列腺癌的诊断价值[J]. 临床医学, 2020, 40(8): 43-44. Guo J. Diagnostic value of magnetic resonance spectroscopy for prostate cancer[J]. Clin Med, 2020, 40(8): 43-44. DOI:10.19528/j.issn.1003-3548.2020.08.015 |
| [17] |
李宝林. 磁共振波谱成像检查对前列腺癌的诊断价值探讨[J]. 中国实用医药, 2021, 16(32): 22-24. Li BL. The diagnostic value of magnetic resonance spectroscopy for prostate cancer[J]. China Pract Med, 2021, 16(32): 22-24. DOI:10.14163/j.cnki.11-5547/r.2021.32.007 |
| [18] |
夏金翔, 张继. 磁共振波谱成像在前列腺癌诊断中的应用价值[J]. 影像研究与医学应用, 2019, 3(7): 71-72. Xia JX, Zhang J. The diagnostic value of magnetic resonance spectroscopy for prostate cancer[J]. J Imag Res Med Appl, 2019, 3(7): 71-72. DOI:10.3969/j.issn.2096-3807.2019.07.047 |
| [19] |
叶浩翊, 伍志华, 刘志锋. 颅内感染的磁共振波谱成像研究进展[J]. 中国医疗设备, 2022, 37(8): 12-16. Ye HX, Wu ZH, Liu ZF. Advances in magnetic resonance spectroscopy of intracranial infections[J]. Chin Med Dev, 2022, 37(8): 12-16. DOI:10.3969/j.issn.1674-1633.2022.08.003 |
| [20] |
陈晓华, 梁莎, 梁玄菁, 等. 磁共振波谱成像技术在儿童癫痫中的应用研究[J]. 影像研究与医学应用, 2023, 7(6): 84-86. Chen XH, Liang S, Liang XJ, et al. Application of magnetic resonance spectroscopy for diagnosis of pediatric epilepsy[J]. J Imag Res Med Appl, 2023, 7(6): 84-86. DOI:10.3969/j.issn.2096-3807.2023.06.027 |
| [21] |
庞瑜丹, 张玮, 胡喆. 磁共振波谱成像检查对脑胶质瘤的诊断价值[J]. 癌症进展, 2022, 20(24): 2527-2529,2533. Pang YD, Zhang W, Hu Z. Diagnostic value of magnetic resonance spectroscopy in glioma[J]. Oncol Prog, 2022, 20(24): 2527-2529,2533. DOI:10.11877/j.issn.1672-1535.2022.20.24.12 |
| [22] |
Stanescu T, Jans HS, Pervez N, et al. A study on the magnetic resonance imaging (MRI)-based radiation treatment planning of intracranial lesions[J]. Phys Med Biol, 2008, 53(13): 3579-3593. DOI:10.1088/0031-9155/53/13/013 |




