放射性核素210Pb广泛存在于周围环境中,通过吸入、食入等方式或经皮肤、伤口接触等进入人体内,其中食入是210Pb进入人体内的主要途径,对人体造成内照射危害。水中210Pb和210Po通过直接饮用和食物链两种方式进入人体,产生的有效剂量占天然辐射照射所致有效剂量的比例达到80%以上,同时,210Pb的子体210Po属于高放射性、高化学毒性的放射性元素,若进入人体内,会造成内照射伤害,引起中毒或急性放射疾病,这些都引起社会的广泛关注[1-6]。因此,了解环境水体中210Pb的放射性水平,分析环境水样中放射性核素210Pb的活度浓度是十分必要的。
目前行业中现行分析环境水中的210Pb的监测方法是1994年10月24日发布的《水中铅-210的分析方法》[7]与《环境水中210Pb核素放射性活度的快速分析方法》[8]。两者的测量原理均是通过测量210Pb的子体210Bi的β射线的放射性,获得210Pb的活度浓度,测量周期均是一个月。但是前者的缺点是无法确定210Bi的回收率,实验的精密度较差,不利于及时分析环境样品中210Pb的活度浓度。后者的方法依据是《Standard Test Method for Lead-210 in water》(《水中210Pb的标准测试方法》)[9],美国材料与实验协会标准,编号为(D7535-2009),该方法可以通过确定整个分析过程的Pb的化学回收率,提高实验分析的准确度,弥补了前者的不足。
《环境水中210Pb核素放射性活度的快速分析方法》采用强碱性阴离子交换树脂分离Pb,随着新型材料的研发,快速有效分离纯化Pb成为可能,特别是锶(Sr)树脂。本文研究利用新型材料锶(Sr)树脂分析测量地表水中的210Pb,并与强碱性阴离子交换树脂方法进行对比。
1 实验试剂与仪器设备 1.1 实验试剂高锰酸钾溶液、过氧化氢、盐酸、硝酸、氨水、硫酸、饱和硫酸钠溶液、无水乙醇、氨水(NH3·H2O)、Pb载体(含量为10 mgPb/mL)、Fe载体(含量为20 mgFe/mL)、柠檬酸铵溶液(0.05 mol/L)、碳酸铵固体、210Pb-210Bi平衡标液(Eckert & Ziegler Analytics生产)、闪烁液(Ultima GoldTM AB,PerkinElmer Inc.生产)、抗坏血酸溶液(1 mol/L)等,除特别说明外,制样时均使用分析纯试剂,水为去离子水。
1.2 仪器设备BH1227型低本底测量仪(北京中核核仪器厂)、电子天平(北京赛多利斯科学仪器有限公司)。
2 实验步骤 2.1 Sr树脂色层柱分离纯化Pb步骤① 加入铅载体,用于确定Pb的化学回收率。量取5 L样品(pH值为2),加入20 mg铅载体,边搅拌边滴加高锰酸钾溶液,直至呈现浅红色。②富集水中Pb。加入100 mg铁载体,滴加氨水,直至pH值为8.5~9.2,吸附载带水中的210Pb和稳定铅,用10 mL 2.0 mol/L HCl盐酸溶解沉淀,10 mL 2.0 mol/L HCl盐酸清洗滤纸,清洗液合并入烧杯中。③分离纯化Pb。分离纯化Pb的步骤[10]具体操作如下:首先预处理Sr树脂色层柱:使用10 mL 2 mol/L HCl对Sr树脂色层柱进行预处理,使得树脂床的环境为2 mol/L HCl;预处理结束后,向Sr树脂色层柱中倒入上述溶解液,通过重力作用流过色层柱;溶解液过柱完毕后,向色层柱中加入10 mL 2 mol/L HCl,分离溶解液中210Bi;然后依次加入10 mL 1 mol/L HNO3、20mL 0.1mol/L HNO3,分离溶解液中的210Po;最后向色层柱中加入20 mL 0.05 mol/L柠檬酸铵溶液,洗涤210Pb,保留流出液。向上述流出液中加入(NH4)2CO3固体,生成PbCO3沉淀。④确定Pb化学回收率。用差重法计算化学回收率。⑤测量。样品放置一个月后,在BH1227型低本底测量仪进行测量。
2.2 强碱性阴离子交换树脂分离纯化Pb步骤富集水中Pb、确定Pb化学回收率与测量步骤同2.1。水样中的Pb富集后,用10 mL 1.5 mol/L HCl盐酸溶解沉淀,10 mL 1.0 mol/L HCl盐酸清洗滤纸,清洗液合并入烧杯中。将上述溶解液交换柱储液池中,用少量1.0 mol/L HCl清洗烧杯,控制过柱速度为15~20 s每滴。溶液流过玻璃纤维至树脂界面后加入40 mL 1.0 mol/L HCl继续过柱,待溶液流过玻璃纤维至树脂界面后再加入100mL 1.0mol/L HCl继续过柱。当溶液流过玻璃纤维至树脂界面后加入10mL去离子水继续过柱。当溶液流过玻璃纤维至树脂界面后加入70 mL去离子水,用100 mL烧杯接洗脱液,继续过柱直至树脂中水全部流出。将洗脱液至于电热板上直接加热蒸发至近干后,换用水浴蒸发的方式继续加热直至溶液全部蒸干。加入20 mL去离子水在水浴中溶解,冷却后加入两滴2.0 mol/L H2SO4,再加入1mL饱和硫酸钠,充分搅拌2 min以上,直至出现大量白色沉淀。沉淀采用可拆卸式漏斗抽滤,依次用去离子水和无水乙醇洗涤,沉淀在45℃烘箱中烘1 h以上。
3 仪器效率刻度 3.1 Sr树脂色层柱分离纯化Pb仪器效率刻度步骤取2个100 mL烧杯,分别加入20 mg稳定铅载体、放射性活度约为17.70 Bq的210Pb-210Bi平衡标液和20 mL 2.0 mol/L HCl,充分搅拌。Sr树脂色层柱分离纯化Pb步骤同2.1。
3.2 强碱性阴离子交换树脂分离纯化Pb的仪器效率刻度步骤取2个100 mL烧杯,分别加入20 mg稳定铅载体、放射性活度约为17.70 Bq的210Pb-210Bi平衡标液和20 mL 1.0 mol/L HCl,充分搅拌。强碱性阴离子交换树脂分离纯化Pb步骤同2.2。
4 实验结果与讨论 4.1 数据处理化学回收率计算公式如下:
| $ {R_Y} = \frac{{{m_s}}}{{{m_0}}} $ | 1) |
式中,RY为化学回收率,ms为样品源中铅的质量,g;m0为加入的铅载体的质量,g。
仪器探测效率的计算公式为:
| $ E = \frac{N}{{KY{A_0}}} $ | 2) |
式中,E为210Bi的探测效率,%;N为样品源净计数率,min-1;K为转换系数,当A以Bq/L表示时,K为60计数/(min·Bq);Y为铅的回收率,%;A0为加入的210Pb活度,Bq。
水中210Pb活度浓度计算公式如下:
| $ A = \frac{N}{{KEV{R_Y}}} $ | 3) |
式中,A为水中210Pb活度浓度,Bq/L;N为样品源净计数率,min-1;K为转换系数,当A以Bq/L表示时,K为60计数/(min·Bq);E为仪器的探测效率,%;V为取样体积,L;RY为铅的回收率,%。
4.2 数据处理结果本次研究所用水样为安徽省局部区域地表水。分析方式为样品测量与加标测量。实验分析中,取样体积均为5 L,铅载体加入量均为20 mg,铁载体加入量均为100 mg,样品测量时间均为25 h。环境地表水样中210Pb活度浓度分析结果见表 1。加标样品回收率结果见表 2。
|
|
表 1 环境水样(地表水)中210Pb活度浓度分析结果 |
|
|
表 2 加标样品测量结果 |
表 1中,Sr树脂与强碱性阴离子交换树脂分离纯化Pb的化学回收率范围分别为84.13%~95.48%、45.24%~81.99%。表 2中,Sr树脂与强碱性阴离子交换树脂分析加标样品的化学回收率范围分别为92.47%~94.11%、65.78%~71.25%。Sr树脂分离纯化的9个样品的化学回收率全部在80%以上,其中6个样品的回收率在90%以上;强碱性阴离子交换树脂分离纯化处理的7个样品中,1个样品的回收率在50%以下,1个样品的回收率在80%以上,其余7个样品的回收率在60%~80%之间。由此可见,在同等的210Pb放射性活度水平的样品处理中,采用Sr树脂分离纯化Pb的化学回收率较高,并且稳定性较好。
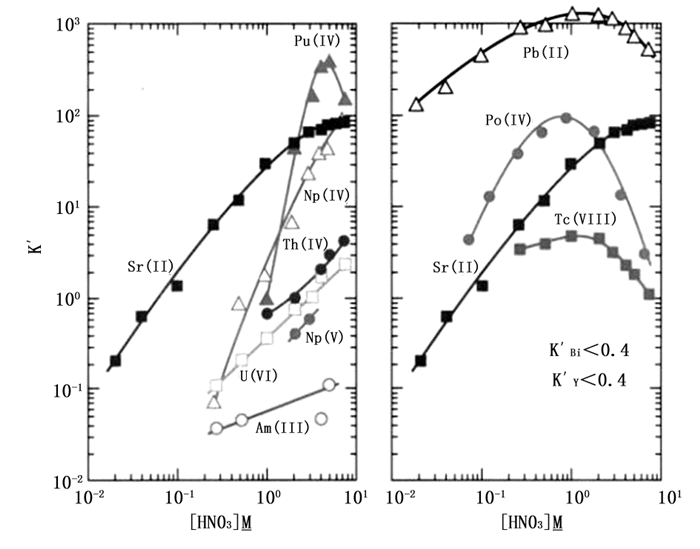
根据厂家提供的产品说明可知,Sr树脂为溶于辛醇的dicyclo-hexano-18 crown-6衍生物,在不同的硝酸浓度下,对不同的金属离子吸附能力不同。具体情况见下图。Sr树脂对Pb的吸附能力较强。在使用20 mL 0.05 mol/L柠檬酸铵溶液洗提210Pb后,从理论上可获得较高的化学回收率。
强碱性阴离子交换树脂为201 ×7季铵Ⅰ型苯乙烯,交换容量(干)≥3.0 mol/kg。共沉淀富集210Pb,用盐酸溶解后,大部分以络阴离子PbCl3-、PbCl42-的形式存在。阴离子交换树脂对PbCl3-、PbCl42-进行交换。
|
图 1 不同硝酸浓度下Sr树脂对不同金属离子的吸附能力图 |
采用强碱性阴离子交换树脂分离Pb时,需要严格控制液体过柱速度与溶液体积,尤其是临届点时的过柱速度的调试,对实验人员的操作要求较高。如若实验人员没有控制好实验条件,把握好实验操作,皆有可能造成Pb的化学回收率降低,稳定性较差。而采用Sr树脂分离Pb,对过柱速度没有严格要求,便于操作,从而使Pb的化学回收率趋于稳定。
从实验分析时间上看,通常情况下,Sr树脂分离Pb的过柱溶液体积共为80 mL,通过重力作用流过色层柱,需要1天;强碱性阴离子交换树脂分离Pb的过柱溶液体积共为240 mL,同时需要控制过柱速度,需要3天。由此可知,前者分离所需时间是后者所需时间的三分之一。
5 结论通过采用锶(Sr)树脂对环境水样中的Pb核素进行分离实验研究,根据实验结果可知,采用新型材料Sr树脂分离Pb,相对于强碱性阴离子交换树脂分离Pb,具有化学回收率较高、稳定性较好、实验分析周期短等特点。但是,新型材料Sr树脂市场价格昂贵,不利于大批量的样品处理。
| [1] |
陈秀云, 翁德通, 杨孝桐. 福建食品和水中210Pb与210Po放射性含量及其所致居民内照射剂量估算[J]. 中国辐射卫生, 1996, 5(4): 214-215. |
| [2] |
蒋衍. 辽宁省饮用水中铅-210和钋-210的含量及其所致居民内照射剂量的估算[J]. 中国辐射卫生, 1992, 1(1): 17-19. |
| [3] |
诸洪达, 王守亮, 孟玮, 等. 我国膳食中90Sr、137Cs、228Ra、226Ra、210Pb和210Po含量及其所致内照射剂量[J]. 辐射防护, 1993, 2(3): 85-92. |
| [4] |
陆梅. 我国参考人主要放射性核素膳食摄入量及其所致内照射剂量的现状[J]. 中国辐射卫生, 1999, 8(2): 120-123. |
| [5] |
Environmental Protection Agency.National Primary Drinking Water Regulations、Radionuclides、Notice of Data Availability[R].2000, Proposed Rule, 40 CFR Parts 21;141-142.
|
| [6] |
Khater EA.210Pb in marine sediment[R].5th international Conference on High Levels of Natural Radiation and Radon Areas.2002, Radiation Dose and Health Effects, Munich, 4-7.
|
| [7] |
中华人民共和国核行业标准.EJ/T 859-94.水中铅-210的分析方法[S].北京: 中国标准出版社, 1994.
|
| [8] |
黄展常. 环境水中210Pb核素放射性活度的快速分析方法[J]. 核技术, 2013, 07: 49-56. |
| [9] |
American Society for Testing and Materials Standards.D7535.Standard Test Method for Lead-210 in water[S].2009.
|
| [10] |
BSI Standards Publication. Water quality-Lead-210-Test method using liquid scintillation counting[S].2013, BS ISO 13163.
|




