副脾是脾脏常见的先天性变异,80%位于脾门,17%位于胰尾[1-2]。胰腺内副脾通常小于3 cm,且常被偶然发现。对于胰腺内副脾(intrapancreatic accessory spleen, IPAS)的主要临床意义在于与其他胰腺肿瘤鉴别,如神经内分泌肿瘤、实性假乳头状瘤、富血供转移瘤等,进而避免不必要的手术[3-5]。因此,对胰腺内副脾的准确诊断比较重要。
1 资料与方法 1.1 研究对象收集2011年1月至2015年12月间发现并于我院临床或核医学证实的IPAS患者5例。男性3例,女性2例,年龄36~55岁,中位年龄44.6岁。5例中1例因腹痛入院,4例为常规体检发现,无明显不适,实验室检查未见明确异常。5例均经临床或核医学脾显像证实。
1.2 仪器与方法使用西门子3.0TVerio机,梯度磁场为45 mT/m,最大梯度切换率200 mT/(m/ms),32射频通道平台,16通道体部线圈。检查序列:轴位作为基础位,包括T2WI、T1WI(同反相位)平扫、DWI(b=0、150、1000)、4期动态增强扫描,层厚为5 mm,间隔为1mm,矩阵100×100。对比剂为Gd-DTPA,用量为0.025 mmol/kg体重,双注射速率为2 ml/s,动脉期扫描时间为注射对比剂后14~35 s,门脉期为60 s,延迟期为3分钟。
2 结果 2.1 影像表现5例胰腺内副脾均位于胰尾部,表现为胰尾类圆形肿物,边缘光滑锐利,直径范围为1.3~3.2cm,邻近胰腺组织呈受压改变。与胰腺实质相比,平扫时肿物于T1WI(同反相位)呈稍低信号,T2WI(压脂或非压脂)呈稍高信号,DWI呈稍高信号,ADC图呈低信号,信号表现与脾脏实质几乎一致。动态增强扫描各期的信号表现与脾脏同步。尤其在增强扫描的动脉后期与脾脏同步表现为“花脾”的特征见图 1。
|
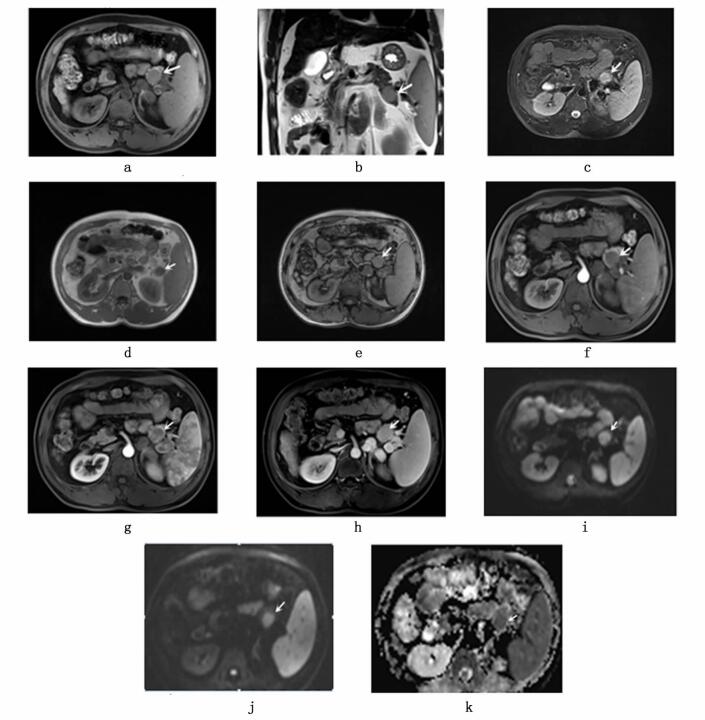
图 1 胰腺副脾MRI影像图 注:a:T1压脂示低于胰腺的胰尾肿块,其信号同脾脏(箭); b:T2WI冠状示略高于胰腺的胰尾区肿块,其信号同脾脏(箭); c:T2WI压脂示低于胰腺的胰尾区肿块,其信号同脾脏(箭); d:T1WI同相位示胰尾区肿块,其信号同脾脏(箭); e:T1WI反相位示胰尾区肿块,其信号同脾脏(箭); f:动脉早期胰尾区肿块,其信号同脾脏(箭); g:动脉后期示胰尾区肿块,其信号同脾脏“花脾”(箭); h:门静脉期示胰尾区肿块,其信号同脾脏(箭); i:低b值DWI示胰尾区肿块,其信号同脾脏(箭); j:高b值DWI示胰尾区肿块,其信号同脾脏(箭); k:ADC图示胰尾区肿块,其信号同脾脏(箭)。 |
5位患者均进行临床随访或核医学脾显像证实,胰尾部结节为脾脏组织。
3 讨论副脾是一种先天性异位脾组织,是由于胚胎第5周位于胃背系膜中的脾原基融合失败所致[6]。副脾最常发生于脾门,其次是胰尾,也可发生于肠系膜、大网膜、脾韧带、女性附件等部位。胰腺内副脾通常无阳性体征且不需要手术及活检。因此准确诊断副脾并与其他胰腺实性富血供肿瘤鉴别是至关重要的。
副脾可以通过多种影像学方法进行诊断,如超声造影、增强CT、超顺磁性氧化铁增强MRI以及99mTc胶体核素显像。以上检查都是通过静脉注射对比剂或巨噬细胞对放射性核素标记的胶体吞噬作用并特异聚集在脾脏组织内。尽管这些检查均有较好的敏感性和特异性,但是胶体核素显像主要依靠巨噬细胞对放射性核素标记的胶体特异性吞噬作用,而且核医学显像空间分辨率低于CT及MRI,如果病灶过小或功能较低,则难以达到满意的显像效果;超声造影则主要依赖于操作者水平;CT则需要应用含碘的造影剂。相比较而言,MRI应用简便,不需要特殊对比剂,且能应用多种序列进行观察, 从而达到诊断目的[7-9]。
IPAS的MRI影像学表现主要有以下几个方面:①IPAS大多位于胰尾部,其他部位十分少见,本组病例病灶均位于胰尾部。②IPAS通常体积较小,大多小于3cm,多呈类圆形,边界清晰,且多为单发。③IPAS与胰腺实质相对比,平扫T1WI呈稍低信号,T2WI呈稍高信号,DWI表现则与脾脏实质相似,表现为较高的信号,不同b值信号与脾脏信号一致。增强扫描各期IPAS强化程度均与脾脏实质相近。本组病例表现与以上均相符。我们的体会是,双动脉期及多组b值DWI技术更具有定性价值,前者在于显示“花脾”,而后者用于IPAS和脾脏的不同b值图像的比对。对此,3.0TMR设备更具有优势。
IPAS需要与胰腺富血供实性肿瘤鉴别,如原发或转移性神经内分泌肿瘤,实性假乳头状瘤等。当此类肿瘤体积较小、无明显囊变坏死时,平扫T1、T2WI及增强扫描表现可与IPAS十分相近,有时难以区分,此时可以应用MRI的DWI序列,虽然均可表现为扩散受限,但文献报道[10],在多组b值上测量ADC值,IPAS灶与脾脏相近,而其他肿瘤则与脾脏的ADC值会有差别。其他方面,功能性神经内分泌肿瘤多有临床症状,无功能性神经内分泌肿瘤体积多较大;实性假乳头状瘤多见于青中年女性,多发生在胰头颈部,发生坏死囊变几率较高。
因此,IPAS具有特征性MRI表现,通过对平扫T1、T2WI、多组b值DWI及动态增强扫描图像观察,能够与胰腺其他肿瘤相鉴别,可准确诊断胰腺内异位副脾,避免不必要的手术创伤。
| [1] |
Dodds WJ, Taylor AJ, Erickson SJ, et al. Radiologic imaging of splenic anomalies[J]. AJR Am J Roentgenol, 1990, 155(4): 805-810. DOI:10.2214/ajr.155.4.2119113 |
| [2] |
Halpert B, Gyorkey F. Lesions observed in accessory spleens of 311 patients[J]. Am J Clin Pathol, 1959, 32(2): 165-168. DOI:10.1093/ajcp/32.2.165 |
| [3] |
Gayer G, Zissin R, Apter S, et al. CT findings in congenital anomalies of the spleen[J]. Br J Radiol, 2001, 74(884): 767-772. DOI:10.1259/bjr.74.884.740767 |
| [4] |
Harris GN, Kase DJ, Bradnock H, et al. Accessory spleen causing a mass in the tail of the pancreas:MR imaging findings[J]. AJR Am J Roentgenol, 1994, 163(5): 1120-1121. DOI:10.2214/ajr.163.5.7976887 |
| [5] |
Hamada T, Isaji S, Mizuno S, et al. Laparoscopic spleen-preserving pancreatic tail resection for an intrapancreatic accessory spleen mimicking a nonfunctioning endocrine tumor:report of a case[J]. Surg Today, 2004, 34(10): 878-881. |
| [6] |
Movitz D. Accessory spleens and experimental splenosis[J]. Chic Med Sch Q, 1967, 26(4): 183-187. |
| [7] |
Kim SH, Lee JM, Han JK, et al. Intrapancreatic accessory spleen:findings on MR Imaging, CT, US and scintigraphy, and the pathologic analysis[J]. Korean J Radiol, 2008, 9(2): 162-174. DOI:10.3348/kjr.2008.9.2.162 |
| [8] |
Kim SH, Lee JM, Han JK, et al. MDCT and superparamagnetic iron oxide (SPIO)-enhanced MR findings of intrapancreatic accessory spleen in seven patients[J]. Eur Radiol, 2006, 16(9): 1887-1897. DOI:10.1007/s00330-006-0193-6 |
| [9] |
Padhani AR, Liu G, Koh DM, et al. Diffusionweighted magnetic resonance imaging as a cancer biomarker:consensus and recommendations[J]. Neoplasia, 2009, 11(2): 102-125. DOI:10.1593/neo.81328 |
| [10] |
Jang KM1, Kim SH, Lee SJ, et al. Differentiation of an intrapancreatic accessory spleen from a small (< 3 cm) solid pancreatic tumor:value of diffusion-weighted MR imaging[J]. Radiology, 2013, 266(1): 159-167. DOI:10.1148/radiol.12112765 |


