2. 山东省医学科学院放射医学研究所;
3. 广饶县妇女儿童医院
腮腺是人体中最大的涎腺组织, 其肿瘤发生率约占全身肿瘤的3%[1]。2005年世界卫生组织(WHO)把腮腺肿瘤分为40多种病理类型, 腮腺基底细胞腺瘤(basal cell adenoma, BCA)虽然是一种少见的良性上皮细胞肿瘤, 约占腮腺良性肿瘤的1%~3%, 远低于常见的多形性腺瘤和Wathin瘤[2], 但是流行病学调查显示近几年腮腺BCA的发生率呈逐年上升趋势, 而且最近几年的研究报道, 腮腺基底细胞腺瘤有4%的恶变率[3], 因此如何准确的诊断腮腺BCA, 对其临床治疗和预后评估具有重要的意义。查阅近年的文献资料, 腮腺BCA的诊断主要靠CT、MRI的常规加动态增强扫描以及DWI, 鉴别诊断困难, 容易误诊[4]。本研究在上述诊断方法的基础上, 测定肿瘤ADC值及分析其时间-信号强度曲线(TIC)的特征, 以期提高其影像诊断的准确率。
1 材料与方法 1.1 一般资料收集我院2012年5月到2015年12月之间经穿刺活检或手术病理证实的17例腮腺基底细胞腺瘤, 临床表现为腮腺区无痛性肿块, 或腮腺区肿物伴局部疼痛、不适; 病程2个月~7年。专科检查:肿块呈类圆形, 质地软, 边界清, 活动度好, 与周围皮肤无粘连。所有患者均行MRI常规扫描及动态增强扫描。同时收集经我院病理证实的23例多形性腺瘤及21例腺淋巴瘤, 并测量病变的ADC值及动态增强曲线。
1.2 仪器与方法采用Siemens Trio 3.0T超高场磁共振仪, 头颈16通道线圈及相关分析软件包, 常规MR扫描结束后行动态增强扫描。扫描部位包括颌颈部横轴位及冠状位T1WI、T2WI脂肪抑制序列; 扫描参数:T1WI:TR 685 ms, TE 24 ms, 矩阵320 × 240, 轴位扫描时间1 min46sec; 冠状位T2WI-STIR (短时反转恢复STIR):TR 3350 ms, TE 35 ms, 矩阵256 × 192, 扫描时间2 min40sec; 横轴位T2WI-FS (频率选择饱和法Fat Sat):TR 5360ms, TE 77 ms, 矩阵320 × 240, 扫描时间1 min45sec。视野(FOV)24 cm × 24 cm, 层厚3 mm, 间隔0.3 mm, 激励次数4次。DWI采用单次激发自旋回波EPI (SS-SE-EPI)序列, 扫描参数:TR 4100 ms, TE95 ms, 激励次数4, 矩阵192 × 173, 层厚与常规扫描保持一致, 在X, Y, Z三个方向上施加扩散梯度, 扩散敏感系数(b值)为0 s/mm2及1000 s/mm2, 扫描时间1 min44sec。增强扫描采用FSE-T1WI序列加脂肪抑制技术, 使用高压注射器经肘正中静脉团注Gd-DTPA, 剂量0.2 mmol/kg, 速率2.5 ml/s, 注射药物之前先平扫一期, 动态增强扫描结束之后行横轴位、冠状位、矢状位的延迟扫描。
1.3 ADC值数据的测量及分析利用上海柯达PACS工作站软件对所有肿瘤的实质部分测量ADC值, 每个肿瘤选择三个最佳层面, 然后取其平均数值; 利用SPSS 22.0统计学软件进行统计学分析。
1.4 MRI动态增强曲线的测量将动态增强扫描的原始图像导入Siemens工作站, 利用其自带的软件进行图像的后处理, 感兴趣区要避开肿瘤的囊变区, 得到其时间-信号强度曲线。
2 结果 2.1 临床与病理表现17位患者女性多见, 女性13例, 男性4例, 男女之比为1:3.25, 发病年龄36~68岁, 平均年龄55.2岁, 其中50岁以上12例, 占70.6%;临床症状多为腮腺区无痛性肿块, 或腮腺区肿物伴局部疼痛、不适, 病程2个月~5年, 近期生长加速来就诊。触诊肿瘤质地软, 边界清, 活动度好, 与周围皮肤无粘连; 均为单发肿瘤, 其中左侧8例, 占47.06%, 右侧9例, 占52.94%。基底细胞腺瘤巨检标本呈类圆形或椭圆形, 直径6~36 mm, 平均(2.57 ± 0.64) mm, 边界清楚, 17例病例均有纤维包膜, 与周围软组织无粘连, 肿瘤切面呈灰白色, 质地中等, 2例无明显囊变, 7例有裂隙样或斑点状小囊变, 8例为大囊变, 囊变病灶占88.2%, 囊变区内含有褐色黏液样物质; 光镜下瘤体主要由小基底样细胞组成, 排列方式多样, 可呈小梁状、小管状或者实性, 周边细胞呈栅栏状排列, 肿瘤内部小静脉及内皮毛细血管较丰富。
2.2 MRI表现2例病灶无囊变, 信号均匀, T1WI呈稍低信号、T2WI呈稍高信号; 7例病灶内部见裂隙样或点状小囊变区, 8例病灶内部见大囊变区, 病灶T1WI呈低信号, T2WI实性部分呈稍高信号, 囊变区则呈明显高信号; 动态增强扫描肿瘤实性部分动脉期快速明显强化, 静脉期持续强化, 随时间延长强化程度有所下降, 15例病灶时间-信号曲线均呈快速强化、缓慢廓清型, 2例病灶呈快速强化、快速廓清型, 病灶囊性部分无明显强化。
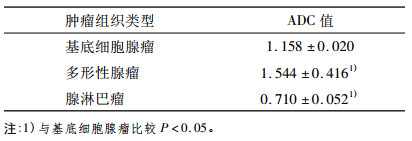
2.3 DWI及ADC值17例病灶DWI (b=1000 s/mm2)均弥散受限表现为不同程度的高信号, 测量所有病灶的ADC值范围为(0.830~1.604)× 10-3 mm 2/s, 平均值(1.156 ± 0.120)× 10-3mm2/s。
3 讨论 3.1 临床表现与病理改变基底细胞腺瘤(BCA)是一种少见的良性上皮源性肿瘤, 1976年由Kleinsasser和Klein首次报道[5], WHO在1991年定义其为单形性腺瘤的一个特殊亚型[6], 80%发生在腮腺。BCA临床症状不典型, 多数以耳垂后缘的无痛性肿物数年近期逐渐增大或腮腺区肿物伴局部疼痛不适来诊, 且以老年女性多见, 本组17例患者中女性13例, 占76.5%, 平均发病年龄(55.2 ± 8.7)岁, 50岁以上患者有12例, 占70.6%, 这与文献报道[7-8]基本一致。基底细胞腺瘤主要有两种瘤细胞构成, 一种瘤细胞体积小, 圆形及立方形, 胞质少, 核圆形, 染色深; 另一种瘤细胞体积大, 多边形或梭型, 胞质丰富, 染色淡, 核圆形及卵圆形。腮腺BCA病理上分为四种类型:梁状型、管状型、实性型和膜性型, 以实性型(约为60%)多见[9]。
3.2 MRI特征腮腺BCA多呈稍长T1、等或稍长T2信号, 这与多形性腺瘤及腺淋巴瘤有时很难鉴别; 由于BCA间质内含有丰富的毛细血管和小静脉, 因而易发生囊变, 文献[7]报道56.8%可发生囊变, 本组囊变病例占88.2%, 高于文献数据, 可能和收集的病例数目相对不足有关; 腮腺BCA的直径一般 < 3 cm, 本组病例直径6~36 mm, 平均(2.57 ± 0.64) mm, 文献报道[4]基本一致。
3.4 ADC值分析及意义文献报道[1]MR-DWI能够反映出组织中水分子弥散情况, 水分子的弥散成度会受到周围组织结构的影响, 因而ADC值的大小可以间接反映肿瘤细胞的密度及水分子弥散受限情况, 不同的肿瘤组织结构不同, 相应的ADC值也会不同, 因此可以根据肿瘤组织的ADC值来推测其可能的病理类型; 本组病例ADC值范围(0.830~1.604)× 10-3 mm 2/s, 平均值(1.156 ± 0.120)× 10-3 mm2/s, 分别与多形性腺瘤及腺淋巴瘤比较(见表 1), 差异有统计学意义, 这与文献报道一致[1]; 个别病灶的ADC值与平均值有些偏差, 原因可能和病灶的感兴趣区的选择及其囊变程度有一定的关系。
|
|
表 1 不同肿瘤组织的ADC值 |
动态增强扫描时间-信号曲线在一定程度上能够反映组织的良恶性, Yabuuchi[10]等人把其分为四个类型:A型:渐进性强化; B型:快速强化, 快速廓清; C型:快速强化, 缓慢廓清; D型:平台型, 提示病变无强化或囊性病变。BCA因为具有丰富的毛细血管, 所以实性部分动脉期明显强化, 静脉期持续强化, 但是强化幅度有不同程度减低, 本组病例15例为C型曲线, 2例为B型曲线, 这与多形性腺瘤(A型曲线)容易鉴别, 但有时与腺淋巴瘤(B型曲线)会有重叠, 这与文献报道[11-12]基本符合, 当TIC重叠时, 可以通过ADC值加以鉴别。
3.6 鉴别诊断① 多形性腺瘤:是腮腺中最常见的良性肿瘤, 女性多见, 可发生于任何年龄段, 平均发病年龄40岁左右, 比BCA略小, 肿瘤直径可> 3 cm, 内部含有丰富的黏液软骨基质, T2WI信号高于BCA, 囊变较BCA少见, 其ADC均值一般高于BCA, 增强扫描动脉期快速强化, 静脉期持续强化, TIC呈渐进性强化(A型), 不同于腮腺BCA, 延迟期强化程度低于BCA。②腺淋巴瘤:发病率仅次于多形性腺瘤, 好发于50岁以上中老年男性, 与长期吸烟有一定关系, 临床可有消长史, 好发部位是腮腺下后象限, 可多发, T1WI及T2WI呈中等信号, T2WI信号低于BCA, ADC均值低于BCA, 动态增强扫描动脉期快速强化, 静脉期快速下降, TIC呈快速强化、快速廓清(B型), 延迟期强化程度减低。③腮腺恶性肿癌:多表现为形状不规则, 可呈分叶状, 信号不均、边缘模糊, 与周围组织分界不清, 多呈浸润性生长, 增强扫描轻中度强化, 延迟期廓清明显。
综上所述, 腮腺基底细胞腺瘤是一种少见的良性肿瘤, 好发于中老年女性, 主要位于腮腺浅叶, 单发类圆形肿块, 有包膜, 易囊变, DWI弥散受限, 其时间-信号曲线、ADC均值及范围与其他常见腮腺肿瘤有明显差异, 掌握这些特征对其诊断与鉴别诊断有很大帮助。
| [1] |
杨功鑫, 等. 腮腺肿瘤的磁共振弥散加权成像评价[J]. 中国医学计算机成像杂志, 2013, 19(6): 489-493. |
| [2] |
KawataR, Yoshimura K, Lee K, et al. Basal cell adenoma of the parotid gland: a clinicopathological study of nine cases-basal cell adenoma versus pleomorphic adenoma and Warthins tumor[J]. EurArch Otorhinolaryngol, 2010, 267(5): 779-783. DOI:10.1007/s00405-009-1139-9 |
| [3] |
Nagao T, Sugano I, Ishida Y, et al. Carcinoma in basal cell adenoma of the parotid gland[J]. Pathol Res Pract, 1997, 193(3): 171-178. DOI:10.1016/S0344-0338(97)80074-X |
| [4] |
姜倩男, 张铎. 腮腺基底细胞腺瘤的MRI诊断价值_姜倩男[J]. 北华大学学报(自然科学版), 2014, 15(1): 78-82. |
| [5] |
Jao W, Keh PC, Swerdlow MA. Ultrastructure of the basal cell adenoma of parotid gland[J]. Cancer, 1976, 37(3): 1322-33. DOI:10.1002/(ISSN)1097-0142 |
| [6] |
Shi L, Wang YX, Yu C, et al. CT and ultrasound features of basal cell adenoma of the parotid gland: a report of 22 cases with pathologic correlation[J]. AJNR Am J Neuroradiol, 2012, 33(3): 434-8. DOI:10.3174/ajnr.A2807 |
| [7] |
李颖, 等. 腮腺基底细胞腺瘤CT和MRI特点[J]. 中国医学影像学杂志, 2012(4): 252-254. |
| [8] |
刘春玲, 黄飚, 周正根, 梁长虹. 腮腺基底细胞腺瘤的CT和MRI特点[J]. 中华放射学杂志, 2009, 43(6): 600-603. DOI:10.3760/cma.j.issn.1005-1201.2009.06.011 |
| [9] |
刘红刚, 高岩. 头颈部肿瘤病理学和遗传学[M]. 北京: 人民卫生出版社, 2006: 303-304.
|
| [10] |
Yabuuchi H, Fukuya T, Tajima T, et al. Salivary gland tumors: diagnostic value of gadolinium - enhanced dynamic MR imaging with histopathologic correlation[J]. Radiology, 2003, 226(2): 345-54. DOI:10.1148/radiol.2262011486 |
| [11] |
Suzuki S, Okamura H, Ohtani I. Bilateral parotid gland basal cell adenomas: case report[J]. ORL J Otorthinolaryngol Relat Spec, 2000, 62(5): 278-281. DOI:10.1159/000027760 |
| [12] |
Lee DK, Chung KW, Baek CH, et al. Basal cell adenoma of the parotid gland: characteristics of 2 - phase helical computed tomography and magnetic resonance imaging[J]. Comput Assist Tomogr, 2005, 29(6): 884-888. DOI:10.1097/01.rct.0000183273.70422.c4 |