2. 安徽医科大学第二附属医院;
3. 中国科学技术大学
2. The Second Hospital of Anhui Medical University;
3. University of Science and Technology of China
131I被广泛用于治疗甲状腺疾病,在治疗甲状腺癌的过程中,由于每例病人131I用量大、治疗时间长,与核医学科目前开展的其他放射性核素治疗项目相比,其对辐射环境产生的影响最大。目前关于131I治疗过程中对外环境产生的辐射水平的数据较少,每个医院甲癌病房的屏蔽设计都有很大差异,有的设计过于保守,造成很大浪费,而有的病房外的辐射水平又不能满足环境保护的要求。为了完善甲癌病房的屏蔽设计,需要对治疗过程中的源强和辐射场分布进行测量。一些文献对相关内容进行了报道[1-11],但是由于关注点不同,仅针对不同时间间隔病人体外的辐射水平、病人服药后体内的131I代谢等情况进行了研究,尚不能反映整个甲癌治疗过程中所产生辐射场的源强和分布。本工作的研究成果将对甲癌治疗病房的屏蔽设计和该类项目的辐射环境管理具有重要参考意义。
1 测量 1.1 测量方法由于患者服用131I后会通过呼吸、汗、唾液、粪、尿代谢排出体外[6],如果要了解整个治疗过程对病房外其他人员产生的外照射影响,就需要连续监控服药后的病人体外一定范围内的辐射水平。
使用被动测量式探测器热释光剂量片(TLD),记录整个治疗过程中甲癌病房内不同点位处的累积剂量水平,了解治疗的不同时间段内病人对周围产生的累积剂量。使用主动式探测器(X-γ剂量率仪)测量病人周围不同距处的γ辐射空气吸收剂量率,了解病人服药后辐射场的分布。
1.2 测量设备热释光剂量片(TLD)使用LiF(Mg,Cu,P)探测器,能量响应在25keV~3MeV之间,量程在10nGy~12Gy之间,读数器为HARSHOWTLD 3500型热释光读数器。
由于服药后病人的表面剂量率较大,而目前常用的便携式剂量率仪表中,大量程探测器通常精度较差,因此,对于剂量率大于100μGy/h的监测点,使用QX -300型G-M管X-γ剂量率仪进行测量,该探测器能量响应在50keV~3MeV之间,量程在10-8~10 Gy/h之间。对于剂量率小于100μGy/h的监测点,使用FH40G型闪烁体剂量率仪,该探测器能量响应在60keV~3MeV之间,量程在10-8~10-4Gy/h之间。
1.3 测量布点 1.3.1 累积剂量监测点四侧墙壁的布点:热释光剂量片布设在甲癌房内距离病床东面2m、西面0.1m、南面1.5m、北面2m处的墙壁上,见图 1。

|
图 1 累积剂量监测布点图 |
病床上、下的布点:热释光剂量片布设在病床正上方距离病床表面1m处; 病床下方的热释光剂量片布设在病床正下方距离病床上表面0.6m处的地面上,见图 1。
每个点位各放置5组热释光片,每24小时取出一组,用于测量累积剂量随治疗时间的变化。
1.3.2 剂量率监测点病人服药后5分钟的剂量率监测点位:在胸部周围1m处测量病人前、后、左、右的γ辐射空气吸收剂量率,测量病人的头部、腹部、腿部外1m处的剂量率,还测量距离病人胸前0.05、0.5、1、2、3m处的剂量率; 不同治疗时段病人周围剂量率监测点位:测量病人服药后24、48、72、96、120h距离胸前病人1m处剂量率。剂量率测量过程中,病人站立在甲癌病房中间。
1.4 参数测量过程中甲癌病房只有一个病人,病房长为5m,宽为4m,高为2.7m。病人为女性,60岁,身高170cm左右。病人为分化型甲状腺癌患者,一次性服用5.55×109Bq(150mCi)的Na131I,用于转移病灶治疗,治疗前病人的甲状腺已全部切除。
2 结果与讨论使用X-γ剂量率仪测量病人服药后5min周围辐射水平的测量结果见表 1。
|
|
表 1 病人服药5min后周围辐射水平(μGy/h) |
由表 1可以看出:①病人服药后5min,病人表面的γ辐射空气吸收剂量率很大,胸部表面0.05米处达到了533μGy/h,距离病人3m处下降到126μGy/h,可以看出,随着距离的增加,剂量率大幅较小,但是在病房的尺度范围内不符合点源随距离的衰减规律; ②服药后的病人周围辐射水平分布不均匀,病人胸前稍大,背后和两侧稍小,头部和腹部较大,腿部较小,可能是由于人体组织结构的差异和131I的代谢方式引起的。
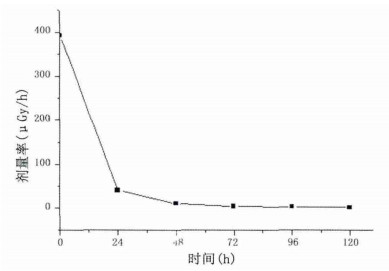
使用X-γ剂量率仪测量病人服药后5min、24 h、48h、72h、96h、120h距离病人胸前1米处的γ辐射空气吸收剂量率结果见图 2。
|
图 2 不同治疗时段病人胸前1米处γ辐射空气吸收剂量率的变化 |
由图 2可以看出,病人服药后5min,其胸前1m处剂量率很大,达到393μGy/h,但随着治疗时间的增加,更多的131I会通过呼吸、汗、唾液、粪、尿代谢排出体外,病人体表的剂量率快速减小,其中前24h剂量率的衰减速率最快,减小到服药后5min后的10%,48h后减小到3%,120h后病人出院时,其胸前1m处的剂量率水平只有1.9μGy/h。
使用热释光剂量片测量了整个治疗过程的前24、48、72、96、120h病房内各监测点的累积剂量,结果见图 3。

|
图 3 病房内不同点位累剂量随时间的变化 |
图 3中,病床北面2m处治疗前24小时的累积剂量测量值与南面1.5m处和东面2m处的累积剂量测量值相比偏大,此点离病房内看电视的座位处很近,可能是由于在对累积剂量贡献最大的前24h治疗期间,这位病人看电视的时间较长。
由图 3可以看出:(1)对于该例病人,整个治疗过程中,在病房内产生的累积剂量最大处为距离病床0.1m的西侧墙壁,达到约2.6mSv,病床正上方1m处的测量结果达到1.6mSv; (2)对于此类病人,前24 h对病房内各点产生的辐射剂量占整个治疗过程产生总剂量的57%~80%,前48h为80%~95%,随着治疗时间的增加,治疗后期对总剂量的贡献很小,与图 2中病人胸前1m处γ辐射空气吸收剂量率随治疗时间衰减规律相符。
3 结论使用主动测量和被动测量相结合的方式,测量了服药后的病人周围辐射场的空间分布和随治疗时间的变化趋势,较好地反映了整个分化型甲状腺癌转移病灶131I治疗过程中所产生辐射场的源强和分布,这些数据对甲癌治疗病房的屏蔽设计和该类项目的辐射环境管理具有重要参考意义。
甲癌治疗过程中服用131I的病人对周围辐射环境影响的大小与服药量、个体的差异、组织的代谢速率、治疗的目的、治疗次数、甲状腺的切除量、病房的大小等因素有关,在本工作中,没有全面考虑每个因素对结果的影响,只针对一例分化型甲状腺癌患者转移病灶131I治疗过程中的辐射水平进行了测量分析,实践过程中可以根据实际情况对结果进行修正。
整个测量过程没有干扰正常的治疗程序,不影响治疗效果,并已获得病人的同意。
| [1] |
Hermus AR, Huysmans DA. Treatment of benign nodular thyroid disease[J]. N Engl J Med, 1998, 338(20): 1438-1447. DOI:10.1056/NEJM199805143382007 |
| [2] |
廖洪春. 131碘治疗甲状腺疾病的辐射风险与防护[J]. 柳州医学, 2013, 26(3): 167-170. |
| [3] |
李云春, 谭天秩, 莫廷树, 等. 碘[131I]-美妥昔单抗注射液的人体药代动力学研究[J]. 生物医学工程学杂志, 2007, 24(4): 857-861. DOI:10.3321/j.issn:1001-5515.2007.04.031 |
| [4] |
梁婧, 张庆召, 林志凯, 等. 碘-131治疗过程中人员受照剂量分析[J]. 中国职业医学, 2015, 42(3): 318-321. |
| [5] |
胡凤琼, 庞华, 杨俊卿, 等. 甲状腺癌患者大剂量131I治疗的辐射防护研究[J]. 重庆医学, 2014, 43(17): 2252-2253. DOI:10.3969/j.issn.1671-8348.2014.17.057 |
| [6] |
刘剑锋, 叶根耀, 谢敏, 等. 甲状腺癌患者大剂量131I治疗后辐射剂量率的监测[J]. 军事医学科学院院刊, 2010, 34(5): 496-497. DOI:10.3969/j.issn.1674-9960.2010.05.026 |
| [7] |
张志东, 暴小林. 放射性核素碘-131在治疗甲状腺癌时医务人员的辐射防护[J]. 医学动物防治, 2007, 23(10): 790-791. |
| [8] |
Cui S, Jiao L, Tan J, et al. Estimating radiation absorbed dose of individuals nearby 131I-treated hyperthyroid patients[J]. Health Phys, 2014, 106(3): 365-369. DOI:10.1097/HP.0b013e3182a1c8d5 |
| [9] |
易艳玲, 石洪成, 陈波, 等. 分化型甲状腺癌患者的131I有效半衰期[J]. 原子能科学技术, 2010, 44(suppl): 612-615. |
| [10] |
Classic K. ICRP.Release of patients after therapy with unsealed radionuclides[J]. Annals of the Icrp, 2004, 34(2): 1-79. DOI:10.1016/j.icrp.2004.08.003 |
| [11] |
池晓华, 刘峰, 李贵平, 等. 距离在甲状腺癌患者131I治疗中的屏蔽作用[J]. 南方医科大学学报, 2014, 34(2): 286-288. |





