2. 中国辐射防护研究院
2. China Institute of Radiation Protection
1936年美国生物物理学家Locher明确提出了硼中子俘获治疗(BNCT)的基本原理[1]。假定10B可以有选择性的集中在肿瘤细胞中,然后用热中子束照射肿瘤组织,那么将在肿瘤组织中产生足以杀死肿瘤细胞的辐射剂量。受照肿瘤组织的定位主要是由聚集在肿瘤中的含硼药物决定的,而不需要用中子束瞄准。与传统的放射疗法相比,BNCT的优点在于能够有选择性的杀死癌细胞,而不损坏健康的组织。
美国的麻省理工学院(MIT)和布鲁克海文国家实验室(BNL)是BNCT研究的先驱[2]。早在上世纪50年代,BNL就做了全球首个用此疗法治疗神经胶母细胞癌的临床试验。后来MIT也做了相关的试验。由于试验结果令人不满意,双方都在1961年停止了这方面的研究工作。导致试验失败的原因有:①试验中所用的含硼药物对肿瘤没有明显的选择性,结果导致正常细胞所受的剂量过大,而肿瘤组织却没有得到足够的剂量; ②热中子束在患者头颅中穿过的深度不够。正是这两点原因阻止了BNCT发展的进程。
最近几年,美国发明了新的含硼化合物—BPA (boron phenyl alanine),这种药物具有较好的亲肿瘤性。1994年,美国的MITR-Ⅱ研究堆建成了第一个用于BNCT治疗的超热中子束流。有了这两大发展,BNL和MIT在1994年又都开始了新的试验。另外,日本也在1968年开始了BNCT的相关临床试验[3]。到1997年5月,日本的研究小组已经用中子俘获疗法做了160多起脑瘤病例临床试验,其中包括大约100例的神经胶母细胞癌病例。欧洲目前也有5个研究中心(荷兰、瑞典、芬兰、意大利和捷克共和国)提供BNCT治疗。
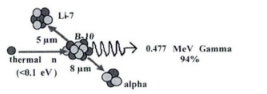
1 BNCT原理硼中子俘获治疗方法(BNCT)的基本原理是用热中子照射聚集在肿瘤位置的10B,利用10B和热中子发生的俘获反应释放出的能量杀死肿瘤细胞,而不伤害正常的组织细胞,从而达到治疗肿瘤的目的。热中子与10B的反应截面是3837靶,比人体中主要元素原子核1H、12C、14N、16O的热中子反应截面都要高出很多倍。热中子在肿瘤细胞中发生核反应10B(n,α) 7Li,反应生成能量为1.47 MeV的α粒子和0. 84 MeV的7Li反冲核,并发射能量为0. 477 MeV的光子。α粒子和反冲核的射程很短(分别为8 μm和5 μm),大约和细胞核的直径差不多。而且它们的LET值很高,几乎所有的能量都能沉积在肿瘤细胞中,从而将肿瘤细胞杀死,而正常组织不会被破坏,如图 1所示。
|
图 1 BNCT利用的核反应示意图 |
这种治疗方法分为两步:①先在患者体内注入含有10B的亲肿瘤药物。这种化学药物有选择性的聚集在肿瘤细胞中; ②照射:用中子束照射肿瘤区域。此中子束对含有10B的肿瘤细胞具有致命的作用,但是对正常的细胞却只有很少的伤害。
2 BNCT中的剂量组成用于硼中子俘获治疗的辐射场是n-γ混合场,射线束在人体组织里产生四种剂量:
2.1 γ剂量(Dγ)伴随中子束产生的γ剂量和组织中的H原子吸收热中子并发生核反应1H(n,γ) 2H所放出的能量为2.2 MeV的γ射线的剂量。
2.2 中子剂量(Dn)这部分剂量来自于超热中子和快中子与组织中的H原子碰撞发生核反应1H(n,n') P所产生的反冲质子在组织中沉积的能量。
2.3 质子剂量(Dp)组织中的14N与热中子发生核反应14N(n,p) 14C,生成的质子和反冲核14C在组织中沉积的能量。
2.4 10B裂变反应产生的剂量即硼剂量(DB)10B吸收一个热中子,发生核反应10B(n,α) 7Li,生成的α粒子和反冲核7Li在组织中所沉积的能量。
3 剂量测量方法为了保证治疗的效果和治疗过程中病人的安全,在治疗前必须确定用于治疗的射线束的特性,即测量中子的通量和伴随γ的剂量,还必须测量出体模中的吸收剂量,制定合适的治疗计划。治疗过程中,由于热中子和超热中子在组织中的衰减很快,四种剂量成分的相对贡献变化显著,治疗过程中必须实时测量病人所受的吸收剂量以保证治疗的效果。目前主要用累积剂量测量和实时监测两种方法进行BNCT的剂量测量[4]。
3.1 累积测量方法累积测量方法的优点是能够精确的测量中子和γ的剂量。常规的测量方法是金丝活化法。但由于热释光探测器(TLD)具有量程宽、尺寸小、可重复使用、灵敏度高等特点而被广泛应用[5]。
目前用的比较多的是LiF热释光探测器。6LiF对热中子和Y都有响应,而7LiF只对γ有响应。因此,一对6LiF和7LiF探测器能够测量热中子和γ剂量。但是目前用于硼中子俘获治疗的中子束的主要成分是超热中子,简单的一对6LiF和7LiF探测器不能测量出超热中子的剂量贡献。为了解决这个问题,波兰的克拉科夫核物理研究所(INP),建立了新的热释光剂量计。新发明的热释光探测器由探测器及屏蔽容器两部分组成。探测器是6LiF(Mg,Ti)片子,屏蔽容器是由非活化的6LiF制成(图 2)。屏蔽容器的作用是吸收掉热中子成分,容器中的6LiF探测器测量到的就是超热中子的剂量[6-7]。采用这种方法可以解决超热中子的剂量测量问题。

|
图 2 小型TL探测器和屏蔽容器的设计(mm) |
相对于累积测量,实时测量的优点是在治疗过程中能够实时监测病人所受的剂量。为了不影响中子场的分布特征,这就要求实时测量系统的探头部分体积很小。用电缆或者光纤连接探头作为信号传输工具,可以让光电倍增管或电子学仪器免受辐射场照射,不被干扰。
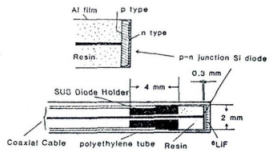
3.2.1 用小型PN结硅探测器测量热中子通量和γ剂量率图 3为小型PN结硅探测器的结构示意图。如图所示,在探测器的端面涂上6LiF,利用核反应6Li (n,α)3H将热中子转换成可探测信号。根据6LiF质量的不同(如2.5、0.25和0.025 pg)可以测量不同通量的热中子(109~105n cm-2s-1)。同时,硅探测器对γ射线也有响应。由于,核反应产生的3H(2.7 MeV)和α粒子(2.1 MeV)的能量较高,形成的脉冲能量高于γ射线。根据此可以甄别出中子和γ的剂量贡献。
|
图 3 小型PN结硅探测器结构 |
日本的原子能研究实验室用BGO闪烁体与光纤连接组成了此BGO闪烁探测器测量系统,其构造如图 4所示[4]。在BGO闪烁体外,用6LiF作屏蔽层可以吸收混合场中的热中子,则探测到的只是γ射线;在BGO闪烁探测器外包一层Cd片,可将热中子转化为γ射线,被BGO闪烁体探测到的剂量代表热中子的剂量贡献。两种不同屏蔽材料(6LiF和Cd片)的BGO闪烁探测器可以分别测出混合场中γ和热中子的剂量。

|
图 4 BGO光纤闪烁探测器结构图 |
光纤闪烁探测器是用光纤作为光导连接探头和光电倍增管,将闪烁体产生的光信号传输到光电倍增管。光纤探测器的关键是探头部分的研制。
名古屋大学的核能学院的做法是将ZnS(Ag)粉末、中子转换体和粘贴胶按重量比1: 1: 2混合粘到光纤的一端作为闪烁探头,厚度是0. 3 mm,光纤的另一端连着小型光电倍增管。测量热中子通量时,用6LiF粉末做中子转换体。利用核反应6Li(n,t) 4He,将中子转换成一个α粒子和氚核。当α粒子或氚核撞击到ZnS(Ag)上,使其闪烁发光。闪烁光通过光纤传输到电子仪器部分,然后被放大记录。而在快中子能量范围内,中子转换体是使用232Th粉末。若闪烁体中不掺杂中子转换体,则可以用来测量γ射线[8-9]。
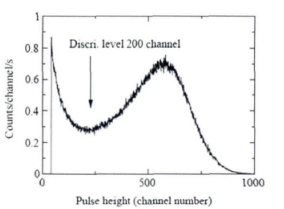
日本国家计量院为了增强中子-γ的甄别能力,研制的小型探测器的探头部分由ZnS(Ag)薄膜和中子转换体6LiF薄片组成。具体方法是将25 μm厚的ZnS喷到12 μm厚的醋酸纤维素上,然后将5μm的6LiF真空蒸发到醋酸纤维素的另一侧。由于α粒子的射程要小于氚核,所以α粒子最终醋酸纤维素阻止了,只有氚核能打到ZnS上。用此探测器测量的中子脉冲谱如图 5所示。低能区的计数是由γ射线贡献的。在中子能区的脉冲峰只是由氚引起的。据此可以在波谷设置阈值,甄别n-γ[10]。为了降低γ对中子计数的影响,在这之后提出用反符合技术消除γ的计数[11]。
|
图 5 中子脉冲谱 |
日本东京大学的方法同样是用光纤传输信号,而闪烁体用的是含硼和不含硼的塑料闪烁体[12]。含硼塑料闪烁体能同时探测到中子和γ,不含硼的塑料闪烁体只对γ有响应。用这两种塑料闪烁体组成的一对光纤闪烁探测器可以分别测量中子和γ的剂量。
4 讨论多年的临床试验表明,硼中子俘获治疗法对肿瘤治疗有很好的疗效。由于用于治疗的中子辐射场的射线成分比较复杂,在制定治疗计划前要估计出各射线成分对人体正常组织的伤害,需根据不同情况使用不同手段准确的测量出各成分的剂量贡献。
目前,我国首个用于临床治疗的BNCT中子照射器已经建造完毕。为了能够更好地开展临床治疗研究,应该进行相应的剂量测量方法的技术攻关,其难点是混合场中的n、γ剂量的甄别。
| [1] |
IAEA.Current Status of Neutron Capture Therapy.IAEA-TECDOC-1223[R].Vienna, 2001.
|
| [2] | |
| [3] | |
| [4] |
Tetsuo Matsumoto, Otohiko Aizawa. Dose measuring system for boron neutron capture therapy[J]. Nuclear Instruments and methods in Physics Research, 1988(A 271): 662-670. |
| [5] |
Aschan C, Toivonen M.TL detectors in BNCT dosimetry.IAEA-TECDOC-1223[R].Vienna: 2001, 165-174.
|
| [6] |
Bilski P, Budzanowski M, Ochab E, et al. Dosimetry of BNCT beams with novel thermoluminescent detectors[J]. Radiation Protection Dosimetry, 2004, 110(1-4): 623-626. DOI:10.1093/rpd/nch218 |
| [7] |
Pawel Bilski, Natalia Golnik, Pawel Olko, et al. Improved dosimetry for BNCT by activation foils, modified thermoluminescent detectors and recombination chambers[J]. NUKLEONIKA, 2004, 49(2): 51-56. |
| [8] |
Mori Chizuo, Osada Taichi, Yanagida Katsuo, et al. Simple and Quick Measurement of Neutron Flux Distribution by Using an Optical Fiber with Scintillator[J]. Journal of Nuclear Science and Technology, 1994, 31(3): 248-249. |
| [9] |
Mori C, Uritani A, Miyahara H, et al. Measurement of neutron and γ-ray intensity distributions with an optical fiber-scintillator detector[J]. Nuclear Instrument and Methods in Physics Research A, 1999, 422: 129-132. DOI:10.1016/S0168-9002(98)01088-2 |
| [10] |
Ito Y, Katano G, Harano H, et al. Development of a tiny neutron probe with an optical fiber for BNCT[J]. Radiation Protection Dosimetry, 2004, 110(1-4): 619-622. DOI:10.1093/rpd/nch136 |
| [11] |
Matsumoto T, Harano H, Shimoyama T, et al. Developmant of a novel small-sized neutron detector based on a Li-glass scintillator[J]. IEEE Nuclear Science Symposium Conference Record, 2005. |
| [12] |
Ishikawa M, Ono K, Sakurai Y, et al. Development of real-time thermal neutron monitor using boron-loaded plastic scintillator with optical fiber for boron neutron capture therapy[J]. Applied Radiation and Isotopes, 2004, 61: 775-779. DOI:10.1016/j.apradiso.2004.05.053 |


