2. 山东省千佛山医院影像科, 山东 济南 250014
VolumeRAD成像技术也称为3D X射线照相技术, 是美国GE公司Discovery XR650型DR上的一种新型的X射线检查技术, 属于数字X射线断层融合技术(Digital Tomosynthesis, DTS)[1, 2], 早在19世纪30年代就有了数字断层的设想, 但受制于设备的发展而迟迟没有在临床应用, 最近几年随着计算机科学的不断发展, 硬件和软件技术不断完善, 使数字断层图像得以采集与显示[3, 4], 尤其是平板探测器(FPD)的改进, 其刷新速度、连续采集能力、DQE的不断提高, 使得VolumeRAD成像技术得以实现, 可以说VolumeRAD成像技术是计算机科学与医学影像学的完美结合[5]。虽然近几年CT和MR的功能不断改进, 其检查范围不断增加, 但普通X射线检查因其经济、简便且辐射剂量低等优点而被临床广泛选择, 探讨与分析VolumeRAD成像技术与CT的图像质量及辐射剂量的差异, 有利于临床上更好的选择X射线检查, 有效地降低病人的费用与辐射剂量。
1 设备与方法 1.1 设备GE XR650型DR、GE Lightspeed 16型CT、Kodak 8900激光相机、GE dragview图像工作站、GE AW4.4图像工作站、Catphan 500 CT质控体模、Baracuda诊断X射线剂量仪。
1.2 方法 1.2.1 CT检查方法将体模置于床上, 并悬挂于箱体前侧, 用水平尺调节体模水平位置, 使之水平。调节诊断床高度, 使体模定位点与激光定位线吻合。确保体模已置于扫描野中心, 使体模轴线垂直于扫描层面。按照临床常规头部条件(120 kV、200 mA)先进行定位像扫描, 定位线选在高对比和低对比分辨力体模的中心进行轴向扫描。高对比分辨力的探测:调整图像达到观察者认为的细节最清晰状态, 但窗位不得大于细节CT值和背景CT值之差, 记录观测者所能观察到的最小线对数(lp/cm)。低对比分辨力的探测:调整图像达到观察者认为的细节最清晰状态, 记录每种对比度的细节所能观察到的最小直径。同时使用诊断X射线剂量仪测量辐射剂量并记录。
1.2.2 VolumeRAD检查方法采集模式选择VolumeRAD检查, 探测器选择胸片架水平位, 将体模垂直放于水平胸片架上, 中心线对准体模中心, 体位选择头部AP位, 先采集DR跟踪图像, 后采集VolumeRAD图像, 条件选择设备默认条件, AEC曝光模式。重建条件选择:起始高度20 mm, 结束高度200 mm, 层间隔2 mm, 采集因子1, 层厚2 mm。高对比和低对比分辨力的探测如CT。同时使用诊断X射线剂量仪测量辐射剂量并记录。
1.3 统计学处理采用SPSS 13.0统计软件对CT和VolumeRAD成像技术下的高对比、低对比分辨力和辐射剂量进行非参数检验, P < 0.05为差异具有统计学意义。
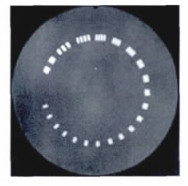
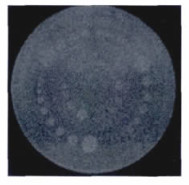
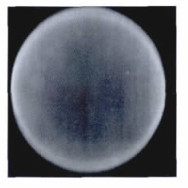
2 结果使用上述方法获取VolumeRAD、CT成像技术的体模图像, 图 1为CT高对比分辨力图像, 图 2为VolumeRAD高对比分辨力图像, 图 3为CT低对比分辨力图像, 图 4为VolumeRAD低对比分辨力图像。通过对图像进行解读, CT的低对比分辨力在对比度1%时为2 mm, 对比度0.5%时为4 mm, 对比度0.3%时为6 mm; 高对比分辨力7 lp/cm; 测量辐射剂量28 mGy。VolumeRAD成像技术的低对比分辨力在对比度1%时为4 mm, 对比度0.5%时为7 mm, 对比度0.3%时为0 mm; 高对比分辨力为9 lp/cm; 测量辐射剂量1.26 mGy。结果见表 1。经Kruskal Wallis Test对两组进行检验, P < 0.05, 差异具有统计学意义。
|
图 1 CT高对比分辨力图像 |

|
图 2 VolumeRAD成像技术高对比分辨力图像 |
|
图 3 CT低对比分辨力图像 |
|
图 4 VolumeRAD成像技术低对比分辨力图像 |
|
|
表 1 低对比度分辨率、高对比度分辨力、辐射剂量对照表 |
与传统DR图像相比VolumeRAD成像技术克服了组织结构的重叠, 提高了病变的检出率, 尤其是小于10 mm的结节性病灶主, 增强了病变检出的灵敏度。VolumeRAD成像技术可使细微结构分离, 提高了病变的特异性, 是常规X射线检查的提高和延伸[6, 7]。与CT相比VolumeRAD成像技术的最大优势是操作简单、辐射剂量低, CT的辐射剂量为28 mGy, VolumeRAD成像技术的辐射剂量为1.26 mGy, 仅为CT的4.5%, 大大降低了病人的辐射剂量。在图像质量中, VolumeRAD成像技术的高对比分辨力为9 lp/cm, 而CT的仅有7 lp/cm, 高于CT, 但低对比分辨力在对比度分别为1.0%、0.5%、0.3%时均低于CT, 尤其是在低对比度下VolumeRAD成像技术对体模的分辨十分困难, 在低对比度情况下图像质量虽不比CT图像质量好, 但在较低的花费和较低的辐射剂量下能够获得清晰满意的诊断图像, 因此VolumeRAD成像技术适合于高对比组织结构或病变的检查。
3.2 VolumeRAD成像技术工作流程从worklist列表中选择病人(patient)或添加行病人(add patient); 选择开始(start)或重新检查(resume); 选择VolumeRAD协议和探测器, 确立采集方式(如固定床卧位采集), 利用自动跟踪功能确定球管和探测器的位置; 摆病人体位并根据病人的解剖部位选择照射野(不得小于100 mm × 100 mm); 如有必要调整曝光参数或使用自动曝光模式(AEC); 采集跟踪图像并对其分析, 如位置和图像质量不满意, 点击采集屏(或OTS屏)上Retake scout键, 根据需要调整病人位置或参数, 重新采集跟踪图像; 如位置和图像质量满意, 按下Reset键, 球管自动移动到预设位置, 按下手闸进行VolumeRAD采集, 球管将按照预设的路径直到曝光结束松开手闸, 在整个采集过程中只有球管转动, FPD保持不动, 采集时间小于15 s。这组投影数据在图像采集工作站中回顾性的重建出冠状面或矢状面的一系列有顺序的图像[8], 其重建方式采用滤波反投影的计算方法, 图像重建时间大约需要两分钟[9]。原始和重建图像将在采集工作站中显示。如对重建图像不满意或是对兴趣区需重建, 可在图像工作站中选择起始高度(探测器距第一层的距离)、结束高度(探测器距最后一层的距离)、层厚、层间隔、采样因子, 点击RECON键进行重建。
3.3 VolumeRAD成像技术的临床应用 3.3.1 VolumeRAD成像技术采集方式与协议VolumeRAD成像技术共有四种采集方式, 固定床卧位采集, 胸片架卧位采集, 胸片架立位采集, 以及胸片架仰卧水平位采集。依据解剖部位和体位, VolumeRAD成像技术共设有默认29种协议可选, 基本涵盖了常用的检查部位。根据病人的体型分为成人和小孩, 成人和小孩又各分了大、中、小三种体型。
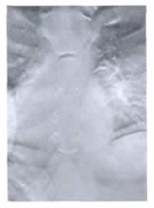
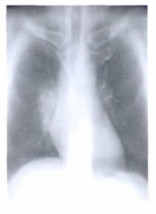
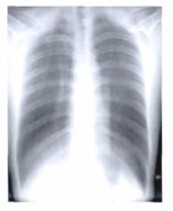
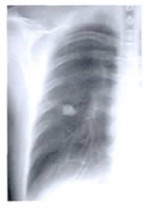
3.3.2 VolumeRAD成像技术在胸部摄影中的临床应用胸部X射线检查是目前影像学检查中最富有挑战性影像, 这不仅包括了胸部解剖结构的复杂性、重叠性和变异性, 而且大多数的疾病如良、恶性肿瘤、感染、外伤等都会发生, 尤其是对肺部小结节的鉴别诊断更是困难。在常规胸部摄影中, 胸片组织结构重叠严重, 细节不易分辨, 漏诊率高达30%之多[10]。VolumeRAD成像技术获取的是类似CT的数字断层图像, 避免了结构的重叠, 增加了局部组织的分辨力, 可显示感兴趣区的深部信息, 能够在不同的层面上可清晰地显示胸骨、胸锁关节、肋骨、气管及支气管、肺组织结构以及肺部小结节的位置(详见图 5~9)。总之, VolumeRAD成像能够为胸部疾病的诊断和鉴别提供了满意的图像, 大大提高了DR的影像诊断能力, 对具有挑战性的肺内结节性病变的诊断显示出较大潜能[11]。
|
图 5 胸骨断层图像 |

|
图 6 气管支气管断层图像 |
|
图 7 胸锁关节断层图象 |
|
图 8 肋骨断层图像 |
|
图 9 肺内小结节断层图像 |
综上所述VolumeRAD成像技术使用较低辐射剂量、方便、快捷地获得类似于CT图像的数字断层图像, 尤其是对高对比组织, 显示了组织结构的内部信息, 提高了图像质量, 使病变的检出率大大提高, 其检查协议涵盖了人体的各个检查部位, 可用于常规X射线检查。
| [1] |
Yan H, Godfrey DJ, Yin FF. Fastreconststrution of digital tomosynthesis using on boardimages[J]. Med Phys, 2008, 35(5): 2161-2169. |
| [2] |
王巍, 刘传亚, 卢传友, 等. 数字合成X线体层成像原理与研究进展[J]. 医学影像学杂志, 2005, 15(7): 606-608. DOI:10.3969/j.issn.1006-9011.2005.07.025 |
| [3] |
James T, Dobbins Ⅲ H. Page McAdams Chest tomosynthesis:Technical principles and clinical update[J]. European Journal of Radiology, 2009(72): 244-246. |
| [4] |
Pascoal A, Lawinski CP, Mackenzie A, et al.a comparison of image quality and effective dose using four digital systems.Radiation Protection Dosimetry[J]Chest radiography 2005, 114:273-277.
|
| [5] |
赵丽琴, 王克杨, 贺文, 等. 数字化断层融合技术对肺结节筛查应用的初步研究[J]. 放射学实践, 2010, 25(11): 1283-1286. DOI:10.3969/j.issn.1000-0313.2010.11.026 |
| [6] |
Dr.Siân Phillips. Why Volume RAD[J]. GE Healthcare, 2010, 9: 22-24. |
| [7] |
MacMahon H, Li F, Engelmann R, et al. Dual energy subtraction and temporal subtraction chest radiography[J]. Journal of Thoracic Imaging, 2008, 23: 77-85. DOI:10.1097/RTI.0b013e318173dd38 |
| [8] |
Sarkar V, Shi C, Rassiah-Szegedi P, et al. The effect of a limited number of projections and reconstruction algorithms on the image quality of megavoltage digital tomosynthesis[J]. Appl Clin Med Phys, 2009, 10(3): 2970. |
| [9] |
Feldkamp LA, Davis LC, Kress JW. Practical cone-beam algorithm[J]. J Opt Soc AMA, 2004, 1: 612-619. |
| [10] |
Stitik FP, tockma MS. Radiaographic screening in the early detection of lung cancer[J]. Radiol Clin N Am, 1978, 16(3): 347-366. |
| [11] |
Gomi T, Nakajima M, Fujiwara H, et al. Comparison between chest digital tomosythesis and CT to detec artificial pulmonary nodules for screening:a phantom study[J]. Br J Radiol, 2012, 85(107): 622-9. |



 ,
, 