手术中放射治疗(intraoperative radiation therapy,IORT)是指经手术切除病灶后或借助手术暴露不能切除的瘤灶,对手术后瘤床、残存瘤灶和淋巴引流区,在直视下进行大剂量照射的治疗方法[1]。
1972年,我国首先开展了IORT治疗肺癌和胃癌; 1979年,开展了腹部胃癌和胆管癌IORT; 1987年,开展了胰腺癌IORT,并在放射治疗科内加速器室内建立了专门IORT手术室,极大推动了IORT的开展。IORT开展初期,大多数采用传统固定式直线加速器,该加速器要求专用带防护屏蔽的加速器机房,防护设计费用较高,而且必须在加速机房附近设置专用IORT手术室,因此该技术开展的工作效率相对比较低。近年来,随着放疗新技术的发展一种专门用于术中放疗的移动式加速器问世,相对于固定式加速器而言,其治疗实施方便,可以在常规手术室进行,无需防护屏蔽要求,减少了昂贵的防护屏蔽费用,提高了手术室的利用率,也提高了IORT工作的效率[2]。
笔者主要通过对美国Mobetron® 1000移动式加速器,在模拟病人治疗时,测量手术室周围辐射水平情况来说明术中放疗移动式加速器在常规手术室(无需屏蔽的手术室)使用的可行性,同时验证移动加速器自身的屏蔽效果。
1 测量方案与测量仪器 1.1 Mobetron® 1000移动式加速器本次测量使用的术中放疗加速器为美国Mobetron® 1000移动式加速器,该移动式加速器主要用于没有放射防护屏蔽的手术室,它自身带有射线阻挡器,用于机架所有运动方向阻挡原射线,放射泄漏主要来自光子泄漏、散射线和电子线产生的X射线污染。由于电子线散射具有一定射程,大多数常规手术室墙足够阻挡电子线散射。
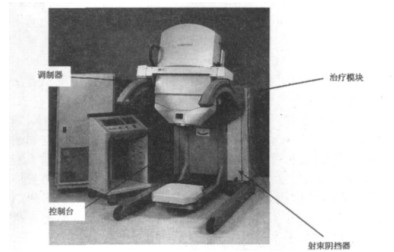
1.2 加速器产品性能结构及组成 1.2.1 结构产品由安装在马达驱动机架上的电子束直线加速器、调制器和操作控制台组成。加速器外观图见图 1。
|
图 1 术中放疗加速器外观图 |
标称能量为4MeV、6MeV、9MeV、12MeV; 最大剂量深度为4MeV时为(0.5 ± 0.2) cm,6MeV时为(1.3 ± 0.2) cm,9MeV时为1.9 ± 0.2cm,12MeV时为2.4 ± 0.2cm; 在治疗野中央区80%内,照射强度不均匀程度差异小于2%。
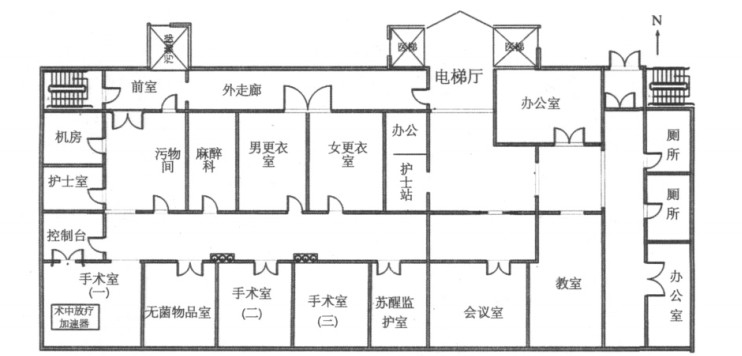
1.3 运行环境术中放疗加速器的使用场所为某医院手术室,该手术室位于病房楼顶的顶层,加速器的控制台位于手术室内背面的小房间,其周围情况见平面布置图 2。
|
图 2 移动式加速器工作场所平面布置图 |
本次测量使用的监测仪表为环境γ辐射监测仪,型号为FHZ672E-10。其性能参数为:测量范围: 1nSv/h~100μSv/h; 能量响应: 48keV~6MeV相对响应之差<± 15% (相对于Cs-137);准确度:<20% (针对Cs-137,剂量率大于100nSv/h)。
该仪器经过实验室检定,手术室周围辐射水平的测试方法按相关国家标准[3, 4]要求进行。
1.4.2 测量条件本次测量时,加速器的电子能量12MeV,输出剂量率为10Gy/min。输出电压380V,功率: 4.2kW。选用的测量方案有: ①治疗床上未放置任何屏蔽材料时,测量手术室周围房间的辐射水平; ②模拟实际治疗(选用20cm厚的液体水模拟需要治疗病人的病灶部位)时,测量手术室周围房间的辐射水平; ③模拟实际治疗,并在治疗床下放置5cm厚的有机玻璃板时,测量手术室周围房间的辐射水平。
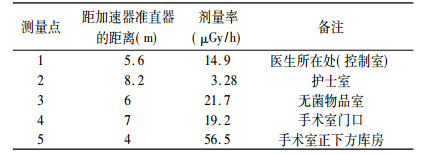
2 测量结果根据上述测量方案,在加速器最大使用工况时,测得不同条件下手术室周围辐射水平见表 1~表 3。术中放疗用加速器工作场所的辐射本底见表 4。
|
|
表 1 未模拟实际治疗情况下手术室周围辐射水平测量结果 |
|
|
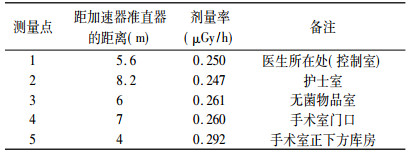
表 2 模拟实际治疗时手术室周围的辐射水平测量结果 |
|
|
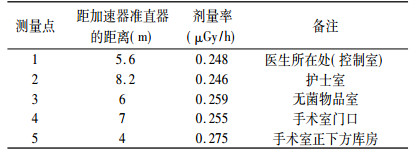
表 3 模拟治疗并在床下放5cm厚有机玻璃板时手术室周围的辐射水平测量结果 |
|
|
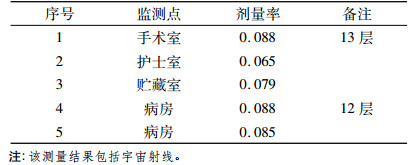
表 4 术中放疗用加速器辐射本底监测结果(μGy/h) |
测量结果表明,在未进行模拟实际治疗,加速器运行产生的射线束直接打在治疗床上时,导致手术室周围的辐射水平很高,最大为56.5μGy/h; 当进行模拟实际治疗时(即在治疗床上放置20cm厚的液体水),加速器产生的射线束经过水层吸收后,致手术室周围的辐射水平明显下降很多; 当模拟实际治疗并在治疗床下在放置5cm厚的有机玻璃板时,手术室周围的辐射水平与未放置有机玻璃时手术室周围辐射水平差别不大,由表可以看出,模拟实际治疗是治疗时手术室周围辐射水平高于本底3倍左右,对环境的影响不大。
3 评价与讨论 3.1 放射工作场所选址适宜性根据本次测量结果,Mobetron® 1000移动式加速器的工作场所为未经特殊屏蔽的手术室,且医院手术室的出入有严格的控制要求,因此,术中放疗加速器在手术室内进行术中放射治疗的方案是合理可行的。
3.2 加速器自身防护效果Mobetron® 1000移动式加速器自身防护性能良好,泄漏辐射率远低于国家标准限值。根据有关资料以及我们的实际测量发现,实际治疗时加速器的泄漏辐射水平均低于国家标准限值,其工作场所无需进行屏蔽,可以达到减少辐射防护成本投入的目的。
3.3 手术室周围辐射水平分析经过实际测量:在未进行模拟实际治疗,加速器运行产生的射线束直接打在治疗床上时,导致手术室周围的辐射水平很高,其原因很可能是:由于加速器产生的电子直接打到金属治疗床上,产生的韧致辐射较大,导致手术室周围辐射水平明显升高。但是在实际治疗中,病人病灶为C、H、O元素组成,属于轻物质材料,当电子打在轻物质材料上时,产生的韧致辐射会大大降低,所以,手术室周围辐射水平明显降低很多。在模拟实际治疗情况下,再在治疗床下放轻物质材料(有机玻璃)吸收电子,其效果与未放吸收材料时相比,手术室周围辐射水平变化不大,主要是因为加速器产生的电子能量为12MeV,而12MeV在水中的最大射程为7.4cm,因此,模拟人体病灶的20cm厚液体水能将大部分电子吸收,再在治疗床下放轻物质吸收材料时效果并不明显。
通过以上测量结果分析,术中放疗加速器在实际使用过程中,其工作场所无需特殊防护,其周围辐射水平能够满足国家相关标准要求。
| [1] |
唐劲天. 肿瘤手术中放射治疗技术[J]. 中日友好医院学报, 14(2). |
| [2] |
姜瑞瑶. 固定式和移动式加速器开展术中放疗比较分析[J]. 医疗卫生装备, 2009, 30(7). |
| [3] |
GB/T 14583-93, 环境地表γ辐射剂量率测定规范[S].
|
| [4] |
GB 18871-2002, 电离辐射防护与辐射源安全基本标准[S].
|