2. 温州医学院附属第一医院病理科
随着现代通讯科学技术的发展与进步, 人群手机持有量迅速增加。由于使用手机时可产生轻微的低强度微波辐射, 人们对其给人和环境污染造成的潜在危险日趋关注。国内外关于手机通信信号暴露危害的研究大多集中于普通人群的植物神经系统、循环和免疫系统等方面[1, 2], 而对于特殊人群, 如孕妇和胎儿的研究很少。手机微波辐射能够穿透皮肤和颅骨[3], 中枢神经系统是机体对微波辐射反应最为敏感的部位之一, 在神经系统发育过程中, 神经细胞粘附分子(neural cell adhesion molecule, NCAM)参与神经细胞的粘附与轴突生长、延伸, 促进突触的可塑性。本研究利用手机对孕鼠进行微波辐射, 观察其新生鼠脑内NCAM表达及髓鞘形成的变化, 以了解手机辐射暴露对发育中的中枢神经系统的影响。
1 材料与方法 1.1 主要仪器及试剂NCAM免疫组化一抗及SABC过氧化物酶试剂盒购自武汉博士德生物工程有限公司。髓鞘染色试剂固蓝、甲酚紫购自Sigma公司。仪器:ML-91型微波漏能测试仪, 江苏宿迁无线电厂生产。
1.2 动物分组及模型制作SD大鼠, 清洁级动物(温州医学院实验动物中心提供), 雌雄2:1合笼。次日检查出阴栓的雌鼠16只, 按随机数字表分入辐射组9只、对照组7只。观察到阴栓当天为孕0d。辐射模型制作:辐射组从受孕第1天开始进行手机微波辐射, 选用市场常见某品牌GSM手机, 保持通话状态, 放置于距离孕鼠腹部5cm处, (大鼠放在小笼中, 活动受限), 每天持续辐射2h, 一直到分娩前一天。手机通话状态频率为900、1 800MHz, 功率密度为(0.2100 ±0.013)mV/cm2, ML- 91型微波漏能测试仪(江苏宿迁无线电厂生产)检测。对照组同时受孕, 与辐射组在同一环境中生活, 但无暴露于手机微波辐射。分娩当天对每窝新生鼠进行称重及性别观察。每窝随机选取2只新生鼠, 于生后7d断头取脑, 多聚甲醛固定, 常规石蜡包埋, 切片备用。
1.3 免疫组化SABC法, 操作步骤按照说明书进行, 根据预实验调整抗体浓度。
1.4 髓鞘染色切片常规脱腊至水, 固蓝溶液常温下2h, 95%乙醇洗5min, 再70%乙醇与蒸馏水交替洗, 直到灰白界限分明, 水洗不再褪色。甲酚紫复染1min, 蒸馏水洗。乙醇脱水, 二甲苯透明, 中性树胶封片。
1.5 结果判定病理图像分析使用美国IPP5.0(ImageProPlus5.0)专业图像分析软件测定阳性细胞的平均光密度值, 代表NCAM表达的相对含量。
1.6 资料分析实验结果以均数加减标准差(x±s)表示, 2组之间样本均数比较采用独立样本t检验, 用SPSS11.0软件处理。
2 结果 2.1 孕鼠妊娠结果对照组孕鼠分娩率6/7(85.7%), 妊娠时间(22 ±2)d, 新生鼠60只全部存活, 未见外观畸形。辐射组妊娠时间(22 ±1)d, 没有早产, 分娩率6/9(66.7%), 新生鼠65只, 其中死胎4只, 未见明显外观畸形。未分娩孕鼠腹部膨隆, 解剖发现其子宫增大、输卵管充血, 提示死胎被吸收。
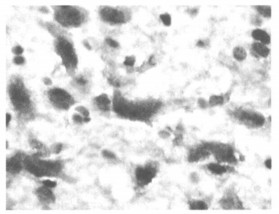
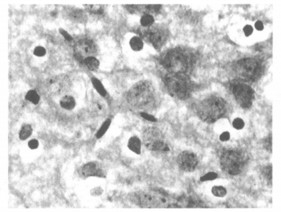
2.2 NCAM表达NCAM在新生大鼠大脑皮层、海马处的神经细胞表达较多。辐射组NCAM的表达水平低于对照组, 两组比较差异有统计学意义(P < 0.05)。见表 1、图 1, 2。
|
|
表 1 2组新生大鼠脑内的NCAM平均光密度值比较 |
|
图 1 对照组新生鼠NCAM强阳性表达(免疫组化染色×400) |
|
图 2 辐射组新生鼠NCAM弱阳性表达(免疫组化染色×400) |
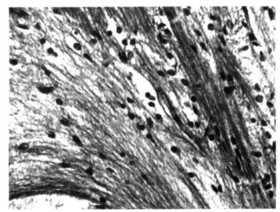
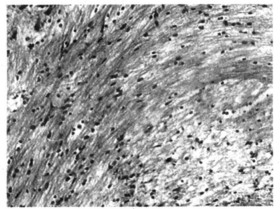
对照组大鼠胼胝体、海马伞附近髓鞘比较集中, 髓鞘完整, 为蓝绿色, 细胞核呈蓝色。辐射组相同部位可见髓鞘, 蓝绿色无脱失、断裂, 未见脂质空泡形成, 无明显髓鞘变性表现。但髓鞘稀疏, 着色较淡, 提示髓鞘形成量少。见图 3, 4。
|
图 3 对照组新生鼠髓鞘完整,为蓝绿色,细胞核呈蓝色(髓鞘染色×200) |
|
图 4 辐射组新生鼠髓鞘蓝绿色无脱失、断裂,未见脂质空泡形成,但髓鞘稀疏,着色较淡。(髓鞘染色×200) |
微波作为环境中普遍存在的物理因素可以使组织细胞DNA发生断裂、染色体发生畸变, 这种损伤作用与微波的频率、功率、辐射间隔时间存在一定的剂量-效应关系[4]。手机信号属于低强度微波辐射, 它们作用于生物体常常不会产生明显的由微波加热而产生的温度升高, 而是直接影响到细胞生物介质以及内部的生化和生理过程, 即非热效应。手机的微波辐射对机体是否有损伤一直存在争论, 而孕期手机辐射暴露将对胎儿造成何种影响更是人们最关注的问题之一。WangBM等[5]研究表明长期暴露于类似手机辐射的脉冲微波, 对成年大鼠的长期空间认知和记忆会造成损害。手机微波辐射还会使去颅骨大鼠的神经细胞凋亡增加[6]。胎儿神经系统处于发育的关键阶段, 颅骨呈开放状态, 对辐射的反应可能更敏感。
NCAM是细胞表面的一种糖蛋白, 介导细胞的粘附和识别。NCAM含有以α2 -8键相连的多聚唾液酸(polysialic acid, PSA), PSA-NCAM主要存在于胚胎发育期及早期的新生动物脑内, 与神经发育关系密切。在出生后的动物中, NCAM的表达主要集中在神经组织中, 参与细胞粘附、细胞迁移, 髓鞘形成, 神经纤维集聚, 突触的生长, 促进突触的可塑性形成等, 在神经发育可塑性方面起重要作用[7]。神经突起在生长过程中需要正确识别细胞信号通路, 与其他突起建立联系, 以接收和传出神经信息, 正是NCAM的存在使这一过程得以完成。海马是脑内和学习记忆关系最为密切的部位, 突触的可塑性是学习记忆的神经基础。海马突触前后膜上存在大量的NCAM, 在突触发生和可塑性脑区均有与轴突在发育阶段生长类似的特征性NCAM的表达。在体外孵育的海马脑片中加入NCAM抗体后可抑制海马CA1区突触传递长时程增强(long term potentia tion, LTP)的产生, NCAM可能影响LTP的诱导。在体动物实验也显示NCAM缺陷的小鼠的LTP的诱导受损, 表明NCAM是影响在体动物突触可塑性的重要因素[8]。本研究发现手机辐射组的新生鼠脑内NCAM表达下调, 提示孕期手机辐射对胚胎及新生大鼠的神经系统发育有潜在的危险, 可能影响新生儿的学习、记忆能力, 动作协调能力等。
无论是中枢神经系统还是外周神经系统, NCAM在髓鞘生成中扮演重要角色。Ono等[9]发现, 髓鞘形成延迟的病人11q23位染色体缺失, 这正是NCAM基因表达位点, 表明NCAM参与髓鞘形成。而脊髓损伤后NCAM表达增多, 也提示NCAM参与脊髓损伤后神经髓鞘的修复[10]。鼠类的髓鞘形成是出生后开始的, 生后7d, 脑的发育存在突然迸发的生长过程。本实验显示新生大鼠胼胝体、海马伞附近髓鞘比较集中, 辐射组动物无明显髓鞘变性表现。但与对照组相比, 髓鞘着色较淡, 提示髓鞘形成减少。神经原纤维变性, 不是继发性神经细胞的坏死和外伤性神经纤维断裂, 而是由于神经纤维本身营养和代谢障碍引起, 出现髓鞘变性脱失和轴突变性。本研究发现手机微波辐射对已形成的髓鞘没有明显破坏作用, 由于髓鞘的变性、修复有多种神经营养因子及细胞因子参与, NCAM的下调不会造成髓鞘严重损害。但辐射组髓鞘生成减少, 提示NACM的下调可能是髓鞘形成延迟的原因之一, 有待进一步跟踪观察。
(志谢: 感谢温州市疾病预防控制中心李娜对微波辐射的检测。)
| [1] |
Oftedal G, Wilen J, Sandstrom M, et al. Symptoms experienced in connection with mobile phone use[J]. Occup Med (Lond), 2000, 50(4): 237-245. DOI:10.1093/occmed/50.4.237 |
| [2] |
Braune S, Wrocklage C, Raczek J, et al. Resting blood pressure increase during exposure to aa radio-frequency electromagnetic field[J]. Lancet, 1998, 351: 1 857-1 858. DOI:10.1016/S0140-6736(98)24025-6 |
| [3] |
Eulitz C, Ullsperger P, Freude G, et al. Mobile phones modulate response patterns of human brain activity[J]. Neuroreport, 1998, 9(14): 3 229-3 232. DOI:10.1097/00001756-199810050-00018 |
| [4] |
Carmela M, Giovanni C, Palolo G, et al. Effects of microwaves(900 MHz)on the cochlear receptor:exposure systems and preliminary results[J]. Radiat Environ Biophys, 2000, 39: 131-136. DOI:10.1007/s004110000049 |
| [5] |
Wang BM, Lai H. Acute exposure to pulsed 2450 MHzmicrowaves affects water-maze performance of rats[J]. Bioelectriomagenetics, 2000, 21: 52-56. DOI:10.1002/(ISSN)1521-186X |
| [6] |
刘伟国, 杨小峰, 朱永坚, 等. 手机微波辐射对去颅骨大鼠神经细胞凋亡的影响[J]. 浙江创伤外科, 2003, 8(2): 4-7. |
| [7] |
Polo Parada L, Bose CM, Plattner F, et al. Distinct roles of different neural cell adhesion molecule (NCAM) isoforms in synaptic maturation revealed by analsis of NCAM 180 kDa isoform-dificientmice[J]. JNeurosci, 2004, 24(8): 1 852-1 864. DOI:10.1523/JNEUROSCI.4406-03.2004 |
| [8] |
Stoenica L, Senkov O, Gerardy-Schahn R, et al. In vivo synaptic plasticity in the dentate gyrus of mice dificient in the neural cell adhesion molecule NCAM or itspolysialic acid[J]. Eur JNeurosci, 2006, 23(9): 2 255-64. DOI:10.1111/ejn.2006.23.issue-9 |
| [9] |
Ono J, Harada K, hasegawa T, et al. Central nervoussysterm abnormalities in chromosome deletion at 11q23[J]. Clin Genet, 1994, 45(6): 325-329. |
| [10] |
王翠芳, 孙正义, 夏亚一. 脊髓损伤后神经细胞粘附分子的表达[J]. 中国组织工程研究与临床康复, 2007, 11(2): 297-300. DOI:10.3321/j.issn:1673-8225.2007.02.032 |



