多晶型现象在制药工业中普遍存在并被广泛研究。不同的晶型可能会影响药物的理化性质, 例如熔点、颜色、形态、溶解度、稳定性, 从而影响其制备工艺和生物利用度[1, 2]。多晶型的不同性质可以显著影响药物的贮存和质量, 最终导致不同的临床疗效和药物安全性。而对药物多晶型的详细了解和专利保护对制药公司也具有重要的商业价值[3]。分子间相互作用是驱动和决定多晶型形成的重要因素, 特别是多晶型中存在的非共价相互作用可对药学相关性能和行为产生显著影响。分析和探索晶体结构中分子间相互作用的性质对于理解新药设计与化学和物理特性的关系至关重要。一系列计算方法可用于揭示多晶型晶体中分子间相互作用的细微差别和相似之处。
Hirshfeld表面分析法是一种相对较新、流行且方便的方法。一般采用Hirshfeld表面分析法探索晶体分子内与分子间的氢键联系, 用于可视化分析和解释分子间相互作用[4]。Hirshfeld表面分析提供了晶体中紧密接触的二维图像, 即指纹图谱, 可以用作比较给定晶体结构的不对称单元中的分子的独特特征[5]。Hirshfeld表面分析图以不同颜色表示原子作为氢键供体和受体的能力, 能够快速轻松地深入了解晶体状态下的分子环境[6]。
通过CrystalExplorer软件系统地研究了吡罗昔康多晶型晶体中分子间的作用方式和作用能。使用AA-CLP方法估算了晶体堆积能, 并评估了库仑、极化、色散和泡利排斥分量的贡献。与完全从头计算的量子力学方法相比, AA-CLP不仅速度极快, 而且还能将分子间能量分解为可理解的化学分量[7]。吡罗昔康(图 1)是一种非甾体抗炎药和镇痛剂, 广泛用于缓解关节炎症状和治疗痛风。作用机制是非选择性抑制环加氧酶(COX) 1和2通路。吡罗昔康具有多晶型现象, 自1982年以来研究人员已对其进行了相当广泛的研究。迄今为止, 已报道了7种无水晶型、1种水合物和3种溶剂化物[8-11]。
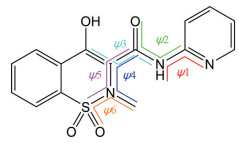
|
Figure 1 Molecular structure of piroxicam. ψ1-6: Torsional angles |
晶体数据来源 本研究所需的吡罗昔康多晶型的晶体结构数据来自剑桥结构数据库(CSD), 具体包括有晶体结构参数的可药用6种无水晶型和1种水合物晶型(表 1)。
| Table 1 Crystal structure parameters of seven piroxicam polymorphs. Forms A-F are the six crystal forms of piroxicam respectively. a, b, c, α, β, γ are the unit cell parameters of the crystal. Z is the number of molecules in the unit cell. BIYSEH and CIDYAP are code names in the CSD database |
软件分析 采用Mercury4.3.1 (美国Cambridge Crystallographic Data Centre Inc公司) 进行吡罗昔康晶型的构象分析和氢键分析。将7种晶型的cif文件导入Mercury, 通过H-bond和contacts list得到吡罗昔康的氢键信息, 通过multiple structures分析获得7种晶型的构象差异。利用CrystalExplorer21.5对吡罗昔康多晶型进行Hirshfeld表面分析, 利用cif文件, 通过Generate Surface与transparency得到吡罗昔康可视结构的Hirshfeld表面分析图。利用CrystalExplorer21.5中的display fingerprint plot可得到吡罗昔康的2D指纹图谱, 选择不同元素种类, 可得到吡罗昔康不同作用力在总作用力的比例。利用CrystalExplorer21.5中的B3LYP/6-31G(d, p) 基组可以计算多晶型分子在3.8 Å范围内的分子间相互作用能, energy frameworks可对吡罗昔康3.8 Å范围内的分子间进行能量框架分析, 能量框架中比例因子为200, 相互作用能量小于5 kJ·mol-1被忽略。采用CLP-PIXEL软件包可进行AA-CLP晶格能量计算, 晶体中分子间各势能为: Eij (kJ·mol-1) = A exp (-BRij) - CRij-6 + 1 389.36qiqj/Rij。其中Rij是原子核位置之间的分子间距离, A、B和C是经验参数, qi是位于原子核位置的原子电荷参数。总晶格能量是晶体中所有原子-原子距离的这些项的总和[12, 13]。
结果与讨论 1 吡罗昔康构象分析吡罗昔康各晶型扭角ψ1 (N3-C11-N2-H), ψ2 (C11-N2-C9-O4), ψ3 (N2-C9-C8-C7), ψ4 (C9-C8-N1-C10), ψ5 (C9-C8-N1-S), ψ6 (C10-N1-S-O2) 如表 2所示。其各晶型的构象叠合图如图 2所示(黑色: 晶A型; 粉色: 晶B型; 绿色: 晶C型; 蓝色: 晶D型; 橙色: 晶E型; 紫色: 晶F型分子1; 红色: 晶F型分子2; 黄色: 水合物分子1; 灰色: 水合物分子2)。
| Table 2 Torsional angles (ψ, degree) of various crystal forms of piroxicam. Monohydrate is piroxicam hydrate |
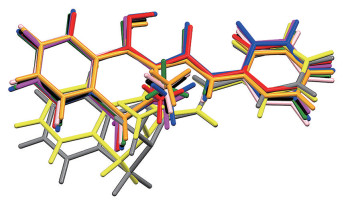
|
Figure 2 Overlay of the molecular conformation of piroxicam. Different colored molecules represent different crystal forms of piroxicam, among which Form F and monohydrate have two piroxicam molecules |
从表 2和图 2可以看出, 吡罗昔康水合物晶型的构象和其他晶型差异较大, 表明由于水分子的介入, 导致吡罗昔康分子在排列中采取了不同的扭转角度。另外6种晶型分子构象较为类似, 只有C7位上的羟基、N1位上的甲基角度略有差异。除水合物外的6种晶型扭角相差不大, 其中ψ1最大相差24.37°、ψ2最大相差17.82°、ψ3最大相差11.86°、ψ4最大相差10.17°、ψ5最大相差4.71°、ψ6最大相差9.31°。
2 吡罗昔康氢键分析吡罗昔康各晶型的氢键信息如表 3所示, 晶A型、晶B型、晶C型、晶D型、晶E型和晶F型都存在分子内氢键O4-H…O3, 只是键长略有不同。晶B型、晶C型氢键联系较为相似, 存在O4-H…O2键, 晶A型、晶D型和晶E型氢键联系较为相似, 为N2-H…O1形成氢键。从表 3中可以清晰地看出, 晶F型由两分子吡罗昔康分子构成, 存在分子间氢键。吡罗昔康水合物的成键联系明显不同于前面6种晶型, 这与其构象分析结果相符。
| Table 3 Molecular hydrogen bond parameters of piroxicam |
7种晶型的表面分析图如图 3所示。红色圆点是由表面内部分子与外部分子形成氢键而产生。氢键作用力越强, 供体与受体之间距离越小, 红色圆点颜色越深, 直径越大。白色区域表示比氢键距离较长的连接而蓝色区域表示相对于白色区域更长的连接。所得表面的亮红点对应上述分子间N-H…O、N -H…N、O-H…O和O-H…N氢键的供体和受体。图 3中, A1、D1、E1为吡罗昔康分子中-NH的N原子(氢键供体), 与受体中磺酰基存在氢键联系(N-H…O); A2、D2、E2处磺酰基的O原子为氢键受体, 与供体中的N-H存在氢键联系(O…H-N)。B1、C1处OH为氢键供体, 与受体中磺酰基的O原子存在氢键联系(O-H…O); B2、C2处磺酰基的O原子为氢键受体, 与供体中的O-H存在氢键联系(O…H-O)。F1为吡啶环上的N原子(氢键受体), 与供体上的N-H键存在氢键联系(N…H-N); F2为N-H (氢键供体), 与受体上的吡啶环N原子存在氢键联系(N-H…N)。吡罗昔康G1处为羰基中的O原子(氢键受体), 水分子为氢键供体。G2处为羰基的O原子(氢键受体), 与配体的六元环中的N存在氢键联系(O…H-N)。G3为吡罗昔康六元环中N原子(氢键供体), 与受体中的羰基存在氢键联系(N-H…O)。
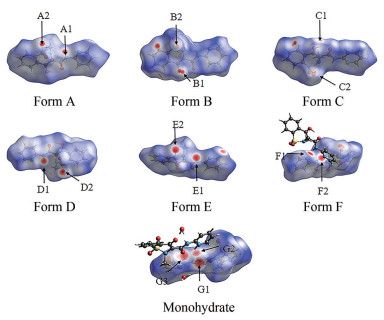
|
Figure 3 Hirshfeld surface analysis diagram of piroxicam. Monohydrate is piroxicam hydrate. A1, A2, B1, B2, C1, C2, D1, D2, E1, E2, F1, F2, G1, G2, and G3 represent the hydrogen bonding sites of different crystal forms, respectively |
Hirshfeld标准距离dnorm可以利用式(1)[14]计算:
| $ d_{\mathrm{norm}}=\left(d_{i}-r_{i}^{\mathrm{vdw}}\right) / r_{i}^{\mathrm{vdw}}+\left(d_{e}-r_{e}^{\mathrm{vdw}}\right) / r_{e}^{\mathrm{vdw}} $ | (1) |
式1中di和de分别表示Hirshfeld表面上的点到表面内部和外部原子的最近距离, rivdw是在Hirshfeld表面内部离Hirshfeld表面最近的原子I的范德华半径, 而revdw是在Hirshfeld表面外部离Hirshfeld表面最近的原子E的范德华半径。
4 吡罗昔康Hirshfeld指纹图谱分析生成的吡罗昔康晶型的2D指纹图谱如图 4所示, 从Hirshfeld指纹图谱分析可知, H-H和O-H作用力是全谱的主要构成部分, H…H作用力依次占晶A型、晶B型、晶C型、晶D型、晶E型、晶F型和水合物的百分比为37.2%、39.3%、37.3%、37.9%、32.7%、36.4%和38.0%。从图 4中可以看出, 在吡罗昔康分子中O原子作为氢键受体形成的峰较尖锐, 说明其O原子作为氢键受体的能力较强, 在7种晶型中, 吡罗昔康的磺酰基中氧原子主要作为氢键受体形成氢键, 所以O…H作用力强于H…O作用力, 分别为15.6%、13.7%、15.2%、13.7%、16.2%、16.0%和19.1%。分子间作用2D指纹图谱反映结构内部分子之间的相互作用方式以及各作用方式对整体作用的贡献程度。一般情况下, 分子间的N/O…H作用的峰出现在右下部, H…N/O作用的峰出现在左下部。
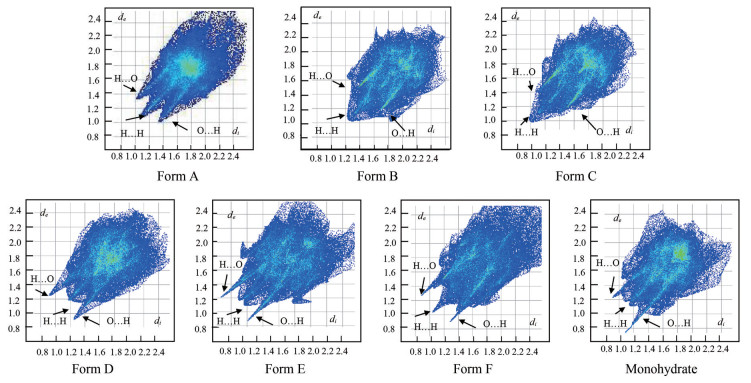
|
Figure 4 Intermolecular interaction fingerprint of piroxicam, di and de denote the closest distances from a point on the Hirshfeld surface to atoms inside and outside the surface, respectively |
采用CLP-PIXEL软件包进行AA-CLP晶格能量计算结果如表 4所示, 其显示了不同类型的相互作用对吡罗昔康晶格能的单独贡献。由表 4可知, 吡罗昔康的相互作用能由库仑、极化、色散和泡利排斥能项组成, 在各种相互作用力中, 色散能总是最大的。在7种多晶型中, 晶D型总能量最大, 水合物的总能量最低, 二者相差59.7 kJ·mol-1, 且水合物静电、排斥、色散、极化能与其他6种晶型相对差异较大。
| Table 4 Atom-atom Coulomb-London-Pauli (AA-CLP) calculation results of piroxicam (kJ·mol-1). Ecoul, Epol, Edisp, Erep and Etot are electrostatic energy, polarization energy, dispersion energy, repulsion energy and total energy, respectively |
理论计算和实际性能存在一定联系, 但有一定差异。能量计算表明, 晶D型、晶B型、晶C型、晶A型、晶F型的能量相差不大, 较为稳定, 晶E型居中, 水合物能量最小, 表明水合物最不稳定, 这与文献按照吡罗昔康多晶型间焓值分析结论基本一致[15]。而实际中, 晶A型的熔点最高, 晶A型在机械条件下和热应力下最稳定, 这也与作者的计算结果基本一致。
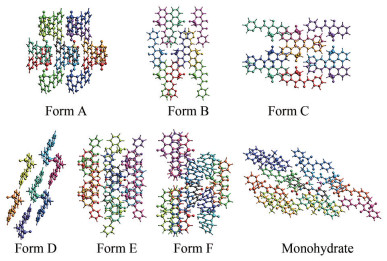
吡罗昔康多晶型晶体中分子间的作用方式和作用能的大小如图 5所示, 图 5中不同颜色分子代表着与中心吡罗昔康分子具有不同的相互作用能(从c轴方向观看)。分析图 5可知, 在以吡罗昔康为中心, 3.8 Å距离范围内, 晶A型、晶C型、晶E型与周围分子存在9种不同的相互作用能。晶B型与周围分子存在7种不同的相互作用能, 晶D型与周围分子存在10种不同的相互作用能, 晶F型与周围分子存在14种不同的相互作用能, 水合物与周围分子存在18种不同的相互作用能。这是利用B3LYP/6-31G(d, p) 波函数, 指定一个吡罗昔康分子, 将该分子周围3.8 Å距离内所有分子作为相互作用能量分析对象, 进行分子间作用能的分析, 可以从理论上系统地研究吡罗昔康多晶型晶体中分子间的作用方式和作用大小。
|
Figure 5 The interaction energy relationship centered on piroxicam observed from the c-axis direction |
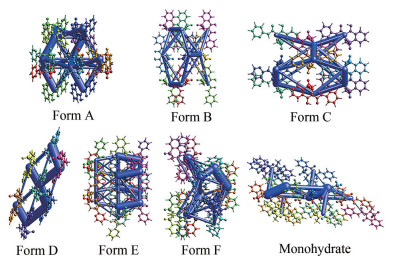
吡罗昔康能量框架如图 6所示。从图中可以看出, 不同晶型的吡罗昔康总体能量框架主要由不同的几何形单体组合而成, 在几何形能量框架单体内部有较小的相互作用能(圆柱体半径较小) 连接。其中晶A型、晶E型、晶F型相互作用能较其他晶型更强。能量框架与机械性能也存在一定联系。研究表明, 吡罗昔康晶A型的机械性能最好, 其次是晶B型和晶C型, 晶D型机械性能最差[16]。而4种晶型的能量框架分析可知, 晶D型的构成几何单元较稀疏, 与晶D型相比, 晶A型、晶B型、晶C型由更加密集、更加有规律的几何小分子构成。而晶A型、晶B型、晶C型中, 晶A型的圆柱体半径最大, 这与4种晶型的机械性能基本相符。
|
Figure 6 Piroxicam "energy frame" diagram viewed from the c-axis direction |
在构建吡罗昔康晶体能量框架时, 通过圆柱体表示分子间相互作用能(圆柱体半径与作用能大小成正比)。能量框架使吡罗昔康晶体结构中的作用能关系可视化, 从而更加有效和便捷地探究吡罗昔康晶体结构中的分子间能量关系。
结论Hirshfeld表面分析、AA-CLP晶格能计算和能量框架图被用来加强分析晶体不同的布局和相互作用在三维结构中呈现。通过计算吡罗昔康分子的Hirshfeld表面和二维指纹图谱, 可以直观揭示分子间相互作用并能够区分晶胞中的不同作用力大小和所占比例, Hirshfeld表面分析证明吡罗昔康多晶型结构中同类型的分子间作用力在所有分子间作用力中所占比例存在一定的差异。采用构象分析可知吡罗昔康水合物与其他晶型构象相差较大。其他6种晶型只有C7位上的羟基、N1位上的甲基角度有所差异。吡罗昔康多晶型间主要通过O3…O4、O1…N2、O4…O2形成氢键。正确计算库仑能是解释有机晶体结构的关键。计算结果清楚地显示了库仑与色散项作为分子极性相对重要性。采用AA-CLP法成功计算得到吡罗昔康晶体中各种作用力的贡献, 从而评估非共价相互作用在晶体组装过程中的重要性。通过AA-CLP可以补充验证实验结果。采用能量框架模型实现了晶体结构中相互作用能的可视化, 加深了对吡罗昔康晶体结构中分子间相互作用能的深刻理解。
作者贡献: 邢文慧、喻红梅、房政钰负责文献检索、能量计算并撰写了草稿; 张丽、邢逞负责数据分析; 龚宁波、吕扬负责论文的设计、指导和审阅。
利益冲突: 本文不存在任何利益冲突。
| [1] |
Lu B, Liu S, Yan D. Recent advances in photofunctional polymorphs of molecular materials[J]. Chin Chem Lett, 2019, 30: 1908-1922. DOI:10.1016/j.cclet.2019.09.012 |
| [2] |
Chistyakov D, Sergeev G. The polymorphism of drugs: new approaches to the synthesis of nanostructured polymorphs[J]. Pharmaceutics, 2020, 12: 34-42. DOI:10.3390/pharmaceutics12010034 |
| [3] |
Zhou Y, Wang J, Xiao Y, et al. The effects of polymorphism on physicochemical properties and pharmacodynamics of solid drugs[J]. Curr Pharm Des, 2018, 24: 2375-2382. DOI:10.2174/1381612824666180515155425 |
| [4] |
Zhang BX, Zhang L, Gong NB, et al. Structural analysis and Hirshfeld surface analysis of two isoniazid cocrystals[J]. Her Med (医药导报), 2018, 37: 12-15. |
| [5] |
Babashkina MG, Frontera A, Kertman AV, et al. Favipiravir: insight into the crystal structure, Hirshfeld surface analysis and computational study[J]. J Iran Chem Soc, 2022, 19: 85-94. DOI:10.1007/s13738-021-02285-x |
| [6] |
Bano H, Hussain S, Khan KM, et al. Crystal structure and Hirshfeld surface analysis of 1-(4-bromophenyl)-2-{[5-(pyridin-3-yl)-1, 3, 4-oxadiazol-2-yl]sulfanyl}ethan-1-one[J]. Acta Crystallogr E Crystallogr Commun, 2017, 73: 623-626. DOI:10.1107/S2056989017004819 |
| [7] |
Gavezzotti A. The atom-atom, Coulomb-London-Pauli (AA-CLP) model for intermolecular electrostatic-polarization, dispersion and repulsion energies[J]. New J Chem, 2011, 35: 1360-1368. DOI:10.1039/c0nj00982b |
| [8] |
Yao CL, Wang L, Wang XY, et al. Size-dependent solution mediated phase transformation of piroxicam monohydrate particles[J]. CrystEngComm, 2021, 23: 2928-2932. DOI:10.1039/D1CE00237F |
| [9] |
Sheth AR, Bates S, Muller FX, et al. Local structure in amorphous phases of piroxicam from powder X-ray diffractometry[J]. Cryst Growth Des, 2004, 5: 571-578. |
| [10] |
Liu X, Michalchuk AAL, Pulham CR, et al. An acetonitrile-solvated cocrystal of piroxicam and succinic acid with co-existing zwitterionic and non-ionized piroxicam molecules[J]. Acta Crystallogr C Struct Chem, 2018, 75: 29-37. |
| [11] |
Thomas LH, Wales C, Wilson CC. Selective preparation of elusive and alternative single component polymorphic solid forms through multi-component crystallisation routes[J]. Chem Commun, 2016, 52: 7372-7375. DOI:10.1039/C6CC01027J |
| [12] |
Gavezzotti A. Calculation of intermolecular interaction energies by direct numerical integration over electron densities. I. electrostatic and polarization energies in molecular crystals[J]. J Phys Chem B, 2002, 106: 4145-4154. |
| [13] |
Drozd KV, Manin AN, Voronin AP, et al. Sublimation thermodynamics of pyrazinoic, dipicolinic and quinolinic acids: experiment and theoretical prediction[J]. J Chem Thermodyn, 2020, 155: 106369-106382. |
| [14] |
Spackman P, Turner M, McKinnon J, et al. CrystalExplorer: a program for Hirshfeld surface analysis, visualization and quantitative analysis of molecular crystals[J]. J Appl Crystallogr, 2021, 54: 1006-1011. DOI:10.1107/S1600576721002910 |
| [15] |
Yao C, Guzei IA, Jin Y, et al. Polymorphism of piroxicam: new polymorphs by melt crystallization and crystal structure prediction[J]. Cryst Growth Des, 2020, 20: 7874-7881. DOI:10.1021/acs.cgd.0c01165 |
| [16] |
Vrecer F. Characterization of piroxicam crystal modifications[J]. Sci Pharm, 2001, 3: 212-213. |
 2022, Vol. 57
2022, Vol. 57


