2. 中南民族大学药学院, 湖北 武汉 430074
2. School of Pharmaceutical Sciences, South-Central Minzu University, Wuhan 430074, China
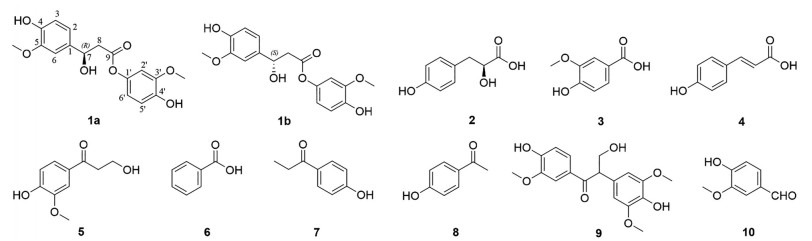
破布木果为紫草科(Boraginaceae) 植物破布木(Cordia dichotoma Forst. f.) 的干燥成熟果实, 别名树子、破布木、树子仔、破果子[1]。主要分布于云南、广西、广东、台湾、福建、新疆等地; 国外分布于越南、印度北部、澳大利亚东北部、菲律宾等国[2]。常生于山坡疏林及山谷溪边, 海拔300~1 900 m处[3]。该药材主要依赖进口, 在维吾尔族地区应用历史悠久, 维吾尔族地区认为破布木果功效生湿生热, 成熟异常黑胆质, 润肺润喉, 止咳化痰, 清音止渴, 通便利尿。用于干寒性或黑胆质性疾病, 喉干咽痒, 咳嗽不爽, 失音口渴, 小便不利, 大便不畅[4]。但因其属药用植物多、分布少、主要依赖于进口等原因, 使得对它的研究在我国没有受到足够重视。目前破布木果的药效成分及相关药理作用研究较为欠缺, 开展破布木果活性成分的综合研究, 可为破布木果的开发利用奠定基础。本研究针对干燥破布木果的85%乙醇提取物, 从其乙酸乙酯萃取部分分离得到10个化合物(图 1), 化合物类型包括苯丙素和简单苯环衍生物, 其中新化合物为一对苯丙素对映异构体。新化合物命名为(R)-破布木酯和(S)-破布木酯, 其他化合物依次鉴定为(S)-2-羟基-3-(4′-羟基苯) 丙酸(2)、香草酸(3)、对香豆素酸(4)、3-羟基-1-(4-羟基-3-甲氧基苯基)-1-丙酮(5)、苯甲酸(6)、对羟基苯丙酮(7)、对羟基苯乙酮(8)、5′-甲氧基楝叶吴萸素B (9) 和香草醛(10)。其中化合物1为新化合物, 化合物3、6、8、9为首次从该属植物中内分离得到, 结构见图 1。
|
Figure 1 Structures of compounds 1-10 |
化合物1 淡黄色片状物; HR-ESI-MS推断其分子式为C17H18O7 (m/z 335.112 4 [M+H]+), 不饱和度为9。1H NMR (600 MHz, CD3OD, 表 1) 谱显示有2个甲氧基氢的信号[δH 3.80 (3H, s, 3-OCH3)、3.86 (3H, s, 3'-OCH3)], 有3个与连氧碳相连的氢的信号[δH 3.78 (1H, m, H-8a)、3.92 (1H, dd, J = 5.2, 9.6 Hz, H-7)、4.15 (1H, m, H-8b)], 有2组苯环上的氢的信号[δH 6.96 (1H, d, J = 1.8 Hz, H-2)、6.83 (1H, dd, J = 8.2, 1.8 Hz, H-6)、6.80 (1H, d, J = 8.2 Hz, H-5)] 和[δH 6.75 (1H, d, J = 8.6 Hz, H-5')、6.63 (1H, d, J = 2.6 Hz, H-2')、6.45 (1H, dd, J = 8.6, 2.6 Hz, H-6')]。13C NMR (CD3OD, 150 MHz, 表 1) 谱中显示有17个碳的信号, 其中有4个与氧相连的碳信号[δC 55.4 (C-7)、56.4 (OCH3)、56.4 (OCH3)、65.3 (C-8)], 1个酯羰基碳的信号[δC 173.8 (C-9)], 结合DEPT显示6个次甲基[(δC 121.8、116.4、115.8、114.3、112.7、106.9)] 和6个季碳[(δC 149.2、149.2、147.4、145.4、144.9、128.1)], 推测此化合物为含有两个ABX系统苯环(A环和B环) 的酯类化合物(图 2)。
| Table 1 1H (600 MHz) and 13C (150 MHz) NMR data of compound 1 (CD3OD) |

|
Figure 2 1H-1H COSY and HMBC of compound 1 |
分析HSQC谱, 进一步确定C-H的数据归属。在HMBC图谱(图 2) 中显示: δH 3.92 (H-7) 与δC 65.3 (C-8) 远程相关, δH 4.15 (H-8b)、δH 3.78 (H-8a) 与δC 55.4 (C-7) 远程相关, 再结合1H-1H COSY图谱中显示δH 4.15 (H-8'b)、δH 3.78 (H-8'a) 和δH 3.92 (H-7') 之间相关, 提示-CH2-CH-结构片段; δH 4.15 (H-8b)、δH 3.78 (H-8a) 与δC 128.1 (C-1) 远程相关, 而δH 3.92 (H-7') 与δC 128.1 (C-1)、112.7 (C-2)、121.8 (C-6) 远程相关, 提示-CH(OH)-与A环直接相连; δH 4.15 (H-8b)、δH 3.78 (H-8a) 和δH 3.92 (H-7) 与δC 173.8 (C-9) 远程相关, 且δC 173.8 (C-9) 与B环无相关信号, 提示-O-CO-CH2-CH-结构片段, 从而确定了化合物的平面结构。再结合Scifinder查询结果, 确定该化合物为新化合物。
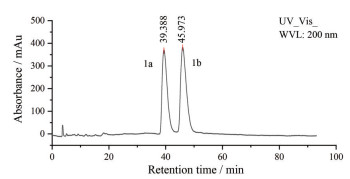
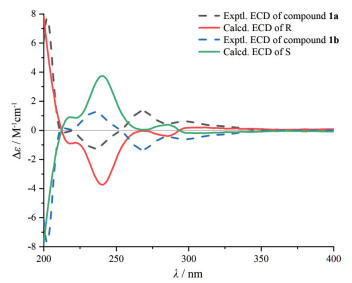
但是该化合物比旋光度很小, 为[α]D20+4.0 (c 0.5, CH3OH), 推测该化合物可能为外消旋体。再通过手性柱在制备液相上分析, 发现有2个峰面积大约为1∶1的峰(图 3), 进一步证实了该化合物为外消旋体, 然后通过半制备手性柱分离得到2个光学纯化合物1a和1b, 分别测得其比旋光度为[α]D20+38.0 (c 0.5, CH3OH)、[α]D20-38.0 (c 0.5, CH3OH)。再测定出2个光学纯化合物1a和1b的CD图谱(图 4), 它们的Cotton效应曲线正好呈现镜像关系。采用计算ECD法进一步明确化合物1a和1b的绝对构型。首先在Sybyl-X 1.1.0中使用MMFF94S力场的随机搜索对化合物1a和1b进行构象分析。随后用Gaussian 09软件在B3LYP/6-31G(d, p) 水平对化合物1a和1b的所有构象进行了密度泛函理论(DFT) 的优化。选择Boltzmann-opulation超过1%的构象体进行ECD计算。然后在B3LYP/6-311G(d, p) 水平上使用含时密度函数理论(TD-DFT) 计算优化的构象。在相同DFT水平上使用SCRF/PCM方法评估MeOH溶液的溶剂效应。最后, 通过SpecDis 1软件生成玻尔兹曼平均ECD光谱。通过比较实验光谱和计算的ECD光谱, 确定了化合物1a的结构为(R)-4'-羟基-3'-甲氧基苯基-3-羟基-3-(4-羟基-3-甲氧基苯基) 丙酸酯, 命名为(R)-破布木酯; 化合物1b的CD图谱刚好与1a相反, 因此鉴定化合物1b的结构为(S)-4'-羟基-3'-甲氧基苯基-3-羟基-3-(4-羟基-3-甲氧基苯基) 丙酸酯, 命名为(S)-破布木酯。
|
Figure 3 High performance liquid chromatogram of compound 1 separated by chiral column |
|
Figure 4 Experimental and calculated ECD spectra of compound 1 |
Bruker DRX-600 MHz核磁共振仪(德国Bruker公司); Waters ACQUITY SQD MS液相质谱联用仪、Waters 2535半制备型HPLC仪(美国Waters公司); Silgreen C18柱(250 mm × 10 mm, 5 μm, 北京绿白草科技发展有限公司); 大赛璐CHIRALPAK IC手性柱(250 mm × 4.6 mm, 5 μm, 日本Daicel公司); YMC-Pack diol柱(150 mm × 10 mm, 5 μm日本YMC公司); GF254薄层硅胶板、柱色谱硅胶(烟台江友硅胶开发有限公司); Sephadex LH-20葡聚糖凝胶(美国Amersham公司); CHP-20PMCI树脂(日本三菱公司); MCI HP20ss (63~150 μm)、HP20大孔树脂(日本三菱公司); 甲醇、乙腈、正己烷和异丙醇(色谱级, 美国TEDIA试剂公司)。
破布木果于2020年9月购于新疆维吾尔自治区和田中药材大市场, 经中南民族大学万定荣教授鉴定为紫草科植物破布木(Cordia dichotoma Forst. f.) 的干燥果实。现存放于湖北省武汉市中南民族大学药学院植物标本库(No. SC0875)。
1 提取与分离破布木干燥果实36 kg, 粉碎过筛, 用85%的乙醇室温浸提(6×20 L, 每次7天), 合并多次提取液, 减压浓缩至无醇味即得浸膏5.92 kg。将浸膏加5倍体积热水分散后, 依次用石油醚、乙酸乙酯、正丁醇萃取得到石油醚部位312 g、乙酸乙酯部位281 g、正丁醇部位794 g。取乙酸乙酯粗提物(270 g) 用大孔树脂柱色谱进行分离, 以水-乙醇梯度洗脱体积分数(10%→20%→30%→40%→45%→50%→60%→65%→75%→85%→90%→95%), 薄层色谱板检测合并得到7个组分Fr.B1~Fr.B7, 其中组分Fr.B1中出现结晶, 过滤得到单体化合物2 (1.85 g); Fr.B3和Fr.B4 (28.4 g) 合并用正相硅胶柱色谱(300~400目) 初步分离, 以二氯甲烷-甲醇梯度洗脱(100∶1→0∶1, v/v), 经TLC检测合并分为Fr.B3-1~Fr.B3-6共6个组分, 其中Fr.B3-2、Fr.B3-3中有结晶析出, 过滤得单体化合物3 (68.4 mg)、化合物4 (50.3 mg)。Fr.B3-2组分用凝胶柱色谱粗分, 以甲醇(加入0.1%甲酸) 洗脱, 合并得6个组分(Fr.B3-2-1~Fr.B3-2-6)。Fr.B3-2-3经半制备高效液相色谱[Silgreen C18柱, 乙腈-水10∶90→35∶65 (v/v), 4.0 mL·min-1, 40 min, 流动相含有0.1%的甲酸] 粗分为16个组分, 其中Fr.B3-2-3-1为纯化合物5 (6.8 mg), Fr.B3-2-3-13为新化合物1 (5.6 mg)。化合物1通过手性柱(CHIRALPAK IC柱, 正己烷-异丙醇82∶18 v/v, 1.0 mL·min-1, 100 min) 分离得到化合物1a (2.2 mg, tR = 39.3 min) 和1b (2.3 mg, tR = 45.9 min)。Fr.B3-2-3-15、Fr.B3-2-3-16经半制备高效液相色谱(Silgreen C18柱, 乙腈-水10∶90→35∶65 v/v, 4.0 mL·min-1, 40 min, 流动相含有0.1%的甲酸) (乙腈-水, 体积比10∶90→40∶60, 30 min) 分离得到化合物6 (10.3 mg)、7 (3.9 mg)。Fr.B3-2-3-6经正向色谱(YMC-Pack NH2柱, 正己烷-正己烷/异丙醇, 1∶1), 体积比60∶40→0∶100, 30 min) 分离得到化合物8 (3.5 mg)、9 (1.4 mg)、10 (1.0 mg)。
2 结构鉴定化合物2 白色针状晶体; ESI-MS: m/z 182 [M+H]+, 其分子式为C9H10O4; 1H NMR (600 MHz, CD3OD) δH 7.07 (2H, d, J = 8.5 Hz, H-3', H-5'), 6.70 (2H, d, J = 8.5 Hz, H-2', H-6'), 4.27 (1H, dd, J = 7.8, 4.4 Hz, H-2), 2.99 (1H, dd, J = 14.0, 4.4 Hz, H-3a), 2.81 (1H, dd, J = 14.0, 7.8 Hz, H-3b); 13C NMR (150 MHz, CD3OD) δC 175.8 (C-1), 155.6 (C-4′), 130.1 (C-3′, C-5′), 128.1 (C-1′), 114.5 (C-2′, C-6′), 71.6 (C-2), 39.4 (C-3)。以上数据与文献[5]报道基本一致, 确定化合物2为(S)-2-羟基-3-(4′-羟基苯) 丙酸。
化合物3 无色针状晶体; ESI-MS: m/z 169 [M+H]+, 其分子式为C8H8O4; 1H NMR (600 MHz, CD3OD) δH 7.55 (2H, m, H-2, 6), 6.84 (1H, d, J = 8.7 Hz, H-5), 3.89 (3H, s); 13C NMR (150 MHz, CD3OD) δC 170.0 (C-7), 152.6 (C-4), 148.6 (C-3), 125.2 (C-6), 123.0 (C-1), 115.8 (C-2), 113.7 (C-5), 56.3 (-OCH3)。以上数据与文献[6]报道基本一致, 确定化合物3为香草酸。
化合物4 白色无定形粉末; ESI-MS: m/z 163 [M-H]-, 其分子式为C9H8O3; 1H NMR (600 MHz, CD3OD) δH 7.60 (1H, d, J = 15.9 Hz, H-β), 7.45 (2H, d, J = 8.6 Hz, H-2, 6), 6.81 (2H, d, J = 8.6 Hz, H-3, 5), 6.28 (1H, d, J = 15.9 Hz, H-α); 13C NMR (150 MHz, CD3OD) δC 171.0 (C=O), 161.1 (C-4), 146.6 (C-β), 131.0 (C-3, 5), 127.2 (C-1), 116.7 (C-2, 6), 115.5 (C-α)。以上数据与文献[7]报道基本一致, 确定化合物4为对香豆素酸。
化合物5 褐色油状物; ESI-MS: m/z 195 [M-H]-, 其分子式为C10H12O4; 1H NMR (600 MHz, CD3OD) δH 7.58 (1H, dd, J = 8.2, 1.9 Hz, H-2'), 7.55 (1H, d, J = 1.9 Hz, H-6'), 6.86 (1H, d, J = 8.2 Hz, H-5'), 3.94 (2H, t, J = 6.2 Hz, H-3), 3.91 (3H, s, 3'-OCH3), 3.16 (2H, t, J = 6.2 Hz, H-2); 13C NMR (150 MHz, CD3OD) δC 199.6 (C-1), 153.3 (C-4'), 149.0 (C-3'), 130.6 (C-1'), 124.7 (C-6'), 115.7 (C-5'), 111.8 (C-2'), 58.9 (C-3), 56.3 (3'-OCH3), 41.6 (C-2)。以上数据与文献[8]报道基本一致, 确定化合物5为3-羟基-1-(4-羟基-3-甲氧基苯基)-1-丙酮。
化合物6 无色片状晶体; ESI-MS: m/z 121 [M-H]-, 其分子式为C7H6O2; 1H NMR (600 MHz, CD3OD) δH 8.12 (2H, dd, J = 8.3, 1.2 Hz, H-2, 6), 7.62 (1H, t, J = 7.4 Hz, H-4), 7.48 (2H, t, J = 6.4 Hz, H-3, 8); 13C NMR (150 MHz, CD3OD) δC 171.1 (C-COOH), 133.9 (C-4), 130.3 (C-2, 6), 129.3 (C-1), 128.6 (C-3, 5)。以上数据与文献[9]报道基本一致, 确定化合物6为苯甲酸。
化合物7 浅黄色柱状晶体; ESI-MS: m/z 149 [M-H]-, 其分子式为C10H12O; 1H NMR (600 MHz, CD3OD) δH 7.89 (2H, d, J = 8.8 Hz, H-2, 6), 6.83 (2H, d, J = 8.8 Hz, H-3, 5), 2.97 (2H, q, J = 7.3 Hz, H-2'), 1.16 (3H, t, J = 7.3 Hz, H-3'); 13C NMR (150 MHz, CD3OD) δC 202.1 (C-1'), 163.7 (C-4), 131.7 (C-2, 6), 129.8 (C-1), 116.2 (C-3, 5), 32.1 (C-2'), 8.9 (C-3')。以上数据与文献[10]报道基本一致, 确定化合物7为对羟基苯丙酮。
化合物8 白色针状晶体; ESI-MS: m/z 137 [M+H]+, 其分子式为C8H8O2; 1H NMR (600 MHz, CD3OD) δH 7.89 (2H, d, J = 8.7 Hz, H-2, 6), 6.84 (2H, d, J = 8.7 Hz, H-3, 5), 2.53 (3H, s, H-2'); 13C NMR (150 MHz, CD3OD) δC 199.4 (C-1'), 164.0 (C-1), 132. 1 (C-2, 6), 130.1 (C-4), 116.2 (C-3, 5), 26.2 (C-2')。以上数据与文献[11]报道基本一致, 确定化合物8为对羟基苯乙酮。
化合物9 白色针状晶体; ESI-MS: m/z 371 [M+Na]+, 其分子式为C18H20O7; 1H NMR (600 MHz, CD3OD) δH 7.63 (1H, dd, J = 8.3, 2.0 Hz, H-6), 7.58 (1H, d, J = 1.9 Hz, H-2), 6.81 (1H, d, J = 8.3 Hz, H-5), 4.75 (1H, dd, J = 8.7, 5.2 Hz, H-α), 4.25 (1H, dd, J = 10.6, 8.7 Hz, H-β), 3.87 (3H, s, 3-OCH3), 3.81 (6H, s, 3'-OCH3, 5'-OCH3), 3.72 (1H, dd, J = 10.7, 5.2 Hz, H-β); 13C NMR (150 MHz, CD3OD) δC 199.5 (C=O), 153.2 (C-4), 149.5 (C-5′), 149.5 (C-3′), 148.9 (C-3), 135.9 (C-4′), 130.3 (C-1'), 129.1 (C-1), 125.2 (C-6), 115.7 (C-5), 112.5 (C-2), 106.6 (C-6′), 65.5 (C-β), 56.7 (5'-OCH3), 56.7 (3'-OCH3), 56.5 (3-OCH3), 56.3 (C-α)。以上数据与文献[12]报道基本一致, 确定化合物9为5′-甲氧基楝叶吴萸素B。
化合物10 无色针状晶体; ESI-MS: m/z 153 [M+H]+, 其分子式为C8H8O3; 1H NMR (600 MHz, CD3OD) δH 9.75 (1H, s, CHO), 7.45 (1H, m, H-5, 6), 6.94 (1H, d, J = 8.0 Hz, H-2), 3.92 (3H, s, OCH3); 13C NMR (150 MHz, CD3OD) δC 192.8 (-CHO), 154.9 (C-4), 149.7 (C-3), 130.5 (C-1), 127.9 (C-5), 116.3 (C-2), 111.2 (C-6), 56.3 (OCH3)。以上数据与文献[13]报道基本一致, 确定化合物10为香草醛。
作者贡献: 杨新洲和庞克坚负责实验设计; 魏沣负责实验实施以及文章的撰写; 邓憬童和程海涛完成数据分析; 杨新洲和庞克坚负责文章的审阅和提出论文写作的建议, 并最终定稿。
利益冲突: 作者声明无利益冲突。
| [1] |
Huang XS, Huang YG, Chen XX. Research advances of Cordia dichotoma Forst. f. fruits[J]. J Med Pharm Chin Minor (中国民族医药杂志), 2016, 22: 55-57. |
| [2] |
Zeng XL, Liu MM, Dai ZP, et al. Study on the examination, efficacy and compounding of Cordia dichotoma Forst. f. Fruits[J]. Chin Pharm (中国药房), 2018, 29: 2149-2151. |
| [3] |
The Chinese Academy of Sciences. Flora of China (中国植物志: 第64卷: 第2分册)[M]. Vol 64. Division 2. Beijing: Sciences Press, 1989: 7-9.
|
| [4] |
Chinese Pharmacopoeia Commission. The Pharmaceutical Standards of Sanitary Ministry of People's Republic of China (中华人民共和国卫生部药品标准)[S]. Urumqi: Xinjiang Health Technology Press, 1999: 85.
|
| [5] |
Ke YY, Tsai CH, Yu HM, et al. Latifolicin in A from a fermented soymilk product and the structure-activity relationship of synthetic analogues as inhibitors of breast cancer cell growth[J]. J Agric Food Chem, 2015, 63: 9715-9721. DOI:10.1021/acs.jafc.5b04028 |
| [6] |
Kong LY, Li X, Pei YH, et al. Isolation and structure elucidation of Baihuaqianhuoside and Pd-C-I from Peucedanum praeruptorum[J]. Acta Pharm Sin (药学学报), 1994, 29: 276-280. |
| [7] |
Peng WW, Song WW, Huang MB, et al. Twelve benzene derivatives from Clausena excavata[J]. Acta Pharm Sin (药学学报), 2014, 49: 1689-1693. |
| [8] |
Peng W, Han T, Liu QC, et al. Chemical constituents from aerial part of Atractylodes macrocephala[J]. China J Chin Mater Med (中国中药杂志), 2011, 36: 578-581. |
| [9] |
Tan GY, Zhang CF, Zhang M. Chemical constituents of the roots of wild Stemona sessilifolia[J]. J Chin Pharm Univ (中国药科大学学报), 2007, 38: 499-501. |
| [10] |
Liu X, Yin CL, Cao Y, et al. Chemical constituents from Gueldenstaedtia verna and their anti-inflammatory activity[J]. Nat Prod Res, 2018, 32: 1145-1149. DOI:10.1080/14786419.2017.1320795 |
| [11] |
Zhang L, Li DL, Chen YC, et al. Study on secondary metabolites of marine Fungus Penicillium sp. FS60 from the south China sea[J]. J Chin Med Mater (中药材), 2012, 35: 1091-1094. |
| [12] |
Chen JJ, Yang CS, Peng CF, et al. Dihydroagarofuranoid sesquiterpenes, a lignan derivative, a benzenoid, and antitubercular constituents from the stem of Microtropis japonica[J]. J Nat Prod, 2008, 71: 1016-1021. DOI:10.1021/np800097t |
| [13] |
Du JL, Jin YS, Qiao LM, et al. Chemical investigation of Ervatamia yunnanensis[J]. Chem Nat Compd, 2010, 46: 459-461. DOI:10.1007/s10600-010-9644-z |
 2022, Vol. 57
2022, Vol. 57


