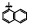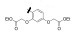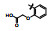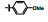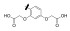作者贡献:杨继是本文的第一作者, 负责化学合成和生物活性测试; 董国强是本文的第二作者, 负责计算机辅助药物设计相关研究; 刘娜、盛春泉是本文的通讯作者, 负责实验设计和把关, 并指导整个研究、稿件修改等工作。
利益冲突:本文的研究内容无任何利益冲突。
2. 中国人民解放军海军军医大学药学院, 上海 200433
2. School of Pharmacy, Second Military Medical University, Shanghai 200433, China
近年来, 侵袭性真菌感染(invasive fungal infections, IFIs)的发病率和死亡率逐年增高[1], 安全有效的抗真菌药物却十分有限。目前, 临床上用于治疗侵袭性真菌感染的药物主要包括多烯类(两性霉素B)、三唑类(氟康唑、伏立康唑、伊曲康唑等)、棘白菌素类(卡泊芬净、米卡芬净)和核酸类(5-氟胞嘧啶)[2], 但这些抗真菌药存在肝肾毒性、耐药性严重和口服生物利用度差等问题[3]。因此, 迫切需要研发全新结构类型和全新作用机制的抗真菌新药。
侵袭性真菌感染的主要致病菌包括念珠菌、曲霉菌和隐球菌[4]。其中, 白念珠菌是发病率最高的致病真菌[5]。分泌型天冬氨酸蛋白酶(secreted aspartyl proteinase, SAP)是白念珠菌分泌的一种蛋白酶, 是白念珠菌致病的重要毒力因子。SAP参与入侵宿主细胞、破坏宿主免疫系统、裂解各种免疫因子的过程, 进而损害宿主免疫应激反应、抵御抗菌药物[6]。因此, 抑制真菌SAP, 可有效降低真菌的致病能力。而靶向真菌毒力因子SAP, 有可能成为抗真菌药物研发的新策略。目前, 研究人员已发现SAP家族的10个成员(SAP1~10)[7], 分子质量介于35~50 kDa之间, 在宿主不同部位、不同感染阶段具有差异性的表达[8]。其中, SAP2与抑制剂的晶体三维结构复合物已被测定, 是SAP家族中最有潜力的药物靶点[9, 10]。目前, 关于SAP抑制剂的研究仍处于起步阶段, 还没有进入临床研究的候选药物。
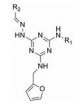
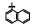
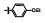
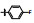
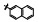
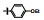
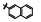
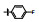
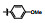
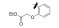
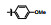
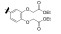
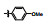
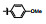
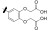
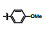
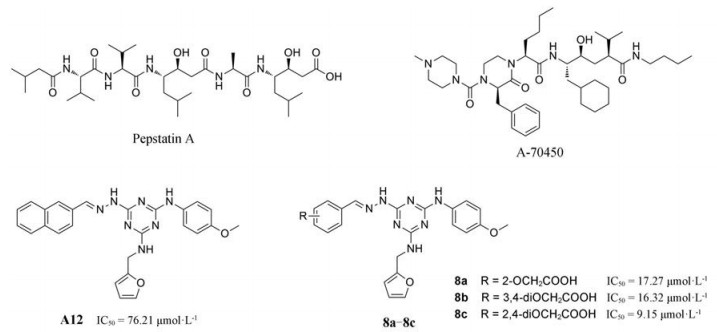
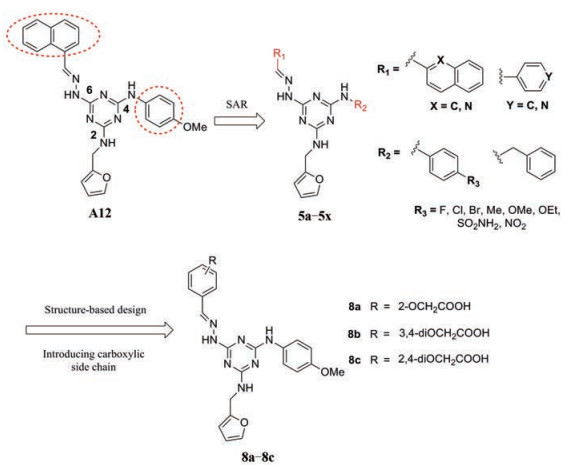
早期的SAP2抑制剂主要是天然的肽类和拟肽类, 因其活性、选择性或体内代谢性质不佳等缺点没有新药研发的价值。课题组前期通过虚拟筛选和结构优化发现了一类非肽类噻唑酮小分子SAP2抑制剂, 为小分子SAP2抑制剂的研究开辟了新的方向[7]。本研究基于前期通过虚拟筛选和抑酶活性测试发现的三嗪类SAP2抑制剂A12 (IC50 = 77.18 μmol·L-1)进行合理设计和结构优化, 设计并合成了27个新型三嗪类衍生物, 并对其进行抑酶活性测试和探讨构效关系。获得了3个高活性的化合物8a~8c, 并对其进行毒力因子相关的活性研究和体内活性评价(图 1)。
|
Figure 1 Chemical structures of peptidic secreted aspartyl proteinase 2 (SAP2) inhibitors and novel triazine SAP2 inhibitors |
|
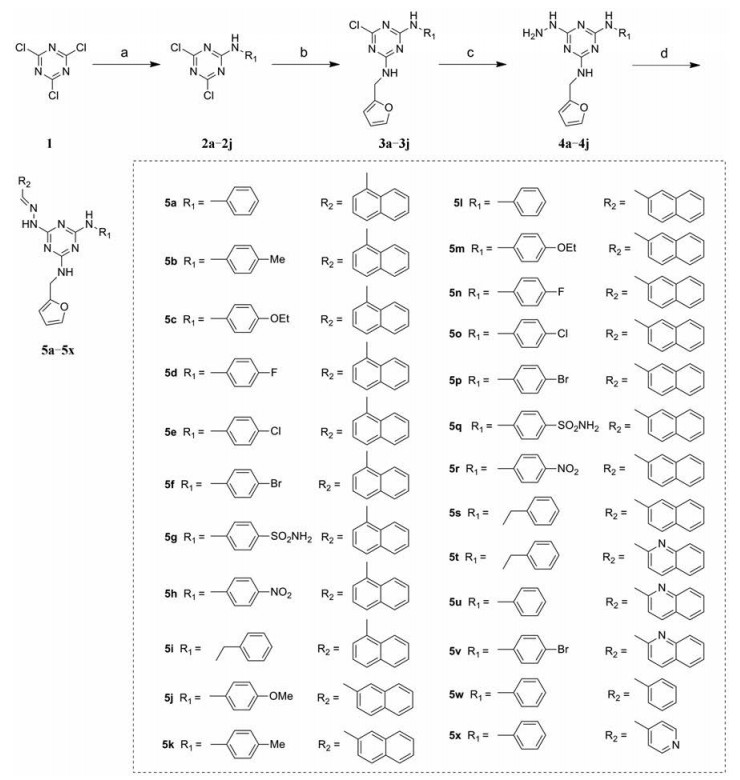
Scheme 1 Synthetic route of target compounds 5a-5x. Reagents and conditions: (a) Substituted aniline or benzylamine, acetone, 0 ℃, 4 h, 63%-92%; (b) Furan-2-ylmethanamine, THF, 5% aqueous Na2CO3, rt, 12 h, 81%-95%; (c) CH2Cl2, reflux, 12 h, 63%-90%; (d) Various aldehyde, toluene, reflux, 3 h, 40%-82% |
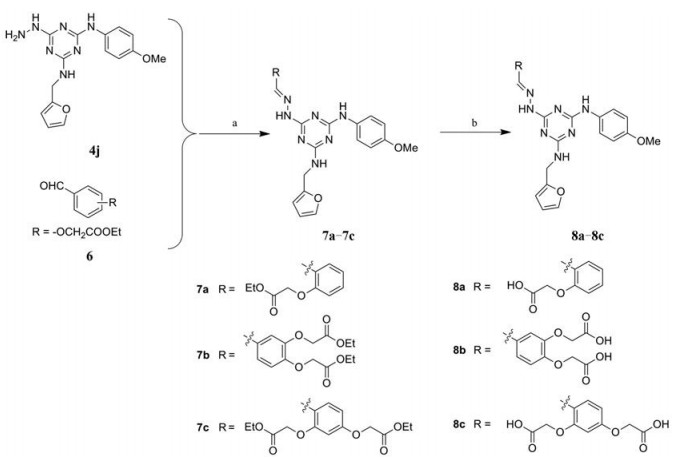
以2, 4, 6-三氯-1, 3, 5-三嗪(1)为起始原料, 与取代的苯胺或苄胺在丙酮中反应得到单取代的产物2a~2j。弱碱性条件下与呋喃-2-基甲胺进一步反应, 得到二取代的中间体3a~3j。与过量的肼反应得到中间体4a~4j, 中间体4a~4j与各种醛反应获得目标化合物5a~5x (合成路线1)。中间体4j与含有单酯或二酯侧链的各种醛反应, 碱性条件下酯基水解, 得到具有羧酸侧链的目标化合物8a~8c (合成路线2)。所有目标化合物经1H NMR、13C NMR和ESI-MS确证其结构, 数据见实验部分。
结果与讨论 1 三嗪类SAP2抑制剂的构效关系三嗪类化合物A12是一个活性中等的SAP2抑制剂(IC50 = 77.18 μmol·L-1), 其构效关系初步探索结果如下: ①在C4侧链的苯基上引入了卤素、烷基、NO2和SO2NH2等取代基。SAP2抑制活性测试结果表明, 甲氧基取代时活性最优, 乙氧基取代活性略有下降; 吸电子基团取代后活性降低明显, 在100 μmol·L-1的浓度下抑制率低于50%;当苯基被苄基取代时, 同样活性下降明显, 在100 μmol·L-1下抑制率为36%。②将C6位侧链中的1-萘基用2-萘基、2-喹啉基、苯基或吡啶基取代后均导致活性显著降低。③在C4位苄基取代和C6位2-喹啉基取代的化合物5t对SAP2的抑制活性有所保持(IC50值为41.67 μmol·L-1, 图 2, 表 1)。
|
Figure 2 Design rationale of the triazine SAP2 inhibitors |
| Table 1 SAP2 inhibitory activity of the thiazolidinone inhibitors. nd = Not determined |
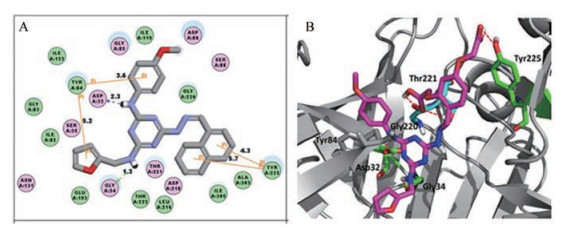
分析先导化合物A12与靶酶之间的结合模式, C6侧链位于S2口袋中, 萘基与Ala303和Ile305形成疏水相互作用, 与Tyr225形成π-π相互作用(图 3A)。
|
Figure 3 Binding modes of the triazine SAP2 inhibitors. (A) Schematic representation of the proposed interactions between lead compound A12 and C. albicans SAP2; (B) Proposed binding pose of inhibitor 8c in the active site of SAP2. The inhibitors are shown in the stick format and hydrogen bonds are shown in dotted red lines. The figures are generated using PyMol (http://pymol.souceforge, net/) |
为了与S2/S3口袋形成氢键相互作用, 设计并合成了带有单或双羧基侧链的苯基来取代萘基(8a~8c)。上述化合物(8a~8c)的抑酶活性显著提高, 100 μmol·L-1下抑制率均为100%, IC50分别为17.27、16.32和9.15 μmol·L-1, 验证了设计策略的合理性。构效关系分析表明, 二羧基取代的化合物(8b、8c)活性优于单羧取代的化合物(8a)。而2, 4-位取代(8c)活性优于3, 4-位取代(8b)。酯基取代类似物(7a~7c)对SAP2无抑制活性, 进一步证实了羧基的重要性(图 2, 表 1)。
化合物8c与SAP2的对接结果显示, 8c与SAP2活性位点的结合模式与先导化合物A12相似。化合物8c的1, 3, 5-三嗪基团位于S1、S2、S1'和S2'口袋的中央位置, C4侧链通过与Tyr84的芳香π-π相互作用而定位于S1口袋。此外, C4胺基与催化残基Asp32形成氢键。C2侧链位于S2'的口袋中, 该口袋与Ile82形成疏水相互作用, 与Gly34形成氢键相互作用。C6侧链的末端苯基与S2口袋中的Ile305形成疏水相互作用。值得注意的是, 两个羧基分别与Gly220、Thr221和Tyr225形成了3个氢键, 对提高SAP2抑制活性具有重要作用(图 3B)。
|
Scheme 2 Synthesis of 8a-8c. Reagents and conditions: (a) Various aldehyde, toluene, reflux, 6 h, 66%-78%; (b) LiOH, THF-MeOH- H2O = 3:2:1, rt, 1 h, 43%-59% |
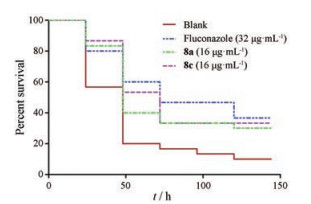
SAP2是真菌的毒力因子, 在真菌侵入宿主和致病过程中发挥重要作用。抑制SAP2不影响真菌细胞的生长繁殖。在体外抗真菌活性实验中, 化合物A12、8a~8c均无活性(MIC > 64 μg·mL-1), 这与SAP2的作用机制一致。因此, 本研究采用念珠菌感染的秀丽隐杆线虫体内模型来评估SAP2抑制剂的抗真菌活性。结果显示, 化合物8a、8c均显示出优秀的体内抗真菌活性:在16 μg·mL-1浓度下, 线虫的生存率与对照药氟康唑组(32 μg·mL-1)相当(图 4)。
|
Figure 4 Kaplan-Meier survival curves of C. elegans with candidiasis treated with compounds 8a, 8c and fluconazole |
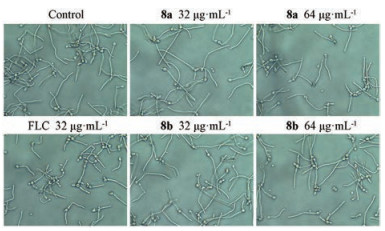
菌丝作为白念珠菌的重要毒力因子, 使真菌细胞更具有黏附和侵袭宿主的能力, 并有助于逃脱宿主免疫系统的攻击[11]。如果能有效抑制白念珠菌菌丝的形成, 则可控制其感染能力。将化合物8a、8b作用于白念珠菌敏感菌C. alb. 5314菌丝生成阶段, 考察化合物对菌丝生成的抑制作用。测试结果显示, 化合物8a、8b在高浓度下均不能抑制菌丝的生长, 而相同浓度的氟康唑可以抑制部分真菌细胞的菌丝生成。该结果表明, SAP2抑制剂对于菌丝生成没有明显抑制作用(图 5)。
|
Figure 5 Inhibitory effect of compounds 8a, 8b and fluconazole (FLC) on hypha of C. albicans |
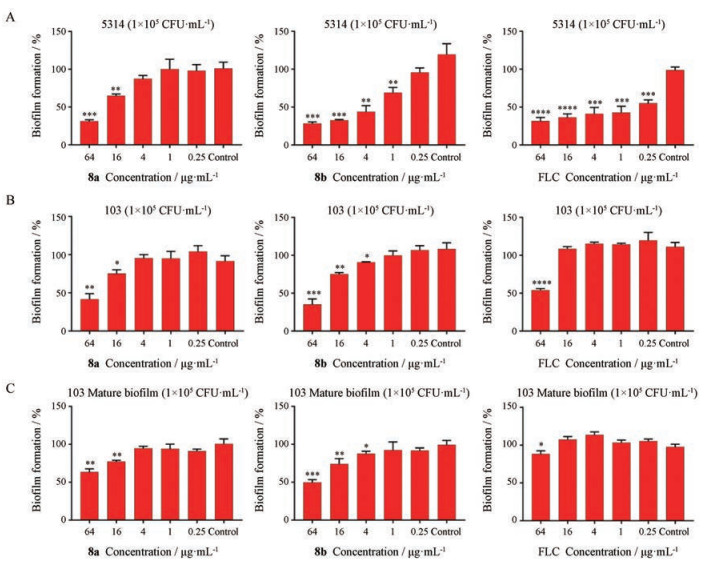
生物被膜是真菌感染的重要致病因素。真菌的耐药程度与生物膜的形成有关, 生物膜越成熟, 真菌的耐药性就越强[12, 13]。将化合物8a、8b作用于白念珠菌敏感菌C.alb. 5314和白念珠菌耐药菌C. alb. 103的被膜生成阶段, 考察目标化合物对被膜形成的抑制作用。测试结果表明, 对于白念珠菌敏感菌5314, 化合物8a在64 μg·mL-1浓度下, 被膜形成抑制率超过70%;化合物8b在16 μg·mL-1时被膜形成抑制率为70%, 与阳性对照药氟康唑相当(图 6A)。对于白念珠菌耐药菌103, 化合物8a、8b在64 μg·mL-1浓度下, 被膜形成抑制率为60%, 优于同浓度氟康唑的活性(图 6B)。
|
Figure 6 (A) Inhibitory effect of compounds 8a, 8b and FLC on C. alb. 5314 biofilm formation. (B) Inhibitory effect of compounds 8a, 8b and FLC on C. alb.103 biofilm formation. (C) Destructive effect of compounds 8a, 8b and FLC on C. alb.103 mature biofilm |
将化合物8a、8b作用于白念珠菌耐药菌C. alb. 103已形成的成熟被膜, 测定化合物对成熟被膜的破坏作用。结果显示, 阳性对照药氟康唑在64 μg·mL-1浓度下, 成熟被膜破坏率仅为10%;化合物8a在64 μg·mL-1时能够破坏40%已形成的成熟被膜; 化合物8b在64 μg·mL-1时能够破坏50%已形成的成熟被膜, 活性明显优于对照药氟康唑(图 6C)。
6 小结综上所述, 本研究基于前期发现的新型三嗪类SAP2小分子抑制剂, 对其进行结构优化和构效关系研究。通过基于结构的合理设计, 显著提高了先导化合物对SAP2的抑制活性。通过分子对接验证了结合模式和药物设计策略。特别是化合物8a和8c, 显示出优秀的抗生物被膜和体内抗真菌治疗效果, 是具有研究前景的新型抗真菌化合物。本研究为小分子SAP2抑制剂的进一步探索及其结构优化研究提供了新的思路。
实验部分核磁共振仪为Bruker 300型、400型、500型和600型, TMS为内标, CDCl3或DMSO-d6为溶剂。在API-3000LC-MS型质谱仪上完成ESI质谱。Biotage快速制备色谱(香港环球分析测试仪器有限公司)。显微熔点测定仪XT4A (温控型, 北京市科仪电光仪器厂)。TLC分析在硅胶板上进行(GF254, 中国青岛海洋化学)。硅胶柱色谱硅胶(60 G, 中国青岛海洋化学)。商品化溶剂皆为市售分析纯或化学纯。
1 化合物合成 1.1 4, 6-二氯-N-苯基-1, 3, 5-三嗪-2-胺(2a)的合成将2, 4, 6-三氯-1, 3, 5-三嗪(1) (9.22 g, 50 mmol, 1 equiv)溶解于30 mL丙酮中, 冰浴搅拌至0 ℃。缓缓滴加溶有苯胺(4.66 g, 50 mmol, 1 equiv)丙酮溶液20 mL。在冰浴下继续搅拌反应2 h, 之后室温反应2 h。反应结束后, 加入冰水20 mL。待固体析出完全后, 抽滤, 得到白色固体10.85 g, 收率: 90%。1H NMR (300 MHz, DMSO-d6) δ: 11.12 (s, 1H, NH), 7.69 (d, 2H, J = 2.36, 7.95 Hz), 7.36 (d, 2H, J = 8.35 Hz), 7.16 (t, 1H, J = 7.40 Hz); ESI-MS (m/z): 239.24 [M-1]。
化合物2b~2j的制备方法与化合物2a相同。部分中间体化合物质谱确证后直接进行下一步反应。
4, 6-二氯-N-(4-甲苯基)-1, 3, 5-三嗪-2-胺(2b), 白色固体, 收率: 92%。1H NMR (300 MHz, DMSO-d6) δ: 11.06 (s, 1H, NH), 7.45 (dd, 2H, J = 2.36, 8.71 Hz), 7.17 (d, 2H, J = 8.32 Hz), 2.26 (s, 3H); ESI-MS (m/z): 255.39 [M+1]。
4, 6-二氯-N-(4-乙氧苯基)-1, 3, 5-三嗪-2-胺(2c), 白色固体, 收率: 65%。1H NMR (600 MHz, DMSO-d6) δ: 10.97 (s, 1H, NH), 7.45 (d, 2H, J = 9.02 Hz), 7.17 (dd, 2H, J = 2.18, 6.90 Hz), 4.01 (dd, 2H, J = 6.97, 13.94 Hz), 1.32 (t, 3H, J = 6.97 Hz); ESI-MS (m/z): 285.46 [M+1]。
4, 6-二氯-N-(4-磺酰胺苯基)-1, 3, 5-三嗪-2-胺(2g), 白色固体, 收率: 82%。1H NMR (300 MHz, DMSO-d6) δ: 10.90 (s, 1H, NH), 7.71~7.85 (m, 4H), 7.69 (s, 2H, NH2); ESI-MS (m/z): 318.20 [M-1]。
4, 6-二氯-N-苄基-1, 3, 5-三嗪-2-胺(2i), 白色固体, 收率: 78%。1H NMR (600 MHz, DMSO-d6) δ: 11.07 (s, 1H, NH), 7.34 (d, 2H, J = 6.80 Hz), 7.31 (d, 2H, J = 6.80 Hz), 7.28 (t, 1H, J = 7.0 Hz), 4.54 (s, 2H); ESI-MS (m/z): 253.05 [M-1]。
4, 6-二氯-N-(4-甲氧苯基)-1, 3, 5-三嗪-2-胺(2j), 白色固体, 收率: 88%。1H NMR (600 MHz, DMSO-d6) δ: 10.96 (s, 1H, NH), 7.45 (d, 2H, J = 9.07 Hz), 7.17 (dd, 2H, J = 2.25, 6.85 Hz), 3.74 (s, 3H); ESI-MS (m/z): 269.19 [M-1]。
1.2 6-氯-N2-(呋喃-2-基甲基)-N4-苯基-1, 3, 5-三嗪-2, 4-二胺(3a)的合成将4, 6-二氯-N-苯基-1, 3, 5-三嗪-2-胺(2a) (2.41 g, 10 mmol, 1 equiv)溶解于30 mL四氢呋喃中, 加入2-呋喃甲胺(0.92 mL, 10 mmol, 1 equiv)及5%的Na2CO3溶液30 mL, 室温搅拌反应12 h, 过滤反应析出固体, 水洗2~5次, 得到白色固体2.81 g, 收率: 93%。1H NMR (300 MHz, DMSO-d6) δ: 10.07 (br s, 1H, NH), 8.59 (br s, 1H, NH), 7.49~7.81 (m, 3H), 7.19~7.38 (m, 2H), 7.02 (t, 1H, J = 7.18 Hz), 6.31~6.48 (m, 1H), 6.15~6.30 (m, 1H), 4.48 (d, 2H, J = 5.05 Hz); ESI-MS (m/z):302.49 [M+1]。
化合物3b~3j的制备方法与化合物3a相同。
6-氯-N2-(呋喃-2-基甲基)-N4-(4-甲苯基)-1, 3, 5-三嗪-2, 4-二胺(3b), 白色固体, 收率: 95%。1H NMR (300 MHz, DMSO-d6) δ: 10.05 (br s, 1H, NH), 8.60 (br s, 1H, NH), 7.37~7.67 (m, 3H), 7.08 (d, 2H, J = 8.32 Hz), 6.33~6.43 (m, 1H), 6.17~6.31 (m, 1H), 4.45 (d, 2H, J = 5.68 Hz), 2.23 (s, 3H); ESI-MS (m/z): 316.36 [M+1]。
6-氯-N2-(呋喃-2-基甲基)-N4-(4-乙氧苯基)-1, 3, 5-三嗪-2, 4-二胺(3c), 白色固体, 收率: 81%。1H NMR (600 MHz, DMSO-d6) δ: 9.96 (br s, 1H, NH), 8.54 (br s, 1H, NH), 7.31~7.71 (m, 3H), 6.87 (d, 2H, J = 9.06 Hz), 6.35~6.45 (m, 1H), 6.20~6.33 (m, 1H), 4.46 (d, 2H, J = 5.86 Hz), 3.99 (dd, 2H, J = 6.96, 13.92 Hz), 1.31 (t, 3H, J = 6.87 Hz); ESI-MS (m/z): 346.47 [M+1]。
6-氯-N2-(呋喃-2-基甲基)-N4-(4-氟苯基)-1, 3, 5-三嗪-2, 4-二胺(3d), 白色固体, 收率: 89%。1H NMR (600 MHz, DMSO-d6) δ: 10.08 (br s, 1H, NH), 8.61 (br s, 1H, NH), 7.54~7.90 (m, 3H), 7.06~7.20 (m, 2H), 6.35~6.46 (m, 1H), 6.17~6.32 (m, 1H), 4.49 (s, 2H); ESI-MS (m/z): 320.37 [M+1]。
6-氯-N2-(呋喃-2-基甲基)-N4-(4-氯苯基)-1, 3, 5-三嗪-2, 4-二胺(3e), 白色固体, 收率: 83%。1H NMR (300 MHz, DMSO-d6) δ: 10.23 (br s, 1H, NH), 8.89 (br s, 1H, NH), 7.52~7.87 (m, 3H), 7.24~7.43 (m, 2H), 6.34~6.43 (m, 1H), 6.20~6.31 (m, 1H), 4.47 (d, 2H, J = 5.46 Hz); ESI-MS (m/z): 336.48 [M+1]。
6-氯-N2-(呋喃-2-基甲基)-N4-(4-溴苯基)-1, 3, 5-三嗪-2, 4-二胺(3f), 白色固体, 收率: 92%。1H NMR (300 MHz, DMSO-d6) δ: 10.16 (br s, 1H, NH), 8.89 (br s, 1H, NH), 7.53~7.83 (m, 3H), 7.35~7.51 (m, 2H), 6.33~6.42 (m, 1H), 6.19~6.31 (m, 1H), 4.47 (s, 2H); ESI-MS (m/z): 382.29 [M+1]。
6-氯-N2-(呋喃-2-基甲基)-N4-(4-磺酰胺苯基)-1, 3, 5-三嗪-2, 4-二胺(3g), 白色固体, 收率: 81%。1H NMR (300 MHz, DMSO-d6) δ: 10.45 (br s, 1H, NH), 8.76 (br s, 1H, NH), 7.65~8.07 (m, 4H), 7.59 (s, 1H), 7.24 (s, 2H, NH2), 6.35~6.66 (m, 1H), 6.22~6.33 (m, 1H), 4.50 (d, 2H, J = 5.37 Hz); ESI-MS (m/z): 381.33 [M+1]。
6-氯-N2-(呋喃-2-基甲基)-N4-(4-硝基苯基)-1, 3, 5-三嗪-2, 4-二胺(3h), 白色固体, 收率: 86%。1H NMR (600 MHz, DMSO-d6) δ: 10.73 (br s, 1H, NH), 8.84 (br s, 1H, NH), 8.13~8.26 (m, 2H), 7.91~8.08 (m, 2H), 7.61 (s, 1H), 6.38~6.44 (m, 1H), 6.30~6.36 (m, 1H), 4.55 (d, 2H, J = 5.74 Hz); ESI-MS (m/z): 347.31 [M+1]。
6-氯-N2-(呋喃-2-基甲基)-N4-苄基-1, 3, 5-三嗪-2, 4-二胺(3i), 白色固体, 收率: 89%。1H NMR (600 MHz, DMSO-d6) δ: 9.44 (br s, 1H, NH), 8.07~8.47 (m, 1H, NH), 7.55 (d, 2H, J = 13.76 Hz), 8.36~8.19 (m, 4H), 6.22~6.42 (m, 1H), 6.09~6.12 (m, 1H), 4.36~4.50 (m, 4H); ESI-MS (m/z): 316.36 [M+1]。
6-氯-N2-(呋喃-2-基甲基)-N4-(4-甲氧苯基)-1, 3, 5-三嗪-2, 4-二胺(3j), 白色固体, 收率: 86%。1H NMR (600 MHz, DMSO-d6) δ: 9.94 (br s, 1H, NH), 8.52 (br s, 1H, NH), 7.38~7.74 (m, 3H), 6.87 (d, 2H, J = 9.04 Hz), 6.32~6.43 (m, 1H), 6.18~6.31 (m, 1H), 4.45 (s, 2H), 3.71 (s, 3H); ESI-MS (m/z): 332.46 [M+1]。
1.3 N2-(呋喃-2-基甲基)-6-肼基-N4-苯基-1, 3, 5-三嗪-2, 4-二胺(4a)的合成将6-氯-N2-(呋喃-2-基甲基)-N4-苯基-1, 3, 5-三嗪-2, 4-二胺(3a) (1.51 g, 5 mmol, 1 equiv)溶解于50 mL二氯甲烷中, 加肼(0.64 mL, 20 mmol, 4 equiv)回流搅拌反应12 h。反应结束后, 分别用水50 mL、饱和NaCl溶液50 mL×2洗涤, 无水硫酸钠干燥, 溶液加入石油醚100 mL, 过滤析出固体, 得到白色固体0.99 g, 收率: 67%。1H NMR (300 MHz, DMSO-d6) δ: 9.03 (br s, 1H, NH), 7.92 (br s, 1H, NH), 7.46~7.83 (m, 3H), 7.24~7.44 (br s, 2H, NHNH2), 7.19 (t, 2H, J = 7.92 Hz), 6.88 (t, 1H, J = 7.07 Hz), 6.30~6.44 (m, 1H), 6.12~6.29 (m, 1H), 4.46 (d, 2H, J = 5.21 Hz), 4.21 (br s, 1H, NHNH2); ESI-MS (m/z): 298.33 [M+1]。
化合物4b~4j的制备方法与化合物4a相同。
N2-(呋喃-2-基甲基)-6-肼基-N4-(4-甲苯基)-1, 3, 5-三嗪-2, 4-二胺(4b), 白色固体, 收率: 65%。1H NMR (300 MHz, DMSO-d6) δ: 8.95 (br s, 1H, NH), 7.91 (br s, 1H, NH), 7.48~7.72 (m, 3H), 7.27 (br s, 1H, NHNH2), 7.00 (d, 2H, J = 8.34 Hz), 6.32~6.40 (m, 1H), 6.15~6.30 (m, 1H), 4.45 (d, 2H, J = 5.07 Hz), 4.14 (s, 2H, NHNH2), 2.20 (s, 3H); ESI-MS (m/z): 312.51 [M+1]。
N2-(呋喃-2-基甲基)-6-肼基-N4-(4-乙氧苯基)-1, 3, 5-三嗪-2, 4-二胺(4c), 白色固体, 收率: 85%。1H NMR (600 MHz, DMSO-d6) δ: 8.86 (br s, 1H, NH), 7.88 (br s, 1H, NH), 7.47~7.71 (m, 3H), 7.22 (br s, 2H, NHNH2), 6.78 (d, 2H, J = 8.32 Hz), 6.34~6.39 (m, 1H), 6.16~6.29 (m, 1H), 4.46 (s, 2H), 4.22 (br s, 1H, NHNH2), 3.96 (dd, 2H, J = 6.91, 13.82 Hz), 1.29 (t, 3H, J = 6.91 Hz); ESI-MS (m/z): 342.52 [M+1]。
N2-(呋喃-2-基甲基)-6-肼基-N4-(4-氟苯基)-1, 3, 5-三嗪-2, 4-二胺(4d), 白色固体, 收率: 66%。1H NMR (600 MHz, DMSO-d6) δ: 9.09 (br s, 1H, NH), 8.01 (br s, 1H, NH), 7.50~7.86 (m, 3H), 7.30 (br s, 2H, NHNH2), 6.78 (d, 2H, J = 8.56 Hz), 6.35~6.40 (m, 1H), 6.17~6.32 (m, 1H), 4.47 (s, 2H), 4.23 (br s, 1H, NHNH2); ESI-MS (m/z): 316.29 [M+1]。
N2-(呋喃-2-基甲基)-6-肼基-N4-(4-氯苯基)-1, 3, 5-三嗪-2, 4-二胺(4e), 白色固体, 收率: 63%。1H NMR (300 MHz, DMSO-d6) δ: 9.21 (br s, 1H, NH), 8.05 (br s, 1H, NH), 7.50~7.89 (m, 3H), 7.32 (br s, 2H, NHNH2), 7.22 (d, 2H, J = 8.76Hz), 6.31~6.41 (m, 1H), 6.13~6.30 (m, 1H), 4.44 (d, 2H, J = 4.88 Hz), 4.19 (br s, 1H, NHNH2); ESI-MS (m/z): 332.37 [M+1]。
N2-(呋喃-2-基甲基)-6-肼基-N4-(4-溴苯基)-1, 3, 5-三嗪-2, 4-二胺(4f), 白色固体, 收率: 84%。1H NMR (300 MHz, DMSO-d6) δ: 9.22 (br s, 1H, NH), 8.02 (br s, 1H, NH), 7.51~7.86 (m, 3H), 7.35 (d, 2H, J = 8.61 Hz), 7.19 (br s, 2H, NHNH2), 6.31~6.40 (m, 1H), 6.15~6.30 (m, 1H), 4.44 (d, 2H, J = 5.17 Hz), 4.20 (br s, 1H, NHNH2); ESI-MS (m/z): 376.47 [M+1]。
N2-(呋喃-2-基甲基)-6-肼基-N4-(4-磺胺基苯基)-1, 3, 5-三嗪-2, 4-二胺(4g), 白色固体, 收率: 89%。1H NMR (300 MHz, DMSO-d6) δ: 9.46 (br s, 1H, NH), 8.16 (br s, 1H, NH), 7.83~8.02 (m, 2H), 7.63 (d, 2H, J = 8.87 Hz), 7.54 (s, 1H), 7.44 (br s, 1H, NHNH2), 6.45~7.29 (br s, 4H, NHNH2, NH2), 6.34~6.40 (m, 1H), 6.17~6.32 (m, 1H), 4.46 (d, 2H, J = 4.10 Hz); ESI-MS (m/z): 377.27 [M+1]。
N2-(呋喃-2-基甲基)-6-肼基-N4-(4-硝基苯基)-1, 3, 5-三嗪-2, 4-二胺(4h), 白色固体, 收率: 75%。1H NMR (600 MHz, DMSO-d6) δ: 9.83 (br s, 1H, NH), 8.25 (br s, 1H, NH), 7.96~8.21 (m, 4H), 7.57 (s, 1H), 7.20 (br s, 2H, NHNH2), 6.39 (s, 1H), 6.22~6.35 (m, 1H), 4.50 (d, 2H, J = 5.17 Hz), 4.34 (br s, 1H, NHNH2); ESI-MS (m/z): 343.34 [M+1]。
N2-(呋喃-2-基甲基)-6-肼基-N4-苄基-1, 3, 5-三嗪-2, 4-二胺(4i), 白色固体, 收率: 90%。1H NMR (600 MHz, DMSO-d6) δ: 8.14~8.49 (m, 1H, NH), 7.45~7.46 (m, 1H, NH), 7.16~7.36 (m, 5H), 7.11 (br s, 1H, NHNH2), 7.20 (br s, 2H, NHNH2), 6.36~6.42 (m, 1H), 5.99~6.26 (m, 1H), 4.34~4.51 (m, 4H), 4.27 (br s, 1H, NHNH2); ESI-MS (m/z): 312.23 [M+1]。
N2-(呋喃-2-基甲基)-6-肼基-N4-(4-甲氧苯基)-1, 3, 5-三嗪-2, 4-二胺(4j), 白色固体, 收率: 71%。1H NMR (600 MHz, DMSO-d6) δ: 8.87 (br s, 1H, NH), 7.84 (br s, 1H, NH), 7.49~7.71 (m, 3H), 7.20 (br s, 2H, NHNH2), 6.78 (d, 2H, J = 8.93 Hz), 6.33~6.38 (m, 1H), 6.15~6.29 (m, 1H), 4.44 (s, 2H), 4.16 (br s, 1H, NHNH2), 3.69 (s, 3H); ESI-MS (m/z): 328.30 [M+1]。
1.4 N2-(呋喃-2-基甲基)-6-[2-(萘-1-基甲烯基)肼基]-N4-苯基-1, 3, 5-三嗪-2, 4-二胺(5a)的合成将N2-(呋喃-2-基甲基)-6-肼基-N4-苯基-1, 3, 5-三嗪-2, 4-二胺(4a) (0.30 g, 0.1 mmol, 1 equiv)溶解于25 mL甲苯中, 加入1-萘甲醛(0.64 mL, 20 mmol, 4 equiv), 利用酯水分离器回流搅拌反应3 h。反应结束后, 减压蒸干溶剂, 加入最少量的CH2Cl2溶解固体, 向溶液中滴加石油醚, 有大量固体析出, 过滤, 得到白色固体0.28 g, 收率: 65%, mp: 144~145 ℃。1H NMR (500 MHz, DMSO-d6) δ: 10.94 (br s, 1H, NH), 9.31 (br s, 1H, NH), 8.46~9.06 (m, 2H), 7.95~8.12 (m, 2H), 7.43~7.94 (m, 8H), 7.26 (t, 2H, J = 7.31 Hz), 6.96 (t, 2H, J = 7.01 Hz), 6.39 (s, 1H), 6.19~6.37 (m, 1H), 4.54 (d, 2H, J = 4.63 Hz); 13C NMR (125 MHz, DMSO-d6) δ: 166.28, 164.68, 153.70, 142.25 (2C), 140.98, 134.06, 130.81, 130.60, 130.00, 129.17, 128.77 (2C), 127.53, 126.60, 126.00, 124.51, 122.06 (2C), 120.17 (2C), 110.95, 107.18, 106.92, 37.65; ESI-MS (m/z): 436.38 [M+1]。
化合物5b~5x的制备方法与化合物5a相同。
N2-(呋喃-2-基甲基)-6-[2-(萘-1-基甲烯基)肼基]-N4-(4-甲苯基)-1, 3, 5-三嗪-2, 4-二胺(5b), 白色固体, 收率: 73%, mp: 136~137 ℃。1H NMR (500 MHz, DMSO-d6) δ: 10.90 (br s, 1H, NH), 9.21 (br s, 1H, NH), 8.44~8.95 (m, 2H), 7.94~8.06 (m, 2H), 7.34~7.93 (m, 8H), 7.06 (d, 2H, J = 7.99 Hz), 6.39 (s, 1H), 6.20~6.36 (m, 1H), 4.53 (s, 2H), 2.26 (s, 3H); ESI-MS (m/z): 450.40 [M+1]。
N2-(呋喃-2-基甲基)-6-[2-(萘-1-基甲烯基)肼基]-N4-(4-乙氧苯基)-1, 3, 5-三嗪-2, 4-二胺(5c), 白色固体, 收率: 65%, mp: 138~140 ℃。1H NMR (500 MHz, DMSO-d6) δ: 10.86 (br s, 1H, NH), 9.13 (br s, 1H, NH), 8.42~8.95 (m, 2H), 7.93~8.04 (m, 2H), 7.44~7.92 (m, 8H), 6.83 (d, 2H, J = 8.78 Hz), 6.39 (s, 1H), 6.17~6.37 (m, 1H), 4.51 (s, 2H), 3.99 (dd, 2H, J = 7.07, 13.99 Hz), 1.32 (t, 1H, J = 6.98 Hz); 13C NMR (125 MHz, DMSO-d6) δ: 166.30, 164.66, 154.01, 153.77, 142.21 (2C), 134.06 (2C), 130.87, 130.61, 129.95, 129.16, 127.50, 126.55, 126.00, 124.52, 121.82 (3C), 114.58 (2C), 110.94, 107.14, 106.89, 63.54, 37.63, 15.23; ESI-MS (m/z): 480.39 [M+1]。
N2-(呋喃-2-基甲基)-6-[2-(萘-1-基甲烯基)肼基]-N4-(4-氟苯基)-1, 3, 5-三嗪-2, 4-二胺(5d), 白色固体, 收率: 45%, mp: 129~130 ℃。1H NMR (500 MHz, DMSO-d6) δ: 10.94 (br s, 1H, NH), 9.36 (br s, 1H, NH), 8.47~9.05 (m, 2H), 7.72~8.12 (m, 5H), 7.42~7.71 (m, 5H), 7.09 (s, 2H), 6.40 (s, 1H), 6.19~6.37 (m, 1H), 4.52 (s, 2H); ESI-MS (m/z): 454.38 [M+1]。
N2-(呋喃-2-基甲基)-6-[2-(萘-1-基甲烯基)肼基]-N4-(4-氯苯基)-1, 3, 5-三嗪-2, 4-二胺(5e), 白色固体, 收率: 56%, mp: 125~127 ℃。1H NMR (500 MHz, DMSO-d6) δ: 10.97 (br s, 1H, NH), 9.47 (br s, 1H, NH), 8.48~9.03 (m, 2H), 7.76~8.08 (m, 5H), 7.49~7.75 (m, 5H), 7.28 (s, 2H), 6.40 (s, 1H), 6.19~6.38 (m, 1H), 4.52 (d, 2H, J = 5.05 Hz); ESI-MS (m/z): 470.45 [M+1]。
N2-(呋喃-2-基甲基)-6-[2-(萘-1-基甲烯基)肼基]-N4-(4-溴苯基)-1, 3, 5-三嗪-2, 4-二胺(5f), 白色固体, 收率: 63%, mp: 123~124 ℃。1H NMR (500 MHz, DMSO-d6) δ: 11.03 (br s, 1H, NH), 9.50 (br s, 1H, NH), 8.56~9.03 (m, 2H), 7.79~8.11 (m, 5H), 7.55~7.78 (m, 5H), 7.45 (s, 2H), 6.44 (s, 1H), 6.27~6.42 (m, 1H), 4.57 (d, 2H, J = 5.04 Hz); ESI-MS (m/z): 514.69 [M+1]。
N2-(呋喃-2-基甲基)-6-[2-(萘-1-基甲烯基)肼基]-N4-(4-磺胺基苯基)-1, 3, 5-三嗪-2, 4-二胺(5g), 淡黄色固体, 收率: 40%, mp: 174~176 ℃。1H NMR (300 MHz, DMSO-d6) δ: 9.91 (br s, 1H, NH), 9.20 (br s, 1H, NH), 8.43 (s, 1H), 7.82~8.21 (m, 5H), 7.44~7.81 (m, 6H), 7.06~7.40 (m, 3H), 6.42 (s, 1H), 6.25~6.40 (m, 1H), 4.61 (s, 2H); ESI-MS (m/z): 515.35 [M+1]。
N2-(呋喃-2-基甲基)-6-[2-(萘-1-基甲烯基)肼基]-N4-(4-硝基苯基)-1, 3, 5-三嗪-2, 4-二胺(5h), 淡黄色固体, 收率: 49%, mp: 265~266 ℃。1H NMR (500 MHz, DMSO-d6) δ: 11.13 (br s, 1H, NH), 10.10 (br s, 1H, NH), 8.61~9.02 (m, 2H), 7.74~8.41 (m, 8H), 7.48~7.71 (m, 4H), 6.41 (s, 1H), 6.22~6.40 (m, 1H), 4.57 (d, 2H, J = 5.49 Hz); ESI-MS (m/z): 481.36 [M+1]。
N2-(呋喃-2-基甲基)-6-[2-(萘-1-基甲烯基)肼基]-N4-苄基-1, 3, 5-三嗪-2, 4-二胺(5i), 白色固体, 收率: 76%, mp: 102~103 ℃。1H NMR (500 MHz, DMSO-d6) δ: 10.78 (br s, 1H, NH), 9.32 (br s, 1H, NH), 8.51~8.92 (m, 1H), 7.10~8.09 (m, 14H), 6.38 (s, 1H), 6.05~6.35 (m, 1H), 4.33~4.76 (m, 4H); ESI-MS (m/z): 450.60 [M+1]。
N2-(呋喃-2-基甲基)-6-[2-(萘-2-基甲烯基)肼基]-N4-(4-甲氧苯基)-1, 3, 5-三嗪-2, 4-二胺(5j), 白色固体, 收率: 68%, mp: 131~132 ℃。1H NMR (500 MHz, DMSO-d6) δ: 10.97 (br s, 1H, NH), 9.13 (br s, 1H, NH), 8.31 (s, 1H), 7.62~8.11 (m, 8H), 7.58 (s, 1H), 7.51~7.57 (m, 2H), 6.86 (d, 2H, J = 7.83 Hz), 6.40 (s, 1H), 6.16~6.36 (m, 1H), 4.52 (s, 2H), 3.74 (s, 3H); ESI-MS (m/z): 466.39 [M+1]。
N2-(呋喃-2-基甲基)-6-[2-(萘-2-基甲烯基)肼基]-N4-(4-甲苯基)-1, 3, 5-三嗪-2, 4-二胺(5k), 白色固体, 收率: 66%, mp: 136~138 ℃。1H NMR (500 MHz, DMSO-d6) δ: 10.94 (br s, 1H, NH), 9.18 (br s, 1H, NH), 8.31 (s, 1H), 7.62~8.13 (m, 8H), 7.58 (s, 1H), 7.50~7.57 (m, 2H), 7.08 (d, 2H, J = 8.14 Hz), 6.40 (s, 1H), 6.20~6.38 (m, 1H), 4.52 (s, 2H), 2.27 (s, 3H); ESI-MS (m/z): 450.41 [M+1]。
N2-(呋喃-2-基甲基)-6-[2-(萘-2-基甲烯基)肼基]-N4-苯基-1, 3, 5-三嗪-2, 4-二胺(5l), 白色固体, 收率: 57%, mp: 127~129 ℃。1H NMR (500 MHz, DMSO-d6) δ: 10.98 (br s, 1H, NH), 9.29 (br s, 1H, NH), 8.32 (s, 1H), 7.68~8.14 (m, 8H), 7.58 (s, 1H), 7.52~7.57 (m, 2H), 7.08 (t, 2H, J = 7.50 Hz), 6.96 (t, 2H, J = 7.23 Hz), 6.40 (s, 1H), 6.21~6.37 (m, 1H), 4.53 (s, 2H); ESI-MS (m/z): 436.37 [M+1]。
N2-(呋喃-2-基甲基)-6-[2-(萘-2-基甲烯基)肼基]-N4-(4-乙氧苯基)-1, 3, 5-三嗪-2, 4-二胺(5m), 白色固体, 收率: 77%, mp: 130~132 ℃。1H NMR (500 MHz, DMSO-d6) δ: 10.89 (br s, 1H, NH), 9.10 (br s, 1H, NH), 8.30 (s, 1H), 7.60~8.09 (m, 8H), 7.57 (s, 1H), 7.51~7.56 (m, 2H), 6.84 (d, 2H, J = 8.16 Hz), 6.39 (s, 1H), 6.18~6.37 (m, 1H), 4.50 (s, 2H), 4.00 (dd, 2H, J = 6.63, 13.50 Hz), 1.32 (t, 1H, J = 6.91 Hz); ESI-MS (m/z): 480.39 [M+1]。
N2-(呋喃-2-基甲基)-6-[2-(萘-2-基甲烯基)肼基]-N4-(4-氟苯基)-1, 3, 5-三嗪-2, 4-二胺(5n), 白色固体, 收率: 48%, mp: 130~131 ℃。1H NMR (500 MHz, DMSO-d6) δ: 11.03 (br s, 1H, NH), 9.35 (br s, 1H, NH), 8.31 (s, 1H), 7.66~8.09 (m, 8H), 7.58 (s, 1H), 7.51~7.57 (m, 2H), 7.10 (t, 2H, J = 7.92 Hz), 6.40 (s, 1H), 6.18~6.37 (m, 1H), 4.51 (s, 2H); ESI-MS (m/z): 454.40 [M+1]。
N2-(呋喃-2-基甲基)-6-[2-(萘-2-基甲烯基)肼基]-N4-(4-氯苯基)-1, 3, 5-三嗪-2, 4-二胺(5o), 白色固体, 收率: 63%, mp: 129~130 ℃。1H NMR (500 MHz, DMSO-d6) δ: 11.02 (br s, 1H, NH), 9.46 (br s, 1H, NH), 8.32 (s, 1H), 7.61~8.12 (m, 8H), 7.59 (s, 1H), 7.51~7.58 (m, 2H), 7.43 (d, 2H, J = 6.84 Hz), 6.40 (s, 1H), 6.21~6.38 (m, 1H), 4.52 (s, 2H); ESI-MS (m/z): 470.39 [M+1]。
N2-(呋喃-2-基甲基)-6-[2-(萘-2-基甲烯基)肼基]-N4-(4-溴苯基)-1, 3, 5-三嗪-2, 4-二胺(5p), 白色固体, 收率: 68%, mp: 135~136 ℃。1H NMR (500 MHz, DMSO-d6) δ: 11.03 (br s, 1H, NH), 9.47 (br s, 1H, NH), 8.32 (s, 1H), 7.61~8.10 (m, 8H), 7.58 (s, 1H), 7.51~7.57 (m, 2H), 7.43 (d, 2H, J = 6.84 Hz), 6.40 (s, 1H), 6.21~6.37 (m, 1H), 4.52 (d, 2H, J = 5.24 Hz); ESI-MS (m/z): 514.40 [M+1]。
N2-(呋喃-2-基甲基)-6-[2-(萘-2-基甲烯基)肼基]-N4-(4-磺胺基苯基)-1, 3, 5-三嗪-2, 4-二胺(5q), 淡黄色固体, 收率: 51%, mp: 161~163 ℃。1H NMR (500 MHz, DMSO-d6) δ: 11.08 (br s, 1H, NH), 9.71 (br s, 1H, NH), 8.33 (s, 1H), 7.76~8.23 (m, 8H), 7.71 (d, 2H, J = 8.16 Hz), 7.59 (s, 1H), 7.51~7.58 (m, 2H), 6.41 (s, 1H), 6.19~6.39 (m, 1H), 4.55 (d, 2H, J = 5.72 Hz); ESI-MS (m/z): 513.28 [M-1]。
N2-(呋喃-2-基甲基)-6-[2-(萘-2-基甲烯基)肼基]-N4-(4-硝基苯基)-1, 3, 5-三嗪-2, 4-二胺(5r), 淡黄色固体, 收率: 75%, mp: 272~274 ℃。1H NMR (500 MHz, DMSO-d6) δ: 11.15 (br s, 1H, NH), 10.10 (br s, 1H, NH), 8.35 (s, 1H), 7.79~8.31 (m, 10H), 7.60 (s, 1H), 7.53~7.58 (m, 2H), 6.41 (s, 1H), 6.27~6.38 (m, 1H), 4.55 (d, 2H, J = 5.93 Hz); ESI-MS (m/z): 481.35 [M+1]。
N2-(呋喃-2-基甲基)-6-[2-(萘-2-基甲烯基)肼基]-N4-苄基-1, 3, 5-三嗪-2, 4-二胺(5s), 白色固体, 收率: 82%, mp: 107~108 ℃。1H NMR (500 MHz, DMSO-d6) δ: 13.10 (br s, 1H, NH), 10.78 (br s, 1H, NH), 8.26 (s, 1H), 7.85~8.08 (m, 5H), 7.47~7.61 (m, 3H), 7.16~7.46 (m, 6H), 6.30~6.42 (m, 1H), 6.04~6.29 (m, 1H), 4.37~4.60 (m, 4H); ESI-MS (m/z): 450.96 [M+1]。
N2-(呋喃-2-基甲基)-6-[2-(喹啉-2-基甲烯基)肼基]-N4-苄基-1, 3, 5-三嗪-2, 4-二胺(5t), 橙色固体, 收率: 43%, mp: 186~187 ℃。1H NMR (500 MHz, DMSO-d6) δ: 13.19 (br s, 1H, NH), 11.18 (br s, 1H, NH), 8.68~8.94 (m, 1H), 8.23~8.59 (m, 2H), 7.14~8.16 (m, 11H), 6.32~6.54 (m, 1H), 6.02~6.31 (m, 1H), 4.36~4.75 (m, 4H); ESI-MS (m/z): 451.63 [M+1]。
N2-(呋喃-2-基甲基)-6-[2-(喹啉-2-基甲烯基)肼基]-N4-苯基-1, 3, 5-三嗪-2, 4-二胺(5u), 橙色固体, 收率: 62%, mp: 181~182 ℃。1H NMR (500 MHz, DMSO-d6) δ: 11.37 (br s, 1H, NH), 9.38 (br s, 1H, NH), 8.42 (s, 1H), 8.34 (s, 1H), 7.53~8.21 (m, 9H), 7.23 (s, 2H), 6.98 (s, 1H), 6.40 (s, 1H), 6.22~6.37 (m, 1H), 4.55 (s, 2H); ESI-MS (m/z): 437.78 [M+1]。
N2-(呋喃-2-基甲基)-6-[2-(喹啉-2-基甲烯基)肼基]-N4-(4-溴苯基)-1, 3, 5-三嗪-2, 4-二胺(5v), 橙色固体, 收率: 62%, mp: 169~171 ℃。1H NMR (500 MHz, DMSO-d6) δ: 11.34 (br s, 1H, NH), 9.52 (br s, 1H, NH), 8.43 (s, 1H), 8.34 (s, 1H), 7.96~8.22 (m, 3H), 7.92 (br s, 1H, NH), 7.67~7.89 (m, 3H), 7.62 (d, 1H, J = 7.51 Hz), 7.59 (s, 1H), 7.45 (s, 2H), 6.41 (s, 1H), 6.24~6.37 (m, 1H), 4.54 (s, 2H); ESI-MS (m/z): 517.56 [M+1]。
N2-(呋喃-2-基甲基)-6-[2-(苯基甲烯基)肼基]-N4-苯基-1, 3, 5-三嗪-2, 4-二胺(5w), 白色固体, 收率: 78%, mp: 116~117 ℃。1H NMR (500 MHz, DMSO-d6) δ: 10.85 (br s, 1H, NH), 9.27 (br s, 1H, NH), 8.16 (s, 1H), 7.62~8.04 (m, 4H), 7.57 (s, 1H), 7.54 (br s, 1H, NH), 7.44 (t, 2H, J = 7.83 Hz), 7.37 (t, 1H, J = 7.16 Hz), 7.26 (t, 2H, J = 7.61 Hz), 6.39 (s, 1H), 6.22~6.36 (m, 1H), 4.51 (d, 2H, J = 5.15 Hz); ESI-MS (m/z): 386.46 [M+1]。
N2-(呋喃-2-基甲基)-6-[2-(吡啶-4-基甲烯基)肼基]-N4-苯基-1, 3, 5-三嗪-2, 4-二胺(5x), 黄色固体, 收率: 65%, mp: 231~232 ℃。1H NMR (500 MHz, DMSO-d6) δ: 11.17 (br s, 1H, NH), 9.34 (br s, 1H, NH), 8.62 (d, 2H, J = 5.47 Hz), 8.12 (s, 1H), 7.59~8.02 (m, 4H), 7.58 (s, 1H), 7.53 (br s, 1H, NH), 7.27 (t, 2H, J = 7.64 Hz), 6.96 (t, 1H, J = 7.14 Hz), 6.39 (s, 1H), 6.20~6.36 (m, 1H), 4.52 (s, 2H); ESI-MS (m/z): 387.30 [M+1]。
1.5 2-{2-[(2-{4-[(呋喃-2-基甲基)胺基]-6-[(4-甲氧基苯基)胺基]-1, 3, 5-三嗪-2-基}肼基)甲烯基]苯氧基}乙酸乙酯(7a)的合成化合物7a~7c的制备方法与化合物5a相同。
2-{2-[(2-{4-[(呋喃-2-基甲基)胺基]-6-[(4-甲氧基苯基)胺基]-1, 3, 5-三嗪-2-基}肼基)甲烯基]苯氧基}乙酸乙酯(7a), 白色固体, 收率: 72%, mp: 180~181 ℃。1H NMR (500 MHz, DMSO-d6) δ: 10.94 (br s, 1H, NH), 9.10 (br s, 1H, NH), 8.04 (s, 1H), 7.59~8.05 (m, 3H), 7.57 (s, 1H), 7.46 (br s, 1H, NH), 7.32 (t, 1H, J = 7.92 Hz), 7.05 (t, 1H, J = 6.99 Hz), 6.97 (d, 1H, J = 8.86 Hz), 6.83 (d, 2H, J = 8.86 Hz), 6.36~6.43 (m, 1H), 6.17~6.35 (m, 1H), 4.89 (s, 2H), 4.49 (s, 2H), 4.18 (dd, 2H, J = 7.17, 14.32 Hz), 3.72 (s, 3H), 1.22 (t, 1H, J = 7.17 Hz); 13C NMR (125 MHz, DMSO-d6) δ: 169.08, 166.22, 164.52, 156.07, 154.73, 142.19, 138.16, 133.96, 130.66, 125.90, 124.23, 121.73 (2C), 113.94 (3C), 113.23, 110.92, 107.27, 106.82, 65.61, 61.19, 55.63, 37.63, 14.51; ESI-MS (m/z): 518.29 [M+1]。
2, 2'-[{4-[(2-{4-[(呋喃-2-基甲基)胺基]-6-[(4-甲氧基苯基)胺基]-1, 3, 5-三嗪-2-基}肼基)甲烯基]-1, 2-苯基}二(氧)]双乙酸乙酯(7b), 白色固体, 收率: 78%, mp: 86~87 ℃。1H NMR (500 MHz, DMSO-d6) δ: 10.74 (br s, 1H, NH), 9.09 (br s, 1H, NH), 8.04 (s, 1H), 7.59~7.87 (m, 2H), 7.56 (s, 1H), 7.44 (br s, 1H, NH), 7.13~7.32 (m, 2H), 6.99 (d, 1H, J = 8.51 Hz), 6.85 (d, 2H, J = 8.21 Hz), 6.36~6.41 (m, 1H), 6.17~6.35 (m, 1H), 4.86 (s, 2H), 4.84 (s, 2H), 4.50 (s, 2H), 4.18 (dd, 4H, J = 7.16, 14.31 Hz), 3.72 (s, 3H), 6.85 (t, 6H, J = 7.14 Hz); HR-ESI-MS (m/z) [M+1]: 620.2466。
2, 2'-[{4-[(2-{4-[(呋喃-2-基甲基)胺基]-6-[(4-甲氧基苯基)胺基]-1, 3, 5-三嗪-2-基}肼基)甲烯基]-1, 3-苯基}二(氧)]双乙酸乙酯(7c), 白色固体, 收率: 66%, mp: 95~97 ℃。1H NMR (500 MHz, DMSO-d6) δ: 10.75 (br s, 1H, NH), 9.07 (br s, 1H, NH), 8.41 (s, 1H), 7.60~8.04 (m, 3H), 7.56 (s, 1H), 7.41 (br s, 1H, NH), 6.83 (d, 2H, J = 8.69 Hz), 6.54~6.73 (m, 2H), 6.35~6.43 (m, 1H), 6.18~6.35 (m, 1H), 4.90 (s, 2H), 4.82 (s, 2H), 4.49 (s, 2H), 4.13~4.24 (m, 4H), 3.72 (s, 3H), 1.18~1.27 (m, 6H); 13C NMR (125 MHz, DMSO-d6) δ: 168.97, 168.92, 166.22, 164.53, 160.03, 157.18, 154.67, 153.79, 142.16, 138.18, 134.06, 126.91, 121.65 (2C), 117.77, 113.94 (2C), 110.91, 108.07, 107.26, 106.76, 100.42, 65.70, 65.34, 61.20, 61.14, 55.62, 37.62, 14.50 (2C); ESI-MS (m/z): 620.32 [M+1]、HR-ESI-MS m/z [M+1]: 620.2469。
1.6 2-{2-[(2-{4-[(呋喃-2-基甲基)胺基]-6-[(4-甲氧基苯基)胺基]-1, 3, 5-三嗪-2-基}肼基)甲烯基]苯氧基}乙酸(8a)的合成将2-{2-[(2-{4-[(呋喃-2-基甲基)胺基]-6-[(4-甲氧基苯基)胺基]-1, 3, 5-三嗪-2-基}肼基)甲烯基]苯氧基}乙酸乙酯(7a) (0.11 g, 0.22 mmol, 1 equiv)和LiOH·H2O (0.014 g, 0.33 mmol, 1.5 equiv)于5 mL混合溶剂(THF-MeOH-H2O = 3:2:1)中, 室温搅拌反应1 h。减压蒸干溶剂, 加入水(20 mL), 1 mol·L-1盐酸调节pH至2.0~3.0, 有沉淀生成。过滤沉淀, 用冷水洗涤, 得到白色固体64 mg, 收率: 59%, mp: 188~189 ℃。1H NMR (400 MHz, DMSO-d6 + D2O) δ: 8.59 (s, 1H), 7.97 (d, 2H, J = 7.60 Hz), 7.43~7.71 (m, 3H), 7.28~7.42 (m, 1H), 7.15~6.93 (m, 2H), 7.89 (d, 2H, J = 8.80 Hz), 6.41 (s, 1H), 6.34 (s, 1H), 4.78 (s, 2H), 4.52 (s, 2H), 3.77 (s, 3H); 13C NMR (125 MHz, DMSO-d6) δ: 170.44, 164.54, 158.85, 156.75, 155.77, 142.86, 142.42, 132.04 (2C), 126.56, 124.14 (2C), 121.59, 114.20 (3C), 113.25, 111.05, 107.67 (2C), 65.43, 55.70, 37.63; ESI-MS (m/z): 490.25 [M+1]。
化合物8b、8c的制备方法与化合物8a相同。
2, 2'-[{4-[(2-{4-[(呋喃-2-基甲基)胺基]-6-[(4-甲氧基苯基)胺基]-1, 3, 5-三嗪-2-基}肼基)甲烯基]-1, 2-苯基}二(氧)]双乙酸(8b), 白色固体, 收率: 43%, mp: 228~229 ℃。1H NMR (400 MHz, DMSO-d6 + D2O) δ: 8.06 (s, 1H), 7.45~7.80 (m, 3H), 7.16~7.44 (m, 2H), 6.94 (d, 1H, J = 8.80 Hz), 6.87 (d, 2H, J = 8.80 Hz), 6.40 (s, 1H), 6.31 (s, 1H), 4.76 (s, 4H), 4.50 (s, 2H), 3.72 (s, 3H); 13C NMR (125 MHz, DMSO-d6) δ: 170.47, 170.39, 165.43, 163.42, 162.44, 156.39, 150.16, 142.97, 142.52, 131.60, 127.35, 122.19 (2C), 118.89, 114.28 (2C), 113.80, 111.08, 107.68 (3C), 101.03, 65.95, 65.56, 55.72, 37.66; HR-MS (ESI) m/z: Calcd. for C26H26N7O8 [M+H]+ 564.183 7, Found 564.184 3。
2, 2'-[{4-[(2-{4-[(呋喃-2-基甲基)胺基]-6-[(4-甲氧基苯基)胺基]-1, 3, 5-三嗪-2-基}2肼基)甲烯基]-1, 3-苯基}二(氧)]双乙酸(8c), 白色固体, 收率: 48%, mp: 233~234 ℃。1H NMR (400 MHz, DMSO-d6 + D2O) δ: 8.52 (s, 1H), 7.92 (d, 1H, J = 8.40 Hz), 7.44~7.75 (m, 3H), 6.91 (d, 2H, J = 8.80 Hz), 6.63 (d, 1H, J = 8.80 Hz), 6.58 (s, 1H), 6.43 (s, 1H), 6.20~6.41 (s, 1H), 4.80 (s, 2H), 4.74 (s, 2H), 4.51 (s, 2H), 3.72 (s, 3H); HR-MS (ESI) m/z: Calcd. for C26H26N7O8 [M+H]+ 564.183 7, Found 564.185 5。
2 SAP2抑酶活性实验本研究参照文献[14]建立SAP2抑酶活性测试方法, 以PepA作阳性对照进行多次测试, 均获得接近文献结果。
在黑色96孔板上每孔依次加入柠檬酸钠缓冲液185 µL、SAP2酶5 µL、抑制剂5 µL, 作三复孔, PepA做阳性对照组, DMSO做空白组。混匀后于30 ℃培养30 min。加入18.75 µmol·L-1底物5 µL, 振板混匀, 使用Bioteck Synergy2多功能酶标仪每10 min测定化合物荧光发光(λex = 340/30 nm, λem = 485/20 nm)。根据单位时间荧光发光的增加程度, 计算出每个浓度下抑制剂的抑制率%。把每个浓度的抑制率与样品浓度的log值进行非线性拟合, 得到活性与剂量的依赖关系, 通过GraphPad Prism 5.0软件直接得到IC50值。
3 真菌感染的线虫体内模型测试实验真菌感染的线虫体模型实验参照Pukkila-Worley等[15]的研究方法建立。
将秀丽隐杆线虫glp-4、sek-1于NGM培养基中, 以大肠杆菌饲养线虫, 15 ℃培养5~6天至育卵期, 离心, 弃上清液, 用M9缓冲液冲洗干净, 加入裂解液, 振荡后收集虫卵, 于M9缓冲液中孵化过夜, 得到Ll期幼虫, 再转移到NGM培养基上25 ℃培养3天, 得L4期成虫。
从4 ℃条件下的SDA板上挑取单菌落C. alb. SC5314于2 mL YEPD液体培养基中, 30 ℃培养过夜, 得到指数生长后期的真菌。次日, 取100 μL菌液于BHI琼脂培养基上(含卡那霉素45 μg·mL-1), 30 ℃培养过夜。L4期线虫成虫用M9缓冲液冲洗干净, 400~500只干净线虫置于白念珠菌落上, 25 ℃培养4 h。用6 mL无菌的M9缓冲液仔细冲洗线虫置于15 mL锥形管中, 反复冲洗4次。在12孔板中各孔加入2 mL培养基(含80% M9、20% BHI、45 μg·mL-1卡那霉素), 每孔放入30只线虫进行培养。待测化合物8a、8c终浓度16 μg·mL-1, 氟康唑为32 μg·mL-1, 并设立空白对照。作三复孔, 加入到上述培养基中, 于25 ℃培养, 每24 h计数观察各孔线虫存活情况。
4 菌丝生长抑制实验从-80 ℃冰箱中吸取10 μL C. alb. SC5314菌种于1 mL YEPD培养基中, 混匀后于30 ℃摇床中培养24 h后, 从中吸取10 μL至1 mL新鲜YEPD培养基中, 继续培养16 h, 使真菌的生长状态处于指数后期。将1 mL YEPD菌液离心, 弃去上清液, 加入PBS缓冲液清洗3次后, 最后一次加入1 mL PBS缓冲液吹打混匀, 稀释103倍到Spider培养基中配成菌悬液。
在12孔板的第一列每孔加入上述菌悬液3 mL, 剩下每孔加入菌悬液1.5 mL。在12孔板的第一列每孔分别加入2 mg·mL-1 FLC的DMSO溶液、2 mg·mL-1化合物8a的DMSO溶液、2 mg·mL-1化合物8b的DMSO溶液和2 mg·mL-1化合物8c的DMSO溶液各96 μL。混匀后含有FLC药物的此行倍半稀释到第二孔, 剩下两孔补加DMSO溶液96 μL作空白对照; 含有化合物8a~8c的3行倍半稀释到第四孔, 设置4个浓度梯度, 即终浓度为64~8 μg·mL-1。
稀释完成后, 做好标记, 放置于37 ℃恒温恒湿箱中培养5 h后, 于荧光倒置显微镜下观察菌丝形成状况并拍照。
5 被膜形成抑制实验分别取指数生长后期的白念珠菌敏感菌株C. alb. 5314和白念珠菌耐药菌株C. alb. 103, 离心, 弃去上清液, 加入PBS缓冲液清洗3次后, 最后一次加入PBS缓冲液1 mL吹打混匀, 用RPMI 1640培养液稀释成1×105 CFU·mL-1菌悬液。
于96孔板上B1:G11每孔加入待测菌株菌悬液100 μL, 放置于37 ℃恒温恒湿箱中培养1.5 h (成熟被膜实验需培养24 h)后, 期间在另一空白96孔板上B1:G1每孔加入RPMI 1640培养液200 μL, B2:G12每孔加入待测菌株菌悬液100 μL, B1:D1每孔加入2 mg·mL-1待测药物的DMSO溶液6.4 μL, E1:G1每孔加入2 mg·mL-1 FLC的DMSO溶液6.4 μL, 混匀后倍半稀释至第10列。
从37 ℃恒温恒湿箱中取出培养1.5 h后的96孔板, 轻轻吸弃RPMI 1640培养液, 用PBS缓冲液重复清洗3次, 将稀释好的化合物每孔对应加入, 于37 ℃恒温恒湿箱中培养24 h后, 吸走上层药液, PBS缓冲液清洗3次, 避光条件下, B1:G12每孔加入XTT/menadione溶液100 μL, 37 ℃恒温恒湿箱中培养3 h后, 每孔吸取上清液80 μL至空白96孔板, 使用酶标仪于490 nm波长下测各孔OD值。与空白组比较, 以OD值下降80%以上的最低药物浓度为SMIC80。
| [1] |
Lai CC, Tan CK, Huang YT, et al. Current challenges in the management of invasive fungal infections[J]. J Infect Chemother, 2008, 14: 77-85. DOI:10.1007/s10156-007-0595-7 |
| [2] |
Odds FC. Genomics, molecular targets and the discovery of antifungal drugs[J]. Rev Iberoam Micol, 2005, 22: 229-237. DOI:10.1016/S1130-1406(05)70048-6 |
| [3] |
Liu N, Tu J, Dong G, et al. Emerging new targets for the treatment of resistant fungal infections[J]. J Med Chem, 2018, 61: 5484-5511. |
| [4] |
Brown GD, Denning DW, Gow NA, et al. Hidden killers:human fungal infections[J]. Sci Transl Med, 2012, 4: 165rv113. |
| [5] |
Rueping MJ, Vehreschild JJ, Cornely OA. Invasive candidiasis and candidemia:from current opinions to future perspectives[J]. Expert Opin Investig Drugs, 2009, 18: 735-748. DOI:10.1517/13543780902911440 |
| [6] |
Naglik JR, Challacombe SJ, Hube B. Candida albicans secreted aspartyl proteinases in virulence and pathogenesis[J]. Microbiol Mol Biol Rev, 2003, 67: 400-428. DOI:10.1128/MMBR.67.3.400-428.2003 |
| [7] |
Dong G, Liu Y, Wu Y, et al. Novel non-peptidic small molecule inhibitors of secreted aspartic protease 2(SAP2) for the treatment of resistant fungal infections[J]. Chem Commun (Camb), 2018, 54: 13535-13538. DOI:10.1039/C8CC07810F |
| [8] |
Hube B, Naglik J. Candida albicans proteinases:resolving the mystery of a gene family[J]. Microbiology, 2001, 147: 1997-2005. DOI:10.1099/00221287-147-8-1997 |
| [9] |
De Bernardis F, Sullivan PA, Cassone A. Aspartyl proteinases of Candida albicans and their role in pathogenicity[J]. Med Mycol, 2001, 39: 303-313. DOI:10.1080/mmy.39.4.303.313 |
| [10] |
Cutfield SM, Dodson EJ, Anderson BF, et al. The crystal structure of a major secreted aspartic proteinase from Candida albicans in complexes with two inhibitors[J]. Structure, 1995, 3: 1261-1271. DOI:10.1016/S0969-2126(01)00261-1 |
| [11] |
Liu N, Zhong H, Tu J, et al. Discovery of simplified sampangine derivatives as novel fungal biofilm inhibitors[J]. Eur J Med Chem, 2018, 143: 1510-1523. DOI:10.1016/j.ejmech.2017.10.043 |
| [12] |
Li DD, Zhao LX, Mylonakis E, et al. In vitro and in vivo activities of pterostilbene against Candida albicans biofilms[J]. Antimicrob Agents Chemother, 2014, 58: 2344-2355. DOI:10.1128/AAC.01583-13 |
| [13] |
Jiang Z, Liu N, Hu D, et al. The discovery of novel antifungal scaffolds by structural simplification of the natural product sampangine[J]. Chem Commun (Camb), 2015, 51: 14648-14651. DOI:10.1039/C5CC05699C |
| [14] |
Büchold C, Hemberger Y, Heindl C, et al. New cis-configured aziridine-2-carboxylates as aspartic acid protease inhibitors[J]. ChemMedChem, 2011, 6: 141-152. DOI:10.1002/cmdc.201000370 |
| [15] |
Pukkila-Worley R, Peleg AY, Tampakakis E, et al. Candida albicans hyphal formation and virulence assessed using a Caenorhabditis elegans infection model[J]. Eukaryot Cell, 2009, 8: 1750-1758. DOI:10.1128/EC.00163-09 |
 2020, Vol. 55
2020, Vol. 55