2. 武汉药品医疗器械检验所, 湖北 武汉 430075
2. Wuhan Institute for Drug and Medical Device Control, Wuhan 430075, China
紫草是一味传统的清热凉血中药, 始载于《神农本草经》[1, 2]。依据《中国药典》 (2015年版), 其基原为紫草科(Boraginaceae)软紫草属多年生草本植物新疆紫草(Arnebia euchroma (Royle) Johnst.)和内蒙紫草(A. guttata Bunge.)的干燥根, 习称“软紫草”和“内蒙紫草”[3]。而从本草考证来看, 紫草的原植物还有紫草(Lithospermum erythrorhizon Sieb. et Zucc.)、滇紫草(Onosma paniculatum Bur. et Franch.)等, 习称“硬紫草”、“滇紫草”或“紫草皮”[4-6]。因此, 广义而言, 紫草是一个多来源的中药品种。临床上, 紫草有凉血活血、解毒透疹之功, 其中药饮片广泛用于方剂组方, 同时也是一种重要的中成药入药药材, 仅在《中国药典》中收载与紫草相关的成方制剂就有15种。各处方中的紫草除了“小儿宝泰康颗粒”用滇紫草外, 均为药典规定品种[3]。此外, 紫草还被广泛地应用于食品和化妆品工业中[7, 8]。
研究表明, 紫草含有多种活性成分, 主要如萘醌类、单萜苯酚及苯醌类、黄酮类、酚酸类及多糖类等, 其中, 萘醌类化合物具有良好的抗氧化、抗炎、抗肿瘤、抗HIV-1以及促进伤口愈合等活性, 尤以紫草素(shikonin)的研究最为多见[9]; 另一方面, 紫草含有一类具有肝毒性的吡咯里西啶生物碱(pyrrolizidine alkaloids, PAs)成分。该成分在植物界广泛分布, 且主要集中于紫草科(Boraginaceae)、菊科(Asteraceae)和豆科(Fabaceae)植物[8, 10], 分别如新疆紫草、千里光(Senecio scandens Buch.-Ham.)和野百合(Crotalaria sessiliflora L.)等。其生物合成途径曾通过同位素示踪技术得到研究, 已知其千里光次碱(necine base)结构(图 1A)是由鸟氨酸或精氨酸形成腐胺后再逐步衍生而来[11]。长期大量摄入该类成分可诱发肝窦阻塞综合征(hepatic sinusoidal obstruction syndrome, HSOS, 或称肝小静脉闭塞病hepatic veno-occlusive disease, HVOD, 以下称为HSOS)[12], 早期报道该病多与造血干细胞移植使用化疗药物预处理有关[13]。由于量-毒关系不明确及个体差异问题, PAs引起的肝毒性常具有隐匿性, 因此也被称为“冰山病” (iceberg disease)[14]。研究表明, 紫草不同来源的植物中均存在PAs成分, 被认为是该科植物起毒副作用的主要物质[15, 16]。本文以“紫草”、“吡咯里西啶生物碱”、“肝毒性”、“代谢活化”、“Boraginaceae”、“pyrrolizidine alkaloid”、“liver toxicity”及“metabolic activation”等为关键词, 检索了SciFinder Scholar、PubMed、Web of Science及中国知网等数据库中收录的近20年来有关紫草吡咯里西啶生物碱及其代谢毒性的研究文献, 剔除了以“萘醌”、“药理学”、“药效学”和“临床疗效”为主要内容的文献, 获得有效文献70余篇。以下就目前紫草及其相关品种中吡咯里西啶类成分及其代谢毒性研究概况做一综述, 以期为深入了解紫草类中药临床用药风险及开展安全性评价研究提供参考。
|
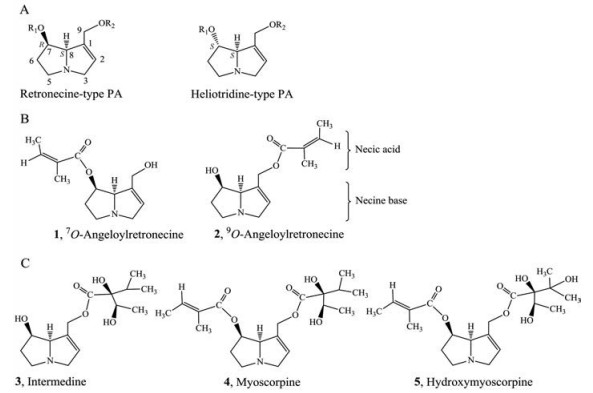
Figure 1 Structures of hepatotoxic pyrrolizidine alkaloids (PAs) found in Chinese medicinal herb "Zicao". A: Two core structures of necine bases of PAs in Boraginaceae plants; B: Two PA components found in Arnebia euchroma; C: Three PA components found in Lithospermum erythrorhizon |
吡咯里西啶生物碱(PAs)是紫草科植物普遍具有的一类次生代谢产物[16]。从结构来看, PAs分子一般包括千里光次碱(necine bases)和千里光酸(necic acids)两个部分(图 1)。而根据千里光次碱结构, 常见的PAs可分为retronecine型(7位为R构型)、heliotridine型(7位为S构型)、otonecine型和platynecine型[8, 10]。除了platynecine型吡咯环为饱和结构, 其余三者在其C1和C2位置均为双键, 因与肝毒性相关, 故又称为肝毒性PAs。紫草科植物中的PAs主要为retronecine型和heliotridine型PAs, 分别如石松胺(lycopsamine)和天芥菜碱(heliotrine), 均为1, 2位不饱和结构(图 1和图 2); 千里光酸部分则主要包括7-位或9-位单酯取代型和7, 9-双酯取代开环型等[10]。根据Roeder等[8]早期的研究, 新疆紫草中含有O7-angeloylretronecine (化合物1)和O9-angeloylretronecine (2), 硬紫草中含有intermedine (3)、myoscorpine (4)和hydroxymyosorpine (5), 均为retronecine型的PAs (表 1, 图 1)。
|
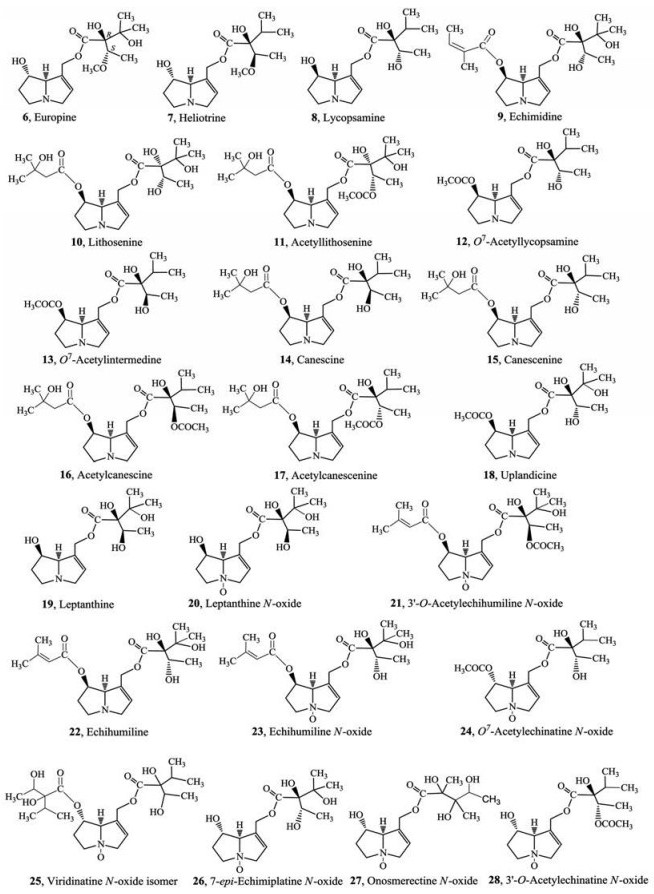
Figure 2 Structures of hepatotoxic PAs found in the relative plants of Chinese medicinal herb "Zicao" |
| Table 1 A list of hepatotoxic PAs in Chinese medicinal herb "Zicao" and its relative plants. aAs the stereoisomerism is very common in PAs of Boraginaceae plants, the PA components identified only by GC or LC tandem MS are not included in this list. As for many other proposed PAs, see the main text for details; bSee Figures 1 and 2 for structures; cRE: Retronecine-type PA; HE: Heliotridine-type PA. AE: Arnebia euchroma (Royle) Johnst.; LE: Lithospermum erythrorhizon Sieb. et Zucc. The relative plants of Chinese medicinal herb "Zicao": AB: Arnebia benthamii (Wall. ex G. Don) I. M. Johnst.; LO: Lithospermum officinale L.; LC: L. canescens; OAW: O. arenaria Waldst. et Kit.; OL: O. leptantha Heldr.; OE: O. erecta Sibth. & Sm.; OK: O. kaheirei Teppner |
近年来, 高分辨和高灵敏的分析技术(特别是色谱质谱联用技术)在紫草PAs成分的研究中得到了运用。Smyrska-Wieleba等[17]采用亲水作用液相色谱与电喷雾离子化四级杆飞行时间质谱联用(HILIC/ESI-QTOF-MS)方法对新疆紫草中PAs成分进行了分析。该研究证实了已报道的O7-angeloylretronecine和O9-angeloylretronecine两种PAs, 同时还发现了intermedine (或石松胺)、intermedine N-oxide (或其差向异构体)、leptanthine N-oxide (或echimiplatine N-oxide)、蓝蓟定氮氧化物(echimidine N-oxide)或其差向异构体以及O7-angeloylretronecine和O9-angeloylretronecine两种成分的氮氧化物(痕量)等6种PAs成分的存在。此外, 有不少对其他软紫草属植物的研究报道, 如Ahmad等[18]采用HPLC方法并以已知结构的PAs作为对照品, 从巴基斯坦克什米尔地区药用紫草A. benthamii (Wall. ex G. Don) I. M. Johnst.的地上部分鉴定出欧天芥菜碱(europine) (6)、天芥菜碱(7)、石松胺(8)和蓝蓟定(9) 4种PAs成分(表 1, 图 2)。
相比于新疆紫草, 内蒙紫草未见PAs的报道, 硬紫草和滇紫草中PAs成分的研究亦不多见, 但有不少同属其他植物的报道。例如, Krenn等[19]从小花紫草(L. officinale L.)中分离并鉴定了两种7, 9-双酯取代开环型PAs, 即O7-3-hydroxy-3-methylbutanoyl-O9-(-)hydroxyviridiflorylretronecine (lithosenine) (10)及其乙酰化物(acetyllithosenine) (11); Wiedenfeld等[20]从L. canescens分离得到7种PAs, 分别是:石松胺、O7-acetyllycopsamine (12)、O7-acetylintermedine (13)、7-(3-hydroxy-3-methylbutanoyl) rinderine (canescine) (14)、7-(3-hydroxy-3-methyl butanoyl)echinatine (canescenine) (15)及后两种的乙酰衍生物[acetylcanescine (16)和acetylcanescenine (17)], 这些成分的结构均应用光谱方法确定(表 1, 图 2)。
在滇紫草属(Onosma)研究方面, El-Shazly等[21]从O. arenaria Waldst.et Kit.中分离并鉴定了一种主要PA成分uplandicine (18, 相当于7位被乙酰基取代的蓝蓟定, 图 2), 并通过质谱数据以及科瓦茨保留指数检出其他9种PAs, 即5, 6-dihydro-7, 9-dimethoxy-7H-pyrrolizine、7-acetylretronecine、9-(butyryl-2-ene) supinidine、7-acetyl-9-(2-methylbutyryl) retronecine、7-acetyl-9-(2, 3-dimethylbutyryl) retronecine、7-acetyl-9-(2-hydroxy-3-methylbutyryl) retronecine、3'-acetylsupinine、7-acetyl-9-(2, 3-dihydroxybutyryl) retronecine和7-acetyllycopsamine。Kretsi等[22]从希腊特有滇紫草属植物O. leptantha Heldr.中分离并鉴定了5种PAs, 包括3个新成分, 分别为leptanthine (19)、leptanthine N-oxide (20)、3'-O-acetylechihumiline N-oxide (21)和两个已知化合物, 分别为echihumiline (22)及其氮氧化物(23)。Damianakos等[23]从另一希腊产滇紫草属植物O. erecta Sibth. & Sm.的地上部甲醇提取物中分离鉴定了4个新氮氧化物, 分别为O7-acetylechinatine N-oxide (24)、viridinatine N-oxide的立体异构体(25)、7-epiechimiplatine N-oxide (26)和onosmerectine N-oxide (27)。Orfanou等[24]从O. kaheirei Teppner地上部分发现了一个新PA成分, 即3'-O-acetylechinatine N-oxide (28)与两个已知PAs, 即O7-acetylechinatine N-oxide和7-epiechimiplatine N-oxide。
Mellidis等[25]曾采用GC/MS方法从异叶滇紫草O.heterophylla中发现heliotridine和1-methylenepyrrolizidine (分子式C8H13N)两种PAs; Roeder等[26]也通过GC等方法从O. alborosea、O. sanguinolenta和O. arenaria subsp. pennina中检测到intermedine、石松胺、O7-acetylintermedine和O7-acetyllycopsamine; Mroczek等[27]以大气压化学电离(APCI)为离子源接口通过反相高效液相色谱与离子阱质谱联用(HPLC/IT-MS)对O. stellulatum W.K.中的生物碱成分进行了分析, 检出12种不同结构的PAs, 分别暂定为O7-acetylintermedine、dihydroechinatine、heliospathuline及其氮氧化物、leptanthine及其氮氧化物、trachelanthamine N-oxide、uplandicine、蓝蓟定及其氮氧化物、石松胺及其氮氧化物, 其中, 除了dihydroechinatine和trachelanthamine N-oxide外, 均为1, 2位不饱和的retronecine型PAs, 但这些化合物necic acid部分的立体构型尚需确证。Damianakos等[28]采用GC/MS方法, 通过EI质谱数据和已发表PAs化合物的保留时间指数值从O. erecta Sibth. & Sm.和O. kaheirei Teppner中检测到7-epiechimiplatine, 从O. erecta、O. kaheirei和O. leptantha Heldr.中检出7-O-acetylechinatine, 另从O. leptantha中还检出7-O-acetyllycopsamine、heliosupine、蓝蓟定、echihumiline、3'-O-acetylheliosupine和大环型jacozine等PAs成分。
本研究组[29]曾利用三重四级杆串联质谱与高效液相色谱联用技术(HPLC-ESI-TQ-MS/MS)以及1, 2位不饱和PAs的特征碎片离子峰信息(即m/z 120和138), 对新疆紫草和紫草皮水提物的PAs成分进行了初步分析。从新疆紫草水提物中检测出intermedine (或其异构体)、myoscorpine N-oxide、heliosupine N-oxide、heliosupine-13-acetate等4种PAs成分; 从紫草皮(来源于滇紫草等植物的根部栓皮[6])水提物中检出了欧天芥菜碱及其异构体、天芥菜碱、intermedine、intermedine-13-acetate及其异构体、heliosupine及其异构体、heliosupine N-oxide、heliosupine-13-acetate及其异构体等十余种PAs。尽管这些PAs的准确结构还有待阐明, 但从分析中不难看到, 这些成分均为开环类不饱和型PAs, 而且多存在同分异构现象。
综上可见, 不同来源的紫草所含PAs的基本结构都为开环类不饱和型PAs, 其中双酯类、单酯类PAs各占一定比例; 各类紫草药材中PAs的分布既有区别又有一定的重叠, 但其准确的结构(特别是necic acid部分手性构型)、类型和数量以及在药材中的含量等尚不清楚, 还有待进一步研究。
2 PAs的代谢毒性及其机制研究大量实验研究与临床案例表明, 长期和大量摄入PAs会造成肝巨细胞症和肝纤维化, 诱发HSOS[10, 12-15]。此外, PAs还可能具有肺毒性、遗传毒性、神经毒性和胚胎毒性等[30, 31]。PAs的毒性与其结构和性质有关, 且因动物种属、个体的差异而不同[32-35]。就千里光次碱结构而言, 如其1, 2位为不饱和结构, 且与千里光酸形成酯, 这类PAs容易被代谢活化形成吡咯代谢物, 因而往往具有较强的肝毒性。
2.1 PAs的代谢活化与肝毒性一般认为, PAs的毒性主要与其体内代谢活化有关。研究表明[34, 35], PAs的代谢活化有赖于肝P450酶系(CYPs)的作用, 产生具有强亲电活性的吡咯酯类化合物(或称代谢吡咯)。代谢吡咯生成后一方面与细胞内重要的生命物质或大分子亲核体(如DNA、RNA、蛋白质等)发生非特异性的不可逆结合, 形成吡咯-蛋白加合物(pyrrole-protein adducts)或吡咯-DNA加合物(pyrrole-DNA adducts)[30, 31]; 另一方面可与小分子亲核物质(如还原型谷胱甘肽, 以下简称GSH)结合形成易于排泄的次生吡咯代谢物, 如7-GS-DHP (图 3, M-M3)等[32, 34]。后者可以看作是一个去活化过程, 但同时又可使细胞内氧化还原平衡遭到破坏, 引起机体的氧化应激损伤[33, 36]。这些作用可使肝细胞膜和线粒体等细胞器受损或发生功能障碍, 造成肝细胞坏死, 并最终导致肝损伤。相比于‘代谢吡咯’, 吡咯-蛋白加合物形成后较为稳定, 可以反映PAs在体内代谢活化过程及程度, 因此, 有研究将此代谢物作为一种基于机制的特异性化学标志物[37]。
|
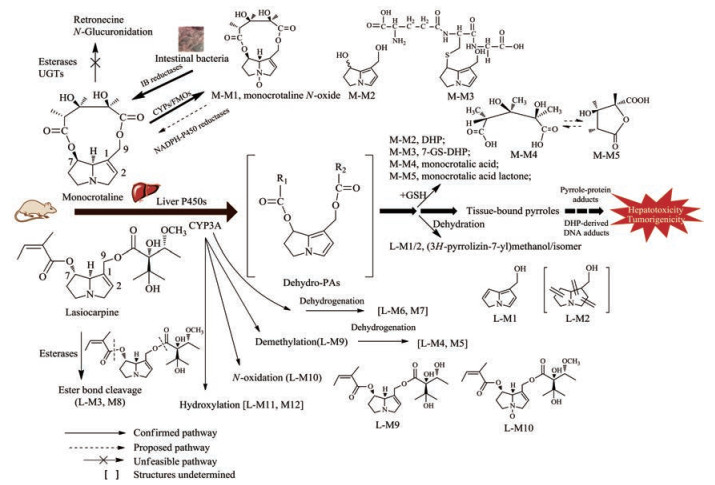
Figure 3 The main metabolic pathways and associated toxic insults (hepatotoxicity and tumorigenicity) of two representative 1, 2-unsaturated PAs (one is retronecine-type, monocrotaline and another heliotridine-type, lasiocarpine) in rats. M-M1−M-M5: 5 common metabolites produced in rat livers both in vivo and in vitro from monocrotaline; L-M1−L-M12, 12 metabolites produced by rat liver microsomes in vitro from lasiocarpine. GSH: Reduced glutathione; DHP: (±)-6, 7-Dihydro-7-hydroxy-1-hydroxymethyl-5H-pyrrolizine; UGTs: UDP glucuronosyl transferases; CYPs: Cytochromes P450s; FMOs: Flavin-containing monooxygenases; IB: Intestinal bacteria. Given the relevance to structure and species, the metabolic pathways for different PAs may vary from each other. As the PA composition in different sources of "Zicao" is underappreciated, their specific PAs and underlying toxicological mechanisms may be further studied. |
迄今国内外已有许多研究组采用肝微粒体酶或基因重组CYPs亚型酶, 运用体外温孵等方法分别对不同类型和结构PAs的代谢进行了研究, 以大量的数据证实了PAs在CYPs介导下的代谢活化及其与肝毒性之间的关联[34, 38-43]。为了了解不同结构的PAs代谢活化的差异及其毒性的构效关系, Ruan等[34]考察了retronecine型、otonecine型和platynecine型3种类型共12个PAs在小鼠体内吡咯-蛋白加合物的形成情况, 并且利用人肝微粒体和重组人CYPs亚型酶研究了PAs结构和酶类型对代谢的影响。结果表明, 具有饱和型千里光次碱结构的platynecine型PAs不被代谢活化, 而在相似的千里光酸结构下, retronecine型PAs (如千里光宁)比otonecine型PAs (如克氏千里光碱)产生更多的吡咯-蛋白加合物, 说明千里光次碱的结构影响PAs的毒效。同样就千里光酸部分进行比较, 开环双酯型PAs, 如毛果天芥菜碱(lasiocarpine, 亦即heliotridine型PA)产生的吡咯-蛋白加合物最多, 其次为大环(闭环)双酯(如倒千里光碱、千里光菲灵碱、千里光宁等), 最少的为单酯型PAs (如石松胺和天芥菜碱, 如表 1和图 2)。其次, 仅CYP3A4和CYP3A5两种CYPs亚型可使otonecine型PAs (如clivorine和克氏千里光碱)代谢活化; 同时, 该亚型对除野百合碱(monocrotaline)外的其他retronecine型PAs的活性也最高, 而CYP2A6对野百合碱活性最好。除了以上3种亚型, CYP1A1、CYP1A2、CYP2B6、CYP2C9、CYP2C19、CYP2D6和CYP2E1对retronecine型PAs (如倒千里光碱、千里光菲灵碱、千里光宁、全缘千里光碱、riddelliine、野百合碱和毛果天芥菜碱)亦具有代谢活化作用。作为紫草科植物中常见的开环型PAs, 毛果天芥菜碱在人及其他动物种属(猪、大鼠、小鼠、兔和羊)肝微粒体中的体外代谢轮廓及其差异也得到了较为系统的研究[40-42], 结果发现了12种代谢物且涉及5种主要代谢途径, 即脱氢(dehydrogenation, 产生吡咯代谢物L-M1/M2/M4-M7)、酯水解(ester bond cleavage, L-M3/M8)、去甲基(demethylation, L-M9)、氮氧化(N-oxidation, L-M10)以及羟基化作用(hydroxylation, L-M11/M12)。除酯水解途径外, 其他途径均由CYPs (特别是CYP3A)所介导(图 3)。从代谢活化的角度进行比较, 人肝微粒体脱氢作用最强, 其次是小鼠、猪、大鼠, 而对PAs毒性具有耐受性的种属(兔和羊)则较低。进一步研究[42]发现在加入GSH并有人肝胞浆酶的参与下, 毛果天芥菜碱可产生3种GSH吡咯结合物, 除了已知的7-GS-DHP(OH) (m/z 441)和7, 9-diGS-DHP (m/z 730), 还新发现了一种GSH吡咯结合物7-GS-DHP(CHO) (m/z 439), 其结构为7-GS-DHP(OH)上9位羟基进一步发生氧化形成甲醛基。有趣的是, 该研究组[43]还发现毛果天芥菜碱等PAs经人肝微粒体代谢产生一种不同于吡咯醇(DHP)的次生吡咯代谢物3H-吡咯嗪-7-烯-甲醇((3H-pyrrolizin-7-yl) methanol, m/z 135), 从结构上看为DHP的7位羟基脱水物(图 3, L-M1)。
PAs的代谢活化也可能是引发其遗传毒性或致癌性的重要原因。实验表明, 许多retronecine型PAs (如riddelliine、倒千里光碱和野百合碱)、heliotridine型PAs (如毛果天芥菜碱和天芥菜碱)以及otonecine型PAs (如clivorine)在体内外均可产生DHP衍生的DNA加合物[44, 45], 而此类DNA加合物水平与肝肿瘤发生呈正相关[31]。比较发现, DHP-DNA加合物在大鼠肝内的形成水平依以下顺序递减:倒千里光碱、毛果天芥菜碱、riddelliine、野百合碱、riddelliine N-oxide、克氏千里光碱、天芥菜碱、clivorine、石松胺、retronecine及platyphylliine (1, 2位饱和型PA)。其中, 单酯不饱和型PAs (如石松胺和天芥菜碱)一般弱于双酯不饱和型PAs (如倒千里光碱、毛果天芥菜碱、riddelliine等), 十一元大环双酯型PAs (如野百合碱)弱于十二元大环双酯型PAs (如倒千里光碱), 而无酯基的retronecine和饱和型PAs最弱[31, 45]。
在体内, CYPs介导的代谢活化同样在许多源自中草药的大环双酯型PAs所致肝毒性中扮演着重要的角色, 例如, Wang研究组[46, 47]对千里光中的千里光宁和阿多尼弗林碱的研究, Lin等[12]对菊三七中千里光宁的研究, 以及Tang等[48-51]对自消容中野百合碱、山紫菀中isoline和clivorine的研究等。但是, 类似的研究对于毛果天芥菜碱等开环类PAs还很少见。中药紫草及其近缘植物中不乏7, 9-双酯取代开环型(如myoscorpine和hydroxymyosorpine)和7-或9-单酯取代开环型(如石松胺和intermedine) PAs成分(图 1和2), 其代谢特征及其与毒性的相关性值得进一步探讨。
值得注意的是, CYPs不仅在PAs的代谢活化中发挥作用, 而且还参与其他代谢过程, 如介导PAs的氮氧化作用等。此外, 在体内其他Ⅰ相代谢酶, 如酯酶、黄素单氧化酶(FMOs)和NADPH-P450还原酶, 和Ⅱ相代谢酶, 如尿苷二磷酸葡萄糖醛酸转移酶(UGTs)和谷胱甘肽转移酶(GSTs)以及肠内菌群等均可能对PAs的代谢发挥作用[31, 52-57], 一些酶(如酯酶)及其代谢途径还可能在其中扮演解毒作用[48, 53], 但具体是哪些酶或代谢途径起作用以及起什么作用, 还应考虑PAs的分子结构、暴露量、药物代谢的种属和性别差异等因素[10, 35]。据报道已知结构的PAs及其氮氧化物多达660余种[31, 57], 尽管不同类型的PAs可能存在相似的代谢或毒性机制, 但结构的差异必然导致其不同的代谢活化效率与清除途径, 这些途径或共存于同一种PA分子或分属于不同的PA分子, 并在不同种属动物身上引起不同的毒性反应。以研究较多的野百合碱为例, 有报道表明该PA可被豚鼠肝酯酶(GPH1)水解为retronecine[48, 57], 而大鼠和小鼠的肝酯酶则对一些含乙酰基的PAs (如isoline和clivorine)发挥水解(去乙酰化)作用[32, 48]。本研究组[49]进一步考察了野百合碱在体内外代谢及毒性机制, 结果发现了5种共有代谢物, 即野百合碱氮氧化物(M-M1)、2个吡咯代谢物(DHP和7-GS-DHP, M-M2/3)及其相应的‘千里光次酸’部分(monocrotalic acid及其内酯M-M4/5), 分别代表了氮氧化和氧化脱氢(代谢活化)途径(图 3); 其中, CYP1A1/2与CYP3A除了介导野百合碱的代谢活化, 还与CYP2C及FMOs共同参与了野百合碱氮氧化物的形成。同时, 研究还发现NADPH-P450还原酶以及肠内菌群可能逆转野百合碱的氮氧化作用, 从而延缓其体内清除[52, 56]。由此得出, 在大鼠中野百合碱主要受到肝CYPs、FMOs、NADPH-P450还原酶以及肠内菌群等的代谢作用, 而酯酶或Ⅱ相代谢酶(如UGTs)等则可能不起作用。与酯酶类似, Ⅱ相代谢酶也具有明显的种属特异性, 如He等[54, 55]发现对野百合碱等PAs耐受的动物种属(如兔、牛、猪和羊)均有较强的N-葡萄糖醛酸化的活性, 而对PAs毒性较为敏感的大鼠和小鼠等动物则几乎没有活性。通过选择性化学抑制的方法可使PAs的肝毒性显著增强, 提示酯酶和/或UGTs介导的代谢可能与代谢活化相竞争, 从而在人或某些动物种属体内起到解毒作用[48, 54]。
由此可见, PAs代谢机制及其毒性作用呈现多样性, 这种多样性不仅体现在不同结构的PAs之间, 还体现于不同种属及代谢酶的多态性之间, 而其最终毒性有赖于各种代谢途径及其机制之间的平衡[57, 58]。
2.2 紫草及其PAs的毒性研究由中药紫草引起毒性的临床病例尚无报道, 有关动物体内毒性的研究亦不多见。曾有报道以云南产紫草煎剂对小鼠灌胃给药的LD50值为110.2 g·kg-1体重[1]; 滇紫草水煎液以最大给药量84.8 g·kg-1体重(相当于人拟用量的254倍)对小鼠灌胃给药, 观察14天, 未见明显异常及毒性[5]。但也有研究显示紫草具有一定的毒性, 如给予小鼠30%新疆紫草药饵, 1周内体重减轻30%左右, 15天内有40%死亡[59]; 新疆紫草的水煎液(剂量为5.0 g·kg-1以上时)对小鼠具有潜在的遗传毒性, 且呈剂量依赖性[60]等。此类研究均较为初步, 其毒性成分尚不得知。
值得注意的是紫草中的PAs多为开环类1, 2-不饱和型PAs成分(表 1), 其中不乏双酯型PAs (如myoscorpine等)。以毛果天芥菜碱为例, 其对大鼠腹腔(i.p.)单次给药后的LD50值为77 mg·kg-1体重, 明显高于其他一些大环双酯型PAs的毒性, 例如:野百合碱的LD50值为109 mg·kg-1体重[10, 51], clivorine为91 mg·kg-1体重[32]。但也有一些开环双酯型PAs毒性表现不强, 例如:蓝蓟定对大鼠(Wistar)口服给药后的LD50值为518 mg·kg-1体重, 而毛果天芥菜碱则为110 mg·kg-1体重(SD大鼠); 而且以蓝蓟定饲喂Wistar大鼠28天的NOAEL (未观察到有害作用剂量)为2.5 mg·kg-1体重, 远高于毛果天芥菜碱的0.6 mg·kg-1体重[61]; 单酯型的PAs毒性一般较低, 例如:腹腔给予大鼠天芥菜碱的LD50为296 mg·kg-1体重, 石松胺则超过了1 000 mg·kg-1体重等[62]。此外, 毛果天芥菜碱对实验动物有致癌作用, 每日以0.2 mg·kg-1体重对大鼠灌服即可诱导肿瘤发生, 在已确证有致癌作用的PAs (如野百合碱、riddelliine、clivorine、克氏千里光碱和symphytine)中显示了最强的致癌潜力[14, 63]。除了毛果天芥菜碱等少数PAs, 大多紫草类特征性PAs成分的毒理学研究还很少, 尚需进一步研究。
由于PAs的毒性与其结构及种属差异相关, 而且在实际应用中受到暴露量及服用期限不确定性的影响, 针对紫草科植物及其制品中PAs的主要存在类型和定量分析研究正逐渐展开[64-69]。例如, 紫草科天芥菜属植物Heliotropium popovii subsp. gillianum曾造成阿富汗爆发多起HSOS事件, Molyneux等[64]采用NMR及薄层色谱技术对其地上部中PAs成分进行了定性和定量分析, 发现含有天芥菜碱和毛果天芥菜碱, 其相对比例为91:9, 总PAs含量(含氮氧化物)为1.9% (以干品计)。Lin研究组[66]采用LC-MS/MS方法对中国市场上销售的蜂蜜产品中PAs的混入情况进行了分析, 结果表明, 58%的样品含有PAs, 含量范围为0.04~288.07 μg·kg-1, 石松胺和蓝蓟定是其中最主要的PAs成分, 而其主要来源可能为紫草科蓝蓟属(Echium)和菊科千里光属(Senecio)植物。对于中药‘紫草’, Roeder[8]曾报道新疆紫草中1和2 (表 1, 图 1)的总得率为0.001%, 硬紫草中3~5的总得率为0.02%, 但其准确含量还有待考察。迄今紫草中PAs的定性定量分析报道还很少, 进一步开展有关研究将有助于了解该类中药的用药风险, 并为设定合理的安全限量提供线索。
3 紫草类中药品种安全性研究的现状分析紫草科植物是PAs的重要来源之一, 同时也是许多传统草药、食物或膳食补充剂的植物来源, 多来源的中药紫草亦出自于此。尽管一些基原植物(如内蒙紫草和滇紫草)肝毒性PAs成分的研究(包括结构类型、数量和含量等)还比较缺乏[8, 10], 但已知来源的紫草类药材均可能含有肝毒性PAs成分。其次, 目前我国药材市场上常见的紫草药材除新疆紫草和内蒙紫草外, 还有云南、四川等地区的习惯用药滇紫草, 以及地区习用品(如帕米尔紫草和长花滇紫草等), 甚至还有巴基斯坦等国流入境内的非药典品[2, 9]。另据《中华本草》[1], 紫草科近30个品种在我国作为中草药使用, 其中紫草属4个、软紫草属2个和滇紫草属3个不等, 许多品种的PAs成分尚未了解。这些都可能对保证紫草药典正品的基原、品质和临床应用的有效性和安全性等产生影响[9, 10]。
另一方面, 尽管一些常见PAs (如野百合碱、千里光宁、clivorine和毛果天芥菜碱等)的代谢与毒性的研究已较为深入, 但许多紫草及其相关品种特征性PAs的代谢及其毒性机制还不清楚。同时, 大量研究主要为单一PA成分的体内外代谢和动物毒性实验, 而且多从一个代谢途径或分子机制来探讨PAs的毒性, 较少从整体上全面系统地考察和表征, 而对吡咯代谢物作用靶点的特异性及作用方式等认识不足, 也致难以找到有效的毒性标志物。特别是对于复杂体系如含PAs中草药来说, 此类研究还很少, 许多品种因缺乏安全性相关的基础研究, 其潜在的用药风险往往被低估。其次, 在临床上, 紫草可能因复方用药、用量少或使用时间不长等原因使人体对PAs的每日暴露量不高, 加之PAs体内代谢多样化、个体差异等因素, 常使其毒性难觅踪影, 因而很可能“忽略”由PAs带来的危害。研究表明, 即使PAs含量较低的药材, 如患者长期或过量使用, 由PAs蓄积导致的中毒危险依然存在, 特别是自医用药或误服滥用以及药材来源混杂的情形[12, 37]。从药物相互作用的角度来看, 有研究[70]发现紫草素等含酚羟基的萘醌类成分可拮抗野百合碱诱导的HSOS。本研究组[36]研究也表明川紫菀多糖在体内可以拮抗clivorine等PAs的肝毒性, 而对自消容水提物的毒代动力学研究[49]显示提取物中可能存在影响野百合碱吸收和代谢的组分, 或抑制其解毒(氮氧化)或增强其代谢活化(脱氢)作用。这些现象提示在体内紫草非PAs组分可能与PAs发生相互作用, 从而影响PAs的吸收、分布、代谢和排泄, 使其实际暴露量及毒反应终点发生改变[49-51]。紫草用途广泛, 除了在中医药中的应用, 还被广泛地应用于食品、化妆品和染料工业中[7-9, 71], 这种组分间相互作用的存在可能助长紫草安全风险的不确定性和隐匿性, 从而增大其防范与控制的难度。
从文献调研不难看出, 国内外已经针对相关的植物药(如聚合草)、食品(如蜂蜜)等开展了大量的研究, 获得了许多有关紫草科PAs及相关草药或植物药不良反应或毒害的证据[62-69]。为防范PAs潜在的肝毒性、致癌性及引发HSOS的风险, 世界卫生组织(WHO)、欧洲药品局(EMA)以及其他许多国家或地区都陆续制定和发布了含1, 2-不饱和PAs植物药及其制品的安全使用指南, 对PAs的每日摄入限量进行了规定[10, 14, 72]。如按照这些标准, 紫草潜在的用药风险是存在的。如以上述新疆紫草和硬紫草中已知PAs的得率[8]计算, 人临床应用可能产生的每日PAs暴露量(按日服剂量3~9 g计[1]), 新疆紫草可达30~90 μg, 硬紫草则为600~1 800 μg。该暴露量远高于EMA于2016年公布的成人(50 kg体重)每日不饱和PAs最大摄入限量(0.35 μg·d-1); 而硬紫草可能超过WHO的国际化学品安全规划署(IPCS)于1989年推测导致HSOS的每日最低摄入量(70 kg体重成人每日1 mg PAs)[10, 73]。这些法规或指南对我国含PAs中药临床用药风险的防控以及限量标准的制定无疑具有良好的示范和促进作用。日前国家药品监督管理局(CFDA)发布了《中药药源性肝损伤临床评价技术指导原则》, 显示了中药药源性肝损伤问题的重要性[74]; 与此同时, 有研究提出了基于整合证据链的中药肝损伤客观辨识模式和方法, 可为客观评价中药肝损伤临床发生率、准确辨识损肝“元凶”及易感人群等提供参考[75]。这些措施与方法仍在不断发展与完善, 也将促进包括紫草在内的含PAs中药品种整理、PAs类型与含量分析以及安全性评价等的基础研究, 推动相应法律法规的建立。
4 结论与建议PAs是一类天然的植物性毒素。目前, 含PAs中药与天然药物的毒副作用与安全性已受到国内外的普遍关注。紫草是我国常用传统中药之一, 其植物来源多样且应用广泛, 但研究表明含有肝毒性PAs成分。通过大量文献查阅, 本文从PAs的成分化学及其代谢毒性两个方面对紫草的安全性研究现状及进展进行了总结。结果发现, 紫草3种不同的基原植物(新疆紫草、硬紫草和滇紫草)均含有多种开环类1, 2位不饱和结构的PAs成分, 其结构、含量、代谢及毒理作用虽未完全阐明, 但从类似成分(如毛果天芥菜碱和天芥菜碱)的研究推测在体内均可能发生代谢活化并有导致肝毒的风险, 特别是7, 9-双酯取代开环型PAs。另外, 紫草在使用时可能受到代谢多态性及组分间相互作用的影响, 因而其肝毒性具有一定的不确定性和隐匿性, 特别是在长期应用的场合。鉴于目前紫草药材市场较为混乱的现象, 且由于紫草类药材均可能存在结构类型和含量不一的肝毒性PAs成分, 有必要对市场上的紫草样品进行全面的质量及安全性分析。
为了能明确紫草潜在的毒性作用, 同时为了防患于未然, 首先应阐明其毒效物质基础及其作用机制, 而对PAs代谢毒性及其解毒机制的研究不仅有助于对PAs及其相关中草药毒性本质的了解, 还可能发展新颖有效的防治方法。其次, 从中药“多组分、多靶点”的作用本质出发, 改变以往以单一PA成分为主体的研究思路, 采用基于整体动物模型的毒效与毒代动力学相结合的研究模式, 重点考察和解析给药后毒(药)效组分群的体内动态、组分间相互作用、体内代谢指纹、内源性小分子变化轨迹、毒(药)效相关性以及发掘基于机制的毒性标志物等, 从整体水平揭示紫草中潜在毒性成分的化学本质、作用机制及其用药风险, 从而为全面系统评价紫草的安全性和指导其临床合理用药提供科学依据。
| [1] | Chinese Herbals Editor Board, the State Administrative Bureau of Chinese Medicine of China. Chinese Herbals (中华本草)[M]. Shanghai: Shanghai Science and Technology Press, 1999: 525-557. |
| [2] | Zheng HJ, Zhan YH. Handbook for Identification of Modern Chinese Materia Medica (现代中药材鉴别手册)[M]. Beijing: China Medicinal Science and Technology Press, 2000: 355-357. |
| [3] | Chinese Pharmacopoeia Commission. Pharmacopoeia of the People's Republic of China (中华人民共和国药典)[S]. 2015 Ed. Vol Ⅰ. Beijing: China Medical Science Press, 2015: 340, 540. |
| [4] | Wu D, Li CY. Textual research on Arnebia[J]. Lishizhen Med Mater Med Res (时珍国医国药), 2008, 19: 2042–2043. |
| [5] | The Editor Board of Yunnan Food and Drug Administration Bureau. Yunnan Chinese Materia Medica Standards (云南省中药材标准) [S]. 2005 Ed. Vol 6. Kunming: Yunnan Science and Technology Press, 2010: 99, 485. |
| [6] | The Editor Board of Sichuan Food and Drug Administration Bureau. Sichuan Chinese Materia Medica Standards (四川省中药材标准) [S]. 2010 Ed. Chengdu: Sichuan Science and Technology Press, 2011: 608-609. |
| [7] | Malik S, Bhushan S, Sharma M, et al. Biotechnological approaches to the production of shikonins: a critical review with recent updates[J]. Crit Rev Biotechnol, 2016, 36: 327–340. DOI:10.3109/07388551.2014.961003 |
| [8] | Roeder E. Medicinal plants in China containing pyrrolizidine alkaloids[J]. Pharmazie, 2000, 55: 711–726. |
| [9] | Cheng M, Tang J, Li S. Recent advances in the research on pharmacological actions and quantitative analyses of naphthraquinones in Chinese medicinal herb "Zicao"[J]. Acta Pharm Sin (药学学报), 2018, 53: 2026–2039. |
| [10] | Tang J, Masao H. Pyrrrolizidine alkaloids-containing Chinese medicines in the Chinese pharmacopoeia and related safety concerns[J]. Acta Pharm Sin (药学学报), 2011, 46: 762–772. |
| [11] | Hartmann T, Ober D. Biosynthesis and metabolism of pyrrolizidine alkaloids in plants and specialized insect herbivores[J]. Top Curr Chem, 2000, 209: 207–243. DOI:10.1007/3-540-48146-X |
| [12] | Lin G, Wang JY, Li N, et al. Hepatic sinusoidal obstruction syndrome associated with consumption of Gynura segetum[J]. J Hepatol, 2011, 54: 666–673. DOI:10.1016/j.jhep.2010.07.031 |
| [13] | Li H, Zhang M. Research advances in sinusoidal obstruction syndrome[J]. J Clin Hepatol (临床肝胆病杂志), 2016, 32: 1429–1432. |
| [14] | European Medicines Agency. Public Statement on the Use of Herbal Medicinal Products Containing Toxic, Unsaturated Pyrrolizidine Alkaloids (PAs)[EB/OL]. London: European Medicines Agency, 2014-11-24[2018-09-06]. http://www.ema.europa.eu/docs/en_GB/document_library/Public_statement/2014/12/WC500179559.pdf. |
| [15] | Cai H, Sun F. Pyrrolizidine alkaloids-containing plants and hepatic veno-occlusive disease[J]. Adv Drug React J (药物不良反应杂志), 2007, 9: 229–234. |
| [16] | Liu QH, Yuan JQ, Yang JS. Chemical constituents and pharmacological activities of pyrrolizidine alkaloids in Boraginaceae[J]. Chin Pharm J (中国药学杂志), 2005, 40: 561–564. |
| [17] | Smyrska-Wieleba N, Wojtanowski KK, Mroczek T. Comparative HILIC/ESI-QTOF-MS and HPTLC studies of pyrrolizidine alkaloids in flowers of Tussilago farfara, and roots of Arnebia euchroma[J]. Phytochem Lett, 2016, 20: 339–349. |
| [18] | Ahmad L, He Y, Hao JC, et al. Toxic pyrrolizidine alkaloids provide a warning sign to overuse of the ethnomedicine Arnebia benthamii[J]. J Ethnopharmacol, 2017, 210: 88–94. |
| [19] | Krenn L, Wiedenfeld H, Roeder E. Pyrrolizidine alkaloids from Lithospermum officinale[J]. Phytochemistry, 1994, 37: 275–277. DOI:10.1016/0031-9422(94)85040-2 |
| [20] | Wiedenfeld H, Pietrosiuk A, Furmanowa M, et al. Pyrrolizidine alkaloids from Lithospermum canescens Lehm[J]. Z Naturforsch C, 2003, 58: 173–176. |
| [21] | El-Shazly A, Abdel-Ghani A, Wink M. Pyrrolizidine alkaloids from Onosma arenaria (Boraginaceae)[J]. Biochem Syst Eco, 2003, 31: 477–485. DOI:10.1016/S0305-1978(02)00177-1 |
| [22] | Kretsi O, Aligiannis N, Skaltsounis AL, et al. Pyrrolizidine alkaloids from Onosma leptantha[J]. Helv Chim Acta, 2003, 86: 3136–3140. DOI:10.1002/(ISSN)1522-2675 |
| [23] | Damianakos H, Sotiroudis G, Chinou I. Pyrrolizidine alkaloids from Onosma erecta[J]. J Nat Prod, 2013, 76: 1829–1835. DOI:10.1021/np300785g |
| [24] | Orfanou IM, Damianakos H, Bazos I, et al. Pyrrolizidine alkaloids from Onosma kaheirei Teppner (Boraginaceae)[J]. Rec Nat Prod, 2016, 10: 221–227. |
| [25] | Mellidis AS, Papageorgiou VP. Pyrrolizidine alkaloids of the plant Onosma heterophylla[J]. Chem Chron, 1988, 17: 67–73. |
| [26] | Roeder E, Wiedenfeld H, Kroeger R. Pyrrolizidine alkaloids of three taxa of Onosma (Boraginaceae-Lithospermeae)[J]. Phyton (Horn, Austria), 1993, 33: 41–49. |
| [27] | Mroczek T, Ndjoko K, Głowniak K, et al. On-line structure characterization of pyrrolizidine alkaloids in Onosma stellulatum and Emilia coccinea by liquid chromatography-ion-trap mass spectrometry[J]. J Chromatogr A, 2004, 1056: 91–97. DOI:10.1016/S0021-9673(04)01443-8 |
| [28] | Damianakos H, Jeziorek M, Pietrosiuk A, et al. The chemical profile of pyrrolizidine alkaloids from selected Greek endemic Boraginaceae plants determined by gas chromatography/mass spectrometry[J]. J AOAC Int, 2014, 97: 1244–1249. DOI:10.5740/jaoacint.SGEDamianakos |
| [29] | Tang J, Cheng M, Wei JX, et al. Identification of pyrrolizidine alkaloids in two major commercial sources of Zicao, a commonly used Chinese medicinal herb, by liquid chromatography coupled to triple tandem quadrupole mass spectrometry[C] // Brochure/Abstract of 2013 International Symposium of New Drug Discovery and Medicinal Chemistry. Wuhan: Chinese Pharmaceutical Association Hubei Branch, 2013: 40. |
| [30] | Edgar JA, Molyneux RJ, Colegate SM. Pyrrolizidine alkaloids: potential role in the etiology of cancers, pulmonary hypertension, congenital anomalies, and liver disease[J]. Chem Res Toxicol, 2015, 28: 4–20. DOI:10.1021/tx500403t |
| [31] | Fu PP. Pyrrolizidine alkaloids: metabolic activation pathways leading to liver tumor initiation[J]. Chem Res Toxicol, 2017, 30: 81–93. DOI:10.1021/acs.chemrestox.6b00297 |
| [32] | Lin G, Tang J, Liu XQ, et al. Deacetylclivorine: a gender-selective metabolite of clivorine formed in female Sprague-Dawley rat liver microsomes[J]. Drug Metab Dispos, 2007, 35: 607–613. DOI:10.1124/dmd.106.014100 |
| [33] | Liang Q, Sheng Y, Jiang P, et al. The gender-dependent difference of liver GSH antioxidant system in mice and its influence on isoline-induced liver injury[J]. Toxicology, 2011, 280: 61–69. DOI:10.1016/j.tox.2010.11.010 |
| [34] | Ruan J, Yang M, Fu PP, et al. Metabolic activation of pyrrolizidine alkaloids: insights into the structural and enzymatic basis[J]. Chem Res Toxicol, 2014, 27: 1030–1039. DOI:10.1021/tx500071q |
| [35] | Kolrep F, Numata J, Kneuer C, et al. In vitro biotransformation of pyrrolizidine alkaloids in different species. Part Ⅰ: Microsomal degradation[J]. Arch Toxicol, 2018, 92: 1089–1097. DOI:10.1007/s00204-017-2114-7 |
| [36] | Wen JX. Isolation, Purification and Hepatoprotective Effects of Polysaccharides from Ligularia hodgsonii (川紫菀多糖的分离纯化及保肝作用研究)[D]. Wuhan: Wuhan University, 2018. |
| [37] | Gao H, Li N, Wang JY, et al. Definitive diagnosis of hepatic sinusoidal obstruction syndrome induced by pyrrolizidine alkaloids[J]. J Dig Dis, 2015, 13: 33–39. |
| [38] | Li N, Xia Q, Ruan J, et al. Hepatotoxicity and tumorigenicity induced by metabolic activation of pyrrolizidine alkaloids in herbs[J]. Curr Drug Metab, 2011, 12: 823–834. DOI:10.2174/138920011797470119 |
| [39] | Yang X, Li W, Sun Y, et al. Comparative study of hepatotoxicity of pyrrolizidine alkaloids retrorsine and monocrotaline[J]. Chem Res Toxicol, 2017, 30: 532–539. DOI:10.1021/acs.chemrestox.6b00260 |
| [40] | Fashe MM, Juvonen RO, Petsalo A, et al. Species differences in the in vitro metabolism of lasiocarpine[J]. Chem Res Toxicol, 2015, 28: 2034–2044. DOI:10.1021/acs.chemrestox.5b00253 |
| [41] | Fashe MM, Juvonen RO, Petsalo A, et al. In silico prediction of the site of oxidation by cytochrome P450 3A4 that leads to the formation of the toxic metabolites of pyrrolizidine alkaloids[J]. Chem Res Toxicol, 2015, 28: 702–710. DOI:10.1021/tx500478q |
| [42] | Muluneh F, Häkkinen MR, El-Dairi R, et al. A new glutathione conjugate of pyrrolizidine alkaloids produced by human cytosolic enzyme-dependent reactions in vitro[J]. Rapid Commun Mass Spectrom, 2018, 32: 1344–1352. DOI:10.1002/rcm.v32.16 |
| [43] | Fashe MM, Juvonen RO, Petsalo A, et al. Identification of a new reactive metabolite of pyrrolizidine alkaloid retrorsine: (3H-pyrrolizin-7-yl)methanol[J]. Chem Res Toxicol, 2014, 27: 1950–1957. DOI:10.1021/tx5002964 |
| [44] | Xia Q, Chou MW, Edgar JA, et al. Formation of DHP-derived DNA adducts from metabolic activation of the prototype heliotridine-type pyrrolizidine alkaloid, lasiocarpine[J]. Cancer Lett, 2006, 231: 138–145. DOI:10.1016/j.canlet.2005.01.023 |
| [45] | Xia Q, Yan J, Chou MW, et al. Formation of DHP-derived DNA adducts from metabolic activation of the prototype heliotridine-type pyrrolizidine alkaloid, heliotrine[J]. Toxicol Lett, 2008, 178: 77–82. DOI:10.1016/j.toxlet.2008.02.008 |
| [46] | Xiong A, Yang L, He Y, et al. Identification of metabolites of adonifoline, a hepatotoxic pyrrolizidine alkaloid, by liquid chromatography/tandem and high-resolution mass spectrometry[J]. Rapid Commun Mass Spectrom, 2009, 23: 3907–3916. DOI:10.1002/rcm.v23:24 |
| [47] | Wang C, Li Y, Gao J, et al. The comparative pharmacokinetics of two pyrrolizidine alkaloids, senecionine and adonifoline, and their main metabolites in rats after intravenous and oral administration by UPLC/ESIMS[J]. Anal Bioanal Chem, 2011, 401: 275–287. DOI:10.1007/s00216-011-5075-3 |
| [48] | Tang J, Akao T, Nakamura N, et al. In vitro metabolism of isoline, a pyrrolizidine alkaloid from Ligularia duciformis, by rodent liver microsomal esterases and enhanced hepatotoxicity by esterase inhibitors[J]. Drug Metab Dispos, 2007, 35: 1832–1839. DOI:10.1124/dmd.107.016311 |
| [49] | Tang J, Cheng M, Hattori M. Toxicokinetics and bioavailability of monocrotaline from Crotalariae Assamicae Semen decoction after oral administration in rats: comparison with monocrotaline alone[C] //Abstracts of The 11th International ISSX Meeting BEXCO. Busan, Republic of Korea: ISSX, 2016: P244. |
| [50] | Cheng M, Tang J, Gao Q, et al. Analysis on clivorine from alkaloid in aqueous extract of Ligularia hodgsonii and its hepatotoxicity in rats[J]. Chin Tradit Herb Drugs (中草药), 2011, 42: 2507–2511. |
| [51] | Cheng M, Tang J, Jiang L, et al. Toxic effects of aqueous extract of Crotalariae Assamicae Semen in rats and possible mechanism in association with liver damage[J]. China J Chin Mater Med (中国中药杂志), 2013, 38: 1800–1805. |
| [52] | Tang J, Wang Z, Akao T, et al. Human intestinal bacteria mediate reduction of the N-oxides of isoline and monocrotaline to the corresponding parent alkaloids[J]. Asian J Chem, 2013, 25: 2027–2030. DOI:10.14233/ajchem |
| [53] | Tang J, Wang Z, Akao T, et al. Further evidence on the intramolecular lactonization in rat liver microsomal metabolism of 12-O-acetylated retronecine-type pyrrolizidine alkaloids[J]. Nat Prod Commun, 2013, 8: 1545–1546. |
| [54] | He YQ, Liu Y, Zhang BF, et al. Identification of the UDP-glucuronosyltransferase isozyme involved in senecionine glucuronidation in human liver microsomes[J]. Drug Metab Dispos, 2010, 38: 626–634. DOI:10.1124/dmd.109.030460 |
| [55] | He YQ, Yang L, Liu HX, et al. Glucuronidation, a new metabolic pathway for pyrrolizidine alkaloids[J]. Chem Res Toxicol, 2010, 23: 591–599. DOI:10.1021/tx900328f |
| [56] | Tang J, Hattori M. Role of NADPH-P450 reductase in the reverse of monocrotaline N-oxide in the microsomal metabolism of monocrotaline and its toxic implication[C] //Program and Abstract Book of 18th International Symposium on Microsomes and Drug Oxidations. Beijing: Peking Union Medical College Press, 2010: 287. |
| [57] | Fu PP, Xia Q, Lin G, et al. Pyrrolizidine alkaloids-genotoxicity, metabolism enzymes, metabolic activation, and mechanisms[J]. Drug Metab Rev, 2004, 36: 1–55. |
| [58] | Liu W, Li X, Zhou B, et al. Differential induction of apoptosis and autophagy by pyrrolizidine alkaloid clivorine in human hepatoma Huh-7.5 cells and its toxic implication[J]. PLoS One, 2017, 12: e0179379. DOI:10.1371/journal.pone.0179379 |
| [59] | Li Y, Zhou X. Research progress of Arnebia euchroma[J]. Xinjiang J Tradit Chin Med (新疆中医药), 2002, 20: 75–77. |
| [60] | Li X, Yang L, Ji K. Study of Chinese drug Arnebia genotoxicity with micronucleus test[J]. Chin J Reprod Health (中国生育健康杂志), 2003, 14: 167–169. |
| [61] | Dalefield RR, Gosse MA, Mueller U. A 28-day oral toxicity study of echimidine and lasiocarpine in Wistar rats[J]. Regul Toxicol Pharmacol, 2016, 81: 146–154. DOI:10.1016/j.yrtph.2016.08.006 |
| [62] | Coulombe RA. Pyrrolizidine alkaloids in foods[J]. Adv Food Nutr Res, 2003, 45: 61–99. DOI:10.1016/S1043-4526(03)45003-1 |
| [63] | Chen L, Mulder PPJ, Louisse J, et al. Risk assessment for pyrrolizidine alkaloids detected in (herbal) teas and plant food supplements[J]. Regul Toxicol Pharmacol, 2017, 86: 292–302. DOI:10.1016/j.yrtph.2017.03.019 |
| [64] | Molyneux RJ, Gardner DL, Colegate SM, et al. Pyrrolizidine alkaloid toxicity in livestock: a paradigm for human poisoning?[J]. Food Addit Contam A, 2011, 28: 293–307. DOI:10.1080/19440049.2010.547519 |
| [65] | Boppré M, Colegate SM, Edgar JA. Pyrrolizidine alkaloids of Echium vulgare honey found in pure pollen[J]. J Agric Food Chem, 2005, 53: 594–600. DOI:10.1021/jf0484531 |
| [66] | Zhu L, Wang Z, Wong L, et al. Contamination of hepatotoxic pyrrolizidine alkaloids in retail honey in China[J]. Food Control, 2018, 85: 484–494. DOI:10.1016/j.foodcont.2017.10.026 |
| [67] | Mulder PPJ, López P, Castelari M, et al. Occurrence of pyrrolizidine alkaloids in animal- and plant-derived food: results of a survey across Europe[J]. Food Addit Contam A, 2018, 35: 118–133. DOI:10.1080/19440049.2017.1382726 |
| [68] | Avula B, Sagi S, Wang YH, et al. Characterization and screening of pyrrolizidine alkaloids and N-oxides from botanicals and dietary supplements using UHPLC-high resolution mass spectrometry[J]. Food Chem, 2015, 178: 136–148. DOI:10.1016/j.foodchem.2015.01.053 |
| [69] | Staiger C. Comfrey: a clinical overview[J]. Phytother Res, 2012, 26: 1441–1448. |
| [70] | Zhao T, Wu T, Lu D. Prophylaxis of sinusoidal obstruction syndrome by Arnebia euchroma root alcoholic extract in rats model[J]. Chin Pharm J (中国药学杂志), 2005, 40: 1626–1629. |
| [71] | Zhan Z, Hu J, Liu T, et al. Advances in studies on chemical compositions and pharmacological activities of Arnebiae Radix[J]. China J Chin Mater Med (中国中药杂志), 2015, 40: 4127–4135. |
| [72] | Wang D, Huang L, Chen S. Senecio scandens Buch.-Ham.: a review on its ethnopharmacology, phytochemistry, pharmacology, and toxicity[J]. J Ethnopharmacol, 2013, 149: 1–23. DOI:10.1016/j.jep.2013.05.048 |
| [73] | Moreira R, Pereira D, Valentão P, et al. Pyrrolizidine alkaloids: chemistry, pharmacology, toxicology and food safety[J]. Int J Mol Sci, 2018, 19: 1668. DOI:10.3390/ijms19061668 |
| [74] | State Drug Administration of China. Announcement of the State Drug Administration on the technical guidelines for the clinical evaluation of Chinese herbal drugs-induced liver injury (国家药品监督管理局关于发布中药药源性肝损伤临床评价技术指导原则的通告)[EB/OL]. 2018-06-12.[2018-09-06]. Beijing: State Drug Administration of China, http://cnda.cfda.gov.cn/WS04/CL2050/229510.html. |
| [75] | Wang JB, Li C, Zhu Y, et al. Integrated evidence chain-based identification of Chinese herbal medicine-induced hepatotoxicity and rational usage: exemplification by Polygonum Multiflorum (He shou wu)[J]. Chin Sci Bull (科学通报), 2016, 61: 971–980. |
 2019, Vol. 54
2019, Vol. 54


