水凝胶是以水为分散介质, 由高分子聚合物通过离子相互作用、范德华力、氢键、疏水作用力或结晶段交联等方式形成、具有三维网状结构的半固体[1]。卡拉胶作为一种常用的水凝胶辅料, 是从红藻中提取的天然阴离子线性多糖, 由1, 3-苷键连接β-D-半乳糖吡喃基和1, 4-苷键连接的α-D-半乳糖吡喃基为基本单元的线性聚糖形成的交替共聚物[2]。根据硫酸酯基团的数量、位置及3, 6-內醚半乳糖含量的不同, 可将卡拉胶分为7种类型[3], 其中κ-卡拉胶(kappa carrageenan, KC)除具有良好的生物相容性和生物可降解性等特殊性能外, 因其特有的低毒性使其在食品和药学领域中有着极为广泛的应用, 常用作胶凝剂、稳定剂和增稠剂[4]应用于药物缓控释系统、伤口敷料、组织工程[5]及治疗性生物大分子的组织再生和细胞递送等。作为胶凝剂或增稠剂时, KC与其他辅料在适当条件下共混可表现出与仅增大KC浓度不同的黏弹性和胶凝的性质[6, 7]。
流变学是用来研究在外力作用下材料变形和流动的特性。通过剪切速率和剪切时间的变化研究材料的性质[8], 可作为确定给药方式的依据, 如软膏从管状包装中的可挤出性、注射剂的通针性、药物在应用部位的滞留性和延展性等[9, 10], 了解载药基质的流变特性是药物制剂处方设计和制备的关键。因此, 本文系统地研究了6种辅料对KC流变学性质和黏度的影响, 并探究其作用规律, 为拓宽KC在药学领域的应用提供理论参考。
材料与方法材料与仪器KC (美国FMC公司, 型号: GP812, 批号: 10212160);瓜尔胶(Guargum, GG, 相对分子质量: 220 000, 天津博迪化工有限公司, 批号: 160301);透明质酸钠(sodium hyaluronate, HA-Na, 相对分子质量: 150 000, 华熙福瑞达生物医药有限公司, 批号: 150322);羟丙基甲基纤维素(hydroxypropyl methyl cellulose, HPMC, K4M, 美国Colorcon公司, 批号: PD353356);魔芋胶(konjac gum, KGM, 上海源叶生物科技有限公司, 批号: 160301);羧甲基纤维素钠(sodium carboxymethyl cellulose, CMC-Na, 天津博迪化工有限公司, 黏度0.8~1.2 Pa·s, 批号: 151015);黄原胶(xanthan gum, XG, 上海源叶生物科技有限公司, 批号: 160322);去离子水(SZ-93自动双重纯水蒸馏器, 上海亚荣生化仪器厂)。电子天平(ESJ210-4型, 沈阳龙腾电子称量仪器有限公司); 集热式恒温加热磁力搅拌器(DF-101S型, 巩义市予华仪器有限责任公司); 旋转黏度计(DV-T2型黏度温控一体机, 上海尼润智能科技有限公司)。
复配胶的配制 因辅料性质差异, 选择配制方法有所不同。KC与HPMC复配胶:取KC适量, 室温下分散均匀, 置于70 ℃恒温水浴中搅拌20 min后, 将适量的HPMC加入到70 ℃ KC溶液中, 继续搅拌分散10 min, 缓慢降至室温; 其他种类的复配胶:取KC和辅料适量, 在室温下分散混合均匀, 置于70 ℃恒温水浴中搅拌30 min, 完全溶解后停止搅拌, 待其没有气泡后取出; 为使样品充分溶胀, 以上样品在制备均匀后均需室温放置24 h。单体胶溶液的配制方法与复配胶相同, KC质量分数均为0.8%。
流体流型 配制系列浓度的复配胶溶液, 将待测液置于37 ℃样品槽中恒温15 min, 采用旋转黏度计, 选择适宜型号转子从低剪切速率到高剪切速率(23~68 S-1)测定黏度, 绘制剪切速率与黏度和剪切应力的关系曲线。
通过幂律方程Eq.1进一步推导得Eq.2, 对流变曲线进行线性拟合, 得到lnτ~lnγ流变曲线。
| $ \tau {\rm{ = }}K{\gamma ^n} $ | (1) |
| $ \ln \tau = \ln K + n\ln \gamma $ | (2) |
式中, τ为剪切应力; γ为剪切速率; η为表观黏度; K表示稠度系数; n为非牛顿指数。K是η量度, 其值越大说明液体黏度越大; n为非牛顿程度的量度, 表示与牛顿流体的偏离程度, n = 1时为牛顿性流体, 黏度不随剪切速率而变化; 0 < n < 1时为假塑性流体, 黏度随剪切速率的增加而降低; n > 1时为胀塑性流体[9], 黏度随剪切速率的增加而增大。n与1相差值越大, 非牛顿性越强[11]。
浓度对黏度的影响 配制系列浓度的复配胶溶液, 测定溶液在转速100 r·min-1、37 ℃下黏度, 在一定浓度范围内, 绘制对数黏度(lnη)与质量浓度(C)的关系曲线, 通过斜率(k)比较不同复配胶的胶凝能力, k表示浓度的变化能够引起黏度变化的程度, k值越大, 说明复配胶中较小的浓度变化就可引起较大的黏度变化, 黏度对浓度的依赖性越强。
温度对黏度的影响 测定转速为100 r·min-1, 不同温度(310.15、313.15、318.15、323.15和333.15 K)下0.4%复配胶溶液的黏度。根据阿伦尼乌斯[12]方程Eq.3, 取对数得Eq.4, 绘制lnη与1/T的关系曲线, 计算黏流活化能。
| $ \eta {\rm{ = A}}{{\rm{e}}^{\frac{{{E_\eta }}}{{RT}}}} $ | (3) |
| $ \ln \eta {\rm{ = A' + }}\frac{{{E_\eta }}}{{RT}} $ | (4) |
其中, η为表观黏度(Pa·s); A'为常数; R为气体常数(8.314 J·mol-1·K-1); T为绝对温度(K); Eη为黏流活化能(J·mol-1)。Eη表示流动过程中, 流动单元用于克服位垒, 由原位置跃迁到附近“空穴”所需的最小能量, 反映复配胶对温度的敏感程度。Eη越高, 黏度对温度越敏感[13, 14], 反之, 则说明温度对黏度的影响较小, 黏度的热稳定性良好。
辅料种类对黏度的影响 配制复配胶及单体胶溶液, 在转速为100 r·min-1、37 ℃条件下, 分别测定其黏度, 绘制复配胶及单体胶的黏度曲线。
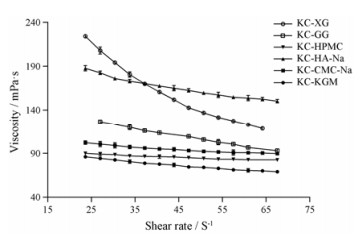
结果与讨论 1 复配胶的流体流型高分子溶液在浓度较小时显示出牛顿流体的特征, 当浓度增大后则显示出非牛顿流体特征。实验中发现0.8% KC溶液在所测条件下呈现出牛顿流体特性, 其黏度随剪切速率的变化不显著。如图 1所示, 当KC与XG、GG、HPMC、HA-Na、CMC-Na和KGM复配后, 其黏度随着剪切速率的增加而逐渐降低, 具有剪切变稀的特点, 剪切应力与剪切速率不成正比, 说明复配胶溶液均为非牛顿流体。
|
Figure 1 Effect of shear rate on the viscosity of different compound gels solution at (37 ± 0.1) ℃. KC: Kappa carrageenan; XG: Xanthan gum; GG: Guargum; HPMC: Hydroxypropyl methyl cellulose; HA-Na: Sodium hyaluronate; CMC-Na: Sodium carboxymethyl cellulose; KGM: Konjac gum. n = 3, x±s |
利用Eq.2对6种复配胶流变学曲线拟合, 结果见表 1。由表中数据可知, 所测数据中所有R2 > 0.994, 说明拟合曲线相关性良好。非牛顿指数n均小于1, 说明复配胶均为假塑性流体, 相同浓度的不同复配胶溶液的假塑性和黏度顺序均为KC-XG > KC-GG > KC-HA-Na > KC-KGM > KC-HPMC > KC-CMC-Na; 同一复配胶浓度越大, 黏度越大, 剪切稀释越明显, 假塑性程度越高。复配胶表现出明显的剪切稀化现象, 即黏度随剪切速率的增加而显著减小, 原因在于:在静置时, 复配胶溶液中的分子舒展卷曲, 随机分布, 不定向排列; 当施加剪切力时, 溶液中的分子由于分子链较长且存在许多支链, 相互缠绕在一起, 阻碍了溶液的流动, 黏度较高; 随着剪切速率的进一步增加, 相互缠绕的分子遭到破坏, 相互缠绕的分子数降低, 且分子链随着剪切力的方向定向排列, 流动阻力降低, 表现为黏度降低[11, 15], 且随剪切速率的增加, 黏度降低的越缓慢。KC-XG复配胶表现出更加明显的剪切稀化现象, 黏度随剪切速率增加而迅速下降, 原因可能是KC与XG分子链间或两者的单体胶分子间缔合力弱, 较低的剪切速率就能使胶体分子链间解缠结, 黏度降低较快[15]。6种辅料单体胶溶液均为假塑性流体, KC与6种辅料复配后表现为假塑性流体的特征, 说明辅料对复配胶的流体流型起主导作用。
| Table 1 Rheological parameters of different compound gels solution at (37 ± 0.1) ℃. τ: Shear stress; γ: Shear rate; K: Consistency coefficient; n: Non-newtonian index; R2: Correlation coefficient. n = 3, x±s |
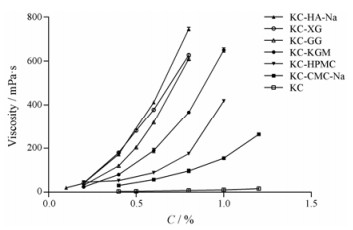
黏度是分子间相互作用的体现, 反映了凝胶内部分子被破坏的难易程度, 主要取决于分子间形成氢键的多少和强弱。由图 2可以看出复配胶黏度随辅料浓度的增加而增大, 与表 1中稠度系数K随浓度增加而增大的结果一致。随着辅料浓度增大, 单位体积分子数增多, 分子链的自由空间变窄, 分子链密度增大, 相互交联分子数目增多, 分子间摩擦力增大, 所以黏度增大。
|
Figure 2 Effect of concentration (C) on the viscosity of different compound gels solution at (37 ± 0.1) ℃. n = 3, x±s |
黏度对数lnη与C拟合结果见表 2。由表中数据可知, 斜率即黏度对浓度的依赖性顺序为KC-HA-Na > KC-GG > KC-XG > KC-KGM > KC-HPMC > KC-CMC-Na > KC, 复配胶溶液的斜率均大于KC单体胶, 说明6种复配胶溶液中, 辅料浓度对复配胶的黏度起主导作用。
| Table 2 Correlation results of different compound gels by lnη-C equation at (37 ± 0.1) ℃. k: Slope. n = 3, x±s |
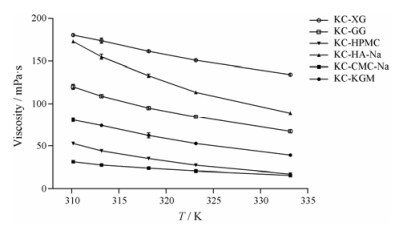
黏度随温度变化曲线见图 3。随着温度的升高, 6种复配胶黏度均降低。升高温度对分子运动具有双重作用:一是分子吸收热量, 动能增加, 分子运动速率加快, 辅料与KC分子形成的螺旋体系被破坏, 聚集的分子数目变少, 分子间相互作用力减小, 液体流动阻力减小; 二是使高分子物质的体积膨胀, 增加了分子间的空隙, 分子链更易移动, 分子间相互作用降低, 黏度下降[16]。黏度与辅料的种类有关, 相同浓度下黏度大小为KC-XG > KC-HA-Na > KC-GG > KC-KGM > KC-HPMC > KC-CMC-Na。
|
Figure 3 Effect of temperature on the viscosity of different 0.4% compound gels solution. n = 3, x±s |
根据方程对复配胶溶液黏度lnη与1/T进行拟合, 结果见表 3。Eη与复配胶的浓度和测定条件有关, 由表中数据可知, 0.4%的6种复配胶Eη值顺序为KC-HPMC > KC-KGM > KC-CMC-Na > KC-HA-Na > KC-GG > KC > KC-XG。6种复配胶温度对黏度的影响程度差别很大, Eη值在11~44 kJ·mol-1, KC-HPMC、KC-KGM、KC-CMC-Na、KC-HA-Na和KC-GG的Eη值大于KC, 说明KC与其复配后需要在更高的温度下才能克服聚合物分子流动过程中的能量障碍, 黏度对温度的敏感度升高。相反, KC-XG的Eη值小于KC, 说明KC-XG与KC相比具有更好的柔性线性分子链, 可以在较低温度下流动, 温度对黏度的影响较小。结合图 3的黏度顺序, KC-XG的黏度最大而黏流活化能最小, 说明黏流活化能是表示流动性的一个参数, 与体系黏度无直接关系[17]。
| Table 3 Correlation results of different compound gels (0.4%) by lnη-1/T equation (310.15-333.15 K). T: Temperature; Eη: Viscous flow activation energy. n = 3, x±s |
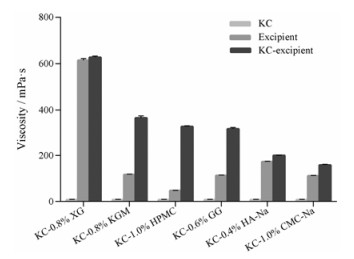
6种辅料与KC复配后的黏度变化见图 4。由图可知, 复配胶黏度均较两者单体胶黏度增大, 且产生了“1+1 > 2”的效应, 说明6种辅料均能与KC产生协同增黏作用[18]。这种协同增黏作用主要与添加的辅料本身的性质及复配胶分子间的相互作用有关, 不同辅料与KC的协同增黏程度不同, 辅料对复配胶的黏度起决定性作用, 故通过比较不同辅料单位浓度引起KC黏度的变化率来判断辅料对KC的增黏程度, 顺序为KC-HPMC > KC-KGM > KC-GG > KC-CMC-Na > KC-HA-Na > KC-XG。
|
Figure 4 Effect of different excipients on the viscosity of 0.8% KC at (37 ± 0.1) ℃. n = 3, x±s |
6种辅料均为高分子化合物, 分子质量和体积很大, 分子结构中均含有大量的亲水基团, 能够与水发生氢键等相互作用, 同时也可能与KC分子中的羟基和硫酸酯基团发生分子间相互作用。KC与辅料间交互作用机制可能是: KC为阴离子聚合物, 在冷却过程中, 分子链经历了从卷曲到双螺旋的构象转换过程, 分子内存在竞争性反应, 螺旋结构可自交联或与辅料分子交联[19, 20]。CMC-Na、HA-Na和XG为阴离子聚合物, 与KC分子交联时存在电荷相斥作用; HPMC、KGM和GG为非离子型聚合物, 故KC与HPMC、KGM、GG分子交联要优于与CMC-Na、HA-Na、XG及自交联。此外, 复配后, 两者单体胶分子链的自由活动空间变窄, 有利于分子链穿过相邻链进而形成较高密度缠结, 且不容易解缠结, 分子缔合增强, 更容易产生局部或连续的凝胶网络结构[21, 22], 溶液中交联结点增多, 分子间和分子内的摩擦力增大, 表现为复配后黏度增大。复配胶黏度大于两者单体胶黏度之和, 通过测定单体胶和复配胶的黏度可能作为判断单体胶间是否存在分子间相互作用的依据。
结论6种辅料与KC复配后均能形成半固体状凝胶, 且对KC的流变学性质产生影响, 可以通过改变辅料种类、浓度和温度来改变KC的流变学性质; 6种辅料均与KC存在协同增黏作用, 加入少量辅料即可显著增加KC的黏度, 采取复配的方式具有减少辅料用量, 增加用药安全性能的优势; 复配胶黏度随剪切速率和温度的增加而降低, 具有剪切稀化的特点, 且浓度越大, 黏度越大, 剪切稀化作用越明显; 复配胶的流变学性质良好, 具有触变性和假塑性特征, 可能作为外用凝胶制剂、乳剂和可注射水凝胶基质应用于药学领域。本文只对复配胶的流变学性质及黏度的影响因素进行了评价, 除此之外, pH、离子强度、分子质量、电荷密度和总聚合物浓度等都会影响到复配胶的流变学性质, 实际应用时还应结合凝胶性质、脱水收缩性和降解性等性质进行全面分析, 综合考虑。
| [1] | Liu S, Li L. Thermoreversible gelation and scaling behavior of Ca2+-induced κ-carrageenan hydrogels[J]. Food Hydrocoll, 2016, 61: 793–800. DOI:10.1016/j.foodhyd.2016.07.003 |
| [2] | Li L, Ni R, Shao Y, et al. Carrageenan and its applications in drug delivery[J]. Carbohydr Polym, 2014, 103: 1–11. DOI:10.1016/j.carbpol.2013.12.008 |
| [3] | Lu M, Xing HN, Ding PT. Research and application of carrageenan in pharmaceutics[J]. J Shenyang Pharm Univ (沈阳药科大学学报), 2015, 32: 400–407. |
| [4] | Prajapati VD, Maheriya PM, Jani GK, et al. Carrageenan:a natural seaweed polysaccharide and its applications[J]. Carbohydr Polym, 2014, 105: 97–112. DOI:10.1016/j.carbpol.2014.01.067 |
| [5] | Zia KM, Tabasum S, Nasif M, et al. A review on synthesis, properties and applications of natural polymer based carra geenan blends and composites[J]. Int J Biol Macromol, 2017, 96: 282–301. DOI:10.1016/j.ijbiomac.2016.11.095 |
| [6] | Kozlowska J, Pauter K, Sionkowska A. Carrageenan-based hydrogels:effect of sorbitol and glycerin on the stability, swelling and mechanical properties[J]. Polym Test, 2018, 67: 7–11. DOI:10.1016/j.polymertesting.2018.02.016 |
| [7] | Li CX, Li CY, Liu ZS, et al. Enhancement in bioavailability of ketorolac tromethamine via intranasal in situ hydrogel based on poloxamer 407 and carrageenan[J]. Int J Pharm, 2014, 474: 123–133. DOI:10.1016/j.ijpharm.2014.08.023 |
| [8] | Hu J, Chen DW, Quan DQ. Rheological properties of poloxamer 407 aqueous solutions[J]. Acta Pharm Sin (药学学报), 2011, 46: 227–231. |
| [9] | Ako K. Influence of elasticity on the syneresis properties of kappa-carrageenan gels[J]. Carbohydr Polym, 2015, 115: 408–414. DOI:10.1016/j.carbpol.2014.08.109 |
| [10] | Song LN, Li HR, Wang HY, et al. Preparation and properties of thermosensitive in situ gel for ophthalmic formulation containing pearl hydrolyzate[J]. Acta Pharm Sin (药学学报), 2016, 51: 1622–1628. |
| [11] | Tong C, Li HR, Li Z, et al. Rheology property study of kappa carrageenan[J]. China Pharm J (中国药学杂志), 2017, 52: 130–134. |
| [12] | Lu YX, He HB, Cui Y, et al. Rheological properties of sucrose acetate isobutyrate in situ gel[J]. Acta Pharm Sin (药学学报), 2007, 42: 445–449. |
| [13] | Hou YL, Li HR, Gao YN, et al. The rheology properties of common hydrophilic gel excipients[J]. Acta Pharm Sin (药学学报), 2014, 49: 1181–1187. |
| [14] | Wu QH, Wu JA. Introduction to Polymer Rheology (高分子材料流变学导论)[M]. Beijing: Chemical Industry Press, 1994: 37-43. |
| [15] | Jiang MF, Xiao M, Nie XW, et al. Interactions between konjac glucomannan and curdlan[J]. Food Sci (食品科学), 2016, 37: 54–58. |
| [16] | Zheng JM. Polymer Science in Pharmaceutics (药用高分子材料学)[M]. Beijing: China Medical Science and Technology Press, 2009: 64. |
| [17] | Li P, Ding Z, Ma LX, et al. Analysis of viscous flow properties of asphalt in aging process[J]. Constr Build Mater, 2016, 124: 631–638. DOI:10.1016/j.conbuildmat.2016.06.136 |
| [18] | Derkach SR, Ilyin SO, Maklakova AA, et al. The rheology of gelatin hydrogels modified by κ-carrageenan[J]. LWT-Food Sci Technol, 2015, 63: 612–619. DOI:10.1016/j.lwt.2015.03.024 |
| [19] | Wei Y. Study on the Gel Properties of κ-Carrageenan and Synergistic Effect of κ-Carrageenan and Konjac Gum (κ-卡拉胶的凝胶化作用及其与魔芋胶协同作用特性研究)[D]. Changsha: Central South University of Forestry and Technology, 2010. |
| [20] | Lin JH, Liang CW, Chang YH. Effect of starch source on gel properties of kappa-carrageenan-starch dispersions[J]. Food Hydrocoll, 2016, 60: 509–515. DOI:10.1016/j.foodhyd.2016.04.024 |
| [21] | Luo X, He P, Lin X. The mechanism of sodium hydroxide solution promoting the gelation of Konjac glucomannan (KGM)[J]. Food Hydrocoll, 2013, 30: 92–99. DOI:10.1016/j.foodhyd.2012.05.012 |
| [22] | Fitzpatrick P, Meadows J, Ratcliffe I, et al. Control of the properties of xanthan/glucomannan mixed gels by varying xanthan fine structure[J]. Carbohydr Polym, 2013, 92: 1018–1025. DOI:10.1016/j.carbpol.2012.10.049 |
 2018, Vol. 53
2018, Vol. 53


