2. 陕西省中药资源产业化协同创新中心, 陕西 西安 712046
2. Shaanxi Collaborative Innovation Center of Chinese Medicinal Resources Industrialization, Xi'an 712046, China
茜草始载于《神农本草经》, 为茜草科(Rubiaceae)植物茜草Rubia cordifolia L.的干燥根及根茎, 属我国传统大宗中药材。其性寒、味苦, 具有凉血止血、祛瘀、通经之功, 临床上主要用于治疗衄血、吐血、便血、崩漏、月经不调、经闭腹痛及风湿关节痛等症, 对心脑血管疾病疗效显著[1]。目前, 茜草的研究主要集中在药理作用和化学成分等方面[2], 分子水平方面则只有运用DNA条形码技术对茜草与其混淆品进行鉴别[3, 4]以及董美芳等[5]采用psbA-trnH基因序列对河南7个野生种群的茜草遗传多样性进行分析的报道。作为陕西道地药材品种之一, 陕产茜草质量较优, 在陕西境内分布极为广泛, 野生资源丰富。本课题组在前期的陕产茜草资源调查及质量控制研究过程中, 采集了陕西境内不同分布区域的野生茜草种质, 现从遗传学的角度探讨陕产茜草不同野生居群的遗传多样性。
遗传多样性是指种内不同居群之间或同一居群不同个体之间遗传变异的总和, 是生物多样性的基础和核心[6]。了解和研究药用植物的遗传多样性, 对于植物资源的保护利用有着十分重要的意义[7]。近年来, 分子标记技术直接以DNA为研究对象, 不受环境、生物组织、发育时期等的影响, 真实反映研究对象在遗传水平上的差异, 因而广泛应用于药用植物的遗传多样性研究。其中, 目标起始密码子多态性分子标记(start codon targeted polymorphism, SCoT)是Collard等[8]于2009年开发的一种新型分子标记, 运用单引物作为正向和反向引物, 扩增基因组DNA, 其引物的设计是依据存在于植物起始密码子ATG附近的共有保守碱基序列, 具有重复性好、引物设计简单、可以在物种间通用等特点, 已成功应用于桃儿七[9]、重楼[10]、黄花蒿[11]、益母草[12]、杜仲[13]等药用植物的遗传多样性研究。本文采用SCoT分子标记技术, 以分布于陕西省8个不同地区的野生茜草居群为研究对象, 研究它们在分子水平上的遗传变异, 检测居群内及居群间的遗传多样性, 从个体水平和居群水平进行聚类分析, 阐明不同野生居群间的亲缘关系, 并进一步探讨地理距离和遗传距离之间的相关性, 以期为今后开展陕产茜草种质资源保护、种质鉴定、育种等工作奠定基础。
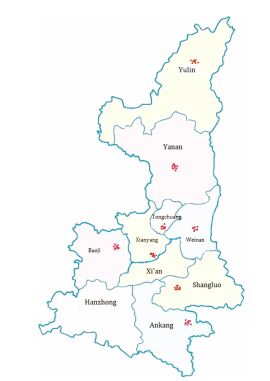
材料与方法材料 本研究所用的茜草材料为分布于陕西省8个市的茜草野生种质资源共64份(图 1和表 1), 采样时选取无病虫害的幼嫩叶片, 放入硅胶中迅速干燥, 编号后带回实验室, 于-20 ℃保存。全部样品由陕西中医药大学中药鉴定学教研室胡本祥教授鉴定为茜草科(Rubiaceae)植物茜草Rubia cordifolia L.。
|
Figure 1 Geographical distribution of Rubia cordifolia populations sampled in Shaanxi |
| Table 1 Details of populations of Rubia cordifolia sampled in Shaanxi |
DNA提取和检测 采用康为世纪新型植物基因组DNA提取试剂盒提取茜草叶片基因组DNA, 基因组DNA提取完毕后, 取DNA样品2.5 μL, 加入loading buffer 0.5 μL, 混匀。用琼脂糖凝胶(1.0%)电泳分离DNA, 电泳时间45 min, 电泳完用凝胶成像分析仪检验, 检测是否可得到一条完整、明亮、清晰的DNA条带, 若有则可以用于下一步实验。将检验合格的所有供试DNA样品储存在-20 ℃冰箱里备用。
SCoT引物合成、扩增与检测 SCoT引物的合成根据已有文献报道整理和自己设计的合计82条引物序列, 由生工生物工程(上海)有限公司合成。对SCoT-PCR反应各组分分别进行优化, 最终确定茜草SCoT-PCR最佳反应体系为:在总体积20 μL的反应体系中, 包括2×PCR Mix (康为) 10 μL、SCoT引物(10 μmol·L-1) 1 μL、稀释至一定浓度的模板DNA 0.5 μL (约35 ng)、ddH2O 8.5 μL。PCR扩增程序为: 94 ℃预变性5 min; 94 ℃变性30 s, 50 ℃退火1.5 min, 72 ℃延伸1 min, 35个循环; 72 ℃延伸10 min。PCR产物用1.5%的琼脂糖凝胶电泳分离, 用DL5000 DNA Marker作对照, 以1×TBE作为缓冲液, 凝胶成像系统观察、照相并保存。
本实验最终从82条SCoT引物中选出14条条带清晰、扩增效果良好、重复性好的引物用于陕产茜草种质资源的多样性分析, SCoT引物编号和序列见表 2。
| Table 2 List of the SCoT primers used in this experiment |
数据处理 对SCoT分子标记产生的条带采用人工计数法, 即观察所有引物产生的所有条带, 在同一位置上, 若存在条带则计为“1”, 无条带计为“0”, 最终形成0/1矩阵。利用POPGENE 3.2软件计算下列参数:各居群以及样本总体的等位基因观察值(Na)、等位基因有效值(Ne)、Nei’s基因多样性指数(H)、Shannon指数(I)、多态性条带数(NP)、多态性百分比(PPB); 8个居群的Nei’s遗传相似系数及遗传距离; 样本总体的总遗传多样性(Ht)、居群内遗传多样性(Hs)、居群间遗传分化系数(Gst)和居群间基因流(Nm)。利用NTSYS 2.10软件根据POPGENE 3.2得到的Nei’s遗传相似系数按非加权组平均法(UPGMA)分别在居群水平和个体水平上进行聚类分析。结合DCFA和AMOVA 1.5软件进行AMOVA分析, 计算居群内、居群间的遗传分化所占比例。利用在线软件IBDWS 3.15分析遗传距离与地理距离的相关性。
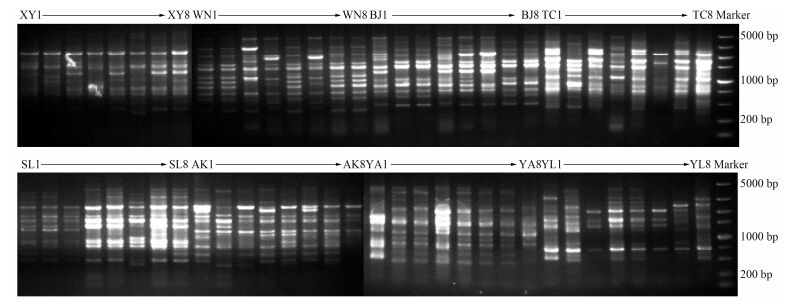
结果与分析 1 SCoT-PCR扩增结果分析本研究利用从82条SCoT引物中选出的14条扩增谱带清晰、多态性较好的SCoT引物, 对供试的8个陕产茜草野生居群64份材料进行PCR扩增和电泳检测。结果显示, 所有样本均能扩增出清晰、稳定的条带, 扩增条带片段大小范围为200~3 500 bp。图 2为引物SCoT对所有陕产茜草样本的扩增图谱。
|
Figure 2 Result of gel electrophoresis of PCR amplification products of all samples of Rubia cordifolia produced with primer SCoT-21 |
统计SCoT所有引物产生的条带数、多态性条带数以及多态性百分率, 见表 3。从表中可以看到, 14条SCoT引物共扩增得到182条带, 其中163条为多态性条带, 每个引物平均扩增得到13条带, 平均多态性百分比为89.56%。引物SCoT39扩增得到条带数目最多, 有15条, 多态性条带为13条, 多态性百分比为86.67%。14条引物的多态性百分比范围为81.82% (SCoT42)~100% (SCoT45)。
| Table 3 Polymorphism of amplification results produced by SCoT primers |
利用POPGENE 3.2软件对SCoT扩增结果进行参数统计分析, 结果见表 4。所有样本的Ne为1.495 6、H为0.293 6、I为0.444 6, 表明陕产茜草在物种水平上具有较高的遗传多样性。居群水平上陕产茜草的多态性条带数范围为58 (XY)~79 (AK); 多态性百分比为31.87 (XY)~43.41% (AK)。样本总体的Na、Ne、H、I、NP及PPB均高于单一居群的相应数值。居群间的H范围介于0.113 5~0.157 3之间, I在0.173 6~0.231 7之间。其中, 安康居群(AK)的H、I、NP和PPB最高, 表明安康居群的遗传多样性水平最高。陕产茜草不同野生居群按遗传多样性水平排序为:安康>榆林>商洛>宝鸡>铜川>延安>渭南>咸阳。
| Table 4 Genetic diversity of eight wild populations of Rubia cordifolia based on SCoT marker. POP: Population; N: No. of plants collected per population; Na: Observed number of alleles; Ne: Effective number of alleles; H: Nei's gene diversity; I: Shannon's information index; NP: Number of polymorphic loci; PPB: Percentage of polymorphic loci; Ht: Variability within population; Hs: Total variability; Gst: Diversity among populations; Nm: Gene flow |
POPGENE 3.2软件分析结果显示, 总体水平上, Ht为0.293 6, Hs为0.130 6。Gst为0.555 3, 表明55.53%的遗传多样性来自于居群间的遗传差异, 44.47%的遗传多样性来自于居群内, 居群间水平略高。样本总体的Nm为0.400 4, 说明居群间存在基因流动, 但程度较低。
AMOVA分析结果(表 5)显示, 居群间差异极显著(P<0.001), 遗传分化系数ΦST = 0.529 1, 表明研究居群的遗传多样性主要分布在群体间, 占52.91%, 而群体内则占47.09%, 与Nei’s遗传多样性分析方法得出的研究结果一致。
| Table 5 Results of analysis of AMOVA of SCoT method of eight wild populations |
利用POPGENE 3.2软件计算种群水平上的遗传距离及遗传相似系数, 结果见表 6。从表中可知, 8个居群的遗传距离范围为0.136 8~0.470 4, 遗传相似系数范围为0.624 8~0.872 1。铜川和宝鸡居群的遗传距离最近, 遗传相似系数最大; 商洛和榆林居群的遗传距离最大, 遗传相似系数最小。
| Table 6 Genetic distance (below diagonal) and genetic identity (above diagonal) of eight wild populations based on SCoT marker |
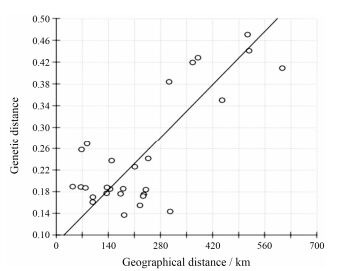
进一步利用在线软件IBDWS 3.15将POPGENE 3.2计算出来的居群间遗传距离数据和Google地图计算出的居群间直线地理距离进行Mantel统计分析, 探讨不同野生居群遗传分化和距离之间的相关性。结果表明(图 3), 陕产茜草不同野生居群间的遗传距离与地理距离存在显著的相关性(r = 0.776 4, P<0.05)。
|
Figure 3 Relationship between geographic and genetic distances |
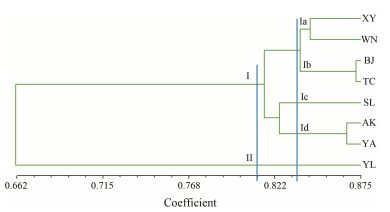
将POPGENE 3.2获得的居群间遗传相似系数矩阵输入NTSYS 2.10软件中, 得到居群聚类分析结果, 见图 4。由图可知, 在相似系数为0.812时, 8个居群可以分为两个类群, 类群Ⅰ包括7个居群, 依次为XY、WN、BJ、TC、SL、AK和YA居群; YL居群单独聚为一类(类群Ⅱ)。在相似性系数为0.838处展开, 类群Ⅰ可分为4个亚类群, 分别为Ⅰa (XY、WN)、Ⅰb (BJ、TC)、Ⅰc (SL)和Ⅰd (AK、YA)。遗传距离最近的居群为BJ和TC, 遗传相似系数为0.870时可区分开来。
|
Figure 4 Cluster analysis of 8 wild populations based on SCoT marker |
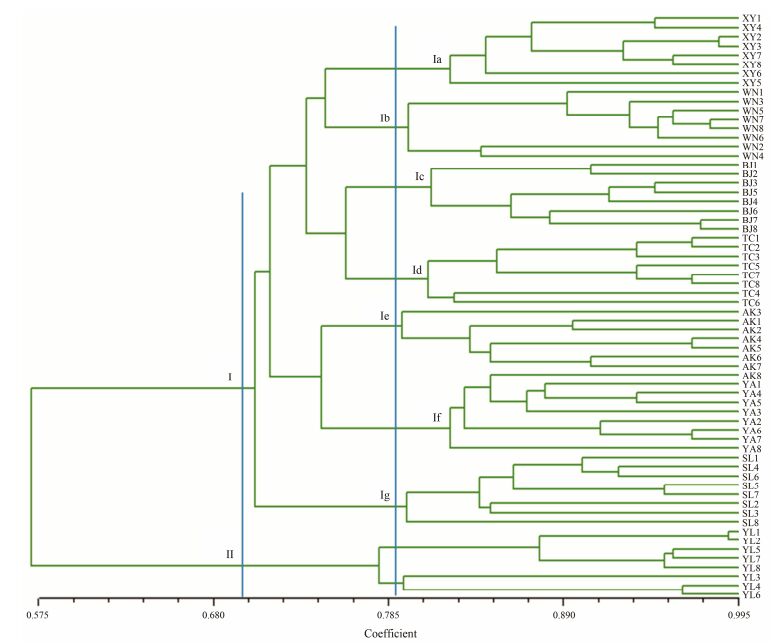
利用NTSYS 2.10软件在个体水平上进行聚类分析, 结果见图 5, 当相似性系数为0.702时, 所有材料聚为两个类群, 类群Ⅰ包括56份材料, 随后在相似系数为0.790处按产地来源聚为7个亚群, 分别为Ⅰa (XY1-XY8)、Ⅰb (WN1-WN8)、Ⅰc (BJ1-BJ8)、Ⅰd (TC1-TC8)、Ⅰe (AK1-AK8)、Ⅰf (YA1-YA8)、Ⅰg (SL1-SL8)。类群Ⅱ只有YL居群, 依次为YL1、YL2、YL5、YL7、YL8、YL3、YL4、YL6。从图中可以看到, 遗传距离最小的是个体YL1和YL2。
|
Figure 5 Cluster analysis of 64 wild individuals based on SCoT marker |
种质资源研究可以为药用植物的遗传育种、资源保护提供重要的理论基础, 而遗传多样性研究是种质资源研究的重要内容, 种质间遗传多样性越丰富, 其应对环境和胁迫的能力就越突出, 分布范围也越广[14]。DNA分子标记在种质资源的收集、遗传多样性研究、种质分类研究和育种等方面发挥着重要作用, 在药用植物的遗传多样性研究中的应用也越来越普遍[15-17], 而对茜草的分子标记研究主要集中在DNA
条形码技术方面, 其中Chen等[3]利用psbA-trnH、matK和rbcL对茜草与其混伪品茜草属其他8个物种以及紫金牛、丹参、川赤芍、蓬子菜的研究表明, psbA-trnH+matK+rbcL组合序列能作为DNA条形码对茜草及其混伪品进行鉴定。Xia等[4]研究显示psbA-trnH分子系统树可将茜草不同居群样本聚为一累, 茜草与其近缘种psbA-trnH序列的种间遗传距离为0.007 51~0.193 38, 远大于种内遗传距离的0~0.003 72。Dong等[5]运用psbA-trnH对河南省7个野生茜草种群的遗传多样性研究则表明河南地区野生茜草具有较高的遗传多样性。目前为止, 尚未见采用分子标记技术对茜草种内遗传多样性进行分析的报道。
SCoT作为一种新型分子标记技术已在多种药用植物的遗传多样性研究中得到了较为成功的应用, 其多样性参数是评价研究对象遗传水平高低的重要依据[18]。茜草是陕西道地药材品种之一, 在陕西分布广泛且具有重要的药用价值和经济意义。本研究利用SCoT分子标记技术对来自8个陕产茜草野生居群的64份材料进行了系统的遗传多样性分析, 14条引物共扩增得到182条带, 其中163条为多态性条带, 每个引物平均扩增得到13条带, 多态性百分比范围在81.82% (SCoT42)~100% (SCoT45) 之间, 平均为89.56%, 表明SCoT标记在茜草基因组中具有丰富的多态性。POPGEN 3.2分析显示, 样本总体的NP、PPB、H和I高于所有单一居群的对应数值。AMOVA分析和Nei’s的遗传多样性分析方法获得的遗传分化系数相似, 分别为ΦST = 0.529 1和Gst = 0.555 3, 均显示陕产茜草野生种质资源的遗传多样性主要分布在居群间, 因此在采取保护措施时应尽量多的保护居群数目。
陕产茜草野生居群之间的基因流Nm = 0.440 8<1, 说明基因交流已严重受阻。植物自然种群间的基因流动是借助于花粉、种子、植株个体以及其携带遗传物质的物体为媒介进行, 其中花粉和种子的扩散是主要的媒介[19], 而本文的研究对象为野生群体, 推测地理隔离阻断了花粉和种子介导的基因流, 是导致陕产茜草野生居群间遗传分化显著的直接原因。相关研究认为亲缘关系与地理距离间存在一定的相关性[20, 21], 本文通过Mantel分析揭示陕产茜草不同野生居群间的遗传距离与地理距离存在显著的相关性(r = 0.776 4, P<0.05), 与上述观点一致。聚类分析结果来看, 个体水平上, SCoT标记可以明确地将各个个体按照其来源地归类, 将来自同一地区的个体聚在一起; 在居群水平上, 8个居群可聚为两大类, 其中距离最远的榆林居群独自聚为一类, 其余7个居群聚为一类, 当遗传关系一定时, 来自关中的咸阳、宝鸡、渭南和铜川可聚为一类, 从另一个层面说明了遗传距离较近的陕产茜草野生居群其地理距离也较近。
综上所述, 本研究采用的SCoT分子标记适合进行茜草种质资源遗传多样性研究, 可对陕产茜草不同野生居群的遗传多样性和亲缘关系作一了解, 有利于对现有优良野生茜草种质资源进行研究, 以期为今后开展陕产茜草的遗传连锁图谱和育种等工作奠定良好基础。
| [1] | Zhang Z, Huang X. The advance on the research of pharmacological activities of Rubia cordifolia L[J]. Mod J Integr Tradit Chin Western Med (现代中西医结合杂志), 2007, 16: 2172–2173. |
| [2] | Li H, Xiao L, Zhang J, et al. The advance on the research of chemistry and pharmacological activities of Rubia cordifolia L[J]. J Chin Med Mater (中药材), 2016, 39: 1433–1436. |
| [3] | Chen Y, Fan G, Liu Y, et al. Identification of traditional Chinese medicine Rubia Radix et and its adulterants using DNA barcodes[J]. Chin Pharm J (中国药学杂志), 2015, 50: 1266–1272. |
| [4] | Xia Z, Wang L, Li H, et al. Molecular authentication of Rubia et Rhizoma based on psbA-trnH gene sequences[J]. Lishizhen Med Mater Med Res (时珍国医国药), 2016, 27: 374–376. |
| [5] | Dong M, Yue W, Hang Y, et al. Analysis on genetic diversity of Rubia cordifolia from various geographical populations in Henan province[J]. Chin Tradit Herb Drugs (中草药), 2013, 44: 2600–2604. |
| [6] | Loreau M, Naeem S, Inchausti P, et al. Biodiversity and ecosystem functioning:current knowledge and future chal-lenges[J]. Science, 2001, 294: 804–808. DOI:10.1126/science.1064088 |
| [7] | Zeng S, Xiao G, Guo J, et al. Development of a EST dataset and characterization of EST-SSRs in a traditional Chinese medicinal plant, Epimedium sagittatum (Sieb. Et Zucc.) Maxim[J]. BMC Genomics, 2010, 11: 94. DOI:10.1186/1471-2164-11-94 |
| [8] | Collard BC, Mackill DJ. Start codon targeted (SCoT) polymorphism:a simple, novel DNA marker technique for generating gene-targeted markers in plants[J]. Plant Mol Biol Rep, 2009, 27: 86–93. DOI:10.1007/s11105-008-0060-5 |
| [9] | Chen D, Zhao J, Liu X, et al. Genetic diversity and genetic structure of endangered wild Sinopodophyllum emodi by start codon targeted polymorphism[J]. China J Chin Mater Med (中国中药杂志), 2013, 38: 278–283. |
| [10] | Li Z, Xin B, Yang H, et al. SCoT genetic diversity of plants in Paris[J]. Guihaia (广西植物), 2014, 3: 008. |
| [11] | Chen D, Cui G, Zhang X, et al. Genetic structure and genetic diversity of Artemisia annua varieties (strains) populations based on SCoT markers[J]. China J Chin Mater Med (中国中药杂志), 2014, 39: 3254–3258. |
| [12] | Zhang W, Hang Y, Xue H, et al. SCoT analysis on genetic diversity among wild populations of Leonurus artemisia in Henan province[J]. Chin Tradit Herb Drugs (中草药), 2013, 44: 1022–1026. |
| [13] | Xiao C, Zhou T, Jiang W, et al. Analysis of genetic diversity of cultivated Eucommia ulmoides from Guizhou Province by phenotypic traits and SCoT markers[J]. J Chin Med Mater (中药材), 2014, 8: 008. |
| [14] | Prado-Martinez J, Sudmant PH, Kidd JM, et al. Great ape genetic diversity and population history[J]. Nature, 2013, 499: 471–475. DOI:10.1038/nature12228 |
| [15] | Khan S, Mirza KJ, Abdin MZ. Development of RAPD markers for authentication of medicinal plant Cuscuta reflexa[J]. Eur Asian J Biol Sci, 2010, 4: 1–7. |
| [16] | Xun Y, Hou B, Geng L, et al. Evaluation of genetic diversity and population structure of Bletilla striata based on SRAP markers[J]. Acta Pharm Sin (药学学报), 2016, 51: 147–152. |
| [17] | Cha M, Zhao Y, Li J, et al. Lycium barbarum L. sequence-related amplified polymorphism (SRAP) cluster analysis prin-cipal coordinates analysis genetic diversity[J]. Acta Bot Bor-Occid Sin (西北植物学报), 2016, 36: 681–687. |
| [18] | Chai X, Dong R, Liu W, et al. Optimizing sample size to assess the genetic diversity in common Vetch (Vicia sativa L.) populations using start codon targeted (SCoT) markers[J]. Molecules, 2017, 22: 567. DOI:10.3390/molecules22040567 |
| [19] | Ai Q, Zhou T, Jiang W, et al. SRAP analysis on genetic diversity for germplasm resources of Dipsacus asper[J]. Chin Tradit Herb Drugs (中草药), 2013, 44: 2155–2159. |
| [20] | Ren PY, Pan MQ. Population genetic structure of five amorphophallus species from the south of Yunnan province by inter-simple sequences (ISSR) markers[J]. J Wuhan Univ (Nat Sci Ed)武汉大学学报(自然科学版), 2013, 59: 99–104. |
| [21] | Zhu T, Jing L, Du T, et al. Genetic diversity analysis on Ephedra intermedia from Gansu based on ISSR[J]. Chin Tradit Herb Drugs (中草药), 2014, 45: 1764–1768. |
 2017, Vol. 52
2017, Vol. 52


