2. 呼吸疾病诊疗与新药研发河南省协同创新中心, 河南 郑州 450046;
3. 黑龙江中医药大学药学院, 黑龙江 哈尔滨 150040
2. Collaborative Innovation Center for Respiratory Disease Diagnosis and Treatment and Chinese Medicine Development of Henan Province, Zhengzhou 450046, China;
3. College of Pharmacy, Heilongjiang University of Chinese Medicine, Harbin 150040, China
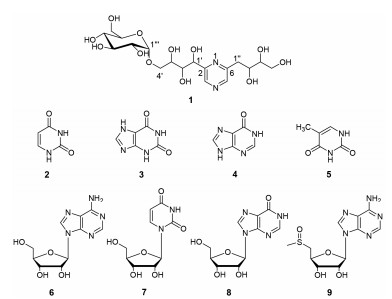
山药是薯蓣科植物薯蓣Dioscorea opposite Thunb.的干燥根茎。始载于《神农本草经》, 列为上品。山药主产于河南温县、武陟、博爱等地, 大都集中在河南沁阳县(旧属怀庆府), 故名“怀山药”, 是河南省“四大怀药”之一。2015版药典中记载:味甘、性平。归脾、肺、肾经。有补脾养胃、生津益肺、补肾涩精的功效[1]。山药不仅是一种常用中药, 而且还是一种上好的养生食材, 自古以来便是药食同源的典范。目前, 关于山药的研究有很多, 但大多集中在其药理作用和机制, 关于其药效物质基础方面的研究比较少。因此, 本文采用多种柱色谱技术和手段, 从怀山药中分离得到9个化合物, 分别是: 2-(1', 2', 3'-三羟基丁基-4'-O-α-D-葡萄糖苷)-6-(2'', 3'', 4''-三羟基丁基)-吡嗪(1)、尿嘧啶[2] (2)、黄嘌呤[3] (3)、次黄嘌呤[4] (4)、胸腺嘧啶[5] (5)、腺苷[6] (6)、尿苷[7] (7)、肌苷[8] (8)和5'-去氧-5'-亚磺酰腺苷[9] (9), 其中化合物1为新的吡嗪衍生物, 化合物3~5、8、9为首次从该植物中分离得到的, 结构见图 1。
|
Figure 1 Structures of compounds 1−9 |
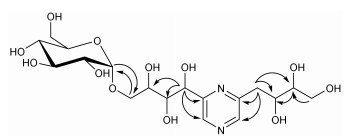
化合物1 为白色粉末(甲醇), 易溶于水。[α]D20 37.05 (c 0.13, CH3OH); HR-TOF-MS给出分子离子峰m/z: 489.171 2 [M+Na]+ (C18H30N2O12Na计算值为489.169 1), 提示化合物的分子式为C18H30N2O12; UV (CH3OH) λ: 209、275 nm; IR (ATR): 3 282、2 925、1 673、1 421、1 200、1 145、1 031 cm−1等。在1H NMR (500 MHz, DMSO-d6)谱中, δH 8.74 (1H, s, H-3) 和8.50 (1H, s, H-5) 处有两个氢信号, 处于较低场, 推测可能是氮杂环上的不饱和氢信号; δH 4.81 (1H, d, J = 3.6 Hz), 根据化学位移和偶合常数推测可能为α-构型糖的端基氢信号。在13C NMR (125 MHz, DMSO-d6)谱中有18个碳信号, 根据DEPT 135谱可知, 季碳有2个: δC 156.9 (C-2) 和154.7 (C-6);仲碳有4个: δC 69.9 (C-6''')、65.0 (C-4')、62.6 (C-4'')和39.9 (C-1''); 其余10个均为叔碳。根据HSQC谱和HMBC谱(图 2), 可知δC 156.9 (C-2)、154.7 (C-6)、145.2 (C-5) 和143.6 (C-3) 是2, 6-二取代吡嗪上的4个碳信号, δC 100.3 (C-1''')、71.7 (C-2''')、73.8 (C-3''')、73.7 (C-4''')、75.3 (C-5''')、62.6 (C-6''')是α-葡萄糖[10]上的碳信号。在HSQC谱中, δH 2.90、3.27与δC 39.9相关, δH 3.40与δC 72.9 (C-3'')有相关, δH 3.84与δC 65.0有相关, δH 3.95与δC 69.9相关; HMBC谱中δH 2.90与δC 72.9有远程相关, δH 3.27和3.40与δC 74.5 (C-2'')均存在远程相关, δH 3.84与δC 72.9有远程相关, 推测可能存在-CH2(CHOH)2CH2OH, δH 2.90、3.27与δC 145.2、154.7都存在远程相关, 说明-CH2(CHOH)2CH2OH片段与δC 154.7的碳相连; δH 5.11与δC 72.5 (C-2')、75.2 (C-3')有远程相关, 结合化学位移推测可能存在-(CHOH)3CH2-的结构片段, δH 5.11与δC 143.6、156.9均存在远程相关, 说明-(CHOH)3CH2-片段与δC 156.9的碳相连; δH 3.95与δC 100.3有远程相关, 同时, δH 4.81与δC 69.9也存在远程相关, 可知, 葡萄糖基与-(CHOH)3CH2-片段中的亚甲基通过1位相连。进一步酸水解, 酯化, 通过HPLC可确定该化合物中的糖是D-葡萄糖。综上所述, 并结合文献[10]中2-(1', 2', 3', 4'-四羟基丁基)-6-(2'', 3'', 4''-三羟基丁基)-吡嗪的波谱数据, 最终确定该化合物的结构是2-(1', 2', 3'-三羟基丁基-4'-O-α-D-葡萄糖苷)-6-(2'', 3'', 4''-三羟基丁基)-吡嗪[2-(1', 2', 3'-trihydroxybutyl-4'-O-α-D-glucopyrano side)-6-(2'', 3'', 4''-trihydroxybutyl)-pyrazine]。其1H NMR和13C NMR数据见表 1。
|
Figure 2 Key HMBC correlations of compound 1 |
| Table 1 1H NMR(500 MHz, DMSO-d6) and 13C NMR(125 MHz, DMSO-d6) spectral data of compound 1 |
核苷类成分是生物细胞维持生命活动的基本组成元素, 参与DNA的代谢, 具有广泛的生物活性。通过本实验发现怀山药含有多种碱基和核苷类成分, 这可能与怀山药的补益作用具有一定的联系, 有待于进一步的研究商榷。
实验部分Bruker AVANCE Ⅲ 500型核磁共振仪(TMS内标)、Bruker maxis HD型飞行时间质谱(德国布鲁克公司), Rudolph AP-Ⅳ型旋光仪(美国鲁道夫公司), Thermo Nicolet IS10红外光谱仪、Thermo EVO300紫外分光光度计(美国热电公司), 赛谱锐思LC50型高压制备液相色谱仪(赛谱锐思北京科技有限公司), UV200型紫外检测器, YMC-Pack ODS-A色谱柱(10 mm × 250 mm. D. S-5 μm, 12 μm) (日本YMC有限公司), Waters e2695高效液相色谱仪, Waters 2998检测器, DIKMA PLATISIL (TMS) ODS柱(4.6 mm × 250 mm, 5 μm), EYELA N-1100型旋转蒸发仪、EYELA A-1000S型水流抽气机、EYELA N-1111型冷冻水循环装置、EYELA FDU-2110型冷冻干燥机(上海爱朗仪器有限公司), 上海一恒DFZ-60508型真空干燥箱(上海一恒科学仪器有限公司)。
柱色谱填料Diaion HP-20、MCI Gel CHP-20 (日本三菱化学公司), Toyopearl HW-40 (日本TOSOH公司), Sephadex LH-20 (Parmacia Biotech公司), 柱色谱所用硅胶H (160~200目)、薄层色谱硅胶(颗粒范围10~40 mm) (青岛海洋化工厂), 其他分析纯和色谱纯试剂为北京化工厂和天津第三化学试剂厂生产, 标准品购自上海源叶生物科技有限公司。
本实验所选怀山药购自焦作市药材生产基地, 经河南中医药大学药学院陈随清教授鉴定为薯蓣科植物薯蓣Dioscorea opposite Thunb.的干燥根茎。
1 提取与分离怀山药10 kg, 75%含水乙醇组织破碎提取, 每次3 min, 过滤, 滤液合并后45 ℃减压浓缩成流浸膏, 加适量水分散溶解后, 依次用石油醚、乙酸乙酯、正丁醇反复萃取, 分别得到石油醚部位(21.02 g)、乙酸乙酯部位(13.76 g)、正丁醇部位(23.46 g)。其中, 正丁醇部位上Diaion HP-20大孔吸附树脂柱, 依次用水、10%、20%、30%、45%、60%、75%、95%乙醇−水梯度洗脱得到8个洗脱组分; 各个洗脱组分在反复通过Sephadex LH-20、Toyopearl HW-40、MCI Gel CHP-20等柱色谱和半制备高效液相色谱柱, 得到化合物1 (7.7 mg)、2 (2.1 mg)、3 (2.4 mg)、4 (22.3 mg)、5 (3.2 mg)、6 (1.6 mg)、7 (1.2 mg)、8 (1.5 mg)和9 (3.2 mg)。
2 酸水解取化合物1 (2 mg), 溶于CF3COOH (4 mL)溶液中, 95 ℃下反应3 h后, 冷却至室温, 反应混合物用等体积(2 mL)的CH2Cl2萃取3次, 含水层浓缩干燥。然后分别将浓缩物和D-葡萄糖的标准品溶于无水吡啶(0.5 mL)和L-半胱氨酸甲酯盐酸盐(1.0 mg)中, 在60 ℃时反应1 h。冷却后分别加入5 μL邻甲苯异硫氰酸酯, 60 ℃下反应1 h。冷却至室温, 用吡啶稀释1倍后, 分别取样品(5 μL), 通过HPLC (乙腈−水25:75, 0.8 mL·min−1)进行分析, 检测波长为250 nm[11]。化合物1的水解产物和D-葡萄糖衍生物分别在tR = 18.8 min处有色谱峰。
3 结构鉴定化合物1 为白色粉末。[α]D20 37.047 (c 0.127 5, CH3OH); HR-TOF-MS m/z: 489.171 2 [M+Na]+ (C18H30N2O12Na计算值是489.169 1); UV (CH3OH) λ/nm: 209, 275; IR (ATR)/cm−1: 3 282, 2 925, 1 673, 1 421, 1 200, 1 145, 1 031; 1H NMR (500 MHz, DMSO-d6)和13C NMR (125 MHz, DMSO-d6)数据见表 1。
| [1] | Chinese Pharmacopoeia Committee. Pharmacopoeia of the People's Republic of China (中华人民共和国药典)[M]. Part 1. Beijing: China Medical Science Press, 2015: 29. |
| [2] | Gao JM, Shen J, Yang X, et al. The constituents of Russula ochroleuca basidiomycetes[J]. Acta Bot Yunnan (云南植物研究), 2001, 23: 385–393. |
| [3] | Sun JL, Deng AJ, Li HZ, et al. Study on the chemical constituents of roots of Linum usitatissimum[J]. China J Chin Mater Med (中国中药杂志), 2009, 34: 718–720. |
| [4] | Chen Y, Li FT, Tao WW, et al. Chemical constituents of Typhae Pollen[J]. Nat Prod Res Dev (天然产物研究与开发), 2015, 27: 1558–1563. |
| [5] | Du WP, Xu P, Liu B, et al. Chemical constituents from shoots of Phyllostachys edulis (Ⅰ)[J]. China Tradit Herb Drugs (中草药), 2015, 46: 334–338. |
| [6] | Zheng XK, Bi YF, Feng WS, et al. Study on the chemical constituents of Selaginella tamariscina (Beauv) Spring[J]. Acta Pharm Sin (药学学报), 2004, 39: 266–268. |
| [7] | Wang ZB, Guo JT, Yang CJ, et al. Chemical constituents from Hydrangea macrophylla[J]. China J Chin Mater Med (中国中药杂志), 2013, 38: 709–713. |
| [8] | Shao JJ, Peng Y, He CN, et al. Isolation and identification the chemical constituents of Przewalskiatangutica Maxim[J]. J Shenyang Pharm Univ (沈阳药科大学学报), 2013, 30: 840–845. |
| [9] | Kawagishi H, Fukuhara F, Sazuka M, et al. 5'-Deoxy-5'-methylsulphinyladenosine, a platelet aggregation inhibitor from Ganoderma lucidum[J]. Phytochemistry, 1993, 32: 239–241. DOI:10.1016/S0031-9422(00)94974-4 |
| [10] | Li Q, Ye WH, Yan AX, et al. Isolation, identification and physiological activities of 2-(1', 2', 3', 4'-tetrahydroxybutyl)-6-(2", 3", 4"-trihydroxybutyl)-pyrazine from Panax notoginseng[J]. Chem J Chin Univ (高等学校化学学报), 2001, 22: 1824–1828. |
| [11] | Tian EL, Yang GZ, Mei ZN, et al. Chemical constituents from stems of Glycosmis pentaphylla[J]. China Tradit Herb Drugs (中草药), 2014, 45: 1358–1362. |
 2017, Vol. 52
2017, Vol. 52


