2. 中国科学院昆明植物研究所, 植物化学与西部植物资源持续利用国家重点实验室, 云南 昆明 650201
2. State Key Laboratory of Phytochemistry and Plant Resources in West China, Kunming Institute of Botany, Chinese Academy of Sciences, Kunming 650201, China
大托叶云实(Caesalpinia bonuc) 是豆科(Leguminosea) 云实属(Caesalpinia) 植物, 又名刺果苏木, 有刺藤本, 刺直或者弯曲, 各部位均有黄色柔毛。在世界热带地区均有分布, 我国主要产于云南、广东、广西、台湾等地[1]。《中华本草》中记载其种子具有活血止痛、解毒消肿等功效, 主要用于治疗胃脘痛、腹痛、目赤肿痛、疮疡; 叶具有清热解毒、去淤止痛、驱虫、通便等功效, 用于治疗间歇性发热、急慢性胃炎、胃溃疡、痢疾、消化不良、肠道虫积、便秘、疖肿等[2]。目前, 已从大托叶云实中发现二萜[3-5]、黄酮[6]和甾体[7]类化合物。卡山烷二萜类成分caesalpinolide A和caesalpinolide B具有抑制乳腺癌、宫内膜癌和宫颈癌细胞增殖作用[5]; 黄酮类化合物4, 4'-dihydroxy-2'-methoxy-chalcone具有抗疟原虫活性[8]。为进一步寻找活性成分, 作者对购自河北安国药材的大托叶云实种子进行研究, 从中分离得到5个化合物并鉴定为3β-乙酰氧基-卡山烷-12, 14(17), 15-三烯-7β-醇(1)、caesalmin C (2)[9]、caesall E (3)[10]、caesalpinin MJ (4)[11]和1-deacetylcaesalmin C (5)[11], 其中化合物1为新化合物, 结构见图 1。

|
Figure 1 Structures of compounds 1-5 |
化合物1 无色油状物(氯仿) HR-ESI-MS m/z: 367.224 3 [M+Na]+ (计算值: 367.224 4), 确定分子式为C22H32O3, 不饱和度为7。红外光谱显示其结构中存在羟基(3 427 cm-1)、羰基(1 730 cm-1)、双键(1 631 cm-1) 等特征信号峰。1H NMR谱(表 1) 显示1个乙酰基上甲基信号δH 2.05 (s), 3个与季碳相连的甲基信号δH 0.95 (s)、0.93 (s)、0.90 (s), 2个连氧次甲基信号δH 4.49 (dd, J=11.8, 4.1 Hz)、3.91 (m), 1个三取代双键质子信号δH 5.86 (br s), 2个环外末端双键质子信号δH 5.30(br s)、5.19 (br s), 3个末端双键质子信号δH 6.33 (dd, J=17.3, 10.8 Hz)、5.36 (dd, J=17.3, 1.2 Hz)、5.06 (dd, J=10.8, 1.2 Hz)。13C NMR谱(表 1) 显示22个碳信号, 包括4个甲基、6个亚甲基(包括2个不饱和亚甲基)、7个次甲基(包括2个不饱和及2个氧取代次甲基) 及5个季碳(包括1个乙酰基上的羰基和1个不饱和季碳)。据以上波谱数据及云实属植物中特征卡山烷二萜类成分[11-13], 推测该化合物为一个羟基和一个乙酰氧基取代的卡山烷二萜结构, 并存在一个三取代双键、一个环外双键及一个末端双键。
| Table 1 1H (600 MHz) and 13C (150 MHz) NMR data in CDCl3 for compound 1 |
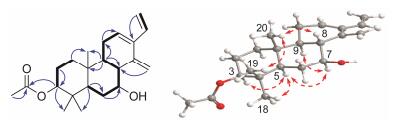
通过HMBC谱中H-11a、H-11b与C-12、C-13 (图 2) 的相关, 以及1H-1H COSY谱中H-9/H2-11/H-12相关, 表明三取代双键位于C-12和C-13; H-17a和H-17b与C-8、C-14、C-13的HMBC相关, 说明环外双键位于C-14和C-17; H-15与C-12、C-13、C-14 (图 2) 的HMBC相关, 提示末端双键与C-13位相连。此外, HMBC谱中H2-2、H3-19与C-3, H-3与乙酰基上的酯羰基, H-8、H2-6、H-5与C-7, 以及1H-1H COSY谱中H2-1/H2-2/H-3, H-5/H2-6/H-7/H-8/H-9相关(图 2), 表明乙酰氧基和羟基分别连在C-3和C-7位。
|
Figure 2 Key 1H-1H COSY (   |
化合物1的相对构型通过ROESY谱确定(图 2)。ROESY谱中, H-5与H-7、H-7与H-9、H-5与H3-18、H-8与H3-20、H3-19与H3-20存在相关, 以及H-5与H3-20不存在相关, 表明7位羟基为β朝向。H-3的耦合常数为11.8和4.1 Hz, 提示3位乙酰氧基同样为β朝向, 该推论进一步通过H-3与H-5、H-3与H3-18的ROESY相关得到确认。据上述分析, 化合物1鉴定为新的卡山烷二萜, 命名为3β-乙酰氧基-卡山烷-12, 14(17), 15-三烯-7β-醇。
实验部分核磁共振仪(Brucker, AV 600 MHz, Avance III 500 MHz, 德国) (TMS为内标); 液质联用仪(Agilent 1290 UPLC/6540 Q-TOF, 美国); 红外光谱仪(Brucker, Tensor-27, 德国); 紫外可见分光光度仪(Shimadzu, Shimadzu UV2401PC, 日本); 全自动数字旋光仪(Jasco, Jasco P-1020, 日本); 分析和半制备型HPLC (Agilent, Agilent 1260, 美国); 半制备色谱柱Zorbax SB-C18 (Agilent, 4.6 mm × 250 mm, 美国); MPLC (上海利穗有限公司); 柱色谱100~200目、200~300目硅胶(临沂市海祥化工厂); 薄层色谱硅胶板GF-254 (临沂市海祥化工厂); Sephadex LH-20 (Pharmacia公司, 瑞典); MCI-gel CHP-20P (Mitsubishi Chemical Corporation, 75~150 μm, 日本); 80~100目聚酰胺粉(国药集团化学试剂有限公司); 色谱甲醇(北京百灵威科技有限公司); 分析纯甲醇(天津市风船化学试剂科技有限公司); 石油醚(沸程60~90 ℃)、氯仿、乙酸乙酯、甲醇、95%乙醇等均为工业纯有机试剂(重蒸使用); 显色剂(10% H2SO4乙醇溶液, 喷洒后适当加热)。
实验药材大托叶云实2016年3月购买于河北安国药材市场, 并由中国科学院昆明植物研究所成晓副研究员鉴定为豆科(Leguminosae) 云实属(Caesalpinia) 植物大托叶云实(Caesalpinia bonduc) 的种子, 标本(20160303a) 保存于中国科学院昆明植物所标本馆。
1 提取分离大托叶云实种子10 kg粉碎后, 用95%乙醇冷浸提取3次, 每次两天, 合并提取液, 减压蒸馏浓缩回收有机溶剂后, 提取物分散到水中用乙酸乙酯萃取3次, 得乙酸乙酯萃取物165.0 g。该萃取物(150.0 g) 经MPLC分离(MCI), 利用甲醇-水(70:30、75:25、80:20、85:15、90:10、95:5) 梯度洗脱, 根据TLC检测合并为5个部分Fr1~Fr5。Fr4 (33.0 g) 经正相硅胶柱色谱(石油醚-乙酸乙酯100:1→2:1) 梯度洗脱, 分为8个部分Fr4.1~Fr4.8。Fr4.1 (4.3 g) 利用丙酮重结晶得化合物2(2.0 g)。Fr4.2 (202.0 mg) 经正相硅胶柱色谱(氯仿-丙酮100:1→9:1), 得化合物3(30.0 mg)。Fr4.3(82.0 mg) 用半制备HPLC分离(甲醇-水, 75:25, 3 mL·min-1, tR=8.1 min), 得到化合物4(12.0 mg)。Fr4.4 (93.0 mg) 用半制备HPLC分离(甲醇-水, 75:25, 3 mL·min-1, tR=10.4 min), 得到化合物1(3.0 mg)。Fr3 (12.4 g) 经正相硅胶柱色谱(石油醚-乙酸乙酯, 9:1→1:1) 梯度洗脱, 分为4个组分Fr3.1~Fr3.4, Fr3.1 (104.0 mg) 经Sephadex LH-20 (氯仿-甲醇, 1:1) 柱色谱后, 利用甲醇重结晶得化合物5(50.0 mg)。
2 结构鉴定化合物1 无色油状物(氯仿), [α]D20+24.2 (c0.20, MeOH); UV末端吸收峰λmax (log ε): 204.6 (3.51)。IR: 3 427, 2 930, 2 856, 1 730, 1 631, 1 614, 1 461, 1 383, 1 251, 1 029 cm-1。
化合物2 无色方晶(丙酮), ESI-MS m/z497 [M+Na]+, C26H34O8。1H NMR (CDCl3, 500 MHz) δH:7.23 (1H, d, J=1.8 Hz, H-16), 6.40 (1H, d, J=1.9 Hz, H-15), 5.58 (1H, br s, H-6, H-7), 5.09 (1H, br s, H-17b), 4.94 (1H, br s, H-17a), 4.89 (1H, br s, H-1), 2.10 (3H, s, 7-OCOCH3), 2.07 (3H, s, 1-OCOCH3), 1.97 (3H, s, 6-OCOCH3), 1.30 (3H, s, H-20), 1.17 (3H, s, H-19), 1.16 (3H, s, H-18); 13C NMR (CDCl3, 125 MHz) δC:75.0 (d, C-1), 22.0 (t, C-2), 32.3 (t, C-3), 38.5 (s, C-4), 79.3 (s, C-5), 75.2(d, C-6), 75.6 (d, C-7), 41.6 (d, C-8), 38.0 (d, C-9), 44.5 (s, C-10), 23.2 (t, C-11), 150.5 (s, C-12), 119.8 (s, C-13), 138.5 (s, C-14), 106.5 (d, C-15), 142.0 (d, C-16), 105.6 (q, C-17), 30.7 (q, C-18), 25.1 (q, C-19), 17.1 (q, C-20), 21.4/169.1 (1-OCOCH3), 21.3/170.8(6-OCOCH3), 21.7/170.8(7-OCOCH3)。以上数据与文献[9]报道数据基本一致, 故鉴定化合物2为caesalmin C。
化合物3 白色粉末(氯仿), ESI-MS m/z 555 [M+Na]+, C28H36O10。1H NMR (CDCl3, 500 MHz) δH: 7.22 (1H, d, J=1.8 Hz, H-16), 6.40 (1H, d, J=2.0 Hz, H-15), 5.64 (1H, br s, H-7), 5.54 (1H, br s, H-6), 5.09 (1H, br s, H-17b), 5.03 (1H, dd, J=12.5, 4.3 Hz, H-3), 4.94 (1H, br s, H-17a), 4.92 (1H, s, H-1), 2.10 (3H, s, 7-OCOCH3), 2.09 (3H, s, 6-OCOCH3), 2.03 (3H, s, 3-OCOCH3), 1.96 (3H, s, 1-OCOCH3), 1.15 (3H, s, H-18), 1.14 (3H, s, H-19), 1.33 (3H, s, H-20); 13C NMR (CDCl3, 125 MHz) δC: 75.0 (d, C-1), 27.4 (t, C-2), 72.0 (d, C-3), 43.2 (s, C-4), 80.7 (s, C-5), 75.5(d, C-6), 75.2 (d, C-7), 41.5 (d, C-8), 37.9 (d, C-9), 44.5 (s, C-10), 23.1 (t, C-11), 150.2 (s, C-12), 119.8 (s, C-13), 138.2 (s, C-14), 106.5 (d, C-15), 142.1 (d, C-16), 105.7 (q, C-17), 24.7 (q, C-18), 19.5 (q, C-19), 17.2 (q, C-20), 21.3/ 170.5 (1-OCOCH3), 21.1/169.3 (3-OCOCH3), 21.7/170.6 (6-OCOCH3), 21.2/170.8 (7-OCOCH3)。以上数据与文献[10]报道数据基本一致, 故鉴定化合物3为caesall E。
化合物4 白色粉末(氯仿), ESI-MS m/z439 [M+Na]+, C24H32O6。1H NMR (CDCl3, 500 MHz) δH: 7.22 (1H, d, J=1.9 Hz, H-16), 6.42 (1H, d, J=2.0 Hz, H-15), 5.52 (1H, td, J=10.0, 3.7 Hz, H-7), 5.10 (1H, J=1.9 Hz, H-17a), 4.93 (1H, br s, H-1), 4.76 (1H, J=2.0 Hz, H-17b), 2.06 (3H, s, 1-OCOCH3), 2.05 (3H, s, 7-OCOCH3), 1.22 (3H, s, H-20), 1.11 (3H, s, H-19), 1.06 (3H, s, H-18); 13C NMR (CDCl3, 125 MHz) δC: 75.5(d, C-1), 22.4 (t, C-2), 29.9 (t, C-3), 38.3 (s, C-4), 77.7 (s, C-5), 31.3 (t, C-6), 71.9 (d, C-7), 41.0 (d, C-8), 38.5 (d, C-9), 43.0 (s, C-10), 22.9 (t, C-11), 150.7 (s, C-12), 119.6 (s, C-13), 139.4 (s, C-14), 106.5 (d, C-15), 141.7 (d, C-16), 105.6 (q, C-17), 28.2 (q, C-18), 25.4 (q, C-19), 17.7 (q, C-20), 21.4/169.1 (1-OCOCH3), 21.5/ 170.4 (7-OCOCH3)。以上数据与文献[11]报道数据基本一致, 故鉴定化合物4为caesalpinin MJ。
化合物5 无色针晶(甲醇), ESI-MS m/z 455 [M+Na]+, C24H32O7。1H NMR (CD3OD, 500 MHz) δH: 7.36 (1H, d, J=2.0 Hz, H-16), 6.53 (1H, d, J=2.0 Hz, H-15), 5.50 (1H, m, H-7), 5.49 (1H, m, H-6), 5.09 (1H, d, J=2.0 Hz, H-17b), 4.89 (1H, br s, H-17a), 3.87 (1H, br s, H-1), 2.07 (3H, s, 7-OCOCH3), 1.89 (3H, s, 6-OCOCH3), 1.21 (3H, s, H-20), 1.12 (3H, s, H-19), 1.11 (3H, s, H-18); 13C NMR (CD3OD, 125 MHz) δC: 72.8 (d, C-1), 25.8 (t, C-2), 32.8 (t, C-3), 39.2 (s, C-4), 80.4 (s, C-5), 76.0 (d, C-6), 76.1 (d, C-7), 42.5 (d, C-8), 39.1 (d, C-9), 44.9 (s, C-10), 23.8 (t, C-11), 152.5 (s, C-12), 120.4 (s, C-13), 140.7 (s, C-14), 107.5 (d, C-15), 142.7 (d, C-16), 105.1 (q, C-17), 31.3 (q, C-18), 25.3 (q, C-19), 17.1 (q, C-20), 21.4/170.9 (6-OCOCH3), 21.8/ 170.9 (7-OCOCH3)。以上数据与文献[11]报道数据基本一致, 故鉴定化合物5为1-deacetylcaesalmin C。
| [1] | Editorial Committee of Flora of China, Chinese Academy of Sciences. Flora of China (中国植物志)[M]. Beijing: Science Press, 1998: 366. |
| [2] | Editorial Board of Chinese Materia Medica. Chinese Materia Medica (中华本草)[M]. Shanghai: Shanghai Science and Technology Press, 1999: 368-369. |
| [3] | Peter SR, Tinto WF, McLean S, et al. Bonducellpins A -D, new cassane furanoditerpenes of Caesalpinia bonduc[J]. J Nat Prod, 1997, 60: 1219–1224. DOI:10.1021/np970308c |
| [4] | Yadav PP, Arora A, Bid HK, et al. New cassane butenolide hemiketal diterpenes from the marine creeper Caesalpinia bonduc and their antiproliferative activity[J]. Tetrahedron Lett, 2007, 48: 7194–7199. DOI:10.1016/j.tetlet.2007.07.206 |
| [5] | Yadav PP, Maurya R, Sarkar J. Cassane diterpenes from Caesalpinia bonduc[J]. Phytochemistry, 2009, 70: 256–261. DOI:10.1016/j.phytochem.2008.12.008 |
| [6] | Ata A, Gale ME, Samarasekera R. Bioactive chemical constituents of Caesalpinia bonduc (Fabaceae)[J]. Phytochemistry Lett, 2009, 2: 106–109. DOI:10.1016/j.phytol.2009.02.002 |
| [7] | Udenigwe CC, Ata A, Samarasekera R. Glutathione S-transferase inhibiting chemical constituents of Caesalpinia bonduc[J]. Chem Pharm Bull, 2007, 55: 442–445. DOI:10.1248/cpb.55.442 |
| [8] | Ogunlanaa OO, Kim HS, Wataya Y, et al. Antiplasmodial flavonoid from young twigs and leaves of Caesalpinia bonduc (Linn) Roxb[J]. J Chem Pharm Res, 2015, 7: 931–937. |
| [9] | Jiang RW, Ma SC, But PPH, et al. New antiviral cassane furanoditerpenes from Caesalpinia minax[J]. J Nat Prod, 2001, 64: 1266–1272. DOI:10.1021/np010174+ |
| [10] | Wu L, Luo J, Zhang YM, et al. Cassane-type diterpenoids from the seed kernels of Caesalpinia bonduc[J]. Fitoterapia, 2014, 93: 201–208. DOI:10.1016/j.fitote.2014.01.011 |
| [11] | Kalauni SK, Awale S, Tezuka Y, et al. Cassane-type diterpenes of Caesalpinia crista from Myanmar[J]. Chem Pharm Bull, 2005, 53: 214–218. DOI:10.1248/cpb.53.214 |
| [12] | Deng ZT, Su J, Ding LF, et al. Six new cassane diterpenoids from the seeds of Caesalpinia sappan[J]. Phytochemistry Lett, 2016, 16: 207–212. DOI:10.1016/j.phytol.2016.04.014 |
| [13] | Chen S, Zhang Y, Niu S, et al. Cytotoxic cleistanthane and cassane diterpenoids from the entomogenous fungus Paraconiothyrium hawaiiense[J]. J Nat Prod, 2014, 77: 1513–1518. DOI:10.1021/np500302e |
 2017, Vol. 52
2017, Vol. 52


