阿尔茨海默病的发生是由于大脑皮层缺失了胆碱乙酰转移酶 (ChAT),不能或降低了由胆碱合成乙酰胆碱的能力,皮层的胆碱能传导功能降低,造成记忆障碍和痴呆。所以,提高神经元的胆碱能活性是治疗痴呆患者的一个切入点。此外,胆碱酯酶 (AChE) 抑制剂也是治疗阿尔茨海默病的重要手段。多奈哌 齐的研制就是从寻找新结构类型的胆碱酯酶抑制剂入手的。
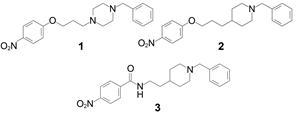
2 苗头化合物及其向先导物的过渡 2.1 随机筛选得到苗头化合物:连接基 -O(CH2)3-N- 的变换日本卫材公司为了研发与他克林结构不同的新型胆碱酯酶抑制剂,用随机筛选方法,发现公司内部为研制抗动脉硬化药物而合成的化合物1对胆碱酯酶有弱抑制作用,对AChE的活性IC50 = 12.6 μmol·L−1。以1作为苗头化合物,对结构逐步修饰,例如将哌嗪环变换为哌啶,化合物2降低了分子的极性,活性提高了36倍,IC50 = 0.34 μmol·L−1。进而将烷氧链的 -O-CH2- 变换成酰胺片段 -CO-NH- ,化合物3的IC50 = 0.055 μmol·L−1,活性提高了5倍,提示虽然化合物3的极性强于2但降低了分子的柔性,可能有利于与酶的结合。
2.2 变换构象和硝基的替换去除3中的硝基,化合物4的IC50 = 0.56 μmol·L−1,活性的下降提示硝基可能提供了与酶结合的因素。而若将酰胺的NH换成CH2,化合物5的活性与4相当,IC50 = 0.53 μmol·L−1,这为以后消除氮原子提供了依据。另外,若将4中N原子甲基化,化合物6的活性提高2倍,IC50 = 0.17 μmol·L−1,可认为N-甲基化产物6不仅消除了氢键 供体,而且由于甲基的阻转异构,改变了分子的走向 (构象)。在6的苯甲酰对位引入苯甲磺酰基 (模拟3的硝基,并提高脂溶性),化合物7的活性有显著提升,IC50 = 0.6 nmol·L−1,活性提高了280倍 (Sugimoto H,Tsuchiya Y,Sugumi H,et al. Novel piperidine derivatives. Synthesis and anti-acetylcholinesterase activity of 1-benzyl-4-[2-(N-benzoylamino) ethyl] piperidine derivatives. J Med Chem,1990,33: 1880−1887)。
|
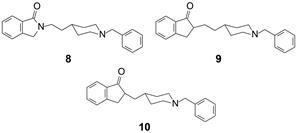
将化合物6的N-CH3与旁侧的苯基形成脂环,得到内酰胺化合物8,其抗乙酰胆碱酯酶活性略有提高,IC50 = 98 nmol·L−1,将8中的酰胺氮原子换成CH,即内酰胺环变成二氢茚酮母核,化合物9的IC50 = 230 nmol·L−1 (消旋物),活性稍有降低。将9中连接茚酮与哌啶的亚乙基缩短为亚甲基,化合物10的IC50 = 150 nmol·L−1 (消旋物)。可以看出,将柔性的开链骨架演化成具有刚性的二氢茚酮为母核的骨架,活性没有显著的改变。从而将化合物10确定为先导化合物进行系统的结构优化。

|
|
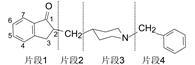
前述的hit-to-lead是分散的非系统性的变换,与先导物的系统优化是不同的。下述的优化过程是将化合物10分成4个片段 (图 1),进行逐段优化。
|
图 1 先导物分成4个片段进行逐段优化 |
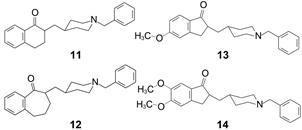
化合物10的二氢茚酮扩环成四氢萘酮11和苯并环庚酮12,评价它们对AChE的抑制活性,表明IC50分别是130、2 100和15 000 nmol·L−1,提示扩环对活性有不利影响,所以仍以10为基础骨架进行优化。
在化合物10的并苯环的4、5、6和7位置上分别用甲氧基作单取代或双取代,报道了9个化合物,对AChE的抑制活性都强于无取代的10,IC50值5.7~ 85 nmol·L−1。其中化合物13和14活性最高,IC50值分别为6.4和5.7 nmol·L−1。
3.2 片段2:亚甲基的变换将活化14的片段2 (-CH2-) 用单键替换,或用不饱和的 =CH、CH= 替换,抑制活性都有不同程度的下降; 用二亚甲基、三亚甲基、四亚甲基或五亚甲基置换,其中三亚甲基化合物的IC50 = 1.5 nmol·L−1,强于14,而其余的活性都弱于14,有趣的是亚甲基链为奇数的化合物比相邻的偶数链化合物的活性高。
|
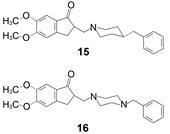
将化合物14的片段3哌啶环的连接方式变换180°,化合物15的活性降低80多倍,IC50 = 480 nmol·L−1,提示连接方式的重要性。用哌嗪环替换的化合物16,活性仍不及14,IC50 = 94 nmol·L−1,说明化合物14 的片段3环的配置和连接方式已是优化状态。
|
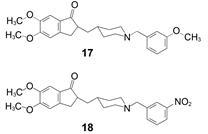
化合物14苄基的苯环上作不同位置的甲基或硝基取代,发现间位取代的化合物17和18的活性略强于14,IC50分别为2.0和 4.0 nmol·L−1,而其他位置的取代均低于14,说明间位取代有利于同酶的结合。用环己甲基、苯乙基或2-萘甲基替换苄基,所得的化合物活性都降低 (Sugimoto H,Iimura Y,Yamanishi Y,et al. Synthesis and structure-activity relationships of acetylcholinesterase inhibitors: 1-benzyl-4-[(5,6-dimethoxy-l-oxoindan-2-yl) methyl]piperidine hydrochloride and related compounds. J Med Chem,1995,38: 4821−4829)。
4 候选化合物的选择: 多奈哌齐通过上述的诸片段的依次优化,综合构效关系,仍显示化合物14为优秀的化合物,进一步评价14的选择性作用,表明对BuChE的抑制作用很弱,IC50 = 7 138 nmol·L−1,与抑制AChE的IC50 = 5.7 nmol·L−1相差1 252倍。对大鼠灌胃5 mg·kg−1,4 h后对脑中的 乙酰胆碱酯酶仍然受到完全抑制。化合物14制成盐酸盐,命名为盐酸多奈哌齐 (donepezil hydrochloride),患者口服生物利用度F几近100%,血浆半衰期t1/2 = 70 h,适于日服一次,经临床研究,于1997年首先在美国上市 (1999年在日本上市),治疗中度阿尔茨海默症患者。多奈哌齐分子中含有1个手性碳原子,该碳原子处于羰基的α位置,容易发生酮−烯醇的互变异构而消旋化,所以临床应用的多奈哌齐是消旋体。
|
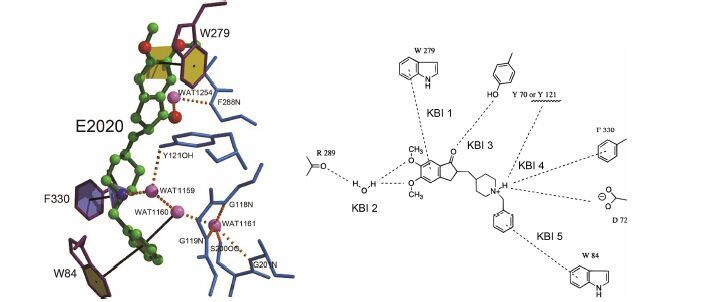
多奈哌齐作为AChE可逆性抑制剂,与底物乙 酰胆碱的结合模式有相当大的区别。AChE的活性中心是个由多个芳香性氨基酸残基构成的峡道 (4.5 Å × 20 Å),ACh-AChE复合物晶体结构表明,季铵离子在峽道的底部,与Trp84发生N+-π相互作用,Gly118与Gly119构成的氧负离子穴接近于乙酰胆碱的羰基氧。然而多奈哌齐与AChE的结合则复杂的多,图 2a是多奈哌齐-AChE复合物晶体结构的结合图,图 2b是多奈哌齐与AChE的分子对接模拟图,二者非常相似。多奈哌齐与乙酰胆碱酯酶大体由5个关键结合位点 (KBI) 构成: ① 茚酮的苯环与Trp279形成π-π堆积作用 (KBI 1); ② 甲氧基与Arg289 (经结构水介导) 形成氢键结合 (KBI 2); ③ 茚酮的羰基氧原子经水分子介导与Phe288氢键结合 (分子模拟的羰基与Tyr70或121氢键结合) (KBI 3); ④ 哌啶经质子化形成的铵离子没有像乙酰胆碱的季铵离子沉入底部与Trp84结合,而是在“半途”与Phe330形成N+-π相互作用、与Asp72成盐以及与Tyr121氢键结合 (KBI 4); ⑤ 苄基沉入到峽道底部,与Trp84发生π-π堆积作 用 (KBI5) (Inoue A,Kawai T,Wakita M,et al. Thesimulated binding of ((±)-2,3-dihydro-5,6-dimethoxy- 2-[[1-(phenylmethyl)-4-piperidinyl] methyl]-1H-inden- 1-one hydrochloride (E2020) and related inhibitors to free and acylated acetylcholinesterases and corresponding structure-activity analyses. J Med Chem,1996,39: 4460−4470; Sussman JL,Harel M,Frolow F,et al. Atomic structure of acetylcholinesterase from Torpedo californica: a prototypic acetylcholine-binding protein. Science,1991,253: 872−879)。
|
图 2 a: 多奈哌齐与AChE复合物晶体结构的结合位点; b: 多奈哌齐与AChE分子模拟示意图 |
 2016, Vol. 51
2016, Vol. 51
