沙门氏菌是一类兼性厌氧革兰阴性菌,无芽孢、有菌毛与鞭毛、无荚膜,一般生存于动物肠道中。沙门氏菌能够特异性地在实体瘤组织的乏氧区内生存繁殖,从而引发免疫反应与肿瘤细胞增殖减慢、坏死凋亡等一系列抗肿瘤效应。为了降低其毒副作用,研究人员敲除了purI和msbB基因得到减毒沙门氏菌菌株VNP20009,降低了毒性,提高了肿瘤靶向性与肿瘤治疗效果[1-6]。而使用VNP20009作为药物传递载体,表达外源药用蛋白与干扰RNA等方法,开展减毒沙门氏菌与药用蛋白、干扰RNA的联合治疗,能够表现出更好的抗肿瘤疗效[7-10]。
肿瘤内呈免疫逃逸的微环境。肿瘤内部的低 pH、乏氧与肿瘤细胞分泌的抗炎因子共同构成了免疫抑制状态的肿瘤内免疫微环境,使肿瘤内部的免疫细胞杀伤肿瘤细胞的能力下降,免疫系统不能有效呈递肿瘤抗原,少量激活的免疫细胞在肿瘤微环境中活性也受到严重抑制[11-13]。据推测VNP20009治疗肿瘤的机制之一可能是通过提高机体的免疫反应水平,进而激发免疫系统消除肿瘤细胞,该机制与肿瘤免疫微环境的改变息息相关。为此,本文通过观察VNP20009对小鼠黑色素瘤模型的治疗效果与瘤内浸润免疫细胞、肿瘤组织细胞因子的变化,探讨VNP20009治疗肿瘤的效果,以及VNP20009对肿瘤免疫微环境的影响。
材料与方法实验材料 减毒沙门氏菌VNP20009菌株、B16F10黑色素瘤细胞购自ATCC); 6~8周龄雌性C57/BL6小鼠购自南京大学模式动物研究所。实验动物合格证号: 201502403; 许可证号: SCXK (苏) 2015-0001。
实验试剂 DMEM培养液、胎牛血清 (FBS)、青霉素/链霉素溶液购自Thermo Inventrogen公司; Percoll淋巴细胞分离液购自美国GE公司; HE染色 试剂盒购自南京建成生物科技有限公司; TUNEL染色试剂盒购自诺唯赞公司; Fc受体阻断剂purified rat anti-mouse CD16/CD32 (Mouse BD Fc Block™,Clone 2.4G2) 购自BD公司; 流式抗体APC rat anti-mouse CD4 anti-CD4 (Clone RM4-5)、FITC rat anti-mouse CD8a (Clone 53-6.7)、PE rat anti-mouse CD11b (Clone M1/70) 购自BD公司; 小鼠TNF-α ELISA试剂盒 (Mouse TNF-α Quantikine ELISA Kit) 与IFN-γ ELISA试剂盒 (Mouse IFN-γ Quantikine ELISA Kit) 购自R&D公司。磷酸盐缓冲液 (phosphate buffer saline,PBS) 购自维森特生物技术 (南京) 有限公司。
实验仪器 台式常温离心机、台式冷冻离心机购自Eppendorf公司; 荧光显微镜购自蔡司公司; 流式细胞仪购自BD公司; 多功能酶标仪购自瑞士TECAN公司。
B16F10小鼠黑色素瘤细胞的培养 使用含10%胎牛血清的DMEM完全培养基,加入100 u·mL-1青霉素与100 u·mL-1链霉素,置培养箱中37 ℃、5% CO2中培养。
VNP20009菌株治疗F10B16黑色素瘤小鼠皮下原位肿瘤模型 将快速生长的F10B16黑色素瘤细胞采用胰酶消化,PBS洗2次后调细胞数为2×106个/mL,在预先刮过毛发的小鼠右腋下皮下接种肿瘤细胞悬液100 μL,每只小鼠接种F10B16细胞2×105个。
待小鼠肿瘤体积长至150 mm3时,将预先复苏 好的VNP20009菌株培养到对数生长期,用PBS洗 涤2次后测量光密度 (OD),根据OD值 (1 OD的VNP20009 = 3.84×108 cfu·mL-1) 稀释菌液至1×105 cfu·mL-1,每只小鼠腹腔注射100 μL,即每只小鼠接种1×104个细菌。
接种细菌后每两天使用游标卡尺测量肿瘤大小,待PBS对照组肿瘤体积平均达到6 000~10 000 mm3时停止实验。
HE染色观察肿瘤组织病理切片 将肿瘤组织完整取出,用4% 多聚甲醛溶液固定至少24 h,石蜡包埋并切片。切片经HE染色后光镜下观察。每张切片随机挑选5个视野用于统计坏死凋亡区面积,取其平均值视为该切片的坏死凋亡区百分比,以每张切片为单位进行统计。
TUNEL法染色观察肿瘤组织细胞凋亡情况 石蜡切片经脱蜡复水后,用蛋白酶K溶液孵育切片20 min,PBS洗3遍后,使用TUNEL凋亡检测试剂盒进行切片TUNEL染色,荧光显微镜下观察肿瘤组织细胞凋亡情况。
减毒沙门氏菌VNP20009在荷瘤小鼠体内的组织分布分析 将VNP20009菌株复苏后,转接到新鲜LB中培养至OD = 0.8,4 ℃、4 000 r·min-1离心5 min收集细菌,用无菌PBS洗涤2次。取肿瘤体积为150 mm3左右的B16F10黑色素瘤模型鼠,每只小鼠腹腔注射细菌1×104 cfu,对照组注射PBS,正常饲养。
注射3天后处死小鼠,无菌条件下取出小鼠肿 瘤、心、肝、脾、肺和肾。称重后用预冷的组织匀浆机60 Hz匀浆180 s,梯度稀释后涂LB平板,37 ℃培养12~16 h后计算菌落数。
瘤内免疫细胞亚群的分析 肿瘤组织剪碎后放于含300 U·mL-1胶原酶与50 U·mL-1的含20% 胎牛血清的RPMI 1640培养基中,消化1.5 h。每30 min吹打消化液,将大块组织吹散。消化完全时将消化 液过75 μm细胞筛以去除杂质,于4 ℃、400×g离心 10 min收集沉淀。沉淀经36% 与63% percoll密度 梯度离心纯化,收集两层percoll中间的免疫细胞层。洗掉percoll后即为瘤内浸润免疫细胞。细胞经Fc Block工作液封闭后,冰上孵育抗体30 min,采用流式机分析 (Fc Block工作液: 含10% FBS,1 μg·mL-1 Fc Block的PBS)。
肿瘤内细胞因子的测定 剪碎肿瘤组织,加入细胞裂解液后匀浆,冰上放置1 h。将组织匀浆混合物于12 000×g离心10 min收集上清,并用BCA法测定上清中的蛋白浓度。最后使用ELISA法测定上清中TNF-α与IFN-γ的含量。
数据处理 采用GraphPad 6软件进行统计学分析,组间数据的比较采用t检验,以P < 0.05为差异有统计学意义。
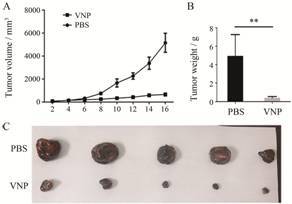
结果 1 VNP20009菌株的肿瘤治疗效果在B16F10黑色素瘤细胞制作的皮下瘤小鼠模型中,通过肿瘤体积曲线与肿瘤重量来评价肿瘤治疗的效果。在肿瘤治疗实验中,VNP20009对肿瘤有明显治疗效果,从肿瘤体积曲线与肿瘤重量上都可以发现注射VNP20009组的肿瘤生长较PBS对照组显著减慢 (图 1)。通过肿瘤组织HE染色的病理切片观察肿瘤内部的情况 (图 2) 以及TUNEL染色观察肿瘤组织细胞坏死与凋亡情况 (图 3),发现细菌治疗组的肿瘤组织内部的坏死凋亡区面积及坏死与凋亡比例均出现增加,说明VNP20009能够导致肿瘤细胞的坏死与凋亡。
|
Figure 1 Anti-tumor efficacy of VNP20009 on B16F10 tumor model. PBS: PBS control group,VNP: VNP20009 treatment group. A: VNP20009 treatment markedly inhibited melanoma growth; B: Tumor weight is reduced after treatment of VNP20009; C: Tumors from control and treatment groups. n = 10,x± s. **P < 0.01 |
|
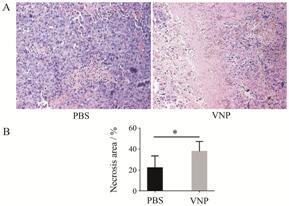
Figure 2 Histochemical analysis of cell death by HE staining (A). PBS: PBS control group,VNP: VNP20009 treatment group. The necrosis area is significantly increased in tumors treated with VNP20009,compared with the untreated control group (B). n = 5,x± s. P < 0.05 |
|
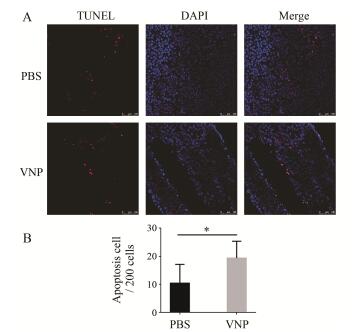
Figure 3 Apoptosis of tumor cells were stained by TUNEL (A) and quantitative analyses (B) ,cell nucleus was stained by DAPI. PBS: PBS control group,VNP: VNP20009 treatment group. n = 8,x± s. P < 0.05 |
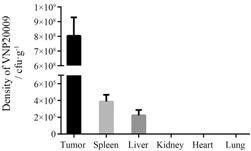
VNP20009菌株能够靶向肿瘤组织,在肿瘤组织内快速生长繁殖。实验数据显示,VNP20009在肿瘤内部的浓度达到平均8×108 cfu·g-1,而在脾、肝中仅能达到3.8×105和2.2×105 cfu·g-1,在心、肾与肺中几乎没有细菌出现。在肿瘤中的菌落密度是正常组织中最高脾脏的平均2 000倍以上,说明VNP20009有很好的肿瘤靶向性 (图 4)。
|
Figure 4 Tissue distribution of VNP20009 measured by colony forming assay. n = 5,x± s. VNP20009 can specially accumulate in solid tumor,and only little bacteria can be found in normal tissues |
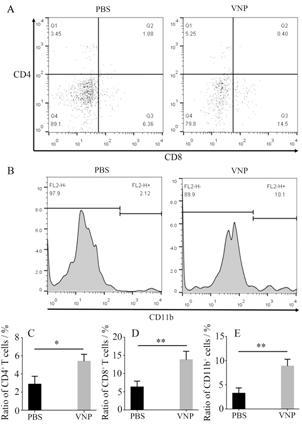
肿瘤内部浸润淋巴细胞是机体抗肿瘤的主要因素之一,通过观察肿瘤内部浸润淋巴细胞的亚群比例,可以了解肿瘤内部免疫细胞对肿瘤细胞杀伤的程度。实验数据显示,注射过沙门氏菌的小鼠肿瘤内部的CD4+、CD8+T细胞与CD11b+单核细胞数量明显提高,其中CD4+T细胞、CD8+T细胞和CD11b+单核细胞分别是PBS对照组的1.87、2.18与2.7倍。CD8+T细胞与CD11b+的单核-巨噬细胞是执行肿瘤免疫杀伤的关键细胞,说明VNP20009能通过提高肿瘤内CD8+T细胞与CD11b+单核-巨噬细胞的浸润水平而发挥杀伤肿瘤细胞的作用 (图 5)。
|
Figure 5 Analysis of tumor infiltrating immunocytes by flow cytometry. PBS: PBS control group,VNP: VNP20009 treatment group. A: Infiltrating CD4+ and CD8+ T cells in within tumor tissue. B: Infiltrating CD11b+ monocytes within in tumor tissue. Quantitative analyses of CD4+ T cells (C),CD8+ T cells (D),CD11b+ monocytes (E). n = 3,x± s. P < 0.05,**P < 0.01 |
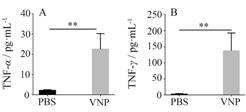
肿瘤组织内的细胞因子含量能在一定程度上反映肿瘤内免疫反应的类型与强度,上述研究数据已经表明: VNP20009能显著提高肿瘤内CD8+T细胞与CD11b+单核-巨噬细胞的数量,而TNF-α与IFN-γ是CD8+T细胞与单核-巨噬细胞分泌的主要细胞因子,也是机体抗肿瘤免疫的重要细胞因子,因而测定了VNP20009治疗后肿瘤组织内TNF-α与IFN-γ的含量。实验结果显示,注射VNP20009能显著提高肿瘤组织内TNF-α和IFN-γ的含量,分别是PBS对照组的10倍与46倍。证明VNP20009能通过提高CD8+T细胞与单核-巨噬细胞的活性增强其在肿瘤内部分泌细胞因子,进而提高肿瘤内的免疫反应,破坏肿瘤免疫微环境中的免疫逃逸效应,而产生抗肿瘤效应 (图 6)。
|
Figure 6 Cytokines analysis. PBS: PBS control group,VNP: VNP20009 treatment group. A: TNF-α in tumor tissues; B: IFN-γ in tumor tissues. n = 4,x± s. **P < 0.01 |
肿瘤治疗药物的抗肿瘤疗效不佳,其原因之一是药物在肿瘤内的浓度不高,而为了药物在肿瘤内能达到合适浓度,还会导致在正常组织中药物浓度过高产生严重不良反应,这成为肿瘤治疗的难点之一,而肿瘤靶向药物是解决这一问题的最佳方案[14-16]。细菌可以靶向性抑制肿瘤的现象早在100年前已被发现,随着目前肿瘤靶向药物的研究热潮,靶向性治疗肿瘤的细菌疗法也被研究者所关注。因为肿瘤内 的乏氧与免疫抑制环境利于细菌生长,减毒沙门氏菌VNP20009能靶向性地在肿瘤组织内生长繁殖,通过竞争营养、分泌毒素以及引起免疫反应等方式使 肿瘤组织坏死、凋亡。本研究证明,VNP20009治疗后,肿瘤生长速度明显减缓,肿瘤细胞大量死亡。说明VNP20009有抑制肿瘤组织生长,促使肿瘤细胞坏死凋亡的良好效果。
肿瘤微环境是肿瘤本身生长所处的内环境,主要由肿瘤细胞和间质细胞、成纤维细胞、免疫细胞等基质细胞,包含各种功能性分子与营养物质的细胞外基质与血管组成,与其说肿瘤是一种均质的组织,现在更倾向于认为其是一个特殊的器官,是动态的、时刻变化的和非均质的。而肿瘤免疫微环境则是指包括免疫抑制性细胞与物质和抗肿瘤的免疫细胞与细胞因子等物质组成的肿瘤组织内的免疫环境。肿瘤免疫微环境整体上是免疫抑制的,不利于免疫杀伤细胞执行肿瘤杀伤的功能[11-13, 17-19]。VNP20009能提高肿瘤组织内部的免疫反应水平,使肿瘤内CD8+T细胞与单核-巨噬细胞浸润增加,进而使主要由T细胞分泌的Th1型细胞因子IFN-γ与TNF-α的含量明显提高。CD8+T细胞中细胞毒性T细胞(CTL) 和单核-巨噬细胞,都是抗肿瘤免疫的效应细胞。CTL可以直接通过分泌穿孔素、颗粒酶和FasL杀伤肿瘤细胞,单核-巨噬细胞也可通过分泌NO或通过抗体依赖性的细胞介导的细胞毒 (antibody-dependent cell-mediated cytotoxicity,ADCC) 作用杀伤肿瘤细胞。不仅如此,CTL与单核-巨噬细胞均可通过分泌细胞因子 (如TNF-α、IFN-γ) 激活免疫反应,提高免疫细胞活性,杀灭肿瘤细胞[20,21]。TNF-α可以通过提高杀伤性T细胞与NK细胞的抗肿瘤活性产生抗肿瘤效应[2122,23],高浓度的TNF-α还可以直接诱导肿瘤细胞凋亡[24]。而IFN-γ不仅可以使免疫反应向Th1型免疫反应极 化,使免疫反应向细胞免疫倾斜,还可以激活杀伤性T细胞、NK细胞与巨噬细胞等肿瘤杀伤细胞,提高对肿瘤细胞的杀伤抑制效应[25,26]。
综上所述,VNP20009能使肿瘤免疫微环境中执行细胞杀伤效应的CD8+T细胞与单核-巨噬细胞浸润增加,肿瘤免疫微环境中的TNF-α与IFN-γ含量明显提高,免疫反应向Th1型反应倾斜,破坏肿瘤免疫微环境中的免疫逃逸效应,使肿瘤杀伤细胞在肿瘤内的数量与活性明显提高,实现抑制肿瘤生长,杀灭肿瘤细胞的作用。结果说明VNP20009可以通过激活机体的免疫反应,提高机体本身肿瘤杀伤细胞的活性来杀伤肿瘤细胞,抑制肿瘤生长,有很好的抗肿瘤疗效。
| [1] | Hayashi K, Zhao M, Yamauchi K, et al. Cancer metastasis directly eradicated by targeted therapy with a modified Salmonella typhimurium[J]. J Cell Biochem , 2009, 106 :992–998. DOI:10.1002/jcb.v106:6 |
| [2] | Zhao M, Yang M, Li XM, et al. Tumor-targeting bacterial therapy with amino acid auxotrophs of GFP-expressing Salmonella typhimurium[J]. Proc Nat Acad Sci U S A , 2005, 102 :755–760. DOI:10.1073/pnas.0408422102 |
| [3] | Zhang L, Gao L, Zhao L, et al. Intratumoral delivery and suppression of prostate tumor growth by attenuated Salmonella enterica serovar typhimurium carrying plasmid-based small interfering RNAs[J]. Cancer Res , 2007, 67 :5859–5864. DOI:10.1158/0008-5472.CAN-07-0098 |
| [4] | Zhao M, Geller J, Ma H, et al. Monotherapy with a tumor-targeting mutant of Salmonella typhimurium cures orthotopic metastatic mouse models of human prostate cancer[J]. Proc Nat Acad Sci U S A , 2007, 104 :10170–10174. DOI:10.1073/pnas.0703867104 |
| [5] | Clairmont C, Lee KC, Pike J, et al. Biodistribution and genetic stability of the novel antitumor agent VNP20009, a genetically modified strain of Salmonella typhimurium[J]. J Infect Dis , 2000, 181 :1996–2002. DOI:10.1086/jid.2000.181.issue-6 |
| [6] | Low KB, Ittensohn M, Le T, et al. Lipid A mutant Salmo-nella with suppressed virulence and TNF-α induction retain tumor-targeting in vivo[J]. Nat Biotechnol , 1999, 17 :37–41. |
| [7] | Chen J, Wei D, Zhuang H, et al. Proteomic screening of anaerobically regulated promoters from Salmonella and its antitumor applications[J]. Mol Cell Proteomics , 2011, 10 :2889–2894. |
| [8] | Ganai S, Arenas RB, Forbes NS. Tumour-targeted delivery of TRAIL using Salmonella typhimurium enhances breast cancer survival in mice[J]. Br J Cancer , 2009, 101 :1683–1691. DOI:10.1038/sj.bjc.6605403 |
| [9] | Loeffler M, Le'Negrate G, Krajewska M, et al. Salmonella typhimurium engineered to produce CCL21 inhibit tumor growth[J]. Cancer Immunol Immunother , 2009, 58 :769–775. DOI:10.1007/s00262-008-0555-9 |
| [10] | Cheng X, Zhang X, Cheng W, et al. Tumor-specific delivery of histidine-rich glycoprotein suppresses tumor growth and metastasis by anti-angiogenesis and vessel normalization[J]. Curr Gene Ther , 2014, 14 :75–85. DOI:10.2174/1566523214666140305223912 |
| [11] | Whiteside TL. The tumor microenvironment and its role in promoting tumor growth[J]. Oncogene , 2008, 27 :5904–5912. DOI:10.1038/onc.2008.271 |
| [12] | Gajewski TF, Meng Y, Blank C, et al. Immune resistance orchestrated by the tumor microenvironment[J]. Immunol Rev , 2006, 213 :131–145. DOI:10.1111/imr.2006.213.issue-1 |
| [13] | Shiao SL, Ganesan AP, Rugo HS, et al. Immune microenvi-ronments in solid tumors: new targets for therapy[J]. Genes Dev , 2011, 25 :2559–2572. DOI:10.1101/gad.169029.111 |
| [14] | Zhen YS. Current situation and prospect of research on anti-tumor drug[J]. Acta Pharm Sin (药学学报) , 1994, 29 :1–8. |
| [15] | He QY. Tumor heterogeneity and drug resistance of targeted antitumor agents[J]. Acta Pharm Sin (药学学报) , 2016, 51 :197–201. |
| [16] | Gao HL, Jiang XG. The development of novel tumor targeting delivery strategy[J]. Acta Pharm Sin (药学学报) , 2016, 51 :272–280. |
| [17] | Wang H, Chen L. Tumor microenviroment and hepatocellular carcinoma metastasis[J]. J Gastroenterol Hepatol , 2013, 28 (Suppl 1) :43–48. |
| [18] | Hanahan D, Weinberg RA. Hallmarks of cancer: the next generation[J]. Cell , 2011, 144 :646–674. DOI:10.1016/j.cell.2011.02.013 |
| [19] | Brown JM. Tumor microenvironment and the response to anticancer therapy[J]. Cancer Biol Ther , 2002, 1 :453–458. DOI:10.4161/cbt.1.5.157 |
| [20] | Hibbs JB Jr, Taintor RR, Vavrin Z. Macrophage cytotoxicity: role for L-arginine deiminase and imino nitrogen oxidation to nitrite[J]. Science , 1987, 235 :473–476. DOI:10.1126/science.2432665 |
| [21] | Chamoto K, Kosaka A, Tsuji T, et al. Critical role of the Th1/Tc1 circuit for the generation of tumor-specific CTL during tumor eradication in vivo by Th1-cell therapy[J]. Cancer Sci , 2003, 94 :924–928. DOI:10.1111/cas.2003.94.issue-10 |
| [22] | Kashii Y, Giorda R, Herberman RB, et al. Constitutive expression and role of the TNF family ligands in apoptotic killing of tumor cells by human NK cells[J]. J Immunol , 1999, 163 :5358–5366. |
| [23] | Prévost-Blondel A, Roth E, Rosenthal FM, et al. Crucial role of TNF-α in CD8 T cell-mediated elimination of 3LL-A9 Lewis lung carcinoma cells in vivo[J]. J Immunol , 2000, 164 :3645–3651. DOI:10.4049/jimmunol.164.7.3645 |
| [24] | Colotta F, Peri G, Villa A, et al. Rapid killing of actinomycin D-treated tumor cells by human mononuclear cells. I. Effectors belong to the monocyte-macrophage lineage[J]. J Immunol , 1984, 132 :936–944. |
| [25] | Boehm U, Klamp T, Groot M, et al. Cellular responses to interferon-γ[J]. Annu Rev Immunol , 1997, 15 :749–795. DOI:10.1146/annurev.immunol.15.1.749 |
| [26] | Cope A, Le Friec G, Cardone J, et al. The Th1 life cycle: molecular control of IFN-γ to IL-10 switching[J]. Trends Immunol , 2011, 32 :278–286. DOI:10.1016/j.it.2011.03.010 |
 2016, Vol. 51
2016, Vol. 51


