2. 中山大学药学院, 广东 广州 510006 ;
3. 中山大学附属第一医院, 广东 广州 510080
2. School of Pharmaceutical Sciences, Sun Yat-sen University, Guangzhou 510006, China ;
3. The First Affiliated Hospital, Sun Yat-sen University, Guangzhou 510080, China
五酯片 (Wuzhi tablet,WZ) 是华中五味子的乙醇提取物制剂,主要活性成分为木脂素类化合物,包括五味子甲素 (schisandrin A)、五味子乙素 (schisandrinB)、五味子丙素 (schisandrin C)、五味子醇甲 (schisandrolA)、五味子醇乙 (schisandrol B)、五味子酯甲 (schisantherinA) 等[1],具有抗肝细胞损伤、改善肝细胞代谢的作用,常用于辅助治疗各种类型肝损伤[1-3]。许多文献[4, 5]报道,五味子提取物及其活性成分可以抑制体外CYP3A的活性。作者[6-9]的研究亦表明单次灌胃给予五酯片及其活性成分可以使大鼠体内CYP3A底物——他克莫司、环孢素及紫杉醇等的血药浓度显著升高。但是,长期服用五酯片对CYP3A活性的影响,以及五酯片是否通过影响CYP3A基因及蛋白表达从而影响其活性尚未清楚。因此,本研究利用实时荧光定量PCR及Western blot法考察五酯片对CYP3A基因及蛋白表达的影响,并利用经典CYP3A探针药——咪达唑仑评价长期灌胃给予五酯片对大鼠体内CYP3A活性影响,阐明五酯片对CYP3A的长期作用。
材料与方法药品与试剂 五酯片 (广西方略药业有限公司,批号: 090910); 咪达唑仑 (midazolam,MDZ,5 mg×1 mL/ 支,江苏恩华药业股份有限公司,批号: 20090501);地塞米松 (dexamethasone,Dex,≥98%,Sigma公司); 肝素钠注射液 (常州千红生化制药股份有限公司,批号: 090625); PE插管 (Polythene 0.98 mm OD,浙江安莱科技有限公司); Trizol试剂 (Invitrogen公司); RT试剂盒 (日本Takara公司); SYBR®Premix Ex TaqTM Ⅱ试剂盒 (日本 Takara公司); Tris (晶欣生物科技公司,批号: 20100327); 硼酸 (天津市百世化工有限公司,批号: 20090630); RIPA蛋白提取试剂 (上海博彩生物科技有限公司); 苯甲基磺酰氟 (上海博彩生物科技有限公司); 丙烯酰胺 (广州国奥生物技术有限公司); N,N '-亚甲基双丙烯酰胺 (广州国奥生物技术有限公司); BCA蛋白测定试剂盒 (Thermo Scientific公司); 色谱分析实验中所用试剂均为色谱纯。
仪器 Roche lightcycler 2.0定量PCR仪(德国罗氏仪器有限公司); PCR仪 (Biometra梯度PCR仪);Mini-PROTEAN3电泳系统 (美国Bio-Rad公司); Mini Trans-Blot转移系统 (美国Bio-Rad公司); GDS-8000UVP凝胶成像系统 (美国UVP公司); 5417-R低温高速离心机 (德国Eppendorf公司); Surveyor高效液相-质谱联用仪 (美国Finnigan公司)。
实验动物 清洁级雄性Sprague-Dawley大鼠27只,220~240 g,由中山大学实验动物中心提供 (合格证号: SCXK (粤) 2009-0011),于SPF级环境饲养,动物室内温度20~25 ℃、相对湿度40%~70%、换气次数10~15次/h,保持12 h光照循环; 期间自由饮水进食,提供实验室标准动物饲料,符合我国《实验动物管理条例》和《医学实验动物管理实施细则》。
五酯片对大鼠肝脏和肠道CYP3A基因及蛋白表达的影响 12只雄性SD大鼠随机分成3组,一 组连续灌胃给予五酯片混悬液14天 (WZ group,0.25 g·kg-1),一组则灌胃给予相同体积的蒸馏水 (control group),另一组连续灌胃给予蒸馏水10天后继续灌胃给予地塞米松 (Dex group,100 mg·kg-1)4天。以上所有大鼠最后一次给药后,禁食12 h,次日断头取其肝脏及肠道 (幽门至幽门以下50 cm),用生理盐水将肝脏表面血迹及肠道内容物冲洗干净,用干净的刀片将小肠黏膜刮下,马上置液氮中保存,按作者已经建好的方法提取RNA及蛋白[10]。采用实时荧光定量PCR方法检测大鼠肝脏及肠道Cyp3a1 (引物: Cyp3a1-F 5'-GGAAATTCGATGTGGAGTGC-3',Cyp3a1-R 5'-AGGTTTGCCTTTCTCTTGCC-3')、Cyp3a2 (引物: Cyp3a2-F 5'-AGTAGTGACGATTCCAACATAT- 3',Cyp3a2-R 5'-TCAGAGGTATCTGTGTTTCCT-3')、Cyp3a9 (引物: Cyp3a9-F 5'-TGGTTATCAGCCTGGTGC-3',Cyp3a9-R 5'-AAAGTTCCGTCGGTTTGT-3')、Cyp3a18 (引物: Cyp3a18-F 5'-TGATGCCACAAGCA CCTC-3',Cyp3a18-R 5'-AGACTTTCATTCACCACC- 3')、内参Gapdh(引物: Gapdh-F 5'-GGCACAGTCAAGGCTGAGAATG-3',Gapdh-R 5'-ATGGTGGTGAAG ACGCCAGTA-3') mRNA含量[11]。采用作者已经建好的Western blot的方法检测CYP3A蛋白含量[10]。
五酯片对大鼠体内咪达唑仑的药动学影响 另取15只大鼠随机分成3组,其中两组连续灌胃给予五酯片混悬液14天 (0.25 g·kg-1),一组则灌胃给予相同体积的蒸馏水 (空白对照组)。第14天,大鼠行右颈静脉插管手术[6-9]。术后恢复12 h后用于实验,给药前12 h禁食。第15天,连续灌胃给予五酯片混悬液14天的2组大鼠,其中一组先灌胃给予五酯片混悬液 (0.25 g·kg-1) 再灌胃给予咪达唑仑 (2 mg·kg-1,合用五酯片组,WZ coadministeredgroup),另一组 给予同体积的蒸馏水后再灌胃给予咪达唑仑 (五酯片预处理组,WZ pretreatment group); 空白对照组则给予同体积的蒸馏水后再灌胃给予咪达唑仑; 于给药前 (0 h)、给药 (咪达唑仑) 后0.083、0.17、0.25、0.5、0.75、1、1.5、2、3和4h从右颈静脉插管处取血约0.25 mL。取血后即从插管处补充同体积的肝素化生理盐水(含50 U·mL-1肝素的生理盐水),所取 血样12 000 r·min-1离心10 min,立即精密吸取上清100 μL置2 mL EP管中,置-80 ℃保存。
数据分析 血样按作者[12]建立的LC-MS/MS方法检测血浆中咪达唑仑、1'-羟基咪达唑仑的浓度,并用PKPP药动学软件包计算药代动力学参数[6-9]。统计学分析用方差分析及非参数检验,P < 0.05有统计学意义。数据处理软件为SAS 8.1(SAS Ver.8.1,SAS Institute Inc.,Cary,NC,USA) 统计学软件。
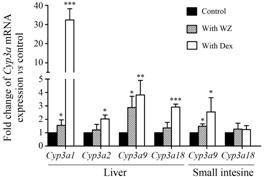
结果 1 五酯片对大鼠肝脏和肠道CYP3A基因表达的影响 1.1 对大鼠肝脏CYP3A基因表达的影响长期灌胃给予五酯片对大鼠肝脏CYP3A基因表达的影 响见图 1。在大鼠肝脏中,长期灌胃给予五酯片组的 Cyp3a1、Cyp3a2、Cyp3a9、Cyp3a18 mRNA表达分别为空白对照组的1.55 ± 0.41、1.21 ± 0.41、2.88 ± 0.84、1.36 ± 0.41(P < 0.05) 倍。长期灌胃给予五酯片使大鼠肝脏中Cyp3a1及Cyp3a9 mRNA表达分别升高54.6% 及188.3%(P < 0.05),而对其他基因包括Cyp3a2、Cyp3a18 mRNA表达影响不大。
|
Figure 1 Changes in mRNAexpression of hepatic Cyp3as of rats after oral administered Wuzhi tablet (WZ,0.25 g·kg-1) for 14 consecutive days or dexamethasone (Dex,100 mg·kg-1) for 4 consecutive days,data were expressed as fold expression compared withvehicle treatment. n = 4,x± s. P < 0.05,**P < 0.01,***P < 0.01 vscontrol group |
长期灌胃给予五酯片对大鼠肠道CYP3A基因表达的影响见图 1。在大鼠小肠中,长期灌胃给予五酯片组的Cyp3a9、Cyp3a18 mRNA表达分别为空白对照组的1.48 ± 0.18 (P < 0.05)、1.27 ± 0.44倍。长期灌胃给予五酯片使大鼠肠道中Cyp3a9 mRNA表达升高48.2% (P < 0.05),而对Cyp3a18 mRNA表达影响微弱。
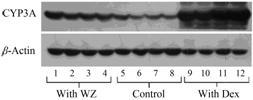
2 五酯片对大鼠肝脏和肠道CYP3A蛋白表达的影响长期灌胃给予五酯片对大鼠肝脏、肠道CYP3A蛋白表达的影响见图 2。在大鼠肝脏中,长期灌胃给予五酯片组的CYP3A蛋白的表达为空白对照组的1.43 ± 0.47倍。在大鼠小肠中,长期灌胃给予五酯片组CYP3A的蛋白表达为空白对照组的0.91 ± 0.14倍。长期灌胃给予五酯片使大鼠肝脏CYP3A的蛋白表达升高43.2%,但对大鼠肠道CYP3A蛋白表达影响微弱。
|
Figure 2 Changes inprotein expression of hepatic CYP3A of rats after long-term treatment of WZ (0.25 g·kg-1) for 14 consecutive days or Dex (100 mg·kg-1) for 4 consecutivedays,data were expressed as fold expression compared with vehicle treatment. n = 4 |
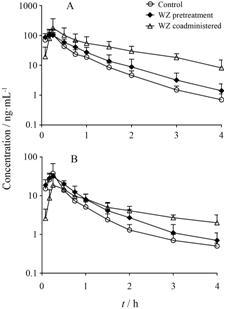
长期灌胃给予五酯片对咪达唑仑药动学影响 的药时曲线见图 3,药动学参数见表 1。长期灌胃 给予五酯片后,未合用五酯片组 (即五酯片预处理组,WZpretreatment group) 咪达唑仑的AUC升高29.9%; 而合用五酯片组 (WZ coadministeredgroup) 咪达唑仑的AUC升高154.2%,咪达唑仑主要的代 谢产物1-羟基咪达唑仑的AUC与咪达唑仑AUC之比 (AUCM/AUCP) 降低了54.8%。
|
Figure 3 Plasmaconcentration-time profiles of midazolam (MDZ) (A),1-hydroxylation midazolam(1-OH MDZ) (B) of rats after oral administrations of MDZ (2 mg·kg-1)with or without WZ (0.25 g·kg-1)pretreated for 14 days. n = 5,x± s |
| Table 1 Pharmacokineticparameters of MDZ and 1-OH MDZ of rats after oral administrations of MDZ (2 mg·kg-1)with or without WZ (0.25 g·kg-1)pretreated for 14 days. n = 5,x± s. Con: Controlgroup,MDZ alone group; WZ pretreatment/ coadministered:Rats of the pretreatment group and the coadministered group were gavaged with WZ(0.25 g·kg-1)for 14 consecutive days. On day 15,rats inthe control group and the pretreatmentgroup received a vehicle (water),while those inthe coadministered group were given with WZ (0.25 g·kg-1).AUCM/AUCP: AUC of 1-OH MDZ/AUC of MDZ |
实验中,五酯片给药天数的确定是参考相关文献。由于药物对于CYP450酶产生的诱导作用与药物本身特性、半衰期及与CYP450酶半衰期有关。当给药时间持续4~14天,药物对代谢酶是否具有诱导作用一般都能体现[13]。因此,本实验选用连续灌胃给予五酯片14天,以考察长期灌胃给予五酯片对大鼠体内CYP3A基因和蛋白表达及酶活性的影响。据文献[14]报道,Cyp3a基因亚型在大鼠体内的分布存在组织差异。在大鼠肝脏主要为Cyp3a1、Cyp3a2、Cyp3a9、Cyp3a18等基因; 而在大鼠小肠中,只能检测得到Cyp3a9及Cyp3a18,检测不到Cyp3a1及Cyp3a2。因此,在肝脏中选择考察Cyp3a1、Cyp3a2、Cyp3a9及Cyp3a18等目的基因的变化,以反映长期灌胃给予五酯片对大鼠肝脏Cyp3a基因表达 (mRNA) 的影响; 而在小肠中,则选择考察Cyp3a9及Cyp3a18等目的基因的变化,以反映长期灌胃给予五酯片对大鼠肠道Cyp3a表达的影响。由于作者的预实验结果表明五酯片对大鼠小肠上、中、下段Cyp3a基因表达影响 的趋势相同,因此,本实验有针对性地考察长期灌胃给予五酯片对大鼠小肠上段 (幽门至幽门以下50 cm) Cyp3a基因表达的影响。
本实验通过考察长期灌胃给予五酯片对大鼠体内CYP3A基因和蛋白表达及对经典探针药——咪达唑仑药动学的影响,评价长期灌胃给予五酯片对CYP3A基因、蛋白表达及活性的影响,初步阐明中药五酯片对CYP3A的影响机制。结果表明,长期灌胃给予五酯片使大鼠肝脏CYP3A基因、蛋白表达升高,却使咪达唑仑的AUC升高。作者研究组另外的研究表明: 灌胃给予五酯片10 h后,大鼠全血、肝脏及肠道中基本检测不到五酯片各木脂素活性成分。但是本研究中,长期灌胃给予五酯片间隔24 h后仍可使大鼠体内咪达唑仑的AUC升高29.9% (未合用五酯片组),证实长期灌胃给予五酯片可抑制CYP3A的活性。可见,五酯片诱导CYP3A mRNA及蛋白表达,却可抑制CYP3A的蛋白活性。五酯片这种对CYP3A基因、蛋白表达水平与酶活性影响不一致的现象提示: 五酯片并非通过降低CYP3A基因、蛋白表达而降低其活性,五酯片对CYP3A存在双向调节机制。
从大量对药物代谢酶功能调控的研究可以发现,存在某些CYP450酶亚型的mRNA及蛋白的表达上升,但相应的活性却下降的现象。如红霉素是经典的CYP3A底物,亦为经典的CYP3A抑制剂,实验表明重复给予SD大鼠4 mmol·kg-1红霉素可以诱导大鼠肝脏CYP450酶,但同时红霉素却与酶形成复合物使酶失去活性[15, 16]。另有研究报道竹桃霉素亦可使CYP3A的蛋白表达升高,但同时抑制了CYP3A的蛋白活性[17, 18]。国内的研究报道[19]白蔹配伍乌头可以通过影响基因转录进而提高CYP1A2、CYP3A1/2的mRNA和蛋白质表达水平,但CYP1A2、CYP3A1/2酶的活性却下降。药物对CYP450酶活性的调控,作用在转录、转录后、翻译、翻译后蛋白修饰等水平上,因此,仅转录 (基因) 水平或者翻译 (蛋白) 水平的上调或者下调,并不能推知最后蛋白活性的增强或者减弱。五酯片对CYP3A基因、蛋白表达水平与酶活性影响不一致的现象提示: 在翻译水平之后可能存在影响和调节CYP3A活性的重要机制和因素,最终导致五酯片对CYP3A蛋白表达及对CYP3A生物活性影响不一致的现象,具体机制有待进一步研究。
| [1] | Huyke C, Engel K, Simon-Haarhaus B, et al. Composition and biological activity of different extracts from Schisandra sphenanthera and Schisandra chinensis[J]. Planta Med , 2007, 73 :1116–1126. DOI:10.1055/s-2007-981559 |
| [2] | Loo WT, Cheung MN, Chow LW. Fructus Schisandrae (Wuweizi)-containing compound inhibits secretion of HBsAg and HBeAg in hepatocellular carcinoma cell line[J]. Biomed Pharmacother , 2007, 61 :606–610. DOI:10.1016/j.biopha.2007.08.023 |
| [3] | Xin HW, Li Q, Wu XC, et al. Effects of Schisandra sphenan-thera extract on the blood concentration of tacrolimus in renal transplant recipients[J]. Eur J Clin Pharmacol , 2011, 67 :1309–1311. DOI:10.1007/s00228-011-1075-7 |
| [4] | Iwata H, Tezuka Y, Kadota S, et al. Identification and characterization of potent CYP3A4 inhibitors in Schisandra fruit extract[J]. Drug Metab Dispos , 2004, 32 :1351–1358. DOI:10.1124/dmd.104.000646 |
| [5] | Wan CK, Tse AK, Yu ZL, et al. Inhibition of cytochrome P450 3A4 activity by schisandrol A and gomisin A isolated from Fructus Schisandrae chinensis[J]. Phytomedicine , 2010, 17 :702–705. DOI:10.1016/j.phymed.2009.12.005 |
| [6] | Jin J, Bi H, Hu J, et al. Effect of Wuzhi tablet (Schisandra sphenanthera extract) on the pharmacokinetics of paclitaxel in rats[J]. Phytother Res , 2011, 25 :1250–1253. DOI:10.1002/ptr.v25.8 |
| [7] | Qin XL, Bi HC, Wang XD, et al. Mechanistic understanding of the different effects of Wuzhi Tablet (Schisandra sphenan-thera extract) on the absorption and first-pass intestinal and hepatic metabolism of tacrolimus (FK506)[J]. Int J Pharm , 2010, 389 :114–121. DOI:10.1016/j.ijpharm.2010.01.025 |
| [8] | Qin XL, Yu T, Li LJ, et al. Effect of long-term co-admini-stration of Wuzhi tablet (Schisandra sphenanthera extract) and prednisone on the pharmacokinetics of tacrolimus[J]. Phytomedicine , 2013, 20 :375–379. DOI:10.1016/j.phymed.2012.11.008 |
| [9] | Xue XP, Qin XL, Xu C, et al. Effect of Wuzhi tablet (Schisandra sphenanthera extract) on the pharmacokinetics of cyclosporin A in rats[J]. Phytother Res , 2013, 27 :1255–1259. DOI:10.1002/ptr.v27.8 |
| [10] | Deng Y, Bi HC, Zhao LZ, et al. Induction of cytochrome P450s by terpene trilactones and flavonoids of the Ginkgo biloba extract EGb 761 in rats[J]. Xenobiotica , 2008, 38 :465–481. DOI:10.1080/00498250701883233 |
| [11] | Chow EC, Maeng HJ, Liu S, et al. 1alpha,25-Dihydroxyvi-tamin D(3) triggered vitamin D receptor and farnesoid X receptor-like effects in rat intestine and liver in vivo[J]. Biopharm Drug Dispos , 2009, 30 :457–475. DOI:10.1002/bdd.v30:8 |
| [12] | Xue X, Huang M, Xiao H, et al. Rapid and simultaneous measurement of midazolam, 1'-hydroxymidazolam and digoxin by liquid chromatography/tandem mass spectrometry: application to an in vivo study to simultaneously measure P-glycoprotein and cytochrome P450 3A activity[J]. J Pharm Biomed Anal , 2011, 55 :187–193. DOI:10.1016/j.jpba.2011.01.018 |
| [13] | Kalra BS. Cytochrome P450 enzyme isoforms and their therapeutic implications: an update[J]. Indian J Med Sci , 2007, 61 :102–116. DOI:10.4103/0019-5359.30351 |
| [14] | Takara K, Ohnishi N, Horibe S, et al. Expression profiles of drug-metabolizing enzyme CYP3A and drug efflux transporter multidrug resistance 1 subfamily mRNAS in small intestine[J]. Drug Metab Dispos , 2003, 31 :1235–1239. DOI:10.1124/dmd.31.10.1235 |
| [15] | Danan G, Descatoire V, Pessayre D. Self-induction by erythromycin of its own transformation into a metabolite forming an inactive complex with reduced cytochrome P-450[J]. J Pharmacol Exp Ther , 1981, 218 :509–514. |
| [16] | Zhang X, Galinsky RE, Kimura RE, et al. Inhibition of CYP3A by erythromycin: in vitro-in vivo correlation in rats[J]. Drug Metab Dispos , 2010, 38 :61–72. DOI:10.1124/dmd.109.028290 |
| [17] | Watkins PB, Wrighton SA, Maurel P, et al. Identification of an inducible form of cytochrome P-450 in human liver[J]. Proc Natl Acad Sci USA , 1985, 82 :6310–6314. DOI:10.1073/pnas.82.18.6310 |
| [18] | Wrighton SA, Maurel P, Schuetz EG, et al. Identification of the cytochrome P-450 induced by macrolide antibiotics in rat liver as the glucocorticoid responsive cytochrome P-450p[J]. Biochemistry , 1985, 24 :2171–2178. DOI:10.1021/bi00330a010 |
| [19] | Shi SY, Jin KT, Wang YG, et al. Inhibitory effect of aconitum coadministration with ampelopsis on cytochrome P450 in rat livers[J]. Her Med (医药导报) , 2007, 26 :975–979. |
 2016, Vol. 51
2016, Vol. 51


