2. 中国药科大学中药学院, 江苏南京 210009
2. School of Traditional Chinese Pharmacy, China Pharmaceutical University, Nanjing 210009, China
他喷他多 (tapentadol,图 1A) 是一种新型双重作用方式的强中枢性镇痛药。100~200 mg剂量的他喷他多镇痛作用相当于60 mg的吗啡。在相同镇痛效能的情况下,他喷他多引起的不良反应发生率低于吗啡[1]。盐酸他喷他多已于2008年1月被美国食品与药品监督管理局批准上市,用于中重度急性疼痛的治疗。他喷他多口服生物利用度约为32%[2],在体循环中主要药物相关物质为葡糖醛酸结合物 (图 1B) 和硫酸结合物 (图 1C),结合型代谢物的血浆浓度约为原形药物的24倍[3]。
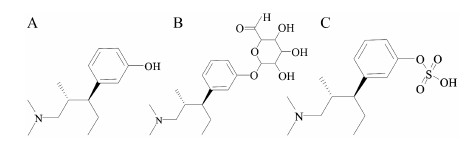 | Figure 1 Chemical structures of tapentadol (A), tapentadol glucuronide (B), tapentadol sulfate (C) |
已有文献[4, 5, 6, 7, 8, 9]报道采用液相色谱-串联质谱 (LC- MS/MS) 法、液相色谱-荧光检测 (HPLC-FL) 法测定血浆中他喷他多,但这些报道的方法并未考虑结合型代谢物对原形药物测定的影响,特别是当采用质谱作为检测器时,结合型代谢物常常发生源内裂解,而影响原形药物的测定[10, 11, 12]。最近的文献[7]报道采用LC-MS/MS法以不同的色谱条件分别测定人血浆中他喷他多和其葡糖醛酸结合物,在对他喷他多进行测定时,文献中也并未考虑结合型代谢物对测定的影响。
本文旨在建立快速灵敏的液相色谱-串联质谱法测定犬血浆中他喷他多,并评价结合型代谢物对原形药物测定的影响。
材料与方法 药品和试剂盐酸他喷他多对照品 (含量100%,批号S021314131128) 购于加拿大TRC公司; 盐酸曲马多对照品 (含量99.2%,批号050101) 由哈尔滨三联药业提供; 他喷他多缓释片 (规格: 每片250 mg,批号: 109E16) 由美国Janssen Pharmaceutical公司生产; 甲醇 (德国Merck公司)、醋酸铵 (美国ROE公司)、氨水 (德国Fluka公司) 均为色谱纯; 去离子水由法国Millipore纯水仪制备。
仪器美国AB Sciex公司的Qtrap 5500型三重四极杆串联质谱仪; 配备电喷雾电离源 (ESI源) 和Analyst 1.5.2定量处理软件; 日本岛津公司的液相色谱系统,包括LC-30AD型输液泵,SIL-30AC型自动进样器和CTO-30A柱温箱。
色谱条件分析柱: XDB C18色谱柱 (50 mm × 4.6 mm,1.8 μm,美国Agilent公司); 预柱: C18保护柱 (4.0 mm × 3.0 mm,美国Phenomenex公司); 流动相: 含0.01% 氨水的5 mmol·L-1醋酸铵-甲醇 (30∶70); 流速: 0.5 mL·min-1; 柱温: 室温; 进样量: 10 μL。
质谱条件离子源为电喷雾电离源 (ESI源); 正离子模式检测; 源喷射电压为4.5 kV; 离子源温度为500 ℃; 离子源气体1 (N2) 压力为50 psi (1 psi ≈ 6.9 kPa); 离子源气体2 (N2) 压力为50 psi; 气帘气体 (N2) 压力为30 psi; 扫描方式为多反应监测; 碰撞气压力为Medium; 扫描时间为150 ms; 各待测物的离子反应分别为: m/z 222 → m/z 121 (他喷他多) 和m/z 264 → m/z 58 (内标曲马多)。
标准系列样品和质控样品的制备精密称取盐酸他喷他多两份,一份用于标准系列样品的制备,另一份用于质控样品的制备。分别以甲醇溶解并定容,获得质量浓度约为1.00 mg·mL-1的储备液 (按碱基计算),以犬空白血浆稀释储备液,获得标准系列样品和质量控制 (QC) 样品。他喷他多标准系列样品质 量浓度分别为0.100、0.200、0.500、1.00、2.00、5.00、10.0和20.0 ng·mL-1。他喷他多QC样品的血浆质量浓度分别为0.100 ng·mL-1 (定量下限)、0.300 ng·mL-1 (低浓度)、1.50 ng·mL-1 (中浓度) 和16.0 ng·mL-1 (高浓度)。
血浆样品预处理取血浆样品25.0 μL,置1.5 mL离心管中。分别加入内标溶液 (2.00 ng·mL-1曲马多,以甲醇-水配制) 25.0 μL和甲醇100 μL,涡流混合1 min,离心5 min (11 000 r·min-1)。取上清液100 μL加入5 mmol·L-1醋酸铵水溶液 (含0.01%氨水) 100 μL,涡流混匀,吸取10.0 μL进行LC-MS/MS分析。
实验动物及给药方案健康雄性比格犬8只 (合格证号: 200700400381; 由上海交通大学农学院教学实验实习场提供),年龄7~8个月,体重8~11 kg。灌胃给予每片250 mg的盐酸他喷他多缓释片。在给药前及给药后0.25、0.5、1.0、1.5、2.0、2.5、3.0、4.0、6.0、8.0、10、12、14和24 h采集静脉血0.6 mL于EDTA抗凝管中,立即在3 500 r·min-1下离心10 min,获得的血浆样品于 -20 ℃冷冻保存。采用Phoenix WinNonlin 6.3软件以非房室模型法计算各待测物的药动学参数。
结 果 1 质谱分析他喷他多结构中含有碱性氮原子,质谱电离时易获得质子,因此优先选择正离子检测方式。在正离子检测模式下,他喷他多及内标曲马多主要生成 [M+H]+ 峰,质荷比分别为m/z 222和m/z 264。选择性对 [M+H]+ 峰进行产物离子扫描分析,生成的主要碎片离子分别为m/z 121和m/z 58,作为他喷他多和内标定量分析时监测的产物离子。在此基础上,对碰撞能量和去簇电压进行优化。
2 方法学验证 2.1 选择性
取6个不同来源的犬空白血浆样品以及相应空白血浆配制的LLOQ样品进行LC-MS/MS分析。与空白对照对比,空白血浆中的内源性物质不干扰他喷他多及内标曲马多的测定。典型色谱图见 图 2。
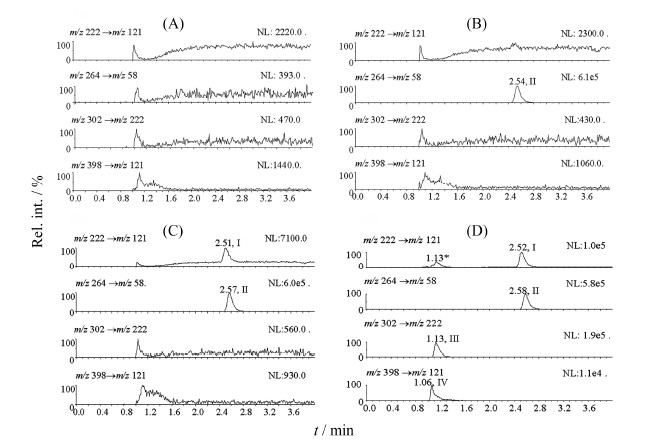 | Figure 2 Typical MRM chromatograms of tapentadol (I), tramadol (II), tapentadol sulfate (III) and tapentadol glucuronide (IV) in Beagle dog plasma. A: Blank plasma; B: Blank plasma spiked with 2.00 ng·mL-1 tramadol; C: Blank plasma spiked with 0.100 ng·mL-1 tapentadol and 2.00 ng·mL-1 tramadol; D: A plasma sample from a Beagle dog 3 h after an oral administration of 250 mg tapentadol sustained release tablet. In-source fragmentation of the conjugated metabolites |
他喷他多标准系列样品按“血浆样品预处理”项下操作,以每个待测物浓度为横坐标,待测物与内标物的峰面积比值为纵坐标,用加权 (W = 1/x2) 最小二乘法进行回归运算,求得的标准曲线的相关系数 (r2) 均大于0.99。测定他喷他多的线性范围为0.100~20.0 ng·mL-1,典型回归方程为: y = 0.252 x - 0.000 534 (r = 0.9986)
2.3 定量下限取LLOQ血浆样品,进行6样本分析,连续测定3天,并根据当日标准曲线计算每一样本测得浓度。求得该浓度他喷他多的日内精密度为4.2%,日间精密度为4.2%,准确度为 -4.0%; 结果表明,LC-MS/MS法测定比格犬血浆样品中他喷他多的定量下限可达0.100 ng·mL-1。
2.4 精密度与准确度取低、中、高3个浓度 (他喷他多血浆样品质量浓度分别为0.300、1.50和16.0 ng·mL-1) 的质控样品,按“血浆样品预处理”项下操作,每一浓度进行6样本分析,测定3天。根据当日的标准曲线,计算QC样品的测得浓度,根据QC样品结果计算本方法的准确度与精密度,数据见表 1。每一浓度水平他喷他多的QC样品的日内精密度 (RSD) 均小于3.4%,日间精密度 (RSD) 均小于5.1%,准确度 (RE) 在-3.2%~0 之间。待测物低、中、高质控样品的日内和日间的精密度和准确度均符合生物样品测定相关要求[13, 14, 15]。
|
|
Table 1 The intra- and inter-day precision and accuracy data of the QC samples of tapentadol (n = 18) |
取低、中、高3个浓度质控样品按“血浆样品预处理”项下操作,每一浓度进行6样本分析。同时另取犬空白血浆25.0 μL,除不加内标溶液外,按“血浆样品预处理”项下操作,取全部上清 液,加入相应浓度对照质控溶液和内标溶液,涡流混匀后进样分析。以每一浓度两种处理方法的峰面积比计算处理回收率,他喷他多在3种浓度下样品的提取回收率分别为85.8%、91.3% 和82.7%。内标曲马多同样经提取处理,其提取回收率为90.0%。待测物及其内标回收率的RSD均小于6.0%,提取回收率重现性好。
2.6 基质效应取6个犬空白血浆及1份溶血空白血浆25.0 μL,除不加内标溶液外,按“血浆样品预处理”项下操作,取全部上清液,加入相应浓度对照质控溶液和内标溶液,涡流混匀后进样分析。同时另取25.0 μL水代替空白血浆,按上述处理。以两种处理方法的峰面积比值计算基质效应。他喷他多低、高两浓度经内标校正的基质效应分别为97.2% 和97.5%,相对标准差均小于2.1%。因此,在本实验选择的色谱和质谱条件下,可忽略基质效应对他喷他多测定的影响。
2.7 稳定性考察了他喷他多低、高两浓度分别为0.300和16.0 ng·mL-1的血浆样品在不同储存条件下的稳定性。结果表明,犬血浆样品室温放置6 h,准确度在 -11.3%~-0.5% 之间; 预处理后的血浆样品4 ℃放置48 h,准确度在2.9%~6.4% 之间; 血浆样品经历3次冷冻-解冻循环,准确度在6.8%~9.5% 之间; 血浆样品 -20 ℃放置43天,准确度在 -4.0%~0.4% 之间。在上述条件下,他喷他多血浆样品均稳定。
3 比格犬药物动力学研究将经过完整方法学验证的方法应用于他喷他多缓释片的比格犬药动学研究。他喷他多单次给药后的血浆药物浓度-时间曲线见图 3。实验数据经WinNonlin 6.3软件处理计算。比格犬给予他喷他多缓释片250 mg后,他喷他多的血浆浓度达峰时间tmax为 (3.80 ± 2.00) h,达峰浓度Cmax为 (7.78 ± 4.16) ng·mL-1,血浆药物浓度-时间曲线下面积AUC0-t 为(72.4 ± 30.0) h·ng·mL-1,血浆消除半衰期t1/2为 (4.28 ± 1.06) h。
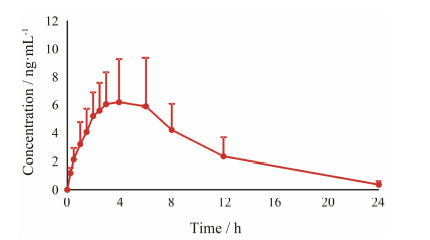 | Figure 3 Mean plasma concentration-time curve of tapentadol after a single oral dose of 250 mg sustained release tablet to Beagle dogs. n = 8,x±s |
本文通过优化流动相的有机相比例和pH值以及不同型号的色谱柱,实现他喷他多和结合型代谢物的色谱分离,整个色谱运行时间仅为4 min,成功避免了结合型代谢物因在离子源内裂解而对他喷他多测定的影响。
在样品储存过程中,结合型代谢物的稳定性可能也会影响原形药物的准确测定。由于缺乏结合型代谢物的对照品,本实验仅通过测定样品的原形药物在储存过程的稳定性来评价结合型代谢物的影响。结果提示,结合型代谢物在-20 ℃储存条件下稳定。
有文献[8]报道当给予犬2.00 mg·kg-1盐酸他喷他多后,原形药物的血浆达峰浓度为87 ng·mL-1,另有文献[9]报道给予犬8.00 mg·kg-1他喷他多缓释片,原形药物血浆达峰浓度约为2910 ng·mL-1,两者结果存在很大差异。本文比格犬给予每片250 mg的他喷他多缓释片 (约相当于23~31 mg·kg-1),测得他喷他多Cmax仅为7.78 ng·mL-1,远低于文献报道值。虽然有制剂因素的影响,但由于色谱未分离而导致结合型代谢物对测定的影响可能是主要因素。
结 论本文建立了灵敏、快速的液相色谱-串联质谱法测定犬血浆中的他喷他多,色谱运行时间短,显著提高了分析通量。方法验证结果表明本方法准确可靠,并成功应用于他喷他多缓释片药物动力学研究。本文也考察了结合型代谢物对他喷他多测定的影响,通过优化色谱条件,实现了原形药物与结合型代谢物的色谱分离,避免了结合型代谢物由于源内裂解对待测物测定的影响。
| [1] | Kleinert R, Lange C, Steup A, et al. Single dose analgesic efficacy of tapentadol in postsurgical dental pain:the results of a randomized, double-blind, placebo-controlled study[J]. Anesth Analg, 2008, 107:2048-2055. |
| [2] | Tzschentke TM, De Vry J, Terlinden R, et al. Tapentadol hydrochloride[J]. Drug Future, 2006, 31:1053-1061. |
| [3] | Terlinden R, Ossig J, Fliegert F, et al. Absorption, metabolism, and excretion of 14C-labeled tapentadol HCl in healthy male subjects[J]. Eur J Drug Metab Pharmacokinet, 2007, 32:163-169. |
| [4] | Jin Y, Jiang X, Zhai N, et al. LC-MS/MS method for the determination of tapentadol in rats[J]. J Shenyang Pharm Univ (沈阳药科大学学报), 2012, 29:143-146. |
| [5] | Bourland JA, Collins AA, Chester SA, et al. Determination of tapentadol (Nucynta®) and N-desmethyltapentadol in authentic urine specimens by ultra-performance liquid chromatographytandem mass spectrometry[J]. J Anal Toxicol, 2010, 34:450-457. |
| [6] | Coulter C, Taruc M, Tuyay J, et al. Determination of tapentadol and its metabolite N-desmethyltapentadol in urine and oral fluid using liquid chromatography with tandem mass spectral detection[J]. J Anal Toxicol, 2010, 34:458-463. |
| [7] | Hillewaert V, Pusecker K, Sips L, et al. Determination of tapentadol and tapentadol-O-glucuronide in human serum samples by UPLC-MS/MS[J]. J Chromatogr B, 2015, 981:40-47. |
| [8] | Giorgi M, Meizler A, Mills PC. Quantification of tapentadol in canine plasma by HPLC with spectrofluorimetric detection:development and validation of a new methodology[J]. J Pharm Biomed, 2012, 67:148-153. |
| [9] | Giorgi M, Meizler A, Mills PC. Pharmacokinetics of the novel atypical opioid tapentadol following oral and intravenous administration in dogs[J]. Vet J, 2012, 194:309-313. |
| [10] | Gao R, Zhong D, Liu K, et al. Simultaneous determination of morinidazole, its N-oxide, sulfate, and diastereoisomeric N-glucuronides in human plasma by liquid chromatographytandem mass spectrometry[J]. J Chromatogr B, 2012, 908:52-58. |
| [11] | Yang Y, Yu J, Lu Y, et al. High-sensitivity liquid chromatography-tandem mass spectrometry method for the simultaneous determination of sodium picosulfate and its three major metabolites in human plasma[J]. J Chromatogr B, 2013, 915-916:1-7. |
| [12] | Jemal M, Ouyang Z, Xia Y. Systematic LC-MS/MS bioanalytical method development that incorporates plasma phospholipids risk avoidance, usage of incurred sample and well thought-out chromatography[J]. Biomed Chromatogr, 2010, 24:2-19. |
| [13] | US Food and Drug Administration. Guidance for Industry:Bioanalytical Method Validation (draft)[S/OL]. 2013. http://www.fda.gov/downloads/Drugs/GuidanceComplianceRegulatoryInformation/Guidances/UCM368107. |
| [14] | European Medicines Agency. Guideline on Bioanalytical Method Validation[S/OL]. 2011. http://www.ema.europa.eu/docs/en_GB/document_library/Scientific_guideline/2011/08/WC500109686.pdf. |
| [15] | Chinese Pharmacopoeia Commission. Pharmacopoeia of the the People's Republic of China (中华人民共和国药典)[M]. Vol II. 2010 ed. Beijing:China Medical Science, 2010:Appendix XIX B. |
 2016, Vol. 51
2016, Vol. 51


