2. 北京博之音科技有限公司, 北京 100068
2. Beijing Bozhiyin Technology Co. Ltd., Beijing 100068, China
自CFDA(2012) 颁布“临床试验数据管理工作技术指南”[1]以来,经过国家主导的大规模临床稽查,我国临床试验数据质量受到空前的重视。申办方、合同研究组织 (CRO)、研究者等充分认识电子化数据采集技术 (electronic data capture,EDC) 的重要性[2]。EDC已超出其电子数据采集单一功能定义,已被认为是电子化临床数据管理模式。FDA认为电子化临床是创新关键路径的重要工具之一,并有一系列技术指南[3]。本文以采用EDC数据管理的临床试验项目为例,展现EDC在临床试验数据质量控制中的优势特点。
资料与方法资料来源 采用DAS for EDC进行电子化数据管理的临床试验项目为调查对象,本系统具备轨迹管理功能,保留了数据管理的过程记录。本次选取2012~2014年的20个注册类临床试验项目,对EDC记录的逻辑核查和数据疑问状态进行分类统计。总样本量为5 404例,321个研究中心,包括化药、中药和生物制品的I~III期临床试验项目。
逻辑核查方法 EDC的电子病例报告表 (eCRF) 设计构建除了完成方案要求采集的字段设置,同时对字段本身、以及字段之间的有效性范围、逻辑关系进行逻辑核查 (edit check) 设置。逻辑核查设置依据为数据核查计划 (DVP),DVP由数据管理员 (DM) 根据方案撰写,并通过申办方和研究者审阅通过。本文统计的逻辑核查指由EDC自动进行的核查,来源于DAS for EDC系统记录。不包括人工核查,人工核查指eCRF中的文本数据等系统不能自动核查内容,由数据管理员人工审核。
数据疑问产生方法 逻辑核查设置完成后,EDC在数据采集同时进行数据核查,数据清理与临床试验同步进行,数据疑问和疑问解答伴随着临床试验全过程不断循环。临床试验过程中,EDC显示的数据疑问处于动态更新中,直到全部疑问解决,数据为“清洁”状态。在所调查的20个临床试验项目中,整理已结束的10个项目的疑问数据,来源于DAS for EDC疑问表记录的最终数据疑问状态,即数据锁定时已解决的全部疑问情况。包括系统疑问和人工疑 问,系统疑问由EDC内置的逻辑核查自动触发; 人工疑问为数据管理员数据核查时发出的疑问,主要是一致性和逻辑性问题; 临床监查员 (CRA) 现场核查 (SDV) 时发出的疑问,主要是真实性和准确性问题。
参数统计方法 本文统计的字段数、逻辑核查数以单个受试者为单位。同适应证的参数合并计算平 均数。字段数为一份eCRF的所有访视期变量合计,如人口学的性别、年龄、身高、体重等,实验检查的ALT、AST等,如果同一字段在5个访视期均有采集,则按5个字段计数。
逻辑核查为一份eCRF的逻辑核查合计,如同一字段在5个访视期均有采集,并且逻辑关系相同,EDC设置1条核查,适用5个访视期,则按1条核查计数。疑问按每份eCRF字段对应的数据点产生疑问计数,如同一字段在5个访视期均有采集,则对应有5个数据点,如有3个数据点产生疑问,则按3条疑问计数。逻辑核查和疑问数包含筛选期、治疗期和随访期。
结果 1 项目特征20个临床试验项目,涵盖14个适应症,包括化学药品10个,中药5个,生物制品5个,其中注册分类1类的7个项目。总样本量为5 404例,321个研 究中心,EDC角色用户包括研究者 (PI)、研究助理 (CRC)、数据管理员、临床监查员 (CRA)、医学审核 (MR),共计1 201人,平均每个项目投入60人 (表 1)。
|
|
表 1 20个临床试验项目特征 |
其中10个已结束的临床试验项目,涵盖8个适应症,其中化学药品6个,中药1个,生物制品3个,总样本量3 164例,187个研究中心,EDC各类角色用户819人,平均每个项目投入82人 (表 2)。
|
|
表 2 10个已完成临床试验项目特征 |
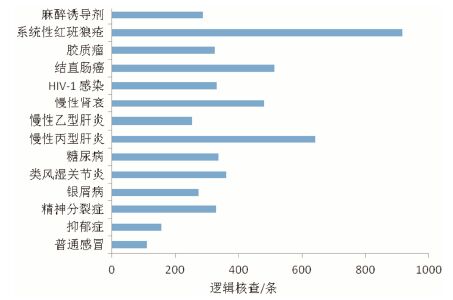
EDC逻辑核查可自动筛查数据疑问,20个临床试验项目字段数共37 518个,平均1 876个/项目,共设置逻辑核查7 242条,平均362条/项目。逻辑核查与项目复杂程度有关,不同适应证差异较大,如系统性红斑狼疮,逻辑核查为916条,普通感冒逻辑核查为110条,麻醉诱导剂临床试验观察期仅24 h,逻辑核查287条 (图 1)。
|
图 1 20个项目平均逻辑核查对比 |
10个已结束项目的样本量共3 164例,23 181个字段,共产生疑问160 319条,受试者疑问发生率为50.7条/例,肿瘤项目的疑问率明显高于一般项目,如晚期结直肠癌的平均每例受试者疑问数为175.4条; 平均每字段的疑问数为6.9条 (表 3)。
|
|
表 3 逻辑核查与疑问数 |
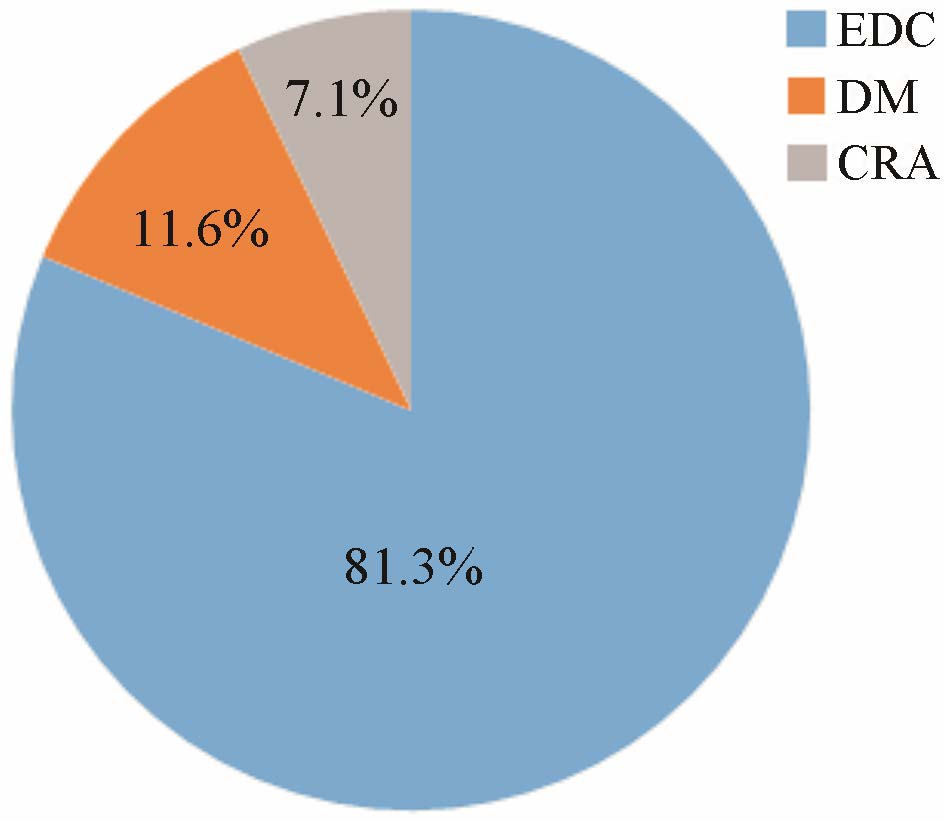
10个项目EDC设置的逻辑核查3 866条,共筛查疑问130 267条 (表 4),平均每条逻辑核查可筛查疑问33.7条,EDC自动筛查疑问率至少为64%,最高为93.8%,平均疑问率为81.3%,其中空值疑问占52.6%,人工疑问大幅减少,数据管理员和CRA的人工疑问分别为11.6% 和7.1% (图 2)。
|
|
表 4 各项目疑问来源比较 |
|
图 2 项目疑问来源构成图 |
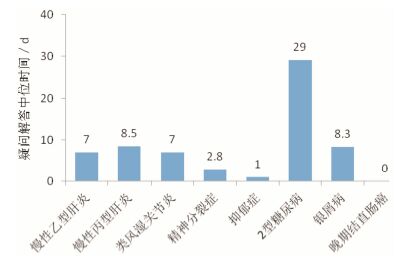
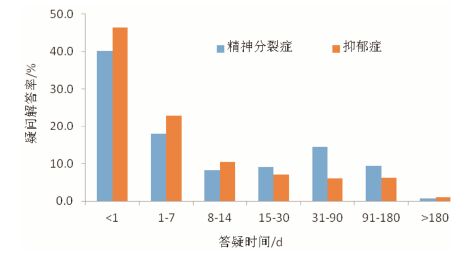
所有项目的疑问解答最短时间均为0天,即疑问产生当天解答,疑问解答最长时间为662天,疑问解答的中位时间最长为29天,最短为0天 (图 3),除糖尿病项目以外,中位答疑时间均在10天以内。通过对2个精神类药物项目疑问解答时间分析,显示40% 以上疑问均可在当天解答,2周内的解答率分别66.3% 和79.6%,超过90天的解答率均在10%以内 (图 4),疑问解答时间长短反映最终数据的可靠性准确性程度,疑问越早解决,核实和修正数据的工作量越小,数据可靠性越强,准确性越高。
|
图 3 各项目疑问解答中位时间比较 |
|
图 4 精神类药物项目疑问解答时间分布图 |
EDC实现了数据采集、数据清理与临床试验同步进行,避免了传统数据管理模式的滞后性,缩短研发周期。通过EDC采集数据,控制了自由写入,可提高数据写入质量,CRA现场SDV发送疑问比例下降,可以将精力更多投入临床监查。临床试验数量大,各变量间逻辑关系错综复杂,如普通感冒项目,疗程5天,逻辑关系有110条,人工筛查难免有疏漏,复杂项目更如此。本文所调查项目的EDC逻辑核查,平均筛查81.3%的疑问,糖尿病项目EDC筛查了93.8%的疑问,大大减轻人力投入,节约人员成本。EDC逻辑核查与项目的数据类型有关,文本类型比重大,人工核查比例会上升,反之,EDC逻辑核查比例上升,人工核查比例下降。在EDC基础上,设计合理的CRF,规范使用EDC可以避免不必要的疑问产生。
本文研究项目的答疑时间显示临床研究者答疑及时,对EDC的依从性较好,本文计算的答疑时间是从数据录入EDC产生疑问到疑问解答的时间,未考察数据录入的及时性,较每次访视而言,如果EDC数据录入滞后,尽管录入后及时答疑,仍然会存在真正滞后性带来的问题。
EDC作为临床试验的技术工具,可为临床试验数据质量提供强大支持,正因为EDC的发展和强大功能,FDA提出了基于风险的临床监查[4],由以往的现场监查 (on-site monitoring) 为主的模式向集中化监查 (centralized monitoring) 转变,这种模式也是普遍基于EDC前提下。CFDA也颁布相关指南[1],鼓励国内制药企业和CRO采用EDC模式的数据管理。EDC不是单纯的计算机技术,软硬件、网络设备、运行环境、规范流程、专业人员和培训都是EDC成功应用不可缺少的条件。
| [1] | Center of Drug Evaluation, CFDA. Technical Guidelines for Data Management in Clinical Trials (临床试验数据管理 工作技术指南) [S]. 2012. [06].http://www.cde. org.cn/news.do?method=largeInfo&id=312673. |
| [2] | Deng YZ, Yu J, Liu C, et al. Current status and trend of clinical data management at electronization time [J]. Chin J New Drugs (中国新药杂志), 2014, 23: 879−884. |
| [3] | FDA. Guidance for Industry: Computerized Systems Used in Clinical Investigations [EB/OL]. 2007. [06].http:// www.fda.gov/downloads/Drugs/GuidanceComplianceRegulatoryInformation/Guidances/UCM070266.pdf. |
| [4] | FDA. Guidance for Industry Oversight of Clinical Investigations: A Risk-Based Approach to Monitoring[EB/OL]. . 2013. [08]http://www.fda.gov/Drugs/GuidanceCompliance RegulatoryInformation/Guidances/default.htm. |
 2015, Vol. 50
2015, Vol. 50


