2. 香港大学李嘉诚医学院艾滋病研究所, 香港;
3. 清华大学医学院药学系, 北京 100084
2. AIDS Institute, Li Ka Shing Faculty of Medicine, The University of Hong Kong, Hong Kong, China;
3. Department of Pharmacology and Pharmaceutical Sciences, School of Medicine, Tsinghua University, Beijing 100084, China
HIV逆转录酶 (reverse transcriptase, RT) 在人类免疫缺陷病毒 (human immunodeficiency virus, HIV) 的复制过程中起着关键的作用, 已经成为抗HIV/ AIDS药物发展中的重要生物靶点。目前, 临床使用的HIV RT抑制剂分为两大类: 核苷类逆转录酶抑制剂 (NRTIs) 和非核苷类逆转录酶抑制剂 (NNRTIs)。NNRTIs可以与HIV-1逆转录酶直接结合形成稳定的复合物, 使酶的构象发生改变, 从而抑制酶的活性, 具有作用靶点明确、作用机制清楚、结构多样、高效、低毒以及可与其他药物协同作用等特点。NNRTIs已经成为抗HIV-1感染的首选药物, 包括: 奈韦拉平 (nevirapine, NVP)、地拉韦啶 (delavirdine, DLV)、依非韦伦 (efavirenz, EFV)、依曲韦林 (etravirine, TMC- 125) 和利匹韦林 (rilpivirine, TMC278) 等。然而, 该类药物存在严重的毒副作用以及具有低耐药基因屏蔽和高交叉耐药的特性, 现有的NNRTIs仍然不能满足临床治疗的需求。与其他逆转录酶不同, HIV-1逆转录酶即使出现单点突变也会引起严重的NNRTIs耐药性, 很多HIV感染者都有过NNRTIs治疗失败的经历[1, 2, 3] 。
(+)-Calanolide A是从藤黄科红厚壳属植物中提取分离得到的吡喃型香豆素类化合物,是最早发现的具有抗HIV-1活性的天然产物之一,并在1996年被证实为HIV-1的RT抑制剂,尤其是可以抑制目前临床最常见的K103N和Y181C等两个耐药病毒株的特点,使其具有临床研究的价值[4, 5]。但 (+)-calanolide A本身开发为药物具有一些缺点,比如治疗指数 (TI) 较低、天然来源难以满足药物开发的需求、以及存在3个手性碳原子致使合成困难等。从20世纪90年 代起,本课题组开始致力于 (+)-calanolide A及其类似物的结构修饰和全合成研究,并取得了积极的进展[6, 7, 8, 9, 10, 11, 12, 13, 14]。研究结果显示 (±)-F18 (10-chloromethyl-11- demethyl-12-oxo-calanolide A) 比天然 (+)-calanolide A少两个手性中心,但其体外抗HIV-1活性 (EC50 = 7.4 nmol·L-1) 及治疗指数 (TI= 1 417) 均优于天然 (+)-calanolide A[11, 13, 14]。体外药效学实验证实 (±)-F18的抗HIV-1活性与奈韦拉平相当[13]。(±)-F18对临床主要耐药病毒株Y181C具有极高的抑制作用,EC50值为0.46 nmol·L-1。目前该化合物已经完成了临床前研究。 (±)-F18的结构中含有1个手性中心 (图 1),为探讨其光学异构体的抗HIV-1活性,本文采用制备型手性HPLC拆分并制备了 (R)-F18及 (S)-F18。两个对映异构体通常会表现出不同甚至相反的生物活性,因此,对 (R)-F18及 (S)-F18分别进行活性评价可为临床研究提供指导作用。
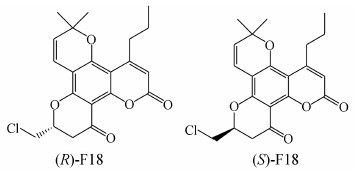
|
Figure 1 Chemical structures of (R)-F18 and (S)-F18 |
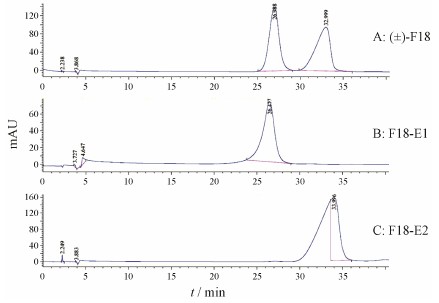
本文建立了消旋 (±)-F18手性高效液相色谱分离的方法。使用Sino-Chiral AD色谱柱 (10 mm × 250 mm, 5 μm), 以正己烷−异丙醇 (90∶10, v/v) 为流动相, 流速为5 mL·min−1, 检测波长为254 nm, 柱温为室温。如图 2所示, 所建立的方法能将两个对映异构体在40 min内手性分离, 其对映体的保留时间分别为26.9和32.9 min。分离得到的两个光学异构体最初分别命名为F18-E1和F18-E2, 测定二者的比旋度分别为: [α]D = +64.3 (F18-E1, 纯度97.4%); [α]D = −69.0 (F18-E2, 纯度98.9%)。
|
Figure 2 Chromatograms of F18 enantiomers |
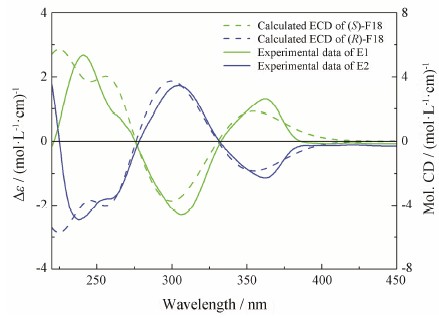
采用量化计算预测手性化合物的圆二色谱 (circular dichroism, CD), 并与实验图谱比较, 是解析CD图谱确定手性化合物绝对构型的常用方法[15, 16, 17]。本文测试F18-E1和F18-E2的CD结果显示 (图 3), F18-E1 (绿色实线) 和F18-E2 (蓝色实线) 的CD图谱呈现对映关系, 说明两者为一对光学对映异构体。理论计算结果显示, F18-E1的实验图谱与 (S)-F18 (绿色虚线) 的理论CD图谱相符, 推测其手性中心的绝对构型为S (图 3); 同理推断F18-E2的构型为R。
|
Figure 3 Comparison ofexperimental and calculated ECD spectra of chiral F18 in dichloromethane |
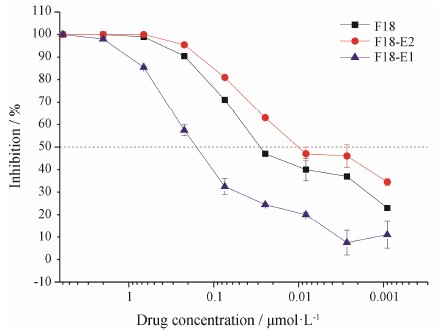
基于细胞水平评价抗HIV-1病毒活性的方法包括活病毒法和重组假病毒法。重组假病毒法与活病 毒法相比, 具有重复性好、灵敏、易操作、无生物危害的特点, 并且还可以定量计算出药物的EC50值[18]。本文采用重组假病毒法建立了细胞水平的抗HIV-1药物评价模型[19], 应用该模型测定了 (±)-F18以及阳性对照奈韦拉平 (NVP) 对野生型病毒株的EC50值分别为0.027和0.037 µmol·L−1。应用该模型进一步测定了 (R)-F18和 (S)-F18对野生型病毒株以及17个NNRTIs耐药株假病毒的抗病毒活性。结果显示 (表 1), 二者对17个NNRTIs耐药病毒株具有相似的耐 药谱。(R)-F18和 (S)-F18均能有效地抑制V179D、Y181C和K103N/P225H耐药病毒株, 对Y188L/H、K103N/Y181C和V106A/G190A/F227L耐药病毒株亦同时显示出耐药性。但是二者对17个NNRTIs耐药病毒株的抗病毒活性存在显著的区别。其中, (R)-F18对于野生型病毒株 (图 4) 以及K101E和P225H耐 药株的抗病毒活性均高于 (S)-F18近10倍。(S)-F18除了对K103N/Y181C/G190A耐药株活性较 (R)-F18高近2倍外, 对其他的耐药株活性均比 (R)-F18低2~6倍。
|
Figure 4 Antiviral efficacies of (±)-F18, (S)-F18 and (R)-F18 against pNL4-3 WT virus |
|
|
Table 1 In vitro antiviral activities of (±)-F18, (S)-F18, (R)-F18 against HIV-1 NNRTI-resistant pseudovirus in GHOST (3)-CCR5 cell line. aEC50, 50% effective concentration, obtained from individual data sets fit to a sigmoidal, dose-response curve by nonlinear regression using the Prism program (Graphpad Software 5) |
本文建立了高效液相色谱分离外消旋 (±)-F18的方法, 并分离得到两个对映异构体。应用圆二色谱技术和量化计算方法确定了两个对映异构体的绝对构型分别为 (R)-F18和 (S)-F18。抗病毒活性研究表明: (S)-F18和 (R)-F18对17个NNRTIs的耐药病毒株有相似的耐药谱, 但二者对不同的NNRTIs耐药病毒 株活性不同。其中, 对于野生型病毒株、K101E和P225H耐药株, (R)-F18较 (S)-F18的抗病毒活性高近10倍; (S)-F18除了对K103N/Y181C/G190A耐药株活性较 (R)-F18高近2倍外, 对其他的耐药株活性均比 (R)-F18低2~6倍。
实验部分 1 材料和试剂F18, 自制, 纯度为99.1%, 通过红外光谱、核磁共振氢谱和碳谱、质谱、X-射线衍射、元素分析对其结构进行了确证。异丙醇和正己烷为色谱纯, 其他试剂均为分析纯。
2 F18光学异构体的分离Agilent 1100高效液相色谱仪 (安捷伦科技有限公司), 配有在线脱气机、二元梯度泵、自动进样器、柱温箱、二极管阵列检测器和HP1100化学工作站。色谱柱: Sino-Chiral AD色谱柱 (10 mm × 250 mm, 5 μm), 购自分水 (北京) 科技有限公司; 流动相: 正己烷−异丙醇 (90∶10, v/v); 流速: 5 mL·min−1; 检测波长: 254 nm; 进样量: 90 μL; 柱温: 室温。
3 F18对映体绝对构型确定CD测定条件: 溶剂为二氯甲烷; 浓度为0.125 mg·mL−1; 扫描测定波长为220~450 nm。仪器: 日本JASCO J-815圆二色光谱仪 (Jasco Inc., Japan)。
4 抗病毒活性测定实验材料: HEK 293T细胞由美国洛克菲勒大 学和艾伦戴蒙德艾滋病研究中心 (ADARC) 馈赠。GHOST (3)-CCR5细胞由美国NIH AIDS Research and Reference Reagent Program提供。QuikChange® II XL定点突变试剂盒购自Stratagene公司 (La Jolla, CA, USA)。转染试剂Polyethylenimine [PEI]购自Polysciences公司 (Warrington, PA, USA)。荧光素酶试剂购自Promega公司 (Promega, Madison, WI, USA)。消旋F18由本课题组合成, 纯度大于99%。Inspire Victor 3多标记酶标仪1420 (Perkin Elmer, Waltham, MA, USA)。
逆转录酶区域NNRTI耐药位点定点突变: 该区域所有耐药位点的定点突变都是在pNL4-3Luc+Env−Vpr− (pNL4-3R−E−Luc+) 分子克隆的基础上用QuikChange® II XL定点突变试剂盒 (Stratagene, La Jolla, CA, USA) 做定点突变。耐药位点的选择都是依据目前临床上NNRTI治疗时较流行的单一或多重耐药位点。
假病毒的制备: pNL4-3R−E−Luc+分子克隆在env和vpr基因上都分别含有移码突变, 因此在病毒制备时不能表达Env和Vpr两个蛋白。同时, 在nef基因上同时插入萤火虫荧光素酶基因。在病毒制备过程中, 用此种克隆与含有env的克隆共转染至细胞, 可以制备出只可感染一次的假病毒。假病毒感染相应细胞 后, 用荧光素酶试剂通过测定细胞内荧光素酶活性来确定病毒制备效率和滴度。野生型或含NNRTI耐药位点的pNL4-3R−E−Luc+克隆与HIV-1ADA克隆用转染试剂polyethylenimine [PEI] 共转至293T细胞中。转染48 h后, 收取上清液, 离心去掉细胞残渣, 分装, −80 ℃保存。
药物抗病毒活性的测定: 抗病毒活性试验的前一天, 将GHOST(3)-CCR5细胞100 μL (含1×104个细胞) 铺至96孔板。第二天, 分别将200 TCID50的病毒和3倍梯度稀释的F18、F18-E1、F18-E2 (起始浓度为6 μmol·L−1) 加入细胞中, 培养终体积为200 μL。同时设置无药孔和无病毒/药孔为对照。细胞感染48 h后, 加入荧光素酶试剂, 用 Inspire Victor 3多标记酶标仪1420测定每个孔的发光值RLU。采用公式 (无药孔RLU−有药孔RLU) / (无药孔RLU−无病毒/药孔RLU) ×100% 计算药物的病毒抑制率。通过GraphPad Prism software 5.0软件 (GraphPad Software Inc., La Jolla, CA) 计算药物抗病毒活性的EC50值。
| [1] | Corbett JW, Ko SS, Rodgers JD, et al. Expanded-spectrum nonnucleoside reverse transcriptase inhibitors inhibit clinically relevant mutant variants of human immunodeficiency virus type 1 [J]. Antimicrob Agents Chemother, 1999, 43: 2893-2897. |
| [2] | Wishka DKG, Graber DR, Kopta LA, et al. (-)-6-Chloro 2-[(1-furo[2, 3-c] pyridine-5-yl-ethyl) thio]-4-pyrimidinamine, PNU-142721, a new broad spectrum HIV-1 non-nuleoside reverse transcriptase inhibitor [J]. Antimicrob Agents Chemother, 2001, 45: 1379-1386. |
| [3] | Adams J, Patel N, Mankaryous N, et al. Nonnucleoside reverse transcriptase inhibitor resistance and the role of the second-generation agents [J]. Ann Pharmacother, 2010, 44: 157-165. |
| [4] | Kashman Y, Gustafson KR, Fuller RW, et al. The calanolides, a novel HIV-inhibitory class of coumarin derivatives from the tropical rainforest tree, Calophyllum lanigerum [J]. J Med Chem, 1992, 35: 2735-2743. |
| [5] | Quan Y, Motakis D, Buckheit R Jr, et al. Sensitivity and resistance to (+)-calanolide A of wild-type and mutated forms of HIV-1 reverse transcriptase [J]. Antivir Ther, 1999, 4: 203-209. |
| [6] | Zhou CM, Wang L, Zhang ML, et al. Synthesis and anti-HIV activity of (±)-calanolide A and its analogues [J]. Acta Pharm Sin (药学学报), 1999, 34: 673-678. |
| [7] | Gao Q, Wang L, Liang XT. Total synthesis of (±)-cordatolide A and its anti-HIV activity [J]. Chin Chem Lett, 1999, 10: 653-656. |
| [8] | Wang L, Liu G, Gao Q, et al. The preparation of racemic and optically active calanolide A and its analogs: CN, 03123628.6 [P]. 2003-05-09. |
| [9] | Wang L, Chen HS, Tao PZ, et al. Improved synthesis and pharmacological evaluation of racemic 11-demethylcalanolide A [J]. Acta Pharm Sin (药学学报), 2008, 43: 707-718. |
| [10] | Ma T, Gao Q, Chen ZW, et al. Chemical resolution of (±)-calanolide A, (±)-cordatolide A and their 11-demethyl analogues [J]. Bioorg Med Chem Lett, 2008, 18: 1079-1083. |
| [11] | Ma T, Liu L, Xue H, et al. Chemical library and structure– activity relationships of 11-demethyl-12-oxo calanolide A analogues as anti-HIV-1 agents [J]. J Med Chem, 2008, 51: 1432-1446. |
| [12] | Liu G, Xue H, Ma T, et al. Tetracyclodipyano-coumarin compounds with anti-HIV and anti-Mycobacterium tubesculosis activities: PCT/CN2007/003139 [P]. 2007-11-05. |
| [13] | Xue H, Lu XF, Zheng PR, et al. Highly suppressing wild-type HIV-1 and Y181C mutant HIV-1 strains by 10-chloromethyl-11-demethyl-12-oxo-calanolide A with druggable profile [J]. J Med Chem, 2010, 53: 1397-1401. |
| [14] | Lu XF, Liu L, Zhang X, et al. F18, a novel small-molecule nonnucleoside reverse transcriptase inhibitor, inhibits HIV-1 replication using distinct binding motifs as demonstrated by resistance selection and docking analysis [J]. Antimicrob Agents Chemother, 2012, 56: 341-351. |
| [15] | Li L, Si YK. Study on the absolute configuration of levetiracetam via density functional theory calculations of electronic circular dichroism and optical rotatory dispersion [J]. J Pharm Biomed Anal, 2011, 56: 465-470. |
| [16] | Li L, Li C, Si YK, et al. Absolute configuration of buagafuran: an experimental and theoretical electronic circular dichroism study [J]. Chin Chem Lett, 2013, 24: 500-502. |
| [17] | Li L, Wang L, Si YK. Electronic circular dichroism behavior of chiral Phthiobuzone [J]. Acta Pharm Sin B, 2014, 4: 167-171. |
| [18] | Chong HH, Xu SH, Li JY, et al. Comparison between recombinant virus assay and live virus assay on evaluating anti-HIV-1 drugs [J]. Chin J Exp Clin Viral (中华实验和临床病毒学杂志), 2011, 25: 73-75. |
| [19] | Chen ZW, Zhou P, Ho DD, et al. Genetically divergent strains of simian immunodeficiency virus use CCR5 as a coreceptor for entry [J]. J Virol, 1997, 71: 2705-2714. |
 2015, Vol. 50
2015, Vol. 50


