2. Department of Anatomy and Neurobiology, Dalhousie University, Canada, 15000
2. Department of Anatomy and Neurobiology, Dalhousie University, Canada, 15000
糖尿病是由于胰岛素分泌绝对或相对不足而不能维持机体正常血糖水平引发的一组代谢紊乱疾 病[1]。1型和2型糖尿病的共同特征是胰岛β细胞的渐进性受损[2]。1型糖尿病以胰岛β细胞绝对缺乏为主要病理特征, 患者胰岛功能严重受损, 胰岛素的分泌绝对不足[1]; 2型糖尿病的重要标志是胰岛素抵抗和β细胞功能受损, 其中胰岛素抵抗被认为是2型糖尿病最根本的病理状态。然而, 除非β细胞受损同时发生, 单独胰岛素抵抗无法导致2型糖尿病的发生, 因为正常的胰岛β细胞能通过增加细胞数量及功能输出来代偿胰岛素抵抗[3]。2型糖尿病患者从肥胖、胰岛素抵抗到最终发生高糖血症的整个过程中, 一直伴随胰岛β细胞功能的变化, 初期为代偿性胰岛素分泌升高; 随着病程的加重, 后期胰岛β细胞功能失代偿, β细胞量减少, 糖代谢稳态被打乱, 血糖水平升高,最终导致2型糖尿病及其并发症的发生[4]。因此, β细胞功能障碍被认为在2型糖尿病发病进程中发挥主要作用。关于β细胞受损, 近年来越来越受到重视[5]。保护胰岛β细胞是治疗糖尿病的一个重要手段。
目前上市的胰岛β细胞保护药物主要针对分子靶点胰高血糖素样肽-1 (glucagon-like peptide-1, GLP-1), 包括GLP-1类似物 (利拉鲁肽、阿必鲁肽)、GLP-1受体激动剂 (艾塞那肽、利西拉来) 和DPP4抑制剂 (西格列汀、维达列汀、阿格列汀)[6]。
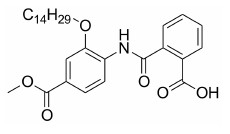
化合物CX09040是本所自行研发的一类新结构小分子化合物之一, 经1H NMR和MS分析, 确证其分子结构为2-(4-甲氧羰基-2-十四烷氧基苯基) 氨甲酰基苯甲酸 [2-(4-methoxycarbonyl-2-tetradecyloxyphenyl)carbamoylbenzoic acid](图 1)。本研究重点观察化合物CX09040对胰岛β细胞的保护作用, 故选择胰岛β细胞保护剂利拉鲁肽作为阳性对照药[7]。
|
Figure 1 The structure of 2-(4-methoxycarbonyl-2-tetradecyloxyphenyl)carbamoylbenzoicacid (CX09040) |
蛋白酪氨酸磷酸酶1B (protein tyrosine phosphatase 1B, PTP1B) 是胰岛素信号传导途径的负调节因子, 在很多生理功能方面起到重要作用, 包括能量平衡和葡萄糖稳态的调节, 是治疗糖尿病的潜在药物作用靶点[8]。近年来,PTP1B对胰岛β细胞的作用受到关注。研究表明, PTP1B基因敲除能促进葡萄糖刺激的胰岛素释放, 促进胰岛β细胞增殖、抑制胰岛β细胞凋亡, 有益于改善β细胞功能[9]。本研究发现具有较强PTP1B抑制作用的化合物CX09040, 对alloxan诱导的β细胞功能受损小鼠具有明显胰岛β细胞保护作用, 提示抑制PTP1B可能成为保护β细胞的新途径。
材料与方法 药物和试剂 化合物CX09040由中国医学科学院药物研究所合成; 胰岛素 (鼠源) 超敏酶联免疫吸附 (enzyme-linked immunosorbentassays, ELISA) 测定试剂盒 (美国Alpco公司); 利拉鲁肽注射液 (批 号: DP50442, 诺和诺德制药有限公司); anti-Actin、anti-Akt、anti-p-Akt (Ser473)、anti-Flag、anti-FoxO1、anti-p-FoxO1 (Ser256)、anti-IRβ等抗体 (美国CST公司); anti-p-IRβ (Tyr1162/1163)抗体 (美国Santa Cruz公司); anti-PDX-1抗体 (美国Abcam公司); anti-PTP1B抗体 (美国Millipore公司); ECL发光液 (北京普利莱基因生物技术公司); 293T细胞 (中国医学科学院协和细胞中心); Anti-Flag M2Affinity Gel (Sigma公司)。 实验动物雄性ICR小鼠, 体重22~24 g, 购于北京华阜康生物科技股份有限公司 [合格证号: SCXK (京) 2014-0004]。实验动物饲养于中国医学科学院药物研究所实验动物中心, 饲养温度21 ℃~22 ℃, 湿度40%~60%, 每天光照/黑暗时间为12 h/12 h。实验动物自由摄食饮水。实验过程符合《北京市实验动物管理条例》的相关规定。
动物适应性喂养1周后, 尾静脉注射alloxan 50mg·kg−1。72h后进行口服葡萄糖耐量实验, 选取血糖−时间曲线下面积 (area under curve, AUC) 值明显大于正常对照组的动物作为胰岛β细胞受损模型小鼠。将模型小鼠随机分为3组 (n = 10): 模型组、利拉鲁肽组和CX09040组, 分别给予水 (灌胃)、利拉鲁肽 (400 µg·kg−1·d−1, 皮下注射) 和化合物CX09040 (100 mg·kg−1, 灌胃), 每天给药一次。设同批正常动物为正常对照组 (n = 10),灌胃等体积水。
口服葡萄糖耐量试验 (oral glucosetolerance test, OGTT) 动物禁食2 h后, 灌胃给予20% 葡萄糖溶液2 g·kg−1 (体重), 检测葡萄糖负荷后30、60和120 min时血糖水平, 观察动物的血糖变化, 并计算血糖−时间AUC, 以评价机体对糖的处置和利用能力。
葡萄糖刺激胰岛素释放(glucosestimulated insulin secretion, GSIS)试验动物禁食2 h后, 灌胃给予20% 葡萄糖溶液2 g·kg−1(体重), 分别检测葡萄糖负荷后10 min血糖水平和相应的血胰岛素水平。计算葡萄糖刺激的胰岛素分泌量、早期相胰岛素分泌指数 (acute insulin response, AIR), AIR = (Ins10 − Ins0) / (G10 − G0), 以评价动物胰岛β细胞的分泌功能。Ins0、Ins10分别为葡萄糖负荷后0、10 min时间点的血胰岛素 (insulin, Ins) 水平; G0、G10分别为葡萄糖负荷后0、10 min时间点的血糖 (glucose, G) 水平。
基因重组人 PTP1B (human PTP1B,hPTP1B) 活性测定 参照文献[10]采用对硝基苯酚磷酸酯 (disodium4-nitropheyl phosphate, pNPP) 法体外测定PTP1B活性。
PTP1B高表达293T细胞内PTP1B活性测定培养于含10% 胎牛血清的改良杜氏伊格尔培养基 (Dulbecco’s modified eagle medium, DMEM) (高糖) 中的293T细胞长至50% 融合后, 进行pMSCVpuro-n-flag-RFP/PTP1B质粒转染; 继续培养48h后, 加 入药物处理, 作用5 h, 收集细胞, 进行免疫沉淀试验。将细胞裂解液与Anti-Flag M2Affinity Gel充分混悬, 对细胞高表达的n-flag-RFP或n-flag-PTP1B蛋白进行结合。用Flag蛋白进行洗脱后, 得到纯化后的n-flag-RFP或n-flag-PTP1B蛋白。Western blotting法检测免疫沉淀产物中PTP1B蛋白含量, 并采用pNPP法测定其PTP1B活性。选用经典的蛋白磷酸酶抑制剂钒酸钠Na3VO4(终浓度1×10−3mol·L−1) 作为阳性对照药。
病理分析连续给药3周, 动物禁食4 h, 断头处死, 开腹以脾脏为标记, 快速分离出胰腺尾部, 置于4% 福尔马林中固定48 h, 经酒精脱水、二甲苯透明、石蜡包埋后切片和苏木精−伊红 (hematoxylin-eosin, HE) 染色, 光学显微镜下观察。运用Image Pro Plus (IPP) 软件 (Media Cybernetics公司) 测量胰岛面积。每张病理切片在光学显微镜下按照Z字型方向随机选取10个视野, 各视野无重合。在4倍物镜下拍摄, 分别进行胰岛数目及胰岛面积的计量。每只动物的胰岛数目及面积来自其病理切片10个视野的总和,以评价动物的胰岛β细胞数。
蛋白质印迹(Western blotting)检测蛋白表达用RIPA裂解液提取小鼠胰腺组织总蛋白, 10% 十二烷基硫酸钠聚丙烯酰胺凝胶电泳 (sodium dodecylsulfate polyacrylamide gel electrophoresis, SDS-PAGE) 分离蛋白, 电转至硝酸纤维素膜, 用牛血清白蛋白 (bovine serum albumin,BSA) 溶液封闭2 h, 加入一抗4 ℃孵育过夜, 分别用山羊抗兔二抗IgG [一抗为肌动蛋白 (Actin)、丝/苏氨酸蛋白激酶 (Akt)、磷酸化的丝/苏氨酸蛋白激酶 (p-Akt)、胰岛素受体β亚基(insulin receptor β subunit, IRβ)、磷酸化的胰岛素受 体β亚基(phospho-insulin receptor β subunit, p-IRβ)、叉头框蛋白O1 (forkhead box transcription factorclass O1, FoxO1)、磷酸化的叉头框蛋白O1 (phospho- forkheadbox transcription factor class O1, p-FoxO1) 和胰十二指肠同源盒1 (pancreaticand duodenal homeobox1, PDX-1)]或山羊抗鼠二抗IgG (一抗为PTP1B) 室温孵育1 h, ECL化学发光显色, 凝胶成像系统采集图像, 用Quantity one图像分析软件对扫描的目的条带图像进行灰度分析。
统计学分析实验数据以x ± s表示,使用SPSS 13.0软件进行统计学分析, 多组间比较采用单因素方差分析 (one-way ANOVA), 两两比较采用最小显著性差异法 (least-significant difference, LSD) 检验。P < 0.05被认为存在统计学差异。
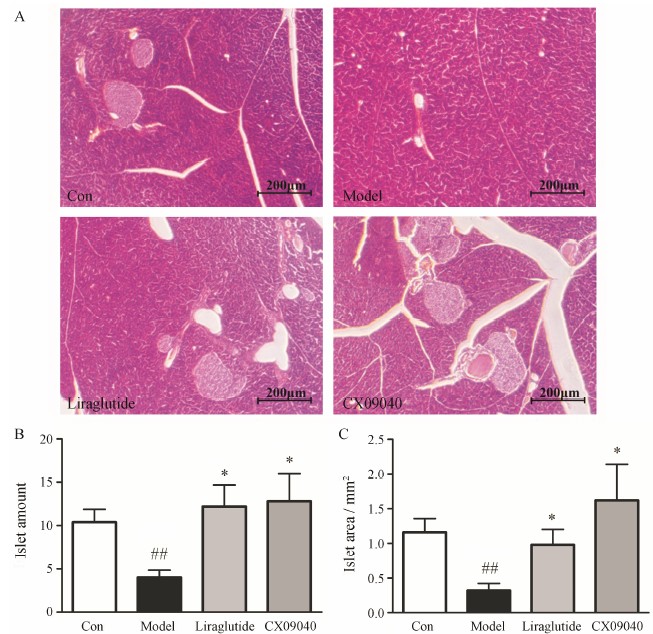
结果 1 化合物CX09040对小鼠胰岛β细胞的保护作用 1.1 对胰岛数量及总面积的影响连续给药3周后, 结果显示 (图 2), 正常对照组动物的胰腺病理切片在4倍物镜下1个视野中可见1~3个胰岛, 面积大小不一; 在胰岛β细胞受损状态下, 模型组的胰岛数量和总面积明显减少, 分别较正常对照组的胰岛数量和总面积减少了61.5% 和71.5%; 给予CX09040治疗后, 动物的胰岛数量和总面积较模型组分别增加了2.2倍和3.9倍; 阳性对照利拉鲁肽组胰岛数量和总面积均较模型组明显增加。
|
Figure 2 Effectof CX09040 on the pathological changes of the pancreas in β celldysfunction mice (HE staining, 40×). A: Pathological sections of the pancreas;B: Number of islets; C: Area of islets. n = 5, x ± s. ##P < 0.01 vs Con group; P < 0.05 vs model group. Con:Control group |
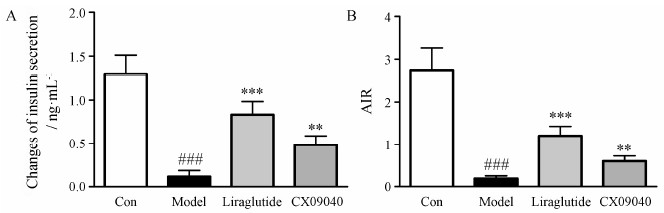
ICR小鼠经过alloxan诱导后胰岛β细胞功能受损 (图 3), 与正常对照组比较, 模型组小鼠葡萄糖刺激的胰岛素分泌量降低了90.9%, 其反映急性相胰岛素分泌的指标AIR降低了93.0%; 连续给予CX09040治疗3周后, 其胰岛分泌功能得到明显改善, CX09040组葡萄糖刺激的胰岛 素分泌量和AIR分别较模型组增加了3.1倍和2.1倍; 同样, 利拉鲁肽也能使其胰岛功能得到明显改善。
|
Figure 3 Effect of CX09040 onthe islet secretion in β cell dysfunction mice. A: Changes of the glucose-stimulated insulinsecretion; B: Values of AIR. n = 10, x ± s. ###P < 0.001 vs Con group; **P < 0.01, ***P < 0.001 vs model group. AIR:Acute insulinresponse |
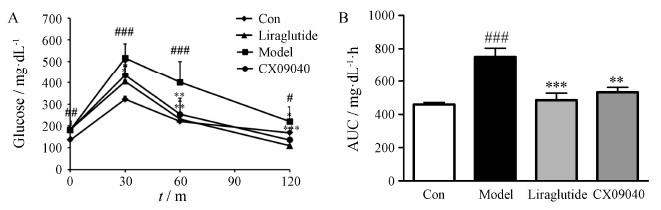
经alloxan诱导的胰岛β细胞受损小鼠, 连续给药2周后, 进行OGTT。 结果显示, 与正常对照组比较, 模型组动物在葡萄糖负荷后血糖水平明显升高, 显示出明显的葡萄糖耐量低减现象 (图 4)。与模型组比较, 利拉鲁肽、CX09040组小鼠葡萄糖负荷后各时间点的血糖水平明显降低 (图 4A), AUC值分别降低了35.5% 和29.0% (图 4B), 说明化合物CX09040具有明显改善胰岛β细胞受损小鼠葡萄糖耐量低减的作用。
|
Figure 4 Amelioration of CX09040 onthe impaired glucose tolerance in mice. A: Changes of the blood glucoselevels after glucose loading; B: Values of area under curve (AUC) in OGTT. n = 10, x ± s. #P < 0.05, ##P < 0.01, ###P < 0.001 vs Con group; P < 0.05, **P < 0.01, ***P < 0.001 vs model group. OGTT:Oral glucosetolerance test |
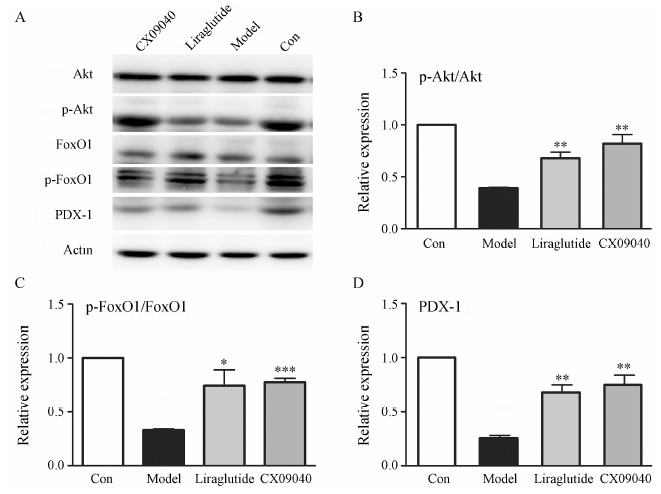
经alloxan诱导的胰岛β细胞受损小鼠, 连续给药3周后禁食4 h, 取胰腺, 观察其对胰岛细胞增殖的调控作用。结果显示 (图 5), 各组动物胰腺的Akt的表达无明显差异。与正常对照组比较, 模型组Akt磷酸化水平下降, p-Akt/Akt比值降低了60.8%; 与模型组相比,利拉鲁肽组和CX09040组的Akt磷酸化水平均明显升高, 其p-Akt/Akt分别上调了73.2%和109.2%(图 5A, 5B)。
|
Figure 5 Effects of CX09040 on theregulation of signaling pathways related to β cell proliferation in β cell dysfunction mice. A: Expressions ofAkt, p-Akt, FoxO1, p-FoxO1, PDX-1 in pancreas; B: Ratio of p-Akt/Akt band intensities quantified by densitometry;C: Ratio of p-FoxO1/FoxO1 band intensities quantified bydensitometry; D: Band intensities of PDX-1 quantified by densitometry. n = 3, x ± s. P < 0.05, **P < 0.01, ***P < 0.001 vs model group |
与正常对照组比较, 模型组的胰腺FoxO1的表达无明显差异, FoxO1磷酸化水平有所降低, 其p-FoxO1/ FoxO1比值降低了66.9%; 与模型组相比, 利拉鲁肽组的胰腺FoxO1表达水平有所升高, FoxO1磷酸化水平显著升高, p-FoxO1/FoxO1升高124.4%; CX09040组的胰腺FoxO1表达水平与模型组比较无明显差异, FoxO1磷酸化水平显著升高, 其p-FoxO1/FoxO1升高133.8% (图 5A, 5C)。
与正常对照组比较, 模型组PDX-1表达水平下调了74.5%; 与模型组相比, 利拉鲁肽组和CX09040组PDX-1表达水平分别升高了166.0% 和193.4%(图 5A, 5D)。
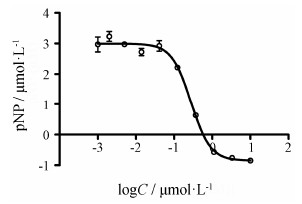
4 化合物CX09040对分子靶点PTP1B的抑制作用4.1 对基因重组hPTP1B活性的影响体外酶学实验显示, 化合物CX09040对基因重组hPTP1B活性具有较强的抑制作用, 其IC50为2.78×10−7 mol·L−1(图 6)。
|
Figure 6 The inhibition of CX09040on recombinant human PTP1B (hPTP1B) activity. n = 3, x ± s. PTP1B:Protein tyrosine phosphatase 1B |
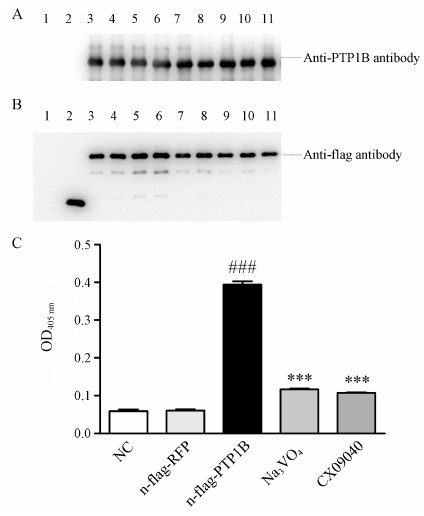
终浓度为1×10−5 mol·L−1化合物CX09040在四氮唑蓝比色分析 (methyl thiazolyltetrazolium, MTT) 实验中对293T细胞未见明显细胞毒作用 (数据略)。用终浓度为1×10−5 mol·L−1CX09040和阳性对照药1×10−3mol·L−1 Na3VO4处理PTP1B高表达293T细胞5h, 收集细胞, 观察样品对细胞内PTP1B活性的影响。 结果显示 (图 7), 正常对照组 (图 7A, 7B, line 1) 未见明显的PTP1B和n-flag-RFP/PTP1B蛋白表达; 与正常对照组比较, 转染pMSCVpuro-n-flag-RFP质粒的阴性对照样品 (图 7A, 7B, line 2), 仅表达n- flag-RFP蛋白, 未见明显的PTP1B蛋白表达; 转染了pMSCVpuro-n-flag-PTP1B质粒 (图 7A, line 3−11) 的模型细胞呈现明显的n-flag-PTP1B蛋白高表达 (图 7B,line 3−11)。样品CX09040对模型细胞的PTP1B蛋白表达无明显作用 (图 7A, line 11; 图 7B, line 11)。与正常对照组比较, 转染pMSCVpuro-n-flag-RFP质粒后, 细胞内PTP1B活性无明显变化; 转染了pMSCVpuro-n-flag-PTP1B质粒后, 细胞内PTP1B活性增加了5.7倍; 样品CX09040和Na3VO4处理后, 模型细胞内PTP1B活性分别降低了72.8% 和70.5% (图 7C)。
|
Figure 7 The effect of CX09040 onintracellular PTP1B activity. A: Expressionof PTP1B in 293T cells; B: Expression of flag in 293T cells; C: IntracellularPTP1B activity; 1: Control group (NC), untreated; 2: pMSCVpuro-n-flag-RFPplasmid transfected; 3: pMSCVpuro-n-flag-PTP1B plasmid transfected; 4−9:pMSCVpuro-n-flag-PTP1B plasmid transfected with othersamples treated; 10: pMSCVpuro-n-flag-PTP1B plasmid transfectedwith Na3VO4 treated; 11: pMSCVpuro-n-flag-PTP1B plasmidtransfected with CX09040 treated. n = 3, x ± s. ###P < 0.001 vs NC group; ***P < 0.001 vs n-flag-PTP1B group |
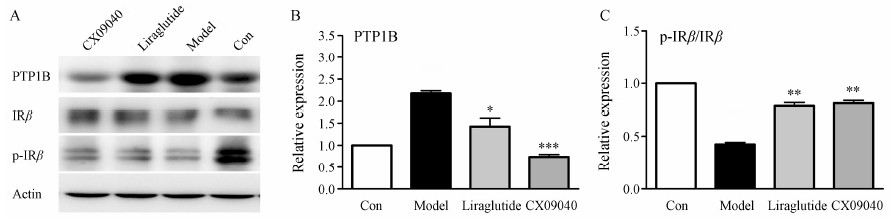
胰岛β细胞损伤小鼠经CX09040治疗3周后, 取胰腺, 观察 其对PTP1B表达的影响。结果显示 (图 8), 与正常对照组比较, 模型组胰腺PTP1B表达水平显著升高, 上调了117.8%; 与模型组比较, CX09040组和利拉鲁肽组的胰腺PTP1B表达分别下调了66.1% 和34.6%。各组动物的IRβ表达无明显差异。与正常对照组比较, 模型组胰腺p-IRβ的表达水平显著降低, 其p-IRβ/ IRβ比值下降了57.6%; CX09040和利拉鲁肽均可逆转p-IRβ表达的下调, 使p-IRβ/IRβ比模型组分别上升了91.8% 和85.8%。
|
Figure 8 Effects of CX09040 on theexpressions of PTP1B, IRβ and p-IRβ in pancreas of β cell dysfunction mice. A: Expressionsof PTP1B, IRβ, p-IRβ; B: Band intensities ofPTP1B quantified by densitometry; C: Ratio of p-IRβ/IRβ band intensities quantifiedby densitometry. n = 3, x ± s. P < 0.05, **P < 0.01, ***P < 0.001 vs model group |
本研究结果显示, 利拉鲁肽对胰岛β细胞受损的小鼠具有促进胰岛β细胞增殖、促葡萄糖刺激的胰岛素分泌等胰岛β细胞保护作用。化合物CX09040与利拉鲁肽具有类似的药效。
胰岛β细胞的数量和功能对维持机体正常糖代谢稳态具有重要意义。在从正常糖耐量向糖尿病发展过程中, β细胞功能呈进行性下降[11]。胰岛β细胞功能广义的定义包括胰岛素的脉冲样分泌、对各种刺激物的反应、胰岛素的储存以及细胞的增殖和凋亡[12]。因此, 胰岛β细胞的功能主要从分泌模式和细胞数量两个方面来评价。Alloxan是一种有毒的葡萄糖类似物, 通过葡萄糖转运体2 (glucose transporter 2, GLUT2) 转运积聚在胰岛β细胞,在胞内谷胱甘肽的作用下, alloxan产生活性氧 (reactive oxygen species, ROS)及其还原产物, 最终在铁催化下, 产生羟基自由基, 这些自由基最终导致了胰岛β细胞的损伤, 甚至死亡; alloxan作为硫醇试剂, 还可选择性地抑制葡萄糖诱导的胰岛素分泌[13]。化合物CX09040结构稳定, 对正常ICR小鼠的安全性较好 (数据略)。正常Wistar大鼠口服CX09040后血药浓度较高, 且达峰快、维持时间长 (数据略), 说明化合物CX09040穿过细胞膜的能力较强。基于前期研究基础和CX09040抑制hPTP1B活性的IC50值, 本研究选择化合物CX09040以100 mg·kg−1灌胃给药。胰岛是由内分泌细胞组成的球形细胞团, 分布于胰腺小叶内, 大小不一, 以胰腺尾部较多。每个胰岛由数个到数百个细胞组成, 胰岛表面包裹一层致密的结缔组织被膜, 与周围外分泌腺有清楚的界限[14]。在本研究中, 通过尾静脉注射alloxan造成糖耐量低减、β细胞受损的小鼠模型, 通过葡萄糖刺激的胰岛素释放实验来评价胰岛β细胞的分泌功能, 直接的组织病理形态学分析以评价胰岛β细胞数量。结果显示, 化合物CX09040具有较好的胰岛β细胞保护功能。在连续给予CX09040治疗β细胞损伤模型小鼠3周后, CX09040组小鼠胰岛数量和总面积较模型组分别增加了2.2倍和3.9倍, 被alloxan破坏的胰岛β细胞数明显增加; 此外, 动物葡萄糖刺激的血胰岛素分泌量和AIR较模型组分别增加3.1倍和2.1倍, 说明模型动物胰岛β细胞的胰岛素分泌功能增强了, 从而使机体受损的葡萄糖耐量得到改善。
胰岛素信号通路对β细胞的生长和生存至关重要[15]。胰岛素与胰岛素受体 (insulin receptor, IR)结合, 激活了IRβ的酪氨酸激酶活性, 随之IRβ自身磷酸化并产生构象变化, 先后激活下游的胰岛素受体底物-2 (insulinreceptor substrate-2, IRS-2) 和Akt, 进而使下游的信号分子FoxO1磷酸化[16, 17]。正常生理条件下, 转录因子FoxO1穿梭于胞核和胞质之间, 其磷酸化能够阻止FoxO1从胞质转位至核内, 减少对胰岛素增殖相关转录因子PDX-1转录的抑制, 上调PDX-1的表达,促进胰岛β细胞的增殖[18, 19]。本实验中发现CX09040能上调IRβ、Akt、FoxO1的磷酸化水平及PDX-1的表达, 提示CX09040可能是通过对胰岛素信号通路的激活来促进胰岛β细胞增殖, 从而增加胰岛细胞量, 继而间接促进了胰岛素的分泌。化合物CX09040是否对β细胞有直接的促分泌作用, 还有待进一步证明。
在抗糖尿病的研究中, PTP1B一直被视为胰岛素抵抗的分子靶点, 是胰岛素信号传导途径的负调节因子[8]; 近期研究发现PTP1B与β细胞保护密切相 关[9, 20]。本研究发现化合物CX09040抑制基因重组hPTP1B的IC50达到10−7 mol·L−1数量级, 抑制活性较强。能否穿过细胞膜是PTP1B抑制剂研究中的瓶颈之一。正常情况下, 细胞内有一定水平的PTP1B表达, 发挥一定的生理功能; 在糖尿病等糖脂代谢紊乱的病理状态下, 细胞内PTP1B表达明显升高[21]。结果显示, 胰岛β细胞受损模型小鼠PTP1B表达明显升高 (图 8A, 8B)。本研究选用细胞实验中常用的工具细胞293T细胞, 转入PTP1B质粒, 形成PTP1B高表达的细胞模型。通过细胞实验证明化合物CX09040可以穿过细胞膜, 抑制细胞内PTP1B活性 (图 7)。在整体动物水平, 化合物CX09040能够抑制β细胞受损模型小鼠胰腺组织内PTP1B的表达及上调其调控的IRβ磷酸化水平。
总之, 化合物CX09040对β细胞受损小鼠具有明显的胰岛β细胞保护作用。抑制分子靶点PTP1B的表达和活性, 进而促进β细胞增殖, 可能是其发挥保护胰岛β细胞作用的重要机制。
| [1] | Handelsman Y, Bloomgarden ZT, Grunberger G, et al. American association of clinical endocrinologists and american college of endocrinology-clinical practice guidelines for developing a diabetes mellitus comprehensive care plan-2015 [J]. Endocr Pract, 2015, 21: 1-87. |
| [2] | Cnop M, Welsh N, Jonas J C, et al. Mechanisms of pancreatic beta-cell death in type 1 and type 2 diabetes: many differences, few similarities [J]. Diabetes, 2005, 54: S97-S107. |
| [3] | Kitamura T. The role of FOXO1 in β-cell failure and type 2 diabetes mellitus [J]. Nat Rev Endocrinol, 2013, 9: 615-623. |
| [4] | Ginter E, Simko V. Type 2 diabetes mellitus, pandemic in 21st century [J]. Adv Exp Med Biol, 2012, 771: 42-50. |
| [5] | Ashcroft FM, Rorsman P. Diabetes mellitus and the β cell: the last ten years [J]. Cell, 2012, 148: 1160-1171. |
| [6] | Wajchenberg BL. Beta-cell failure in diabetes and preservation by clinical treatment [J]. Endocr Rev, 2007, 28: 187-218. |
| [7] | Vilsbøll T, Brock B, Perrild H, et al. Liraglutide, a once-daily human GLP-1 analogue, improves pancreatic B-cell function and arginine-stimulated insulin secretion during hyperglycaemia in patients with type 2 diabetes mellitus [J]. Diabet Med, 2008, 25: 152-156. |
| [8] | Tsou RC, Bence KK. Central regulation of metabolism by protein tyrosine phosphatases [J]. Front Neurosci, 2012, 6: |
| [9] | Fernandez-Ruiz R, Vieira E, Garcia-Roves PM, et al. Protein tyrosine phosphatase-1B modulates pancreatic β-cell mass [J]. PLoS One, 2014, 9: e90344. |
| [10] | Du X, Zhang SE, Liu JZ, et al. Design, synthesis and evaluation of malonic acid-based PTP1B inhibitors [J]. Acta Pharm Sin (药学学报), 2012, 47: 367-373. |
| [11] | Du X, Zhang SE, Liu JZ, et al. Design, synthesis and evaluation of malonic acid-based PTP1B inhibitors [J]. Acta Pharm Sin (药学学报), 2012, 47: 367-373. |
| [12] | Talchai C, Xuan S, Lin HV, et al. Pancreatic β cell dedifferentiation as a mechanism of diabetic β cell failure [J]. Cell, 2012, 150: 1223-1234. |
| [13] | Lenzen S. The mechanisms of alloxan-and streptozotocin-induced diabetes [J]. Diabetologia, 2008, 51: 216-226. |
| [14] | Chen L, Zhang XL, Li J, et al. The semi-quantitative method for evaluating lipid accumulation in pancreas of diabetic mice [J]. Acta Pharm Sin (药学学报), 2011, 46: 664-668. |
| [15] | Ueki K, Okada T, Hu J, et al. Total insulin and IGF-I resistance in pancreatic beta cells causes overt diabetes [J]. Nat Genet, 2006, 38: 583-588. |
| [16] | Heit JJ, Karnik SK, Kim SK. Intrinsic regulators of pancreatic beta-cell proliferation [J]. Annu Rev Cell Dev Biol, 2006, 22: 311-338. |
| [17] | Kaiser G, Gerst F, Michael D, et al. Regulation of forkhead box O1 (FOXO1) by protein kinase B and glucocorticoids: different mechanisms of induction of beta cell death in vitro [J]. Diabetologia, 2013, 56: 1587-1595. |
| [18] | Kitamura T, Nakae J, Kitamura Y, et al. The forkhead transcription factor Foxo1 links insulin signaling to Pdx1 regulation of pancreatic beta cell growth [J]. J Clin Invest, 2002, 110: 1839-1847. |
| [19] | Li Y, Xiao J, Tian H, et al. The DPP-4 inhibitor MK0626 and exercise protect islet function in early pre-diabetic kkay mice [J]. Peptides, 2013, 49: 91-99. |
| [20] | Liu S, Xi Y, Bettaieb A, et al. Disruption of protein-tyrosine phosphatase 1B expression in the pancreas affects β-cell function [J]. Endocrinology, 2014, 155: 3329-3338. |
| [21] | Ma YM, Tao RY, Liu Q, et al. PTP1B inhibitor improves both insulin resistance and lipid abnormalities in vivo and in vitro [J]. Mol Cell Biochem, 2011, 357: 65-72. |
 2015, Vol. 50
2015, Vol. 50


