2. 西南大学 重庆药物过程与质量控制工程技术研究中心, 重庆 400715;
3. 西南大学 生命科学学院, 重庆 400715
2. Engineer Research Center of Chongqing Pharmaceutical Process and Quality Control, Southwest University, Chongqing 400715, China;
3. College of Life Science, Southwest University, Chongqing 400715, China
小檗碱 (berberine,BBR) 是一种黄色的异喹啉生物碱,广泛存在于多种植物的根、茎、花和果实中。现代药理研究已经证明,BBR具有抗炎、抗菌、抗氧化、抗癌、保护心血管、保护神经系统等生理效应,能够治疗糖尿病、高血脂、冠状动脉疾病、脑卒中、阿尔茨海默病、焦虑症、疟疾、胃肠疾病、肾损伤、关节炎、皮肤病、多囊卵巢综合征等[1,2,3]。可见,BBR的生理功能十分丰富,潜在的结构改造和开发应用价值非常大[4]。近年来,许多学者以BBR为先导化合物进行结构修饰,以提高生物利用度和药效、增强靶向性及减少毒副反应,并取得了实质性的进展[5,6,7]。
在BBR结构中引入长链烷基,可以显著提高其生物活性。已有研究证实,经长链烷基修饰过的BBR,抗癌、抗菌活性明显增强[8,9]。本实验室在前期实验中,利用烷基衍生化法首次合成了8-十六烷基小檗碱[10] (8-BBR-C16,图 1),并证明它的降血脂活性与BBR原形相比显著提高[11]。此外,本课题组还得到了新化合物8-辛基小檗碱[12],证明了它的抗菌活性比BBR提高100多倍[13]。
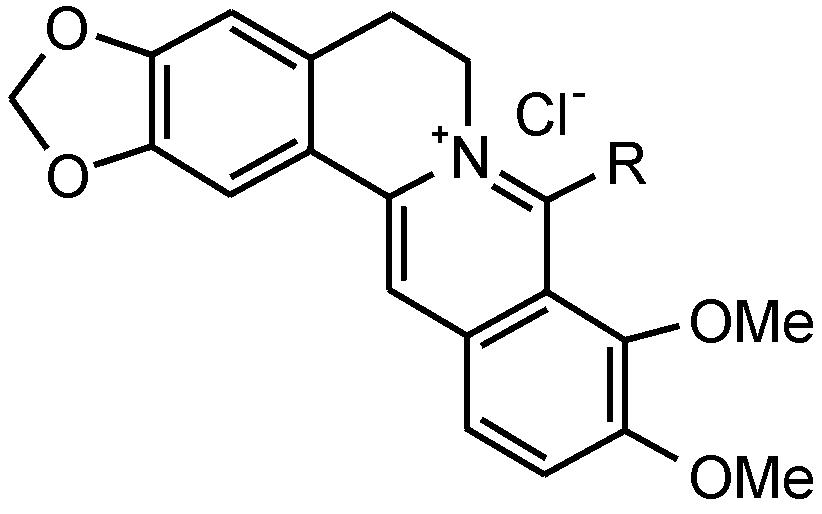 |
Figure 1 Structures of 8-BBR-C16 (R = -CH2-(CH2)14-CH3) and 8-dodecylberberine (R = -CH2-(CH2)10-CH3) |
目前,小檗碱长链烷基衍生物的机制探索仅限于药效活性方面研究,关于该类化合物的药代动力学研究尚未见报道。基于该类化合物的高生物活性,研究它们的药代学对于进一步的开发利用具有重要价值。本文建立了灵敏、准确的高效液相色谱分析方法,定量检测8-BBR-C16在生物样品中的含量,对BBR和8-BBR-C16的药代动力学和组织分布进行对比分析,比较它们在大鼠体内代谢行为的差异,并初步探讨这种差异产生的原因。本文将为小檗碱长链烷基衍生物的作用机制研究、药物结构优化及今后的开发利用提供实验依据。 材料与方法
仪器 e2695-2489高效液相色谱仪 (美国Waters公司),Empower 2.0工作站。
药品与试剂 BBR对照品 (中国兽医药品监察所,批号Z0221206,含量94.5%),8-BBR-C16 (自制,批号1201101,结构式见图 1),8-十二烷基小檗碱 (自制,批号1207071,结构式见图 1); 巴马汀 (自制,批号1205121); Silica Catridges纯硅胶固相萃取柱 (SPE柱,美国Waters公司,批号065133190,规格200 mg/ 3 mL)。
动物 SD大鼠110只,雌雄各半,体重250~300 g,由重庆医科大学实验动物中心提供,生产许可证号: SCXK (渝) 2012-0001。实验前禁食12 h,自由饮水。
色谱分析条件 色谱柱: Phenomenex Luna C8 (250 mm × 4.6 mm,5 µm); 柱温30 ℃; 流速: 1.0 mL·min-1; 检测波长 (紫外检测器): 345 nm; 进样量: 100 µL; 流动相: 乙腈-20 mmol·L-1磷酸二氢钾溶液,用磷酸调至pH 4.0,其中乙腈与磷酸二氢钾溶液的混合比例分别为: 检测BBR (24∶76)、检测8-BBR-C16 (80∶20)。
药物及内标溶液的配制 BBR对照品和巴马汀 (作为BBR的内标) 用水、8-BBR-C16和8-十二烷基小檗碱 (作为8-BBR-C16的内标) 用二氯甲烷-乙腈 (10∶90) 混合溶液,配制得到浓度为1 mg·mL-1药物及内标储备液。二次稀释前述两种内标储备液,得到浓度为10 µg ·mL-1的内标溶液。
样品前处理 ① 血浆样品的前处理: 取血浆样品0.5 mL,加入10 µg·mL-1内标溶液2 µL,混匀,用提取液 [以二氯甲烷-乙腈 (10∶90) 混合溶液为提取液] 6 mL分两次提取,每次振摇10 min,5 000 r·min-1离心10 min (5 ℃)。合并上清液在45 ℃氮气下吹干,残渣用流动相300 µL复溶,过膜,HPLC分析。② 组织样品的前处理: 除胃和小肠仅各取0.1 g外,含BBR其他组织样品取0.5 g,含8-BBR-C16其他组织样品取0.3 g,剪碎,分别加入10 µg·mL-1的内标溶液2、10和6 µL。用二氯甲烷3 mL高速匀浆30 s提取,另二氯甲烷3 mL清洗刀头。合并二氯甲烷,12 000 r·min-1离心5 min (5 ℃)。取下层液体,过纯硅胶SPE柱净化处理。
SPE净化程序 正己烷、二氯甲烷各3 mL依次活化SPE柱,取二氯甲烷提取液全部过柱,再用正己烷和乙酸乙酯各5 mL洗涤,最后甲醇50 mL洗脱。取全部甲醇洗脱液40 ℃旋转蒸发至近干,二氯甲烷5 mL溶解残渣,并于40 ℃氮气下吹干。残渣用流动相300 µL复溶,过膜,HPLC分析。
标准曲线的制备和定量限考察 血浆或空白组织6份,添加得到浓度分别为10、50、100、200、250和300 ng·mL-1 (内标添加浓度为100 ng·mL-1) 的血浆样品和30、200、500、1 000、1 500和2 000 ng·g-1 (内标添加浓度为500 ng·g-1) 的组织样品,对线性范围进行考察。以血浆 (组织) 中药物添加浓度为横坐标 (x),药物与内标峰面积之比为纵坐标 (y),进行线性回归,得回归方程和相关系数r。以信噪比 (S/N) 为10时的药物浓度为最低定量限 (LOQ)。
方法专属性 分别记录空白血浆、空白组织、药物溶液和灌胃后所得血浆、组织的色谱图,并进行图谱比对。
回收率和日内、日间精密度 精密量取空白大鼠血浆或空白组织,添加制得高、中、低浓度分别为300、200和10 ng·mL-1的血浆样品和2 000、1 000和30 ng·g-1的组织样品。回收率考察时10天内重复测定6组,精密度考察时每个浓度日内、日间分别平行测定6组。
稳定性 同回收率项下方法,制得高、中、低浓度样品(n = 5),分别于室温下放置24 h后、处理完在4 ℃放置24 h后、反复冻融3次后、于 -20 ℃放置两周后测定。
大鼠体内药动学和组织分布 110只大鼠随机分成两组,BBR组50只,8-BBR-C16组60只,均以80 mg·kg-1剂量灌胃给药。于给药后0.5、1、1.5、2、3、4、6、8、12、24、48和72 h (BBR不采集48 h和72 h) 各摘取5只大鼠眼球取血约1.5 mL,置肝素化EP管中,5 000 r·min-1离心10 min,分离血浆,于-20 ℃保存。
同时,于1、3、8和12 h等4个时间点分别断颈处死大鼠各5只,取心、肝、脾、肺、肾、脑、子宫、睾丸、胃和小肠,用生理盐水漂洗,用滤纸吸干水分后,于 -20 ℃保存。
数据分析 利用DAS3.2.1软件,按非房室模型拟合药动学参数,达峰浓度 (Cmax) 和达峰时间 (tmax) 采用实测值。 结果 1 方法学考察 1.1 标准曲线和定量限
所得结果表明,两种药物在浓度为10~300 ng·mL-1 (血浆)、30~2 000 ng·g-1 (组织) 时,线性关系良好。BBR在血浆和组织中r分别为0.999 5、0.996 4~0.999 9; 8-BBR-C16在血 浆和组织中r分别为0.999 8、0.997 5~0.999 8。同 时,BBR和8-BBR-C16在血浆中LOQ分别为10和 8 ng·mL-1,在组织中的LOQ分别为25和20 ng·g-1。 1.2 回收率
测得含BBR的高、中、低浓度血浆样品平均回收率为96.0%~104.8%,RSD为2.5%~5.4%,组织样品平均回收率为80.9%~88.5%,RSD为7.5%~10.2%; 含8-BBR-C16的高、中、低浓度血浆样品平均回收率为95.5%~105.5%,RSD为3.4%~5.6%,组织样品平均回收率为81.9%~90.4%,RSD为7.5%~10.8%。表明方法可以满足生物样品定量分析的要求。 1.3 日内、日间精密度
测得含BBR的高、中、低浓度血浆样品日内RSD为3.4%~5.5%,日间RSD为2.5%~5.4%,组织样品日内RSD为5.9%~9.1%,日间RSD为7.5%~10.2%; 含8-BBR-C16的高、中、低浓度血浆样品日内RSD为3.4%~6.4%,日间RSD为3.4%~5.6%,组织样品日内RSD为8.9%~11.4%,日间RSD为7.5%~10.8%。 1.4 方法专属性
从图 2可以看出,BBR和8-BBR-C16 均能和血浆中的内源性干扰成分达到很好的基线分离,药物出峰位置处无干扰,方法的专一性良好。SPE前处理方法去除了脂溶性干扰成分,较好地纯化了样品。
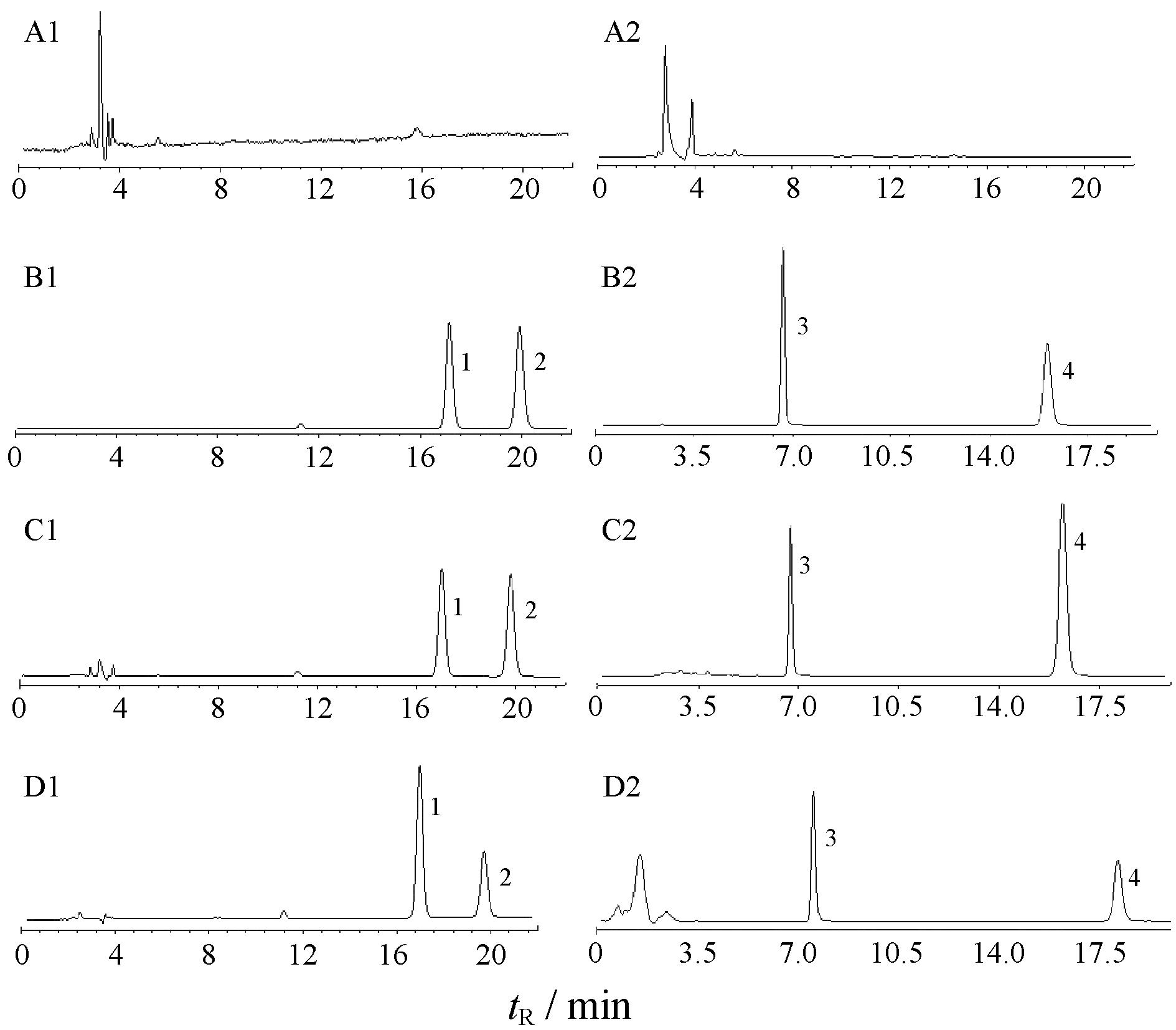 |
Figure 2 Representative chromatograms of A1: Blank plasma; A2: Blank liver; B1: Standard BBR,B2: Standard 8-BBR-C16,C1: Plasma obtained 1 h after oral administration of BBR,C2: Plasma obtained 1 h after oral administration of 8-BBR-C16,D1: Liver obtained 1 h after oral administration of BBR,and D2: Liver obtained 1 h after oral administration of 8-BBR-C16. Peaks 1: Palmatine; 2: BBR; 3: 8-Dodecylberberine; 4: 8-BBR-C16 |
室温下放置24 h后、处理完在4 ℃放置24 h后、反复冻融3次后、于 -20 ℃放置两周后,这4种条件下BBR的高、中、低浓度血浆 (组织) 样品RSD为1.1%~3.3% (7.4%~10.4%)、1.6%~2.5% (8.0%~11.9%)、2.4%~4.1% (5.8%~11.5%) 和1.7%~3.0% (8.3%~11.4%),8-BBR-C16的高、中、低浓度血浆 (组织) 样品RSD为1.0% ~5.6% (10.8%~11.9%)、1.1%~4.8% (7.5%~9.8%)、2.1%~5.0% (8.6%~11.6%) 和1.5%~4.7% (8.8%~10.8%)。结果表明药物在所考察的条件下稳定,符合生物样品测定要求。 2 药动学和组织分布 2.1 药动学
血药浓度-时间曲线见图 3,主要药代动力学参数见表 1。结果表明,结构改造后所得的8- BBR-C16与BBR原形相比,吸收规律发生显著变化,具有以下特点: ① Cmax明显变大,由原形的45.92 µg·L-1升高到1 29.41 µg·L-1。② 生物利用度显著提高。BBR和8-BBR-C16的AUC0-t值分别为201.76 µg·h·L-1、2 609.21 µg·h·L-1。与8-BBR-C16相比,BBR的相对生物利用度仅为7.7%。③ 药物的半衰期变 长,消除变慢,在体内的滞留和循环时间更长。④ 8- BBR-C16的血药浓度 -时间曲线存在明显的双峰。
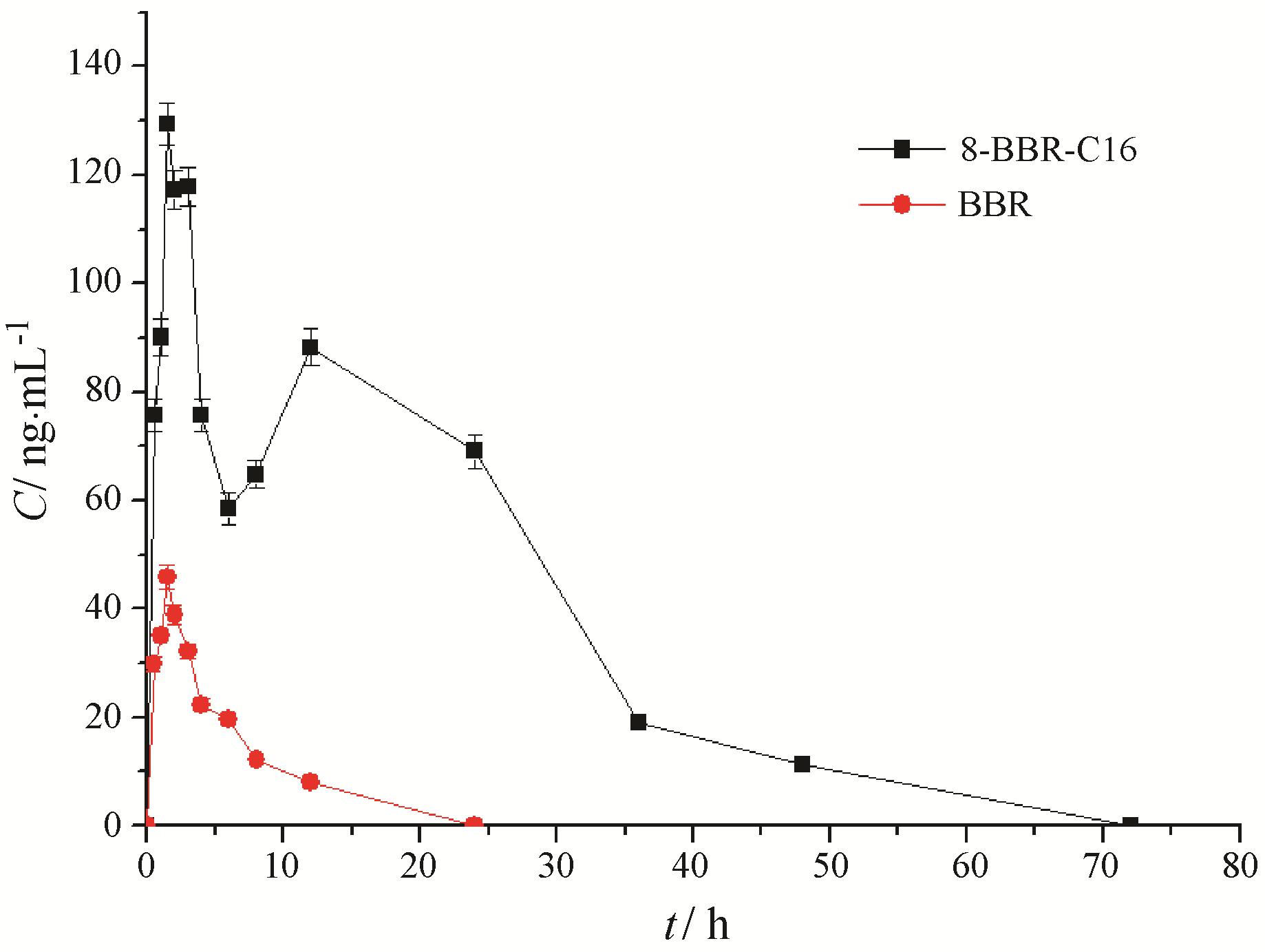 |
Figure 3 Plasma concentration-time curves of BBR and 8-BBR-C16. n = 5,x± s |
|
|
Table 1 Main pharmacokinetic parameters of BBR and 8-BBR- C16. n = 5,x± s. **P < 0.01 vs BBR |
结果表明,8-BBR-C16在大鼠体内的组织浓度大幅提高,分布比例发生变化,分布更为广泛,停滞时间也变长 (图 4)。
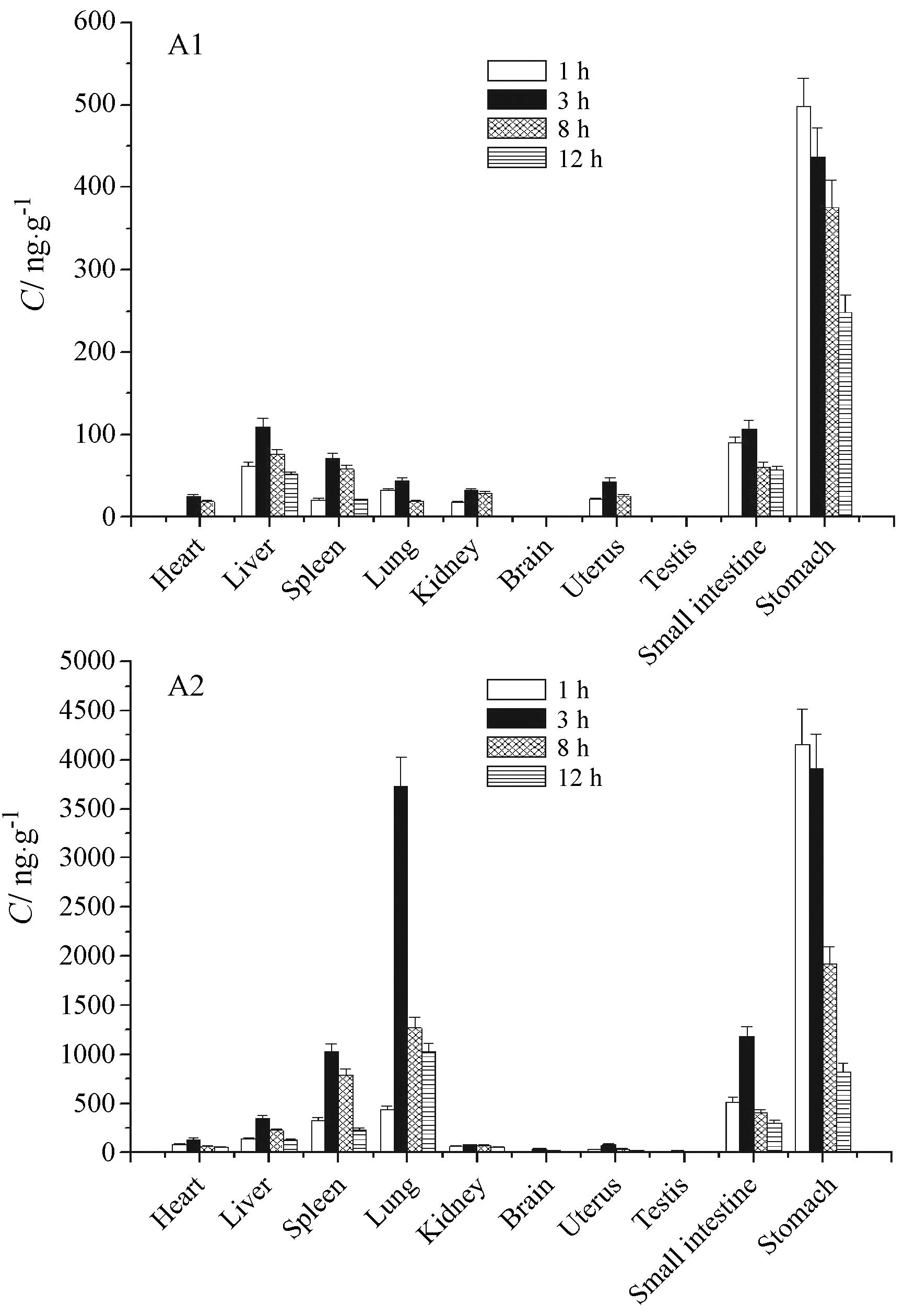 |
Figure 4 Tissue concentrations of BBR and 8-BBR-C16 at 1,3,8,and 12 h. n = 5,x± s. A1: BBR; A2: 8-BBR-C16 |
以往的研究证明,BBR的肠道吸收效率极低,绝对生物利用度低至0.68%[14]。导致BBR生物利用度比较低的原因有两个: 一是药物的物理化学性质。BBR是季铵碱,脂水分配系数为-1.5[15]。药物结构中含有季铵基团者,亲水性强,穿透细胞膜的能力低,限制了药物的跨膜转运和肠道吸收,其生物利用度往往较低[15]。导致BBR生物利用度较低的另外一个原因是BBR为P-gp糖蛋白的底物[16]。P-pg糖蛋白位于细胞膜上,具有药物外排泵作用,它的转运作用导致被吸收的BBR被分泌返回肠道。
药代动力学实验结果显示,二者之间多个药 代动力学参数具有显著性差异。8-BBR-C16的Cmax、AUC0-t分别是BBR的2.8倍和12.9倍,提示8-BBR- C16更利于吸收; tl/2由3.61 h延长到11.90 h,提示8- BBR-C16消除明显变慢。已有报道,中等大小亲脂性取代基的存在是提高药物活性的关键[17],而且烷基具有疏水性,在化合物的碳链中增加一个 -CH2-,则脂水分配系数可以增加2~4倍[18]。因此在BBR中引入烷基增加了先导药物的脂溶性,使8-BBR-C16在大鼠体内的药动学规律发生显著改变。另外,8-BBR- C16血药浓度-时间曲线存在明显的双峰。导致双峰现象的原因可能有分布重吸收和肠肝循环[19]。如果组织中的药物浓度远远高于血浆中的,药物就可能从组织向血浆转运 (分布重吸收),导致血浆中第2个峰的出现[20]。从8-BBR-C16的组织分布结果来看,大多数组织中药物浓度都比血浆中的高很多。所以,分布重吸收是导致8-BBR-C16药-时曲线出现双峰的重要原因。肠肝循环指经胆汁排入肠道的药物,在肠道中重新被吸收,经门静脉返回肝脏的现象。8-BBR- C16是否存在肠肝循环则需要更进一步的实验来确证。小檗碱口服给药具有吸收困难、代谢迅速、血药浓度低的特性[21],上述结果表明,8-BBR-C16脂溶性提高后,在大鼠体内的吸收规律发生明显变化,对提高生物利用度和药物疗效具有积极的意义。
从BBR和8-BBR-C16的组织分布结果中可以 看出,胃肠始终是分布的优势组织,表明它们在胃肠的吸收较慢且不完全。这与文献报道相符,同时也解释了在临床应用中BBR及其制剂是很好的治疗胃肠疾病药物的原因。本实验中,除去胃肠,BBR在肝脏分布浓度最高,与文献[22,23]报道吻合; 其次组织是脾。十六碳烷基链的引入,对药物的组织分布产生了显著影响,大多数组织中药物浓度大幅提高,并改变了药物在体内各组织的分布比例。特别是肺中的浓 度最高 (不包括小肠和胃时),超过了除胃肠外所有组织中药物浓度的总和,显示出较强的肺靶向性。而且,在8和12 h,检测到肺中的药物浓度超过了小肠和胃,说明8-BBR-C16在肺中的消除较慢,使得滞留时间延长。这与肺组织具有较好的亲脂性有关。另外,8-BBR-C16在组织中的分布也更为广泛。例如,在大脑和睾丸中的分布发生了从无到有的转变。影响药物向各种组织分布的主要因素有组织中血流量、组织的毛细血管内膜屏障、药物与蛋白的结合及药物与组织的亲合力[18],也就是药物的分布取决于组织的生物因素及药物的结构因素。组织的毛细血管内膜为多孔性的脂质膜,药物具有较高的脂溶性可以使其容易地通过内膜到达组织内部,使得药物从血液向组织的转运速率提高且组织亲和力增强。本课题组通过十六碳烷基链的引入,达到了使结构优化后的BBR更易通过体内脂质膜的目的。
| [1] | Ye MZ, Fu S, Pi RB, et al. Neuropharmacological and pharmacokinetic properties of berberine: a review of recent research [J]. J Pharm Pharmacol, 2009, 61: 831-837. |
| [2] | Zhao HP, Hong Y, Xie JD, et al. Effect of berberine on left ventricular remodeling in renovascular hypertensive rats [J]. Acta Pharm Sin(药学学报), 2007, 42: 336-341. |
| [3] | Tang J, Feng YB, Tsaoc S, et al. Berberine and Coptidis Rhizoma as novel antineoplastic agents: a review of traditional use and biomedical investigations [J]. J Ethnopharmacol, 2009, 126: 5-17. |
| [4] | Li B, Zhu W, Chen KX. Advances in the study of berberine and its derivatives [J]. Acta Pharm Sin(药学学报), 2008, 43: 773-787. |
| [5] | Zhang WJ, Ou TM, Lu YJ, et al. 9-Substituted berberine derivatives as G-quadruplex stabilizing ligands in telomeric DNA [J]. Bioorg Med Chem, 2007, 15: 5493-5501. |
| [6] | Long YH, Bai LP, Qin Y, et al. Spacer length and attaching position-dependent binding of synthesized protoberberine dimers to double-stranded DNA [J]. Bioorg Med Chem, 2006, 14: 4670-4676. |
| [7] | Feng NP, Zhang ZX, An DK, et al. Analysis of the metabolite of 7-(4-chlorbenzyl)-7, 8, 13, 13a-tetrahydroberberine in rabbit [J]. Acta Pharm Sin(药学学报), 2001, 36: 137-139. |
| [8] | Lo C, Hsu L, Chen M, et al. Synthesis and anticancer activity of a novel series of 9-O-substituted berberine derivatives: a lipophilic substitute role [J]. Bioorg Med Chem Lett, 2013, 23: 305-309. |
| [9] | Iwasa K, Lee D, Kang S, et al. Antimicrobial activity of 8-alkyl- and 8-phenyl-substituted berberines and their 12-bromo derivatives [J]. J Nat Prod, 1998, 61: 1150-1153. |
| [10] | Ye XL, Li XG. Synthesis method and application of long chain alkylberberine salt derivatives: CN, ZL200710078505.X [P]. 2008-01-16. |
| [11] | Yang Y, Ye XL, Li XG. Synthesis and antimicrobial activity of 8-alkylberberine derivatives with a long aliphatic chain [J]. Planta Med, 2007, 73: 602-604. |
| [12] | Ye XL, Li XG. Synthesis method and application of 8- octylberberine hydrochloride: CN, ZL200610095288.0 [P]. 2007-06-06. |
| [13] | Ye XL, He K, Zhu XK, et al. Synthesis and antihyperlipidemic efficiency of berberine-based HMG-CoA reductase inhibitor [J]. Med Chem Res, 2012, 21: 1353-1362. |
| [14] | Chen W, Miao YQ, Fan DJ, et al. Bioavailability study of berberine and the enhancing effects of TPGS on intestinal absorption in rats [J]. AAPS PharmSciTech, 2011, 12: 705- 711. |
| [15] | Battu SK, Repka MA, Maddineni S, et al. Physicochemical characterization of berberine chloride: a perspective in the development of a solution dosage form for oral delivery [J]. AAPS PharmSciTech, 2010, 11: 1466-1475. |
| [16] | Pan GY, Wang GJ, Liu XD, et al. The involvement of P- glycoprotein in berberine absorption [J]. Pharmacol Toxicol, 2002, 91: 193-197. |
| [17] | Kim SH, Lee SJ, Lee J. Antimicrobial activity of 9-O-acyl- and 9-O-alkylberberrubine derivatives [J]. Planta Med, 2002, 63: 277-281. |
| [18] | Li RL. Drug Structure-Activity Relationship(药物构效关系)[M]. Beijing: China Medical Science Press, 2004: 66-68. |
| [19] | Feng J, Xu W, Tao X. Simultaneous determination of baicalin, baicalein, wogonin, berberine, palmatine and jatrorrhizine in rat plasma by liquid chromatography-tandem mass spectrometry and application in pharmacokinetic studies after oral administration of traditional Chinese medicinal preparations containing scutellaria-coptis herb couple [J]. J Pharm Biomed Anal, 2010, 53: 591-598. |
| [20] | Deng YT, Liao QF, Li SH. Simultaneous determination of berberine, palmatine and jatrorrhizine by liquid chromatography- tandem mass spectrometry in rat plasma and its application in a pharmacokinetic study after oral administration of coptis- evodia herb couple [J]. J Chromatogr B, 2008, 863: 195-205. |
| [21] | Liu FQ, Li ZD, Shi XJ, et al. Determination of berberine, palmatine and jatrorrhizine in rabbit plasma by liquid chroma- tography-electrospray ionization-mass spectrometry [J]. J Pharm Biomed Anal, 2011, 56: 1006-1015. |
| [22] | Shen ZF, Xie MZ. Determination of berberine in biological sample by high performance thin layer of fluorescent light density [J]. Acta Pharm Sin(药学学报), 1993, 28: 532- 535. |
| [23] | Zhang R, Li KP, Yang J, et al. Effect of Rhizoma Coptidis coadministration with Cortex Cinnamomi on tissue distribute of berberine in rats [J]. China J Chin Mater Med(中国中药杂志), 2010, 35: 2180-2183. |
 2014, Vol. 49
2014, Vol. 49


