佐匹克隆(zopiclone,API,图 1),化学名称为6-(5-氯吡啶-2-基)-7-[(4-甲基哌嗪-1-基)甲酰氧基]-5,6-二氢吡咯并[3,4-b]吡嗪-5-酮,为吡咯烷酮类化合物,系抑制性神经递质γ-氨基丁酸(GABA)受体激动剂[1-3],具有催眠、镇静、肌肉松弛、抗焦虑和抗惊厥作用,主要用于各种原因导致失眠症的短期治疗。其结构和作用靶点与苯二氮䓬类不同,药效比苯二氮䓬类更强,而成瘾性更低[4]。目前已有片剂、胶囊剂、肠胃外制剂以及微丸制剂等[5-7]。
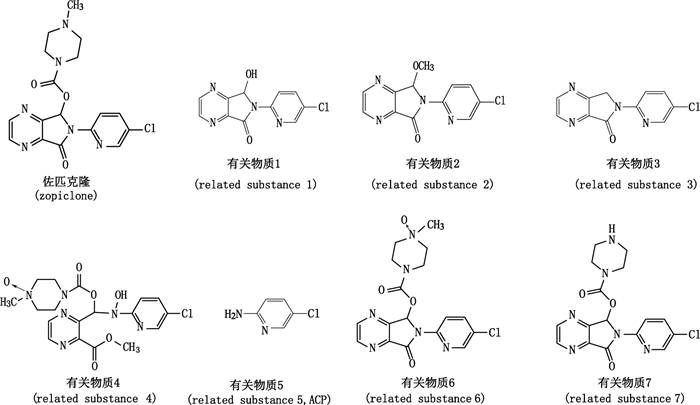
|
图 1 佐匹克隆及其有关物质1~7化学结构图 Figure 1 Chemical structures of zopiclone and its related substances 1-7 |
关于佐匹克隆的药动学研究已有文献报道[8-10],但对佐匹克隆有关物质分析研究尚不完善,多集中于液相色谱或毛细管电泳分析,且多数仅对主要杂质2-氨基-5-氯-吡啶(ACP)进行了分析[11-14],未见对于佐匹克隆有关物质的系统分析和定性研究。
本研究建立了适用于佐匹克隆有关物质鉴定的色谱-质谱联用分析法,使用挥发性条件通过TOF/MS和MS/MS分别测定了主要有关物质的准确质量和二级质谱,结合合成工艺[15-17],推测它们的结构及来源,可为佐匹克隆的生产工艺和质量控制提供参考依据。
1 仪器、药品与试剂1290 Infinity液相色谱-6224飞行时间质谱仪(Agilent公司);TSQ Quantum Ultra AM型三重四极杆质谱(Thermo Finnigan公司);BS 21S分析天平(Sartorius公司,十万分之一天平)。
佐匹克隆片(吉林恒和制药股份有限公司,7.5 mg·片-1);有关物质1、3、5和6对照品(图 1,中国食品药品检定研究院,有关物质1、3、5、6含量分别为98%、98%、98%、100%);甲酸、乙酸铵(AR级,南京化学试剂有限公司),甲醇、乙腈(HPLC级,TEDIA公司),去离子水(市售娃哈哈纯净水)。
2 方法 2.1 色谱条件采用Phenomenex Luna 5u SCX 100A(250 mm×4.6 mm,5 μm)色谱柱,以乙酸铵缓冲溶液(取乙酸铵4.0 g,加水900 mL溶解后,用甲酸调节至pH 4.0,加水稀释至1 L)-甲醇-乙腈(90:5:5)为流动相A,甲醇-乙腈(3:4)为流动相B,线性梯度洗脱[0~5 min,A-B(100:0);5~10 min,A-B(100:0)→A-B(72:28);10~30 min,A-B(72:28)→A-B(58:42);30~35 min,A-B(58:42);35~36 min,A-B(58:42)→A-B(100:0);36~42 min,A-B(100:0)],流速1 mL·min-1,柱温30 ℃,检测波长为303 nm,进样量50 μL。分流比7:3供质谱检测。
2.2 质谱条件电喷雾正离子化,TOF/MS测定喷雾电压3.5 kV,雾化氮气压力275 kPa,气流量10 L·min-1,温度325 ℃,碎片电压135 V,参比离子m/z 121.050 8(质子化嘌呤,C5H5N4+)和922.009 8(质子化氟代膦嗪HP-921,C18H19O6N3P3F24+),质量数扫描范围m/z 100~1200。MS/MS测定的喷雾电压3.5 kV,雾化气压力300 kPa,辅助气压力35 kPa,毛细管温度350 ℃,二级质谱扫描碰撞氩气压力0.16 Pa,碰撞能量15~25 eV。
2.3 溶液配制 2.3.1 供试品溶液及自身对照溶液精密称取佐匹克隆片粉末适量(约相当于佐匹克隆8 mg),置于10 mL量瓶中,加稀释溶剂[0.4%乙酸铵水溶液-甲醇-乙腈(80:10:10)]溶解并稀释至刻度,即得供试品溶液;精密量取上述溶液适量,加稀释溶剂定量稀释,分别制成1%和0.1%的自身对照溶液。
2.3.2 杂质混合对照品溶液取有关物质1、3、5、6的对照品各适量,精密称定,加稀释溶剂溶解并定量稀释成各含约0.8 μg·mL-1的溶液作为杂质混合对照品溶液。
2.3.3 强制破坏试验溶液取佐匹克隆片粉末适量(约相当于佐匹克隆8 mg),加0.5 mol·L-1盐酸溶液1 mL,30 ℃水浴放置20 min,加0.5 mol·L-1氢氧化钠溶液1 mL进行中和,再加稀释溶剂稀释至10 mL,即得质量浓度约为0.8 mg·mL-1的酸破坏试验溶液;取佐匹克隆片粉末适量(约相当于佐匹克隆8 mg),加0.05 mol·L-1氢氧化钠溶液1 mL,室温放置5 min,加0.05 mol·L-1盐酸溶液1 mL进行中和,再加稀释溶剂稀释至10 mL,即得质量浓度约为0.8 mg·mL-1的碱破坏试验溶液;取佐匹克隆片粉末适量(约相当于佐匹克隆8 mg),加3%过氧化氢溶液1 mL,30 ℃水浴放置35 min,加稀释溶剂稀释至10 mL,即得质量浓度约为0.8 mg·mL-1的氧化破坏试验溶液;固体粉末105 ℃烘箱放置12 h,或固体粉末光照(4 500 lx)放置3 d,加稀释溶剂溶解并稀释至10 mL,即得质量浓度约为0.8 mg·mL-1的干法热或干法光破坏试验溶液。同法配制空白溶液。
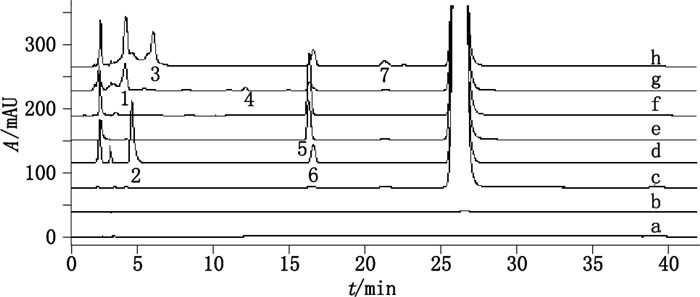
3 结果 3.1 有关物质检查建立的挥发性流动相HPLC分析法,适用于佐匹克隆片有关物质的检查和联用质谱鉴定。取“2.3”项下溶液进样测定,对佐匹克隆片及其强制破坏样品分别进行了分析检查(图 2)。结果表明,采用0.1%主成分自身对照法估算有关物质的含量,佐匹克隆片中仅有关物质5的含量大于0.1%,在强制降解样品中检测到7个主要有关物质(按保留时间顺序编号为1~7),各有关物质色谱分离良好。
|
a.稀释溶剂(dilution solvent)b.0.1%自身对照溶液(0.1% self-reference solution)c.佐匹克隆供试品溶液(zopiclone test sample solution)d.氧化破坏溶液(forced degradation solution under oxidation stress)e.酸破坏溶液(forced degradation solution under acid stress)f.碱破坏溶液(forced degradation solution under base stress)g.干法热破坏溶液(forced degradation solution under dry heat stress)h.干法光破坏溶液(forced degradation solution under photolysis stress) 图 2 佐匹克隆供试品溶液及其强制破坏溶液的高效液相色谱图 Figure 2 HPLC chromatograms of zopiclone test sample solution and its forced degradation test solutions |
强制破坏试验结果表明,本品在苛性条件下均敏感,不稳定。在强酸和强碱条件下主要降解为有关物质5(图 2-e、f),在氧化条件下主要降解为有关物质2和6(图 2-d),在高温条件下降解为有关物质1、4和5(图 2-g),在光照条件下主要产生有关物质1、3、6和7(图 2-h)4个降解产物。
3.2 有关物质结构的质谱解析鉴定TOF/MS测得各有关物质母离子的准确质量和分子式,再经二级质谱测定碎片离子特征,并与佐匹克隆的相应信息进行对比分析,鉴定各主要有关物质的结构(表 1,图 1)。
|
|
表 1 佐匹克隆及其有关物质结构的液质联用鉴定结果 Table 1 Related substances identified in zopiclone by LC-TOF/MS and LC-MS/MS |
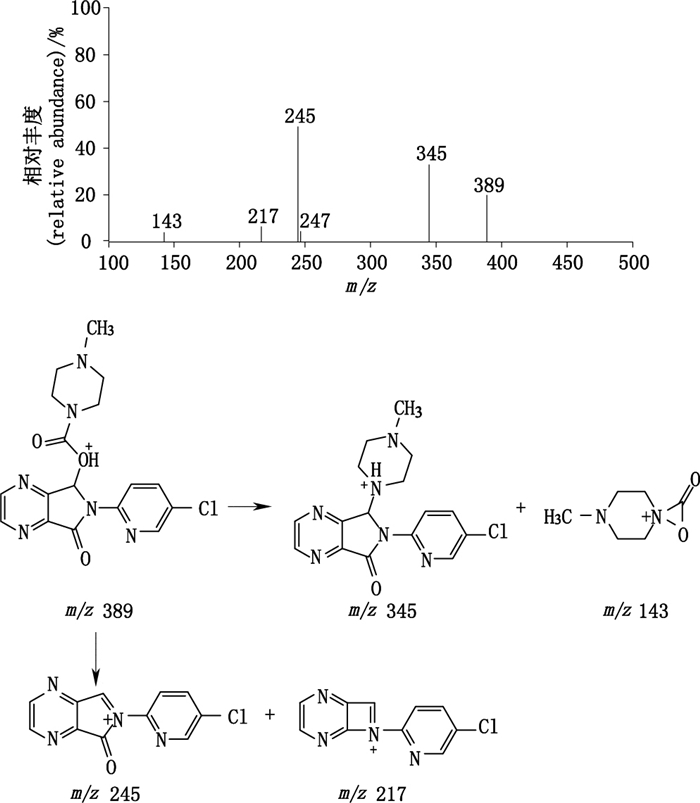
佐匹克隆:ESI+-TOF/MS测得佐匹克隆[M+H]+的准确质量为389.1123,与离子式C17H18ClN6O3+相应。其MS/MS(图 3)中m/z 345的主要特征碎片离子与佐匹克隆[M+H]+丢失CO2相应,这与氨基甲酸酯类物质的母离子易重排裂解形成丢失甲酰酯单元(CO2)[18-19]相符。m/z 245和143的碎片离子与[M+H]+的整个氨基甲酸酯单元裂解相应。佐匹克隆的二级质谱(图 3)分析对解析确证其有关物质结构具有参考意义。
|
图 3 佐匹克隆[M+H]+(m/z 389)离子的二级质谱图及其裂解途径 Figure 3 MS/MS spectrum of zopiclone[M+H]+(m/z 389)ion and its fragmentation pathway |
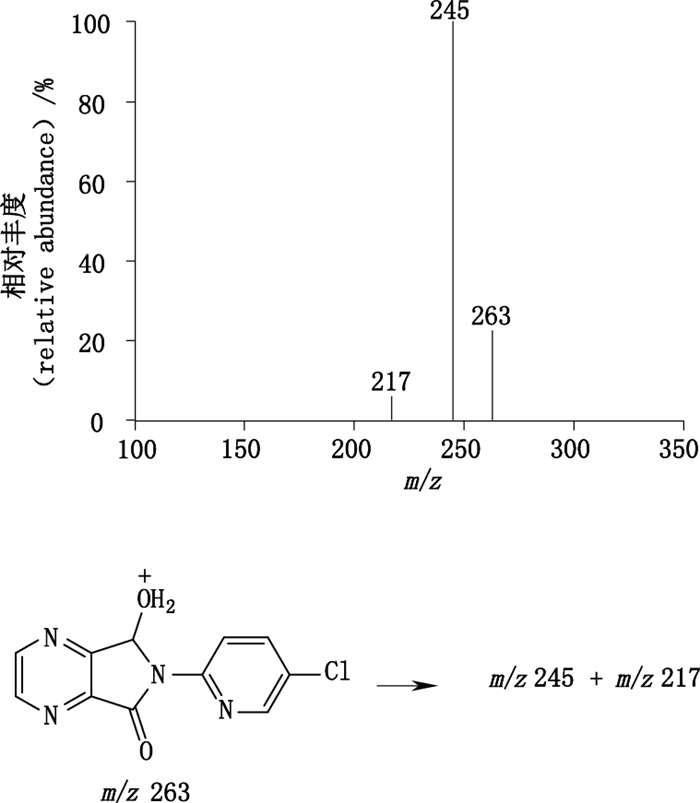
有关物质1:ESI+-TOF/MS测得有关物质1的[M+H]+的准确质量为263.032 9,与离子式C11H8ClN4O2+相应,比佐匹克隆少C6H10N2O,与佐匹克隆脱氨基甲酰单元相应。MS/MS(图 4)中m/z 245和217的主要特征碎片离子与佐匹克隆的相应特征离子相同。结合合成工艺,确证有关物质1为佐匹克隆的脱氨基甲酰单元的主要降解产物,即欧洲药典规定的有关物质B(6-(5-氯吡啶-2-基)-7-羟基-5,6-二氢吡咯并[3,4-b]吡嗪-5-酮)。
|
图 4 有关物质1[M+H]+(m/z 263)离子的二级质谱图及其裂解途径 Figure 4 MS/MS spectrum of related substance 1[M+H]+(m/z 263)ion and its fragmentation pathway |
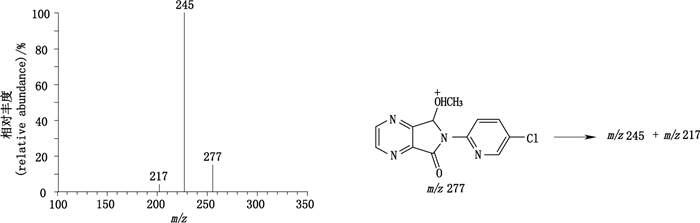
有关物质2:ESI+-TOF/MS测得有关物质2的[M+H]+的准确质量为277.049 0,与离子式C12H10ClN4O2+相应,比佐匹克隆少C5H8N2O,与佐匹克隆丢失氨基甲酰单元后生成甲氧基相符。MS/MS(图 5)中m/z 245和217主要特征碎片离子与佐匹克隆的相应特征离子相同。有关物质2是氧化条件下,佐匹克隆脱氨基甲酰单元的降解产物(6-(5-氯吡啶-2-基)-7-甲氧基-5,6-二氢吡咯并[3,4-b]吡嗪-5-酮)。
|
图 5 有关物质2[M+H]+(m/z 277)离子的二级质谱图及其裂解途径 Figure 5 MS/MS spectrum of related substance 2[M+H]+(m/z 277)ion and its fragmentation pathway |
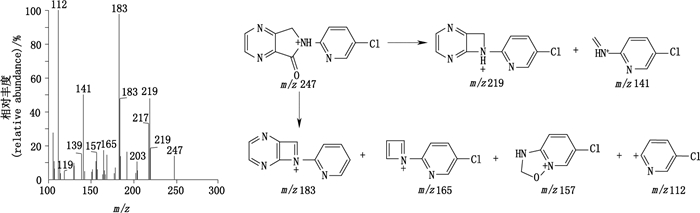
有关物质3:ESI+-TOF/MS测得有关物质3的[M+H]+的准确质量为247.038 2,与离子式C11H8ClN4O+相应,比佐匹克隆少C6H10N2O2,与佐匹克隆丢失氨基甲酸酯单元对应。[M+H]+和m/z 219的碎片离子裂解规律(图 6)与佐匹克隆m/z 245和m/z 217的特征碎片相符,仅不饱和度差1,结合合成工艺,确证有关物质3为佐匹克隆脱氨基甲酸酯单元的主要降解产物,即为欧洲药典规定的有关物质C(6-(5-氯吡啶-2-基)-5,6-二氢吡咯并[3,4-b]吡嗪-5-酮)。
|
图 6 有关物质3[M+H]+(m/z 247)离子的二级质谱图及其裂解途径 Figure 6 MS/MS spectrum of related substance 3[M+H]+(m/z 247)ion and its fragmentation pathway |
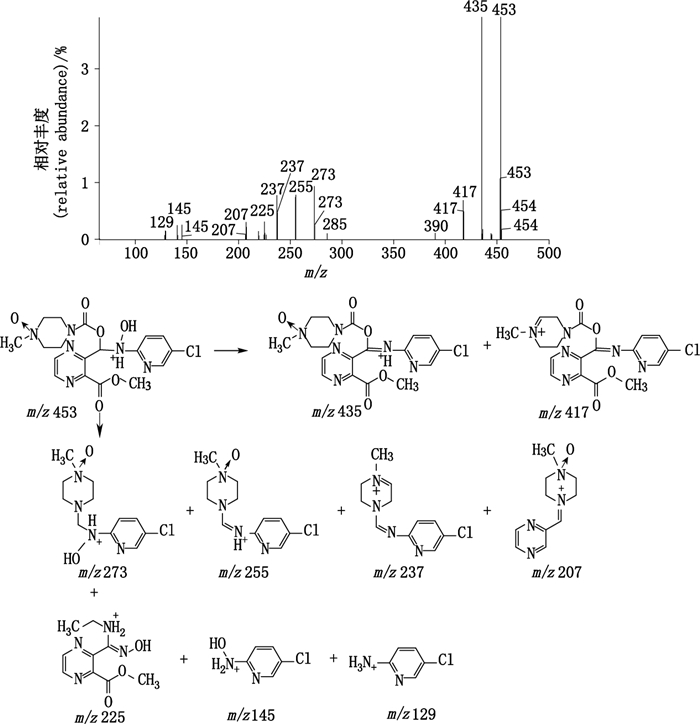
有关物质4:ESI+-TOF/MS测得有关物质4的[M+H]+的准确质量为453.128 4,与离子式C18H22ClN6O6+相应,比佐匹克隆多CH4O3。二级碎片中存在失水碎片m/z 435([M+H]+-H2O)和417([M+H]+-2H2O)(图 7),因此[M+H]+中应包含羟基或氧取代。m/z 129和145的碎片离子分别与佐匹克隆ACP单元和羟基取代ACP对应,由此确证吡咯环的氮原子上被羟基取代。[M+H]+的m/z 273、255、237和207特征碎片离子与佐匹克隆特征碎片不同,可以丢失完整的哌嗪单元或吡啶单元,证明二氢吡咯环为开环结构,结合合成工艺可知开环后哌嗪上连有羧基,易与甲醇反应生成甲酸酯。m/z 273的碎片离子为佐匹克隆的氨基甲酸酯单元丢失CO2后,再丢失吡嗪环单元形成,结合哌嗪环的易氧化性质,确证哌嗪环氧化生成N-氧化物。有关物质4是在高温条件下,佐匹克隆哌嗪环在空气中被氧化为氮氧化物,同时二氢吡咯开环形成甲酸酯的降解产物。
|
图 7 有关物质4[M+H]+(m/z 453)离子的二级质谱图及其裂解途径 Figure 7 MS/MS spectrum of related substance 4[M+H]+(m/z 453)ion and its fragmentation pathway |
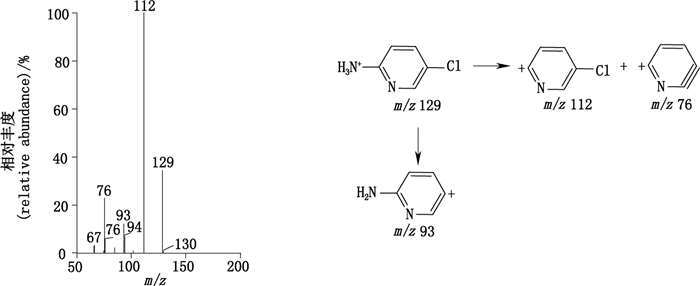
有关物质5:ESI+-TOF/MS测得有关物质5的[M+H]+的准确质量为129.021 1,与离子式C5H6ClN2+相应,比佐匹克隆少C12H12N4O3。m/z 112和93的碎片离子分别为[M+H]+丢失NH3和HCl产物(图 8);m/z 76的碎片离子为[M+H]+同时丢失HCl和NH3产物。有关物质5主要在酸碱条件下,由佐匹克隆的二氢吡咯环开环丢失哌嗪及吡嗪单元产生,结合合成工艺,确证有关物质5为佐匹克隆合成起始原料ACP,即为欧洲药典规定的有关物质2-氨基-5-氯吡啶。
|
图 8 有关物质5[M+H]+(m/z 129)离子的二级质谱图及其裂解途径 Figure 8 MS/MS spectrum of related substance 5[M+H]+(m/z 129)ion and its fragmentation pathway |
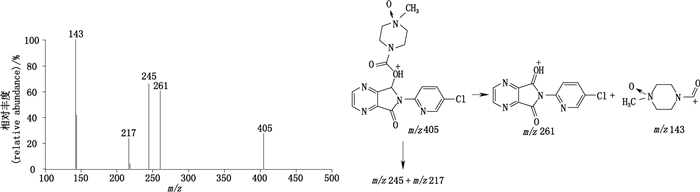
有关物质6:ESI+-TOF/MS测得有关物质6的[M+H]+的准确质量为405.107 3,与离子式C17H18ClN6O4+相应,比佐匹克隆多1个O原子。m/z 261的碎片离子与[M+H]+丢失氨基甲酰单元对应(图 9);m/z 143的碎片离子与佐匹克隆相应特征离子仅O原子位置不同。有关物质6在氧化和光照条件下易产生,结合哌嗪环易被氧化特性,确证为N-氧化佐匹克隆,即为欧洲药典规定的有关物质A。
|
图 9 有关物质6[M+H]+(m/z 405)离子的二级质谱图及其裂解途径 Figure 9 MS/MS spectrum of related substance 6[M+H]+(m/z 405)ion and its fragmentation pathway |
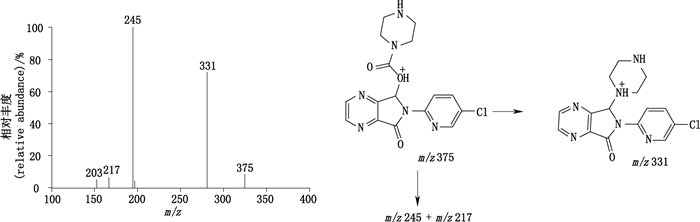
有关物质7:ESI+-TOF/MS测得有关物质7的[M+H]+的准确质量为375.095 8,与离子式C16H16ClN6O3+相应,比佐匹克隆少CH2。m/z 331的特征碎片离子比m/z 345的佐匹克隆特征碎片离子少12,对应1个CH2,裂解规律与佐匹克隆一致(图 3)。m/z 245和217的主要特征碎片离子与佐匹克隆的相应特征离子相同。结合合成工艺,确证有关物质7为哌嗪环上少1个CH2,生成N-去甲基佐匹克隆(图 10)。
|
图 10 有关物质7[M+H]+(m/z 375)离子的二级质谱图及其裂解途径 Figure 10 MS/MS spectrum of related substance 7[M+H]+(m/z 375)ion and its fragmentation pathway |
本研究建立了液-质联用色谱条件用于佐匹克隆有关物质分离和检测鉴定。
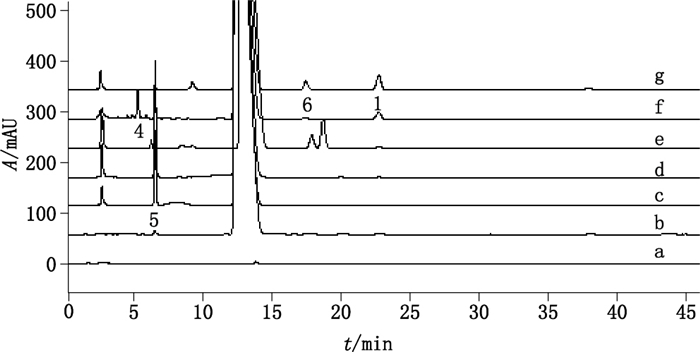
各国药典中关于佐匹克隆有关物质的检测均使用离子对色谱法,这是因为佐匹克隆极性较大,在普通C18色谱柱上保留很弱,然而这种流动相体系无法应用于液-质联用色谱。因此本研究建立LC-MS条件时,比较了Inertsustain C18柱(250 mm×4.6 mm,5 μm)和阳离子交换柱Phenomenex Luna 5u SCX 100A(250 mm×4.6 mm,5 μm),发现C18色谱柱条件中主成分保留较弱,保留机制与离子对条件完全不同,且工艺杂质有关物质3和7均未检出(图 11)。因此最终选择阳离子交换色谱柱条件,流动相为普通的甲醇-乙腈-醋酸盐缓冲液体系。本研究优化了流动相组成及pH,比较了甲醇-醋酸盐缓冲液体系、乙腈-醋酸盐缓冲液体系以及甲醇-乙腈-醋酸盐缓冲液体系,最终选择了pH 4.0的甲醇-乙腈-醋酸盐缓冲液体系。
|
a. 0.1%自身对照溶液(0.1% self-reference solution)b.佐匹克隆供试品溶液(zopiclone test sample solution)c.氧化破坏溶液(forced degradation solution under oxidation stress)d.酸破坏溶液(forced degradation solution under acid stress)e.碱破坏溶液(forced degradation solution under base stress)f.干法热破坏溶液(forced degradation solution under dry heat stress)g.干法光破坏溶液(forced degradation solution under photolysis stress) 图 11 佐匹克隆及其强制降解供试品溶液的高效液相色谱图 Figure 11 HPLC chromatograms of zopiclone and its forced degradation solutions |
在建立的色谱-质谱条件下共检测到7个有关物质,其中已知有关物质4个,未知有关物质3个。结合佐匹克隆合成工艺及强制降解试验结果,可将其分为3类:由起始原料引入的有关物质、合成副产物和降解产物。有关物质5是合成起始原料,在酸碱破坏中易产生。有关物质6和有关物质7均由反应原料1-氯甲酰基-4-甲基哌嗪引入,其中有关物质6为N-氧化佐匹克隆,在氧化条件下易产生;有关物质7为N-去甲基佐匹克隆,在光照条件下易产生。有关物质1和有关物质3均为6-(5-氯-2-吡啶基)-5,7-二氧-5,6-二氢吡咯并[3,4-b]吡嗪还原过程中产生,有关物质1是反应产物,有关物质3是反应副产物,均由佐匹克隆在光照条件下丢失氨基甲酸酯单元产生。有关物质2是氧化条件下,佐匹克隆丢失氨基甲酰单元后,7位羟基发生取代反应生成的羟甲基化合物。有关物质4是在高温条件下,佐匹克隆中哌嗪环在空气中被氧化生成氮氧化物,同时二氢吡咯开环形成甲酸酯的产物。
通过色谱-质谱联用技术对佐匹克隆有关物质进行分析研究,对其工艺杂质来源和降解途径进行了探讨,为其质量控制和工艺优化提供了依据,为稳定性研究奠定了基础。
| [1] |
ABDELRAHMAN MM, NAGUIB IA, EL GHOBASHY MR, et al. Quantitative determination of zopiclone and its impurity by four different spectrophotometric methods[J]. Spectrochim Acta Part A Mol Biomol spectrosc, 2015, 137: 617. DOI:10.1016/j.saa.2014.08.071 |
| [2] |
RÖSNER S, SOYKA M, HAJAK G, et al. Zopiclone for insomnia[J]. Cochrane Database Syst Rev, 2013(8. Art. No.): CD010701. |
| [3] |
DÄMGEN K, LÜDDENS H. Zaleplon displays a selectivity to recombinant GABAA receptors different from zolipdem, zopiclone and benzodiazepines[J]. Neurosci Res Commun, 2015, 25(3): 139. |
| [4] |
PINTO LR, BITTENCOURT LR, TREPTOW EC, et al. Eszopiclone versus zopiclone in the treatment of insomnia[J]. Clinics, 2016, 71(1): 5. |
| [5] |
SWAMY PV, SUSHMA P, CHIRAG G, et al. Parenteral formulation of zopiclone[J]. Indian J Pharm Sci, 2008, 70(1): 99. DOI:10.4103/0250-474X.40342 |
| [6] |
SWAPNA N, JITHAN A. Preparation, characterization and in vivo evaluation of parenteral sustained release microsphere formulation of zopiclone[J]. J Young Pharm, 2010, 2(3): 223. DOI:10.4103/0975-1483.66792 |
| [7] |
LEUFKENS TR, RAMAEKERS JG, de WEERD AW, et al. Residual effects of zopiclone 7.5 mg on highway driving performance in insomnia patients and healthy controls:a placebo controlled crossover study[J]. Psychopharmacology, 2014, 231(14): 2785. |
| [8] |
HJELMELAND K, GUSTAVSEN I, ØIESTAD EL, et al. Zopiclone concentrations in oral fluid and blood after, administration of therapeutic doses of zopiclone[J]. Forensic Sci Int, 2017, 278: 177. DOI:10.1016/j.forsciint.2017.07.004 |
| [9] |
TONON MA, JABOR VA, BONATO PS. Enantioselective analysis of zopiclone and its metabolites in plasma by liquid chromatography/tandem mass spectrometry[J]. Anal Bioanal Chem, 2011, 400(10): 3517. DOI:10.1007/s00216-011-5033-0 |
| [10] |
NILSSON GH, KUGELBERG FC, KRONSTRAND R, et al. Stability tests of zopiclone in whole blood[J]. Forensic Sci Int, 2010, 200(1-3): 130. DOI:10.1016/j.forsciint.2010.04.001 |
| [11] |
EL-SHAHENY RN, ALATTAS A, NASR JJ, et al. Simultaneous determination of zopiclone and its degradation product and main impurity(2-amino-5-chloropyridine)by micellar liquid chromatography with time-programmed fluorescence detection:preliminary investigation for biological monitoring[J]. J Chromatogr B Anal Technol Biomed Life Sci, 2012, 907: 49. DOI:10.1016/j.jchromb.2012.08.034 |
| [12] |
刘惠军, 吴丽红. 佐匹克隆原料及片剂有关物质的HPLC测定[J]. 中国药学杂志, 2008, 43(12): 954. LIU HJ, WU LH. Determination of related substances of zopiclone and its tablets by HPLC[J]. Chin Pharm J, 2008, 43(12): 954. DOI:10.3321/j.issn:1001-2494.2008.12.021 |
| [13] |
TONON MA, BONATO PS. Capillary electrophoretic enantioselective determination of zopiclone and its impurities[J]. Electrophoresis, 2012, 33(11): 1606. DOI:10.1002/elps.201100583 |
| [14] |
NILSSON GH, KUGELBERG FC, AHLNER J, et al. Quantitative analysis of zopiclone, N-desmethylzopiclone, zopiclone N-oxide and 2-amino-5-chloropyridine in urine using LC-MS-MS[J]. J Anal Toxicol, 2014, 38(6): 327. DOI:10.1093/jat/bku042 |
| [15] |
TYAGI OD, SRIVASTAVA TK, PRASAD VSR, et al. Preparation of Zopiclone and Its Enantiomerically Enriched Isomer: US, 8309723 B2[P]. 2012-11-13
|
| [16] |
李光跃, 丁艳.一种佐匹克隆的制备方法: 中国, 103664952 A[P]. 2014-03-26 LI GY, DING Y. A Method for Preparation of Zopiclone: China, 103664952 A[P]. 2014-03-26 |
| [17] |
沈大冬, 姜金娣, 张金霞, 等. 右旋佐匹克隆的合成新方法[J]. 中国药物化学杂志, 2014, 24(5): 387. SHEN DD, JIANG JD, ZHANG JX, et al. Novel synthesis of eszopiclone[J]. Chin J Med Chem, 2014, 24(5): 387. |
| [18] |
RIEMER D, HIRAPARA P, DAS S. Chemoselective synthesis of carbamates using CO2 as carbon source[J]. ChemSusChem, 2016, 9(15): 1916. DOI:10.1002/cssc.v9.15 |
| [19] |
董宇, 仇峰, 张玉峰, 等. 氨基甲酸酯类化合物电喷雾多级质谱分析中一种特殊的中性丢失CO2的重排反应[J]. 质谱学报, 2005, 26(1): 6. DONG Y, QIU F, ZHANG YF, et al. An unusual rearrangement process of neutral loss of CO2 in carbamates by electrospray ionization-multistage mass spectrometry[J]. J Chin Mass Spectrom Soc, 2005, 26(1): 6. DOI:10.3969/j.issn.1004-2997.2005.01.002 |
 2019, Vol. 39
2019, Vol. 39 
