| 单晶LiNi0.83Co0.1Mn0.07O2正极材料的合成及电化学性能 |
b. 江西理工大学,动力电池及其材料重点实验室,江西 赣州 341000
b. School of Materials Science and Engineering; b. Jiangxi Key Laboratory of Power Battery and Materials, Jiangxi University of Science and Technology, Ganzhou 341000, Jiangxi, China
近年来,随着电动汽车行业的蓬勃发展,动力电池的性能的缺陷渐渐暴露出来,例如,能量和功率密度的不足。富镍的LiNixCoyMn1-x-yO2(x > 0.8)正极材料因其具有较大的放电容量且材料的价格低廉,从而在电动汽车行业引起极大的关注。但是,这些材料在充放电过程中会发生严重的性能退化,如电压降低时结构发生剧烈的转变,尤其是在高温、高电压(> 4.3 V)的测试条件下,材料的结构处于高度脱锂状态[1-4]。应对上述问题,许多学者提出了针对性的解决方案,主要针对其性能优化的研究。如:组分调节,将材料表面涂层和改善形貌[5-8]。经研究分析,氧替代阴离子和采取颗粒形貌控制是改善电化学性能最有效的2个方法。学者通过大量研究,发现单晶镍钴锰三元正极材料颗粒表面较光滑、一次颗粒大小均匀,这使材料能充分接触导电剂,显著提高锂离子传输能力[9-13]。单晶正极材料不仅在较高电压条件下可以极大发挥材料的放电容量,还可以提高材料的结构稳定性、循环性能等[14]。正是因为单晶正极材料具有这些优点,在当下的企业与各大高校,单晶正极材料成为热门的研究方向。
本文采用共沉淀-高温固相法合成了单晶型LiNi0.83Co0.1Mn0.07O2锂离子电池正极材料。经过测试,该材料为单晶材料,减小了与电解液的接触面,大大降低电池循环过程中产生的副反应,进而提高材料的电化学性能。
1 实验三元镍钴锰前驱体的制备:将硫酸镍、硫酸钴、硫酸锰原料按摩尔比n(Ni):n(Co):n(Mn)=0.83:0.1:0.07称量,混合后加入去离子水配成金属离子浓度为2 mol/L的溶液。称取NaOH并加入络合剂氨水溶液与去离子水配成4 mol/L的混合碱溶液(氨水浓度为0.5 mol/L)。通过蠕动泵分别将2种溶液滴入装有底液的反应釜中,并保持反应釜内部温度在55 ℃左右,在320 r/min搅拌速度下进行沉淀反应,反应过程中持续通氮气进行保护,待充分反应后继续搅拌3 h。最后将反应得到的沉淀物陈化12 h后开始对料液进行固液分离,分离后的固体产物经洗涤、烘干后,得到具有小粒径且一次颗粒偏大的镍钴锰前驱体。
将上述步骤得到的前驱体,按照锂配比n(Li): n(M)=1.09(M是前驱体中金属元素总称)称取相应的碳酸锂和前驱体并使用球磨机将其混合均匀,在通入纯氧的管式炉内进行第1次烧结,共制备3份材料。设计的烧结制度为:从室温25 ℃加热1.5 h到550 ℃,在550 ℃下保温4 h后快速升温到750 ℃并保温4 h,保温结束后分别快速升温到840、860、880 ℃并保温烧结15 h,再随炉温自然冷却,冷却后进行破碎处理得到最初的3份单晶正极材料。将最初得到的正极材料置于通入氧气的管式炉中进行第2次烧结:从室温加热3 h到750 ℃,然后在750 ℃下保温5 h,再随炉温自然冷却,将冷却所得物料经粉体处理,得到3份单晶正极材料样品[15-16]。
采用日本理学MiniFlex 600型转靶衍射仪(XRD)对产物进行物相分析,测试条件为:Cu Kα辐射,λ=0.154 06 nm,60 kV管电压,50 mA管电流,扫描范围2θ=10°~80°,步长为0.02°,扫描速率为2°/min;采用德国ZEISS EVO/MA10型扫描电镜表征对所得到的材料进行测试。
以制备好的单晶正极材料、黏结剂PVDF、导电剂SP三者按质量比80:10:10称取一定质量,固含量按45%确定NMP的量。先将PVDF溶于NMP中,再将称取好的正极材料样品、导电材料SP放入研钵中手动研磨均匀后,将溶解好的PVDF加入混好的固体材料中,球磨机匀浆10 h后得到成黏稠度合适的流动性浆料,通过涂布机将制备好的浆料均匀地涂敷在集流体铝箔上,在120 ℃鼓风干燥箱干燥30 min后裁片并制备成实验需要的正极极片,其中金属锂片作为负极。最后将制备好的极片在充有氩气保护的手套箱中分别组装成CR2032扣式电池进行检测,电压设定为2.75~4.3 V,使用中国深圳市新威尔电子有限公司生产的电化学测试仪设备进行电化学性能测试。
此外,本文将使用赣峰锂业公司生产的LiNi0.83Co0.1Mn0.07O2多晶二次颗粒样品,与实验合成性能较好的单晶材料作为对照。
2 结果与讨论 2.1 SEM分析图 1所示是LiNi0.83Co0.1Mn0.07O2在不同温度下制备的a1、a2、a3样品扫描电子显微镜图,从图 1可以看出,随温度的逐渐增加,样品的颗粒粒径不断变大:①在840 ℃条件下制备的a1样品,一次颗粒较小,大部分在0.5 μm左右,且还有部分较大的颗粒,单晶颗粒也相对较小;②在860 ℃条件下制备的a2样品粒度分布比较集中,颗粒单晶度较高、表面较为光滑、颗粒形貌较为完整并且结晶度也较高,大部分一次颗粒粒径在1 μm左右;③在880 ℃条件下制备的a3样品一次颗粒较少,大部分颗粒已经团聚在一起,单晶颗粒已经不明显,大部分团聚颗粒粒径超过1 μm。对于单晶材料来说颗粒并不是越大越好,太大容易造成Li+/Ni2+混排,并且降低正极材料的导电能力,最终影响单晶正极材料的电化学性能[17-18]。从a1、a2、a3样品对比可以明显得出a2样品形貌、颗粒粒径、分散程度是实验所需要的,a1样品的颗粒太小,比表面积较大,容易与电解液反应导致材料的循环性能下降,而a3样品大部分一次颗粒已经团聚成为较大的二次颗粒团聚体,与实验需要的一次颗粒单晶体相反,且颗粒太大对于锂离子的传输性能有不利的影响,阻抗也会变大。
 |
| 图 1 样品扫描电镜像 Fig. 1 The SEM images of samples |
通过图 1的形貌观察并对比分析,a2样品满足了本文实验所需要的单晶形貌,所以选择a2样品继续实验。图 2所示是单晶样品a2一次颗粒与多晶二次颗粒样品(多晶样品为赣峰锂业公司生产)扫描电子显微镜图,从图 2(a)中可以看出,材料粒度分布比较集中,颗粒单晶度较高、表面较为光滑、少数由一次粒团聚形成,大部分一次颗粒粒径超过了1 μm。图 2(b)所示是多晶材料的类球形二次颗粒图,球形二次颗粒表面疏松多孔,其一次颗粒大部分粒径为0.3~0.4 μm,仅有少数较大一次颗粒存在。对于多晶材料而言,虽然一次颗粒较小有利于充放电性能提高,但是与此同时将会增加材料的比表面积,导致材料容易与电解液反应,不利于稳定循环。此外,由一次颗粒团聚形成的球形颗粒在循环后期会因为相变应力的积累导致二次颗粒破碎产生新表面,与电解液反应导致循环性能降低。
 |
| 图 2 单晶与多晶样品扫描电镜像 Fig. 2 The SEM images of single crystal and polycrystalline samples |
2.2 RD分析
图 3所示为单晶样品a1、a2、a3的XRD测试图。
 |
| 图 3 单晶样品的XRD图谱 Fig. 3 XRD patterns single crystal of samples |
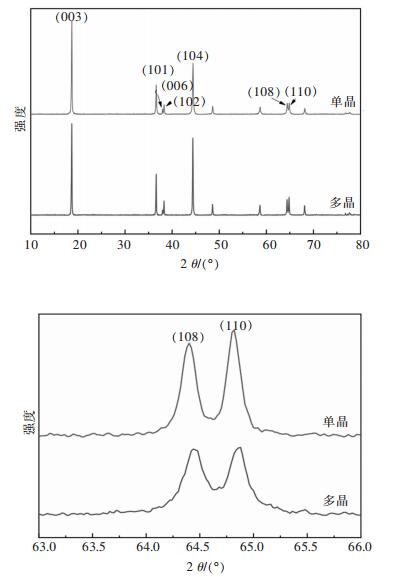
通过与LiNiO2的标准PDF卡片(PDF#09-0063)对比发现,样品均为六方晶系α-NaFeO2层状结构,属于R-3 m点群,结晶度较高,且没有明显的杂质峰。样品中(006)/(102)和(108)/(110)两对衍射峰分裂较为明显,I(003)/I(104)分别是1.3、1.8和1.18,其中a1和a2样品的I(003)/I(104)比值均大于1.2,表明这两个样品都具有良好的层状结构、阳离子混排程度较轻[19]。而a3样品的I(003)/I(104)比值小于1.2,说明该样品的阳离子混排较为严重。
图 4所示是阳离子混排程度最轻的单晶样品a2与多晶颗粒样品的XRD测试图,2种材料都具有较轻的阳离子混排。此外,单晶样品a2的(108)与(110)的峰强度和分裂程度明显大于多晶颗粒样品,所以样品a2具有更加良好的层状结构。综合以上分析说明本实验制备的单晶材料a2将具有良好结构稳定性、较好锂离子脱嵌能力、较好的循环性能。
 |
| 图 4 单晶与多晶样品的XRD图谱 Fig. 4 XRD patterns single crystal and polycrystalline of samples |
2.3 电化学性能分析
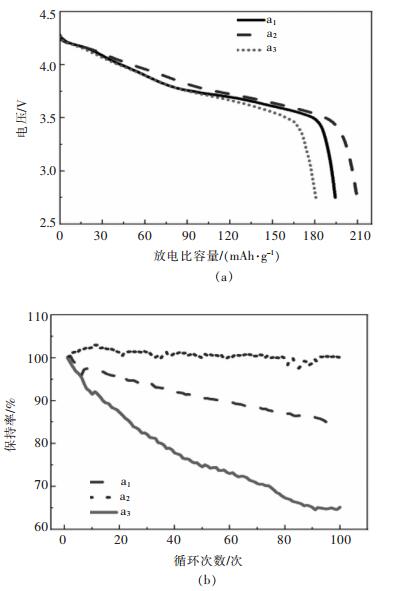
图 5所示是不同温度下烧制的单晶样品电化学性能对比图,图 5(a)是单晶样品放电比容量对比图,图 5(b)是不同温度下烧制的样品克容量保持率对比图,从图 5(a)可得,a1、a2、a3的放电比容量分别为194.3、209.06、180.5 mAh/g,从图 5(b)可知a1、a2、a3的克容量保持率分别为84.3%、100.09%、65.13%。通过对比发现,860 ℃烧制的a2单晶样品克容量最高、克容量保持率最高。840 ℃条件下制备的a1单晶样品无论是克容量的发挥还是循环稳定性都较860 ℃烧制的a2单晶样品差,说明烧结温度较低,前驱体与碳酸锂反应不充分、单晶颗粒的生长发育不完整和小颗粒与电解液发生副反应等一系列问题影响了材料的电化学性能发挥。880 ℃烧制的a3单晶样品电化学性能较a2单晶样品更差,说明烧结温度进一步提高,导致单晶颗粒生长过大、颗粒相互团聚、阳离子混排加剧和循环后期二次颗粒破碎后与电解液反应等问题降低了材料的电化学性能。因此,选择合适的烧结制度对材料的性能发挥至关重要[20-21]。
 |
| 图 5 不同温度烧制单晶样品的化学性能对比 Fig. 5 Comparison of chemical properties of single crystal samples by different temperatures |
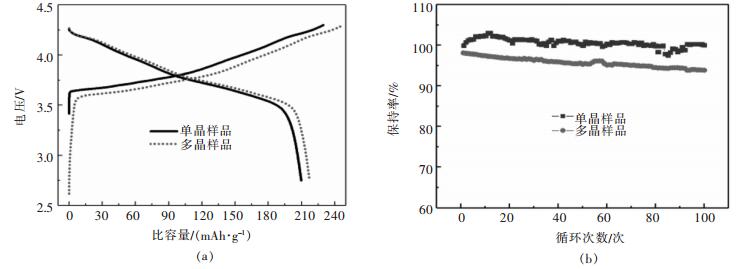
图 6所示是性能较好的a2单晶样品与多晶颗粒样品的电化学性能对比图,图 6(a)是多晶与单晶样品的首次充放电比容量对比图,图 6(b)是多晶与单晶样品的克容量保持率对比图,从图 6(a)可知,单晶与多晶样品首次放电比容量分别为209.63、217 mAh/g,首次库仑效率分别为91.19%、87.9%,由图 6(b)可得单晶样品与多晶样品循环100圈后克容量保持率分别为100.09%、93.84%。通过对比可知,单晶样品的首效最高、克容量保持率最高且循环非常稳定,但是会损失一部分放电容量;多晶样品的容量发挥较好是因为其具有较小的一次颗粒有利于充放电,但是多晶材料较小的一次颗粒以及循环后期二次颗粒破碎后产生的新表面,也容易与电解液发生副反应,导致首效较低、循环性能衰退。
 |
| 图 6 单晶与多晶样品电化学性能对比 Fig. 6 Comparison of electrochemical performance of single crystal and polycrystalline samples |
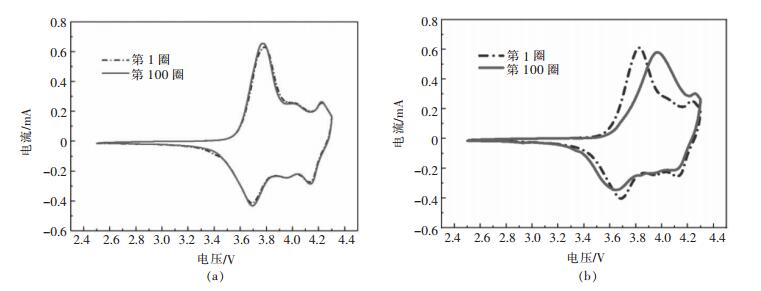
图 7所示是860 ℃条件下烧制单晶样品a2与多晶样品的循环第1圈和第100圈的循环伏安曲线对比图,图 7(a)表示单晶样品第1圈和第100圈循环伏安曲线基本重合,有两对明显的氧化还原峰,且峰出现的位置一致,说明单晶材料在循环的过程中晶体结构是非常稳定的[22-23]。从图 7(b)可知市场上的多晶样品第1圈和第100圈循环伏安曲线已不重合,且其中第100圈的一对氧化还原峰已经不明显,说明材料的结构发生了不可逆变化,容量已经出现明显衰退。综合对比分析可知,860 ℃条件下烧制单晶样品a2较多晶样品具有更好的循环稳定性。
 |
| 图 7 单晶和多晶样品不同循环次数的循环伏安曲线 Fig. 7 Cyclic voltammetry curves of single crystaland and polycrystalline samples with different cycles |
3 结论
1)通过设计合理烧结制度并对温度进行考察,发现在860 ℃条件下烧制的单晶型颗粒正极材料,提高了Li+ 传输性能的同时减少了材料表面和电解液之间的界面反应,具有较优库仑效率和循环性能。首次充电比容量达到了209.63 mAh/g,首效为91.19%,循环100圈后容量保持率为100.09%。
2)与市场上的多晶LiNi0.83Co0.1Mn0.07O2三元正极材料相比,单晶LiNi0.83Co0.1Mn0.07O2正极材料的循环性能更优,容量发挥差距不是很大。该单晶材料将在一定程度上为解决高镍三元正极材料循环不稳定的现象提供一种解决方法,具相当大的市场应用前景。
| [1] |
MANTHIRAM A, SONG B, LI W. A perspective on nickel-rich layered oxide cathodes for lithium-ion batteries[J].
Energy Storage Materials, 2017(6): 125–139. DOI: 10.1016/j.ensm.2016.10.007. |
| [2] |
ZHANG J, YANG Z, GAO R, et al. Suppressing the structure deterioration of Ni-rich LiNi0.83Co0.1Mn0.07O2 through atom-scale interfacial integration of self forming hierarchical spinel layer with Ni gradient concentration[J].
ACS Applied Materials Interfaces, 2017, 9: 29794–29803. DOI: 10.1021/acsami.7b08802. |
| [3] |
HWANG S, JO E, CHUNG K Y, et al. Structural evolution of LiNiyMnzCo1-y-zO2 cathode materials during high-rate charge and discharge[J].
Journal Physical Chemistry Letts, 2017(8): 5758–5763. DOI: 10.1002/chin.197346146. |
| [4] |
ZHANG H, KARKI K, HUANG Y, et al. Atomic insight into the layered/spinel phase transformation in charged LiNi0.80Co0.15Al0.05O2 cathode particles[J].
Journal Physical Chemistry C, 2017, 121: 1421–1430. DOI: 10.1021/acs.jpcc.6b10220. |
| [5] |
LIU W, LI X, XIONG D, et al. Significantly improving cycling performance of cathodes in lithium ion batteries: the effect of Al2O3 and LiAlO2 coatings on LiNi0.6Co0.2Mn0.2O2[J].
Nano Energy, 2018, 44: 111–120. DOI: 10.1016/j.nanoen.2017.11.010. |
| [6] |
ZHANG L, WANG H, WANG L, et al. High electrochemical performance of hollow corn-like LiNi0.83Co0.1Mn0.07O2 cathode material for lithium-ion batteries[J].
Applied Surface Science, 2018, 450: 461–467. DOI: 10.1016/j.apsusc.2018.04.224. |
| [7] |
HAO Y, SONG W, WANG M, et al. Lithium-ion conductive coating layer on nickel rich layered oxide cathode material with improved electrochemical properties for Li-ion battery[J].
Journal Alloys and Compounds, 2019, 784: 1311–1322. DOI: 10.1016/j.jallcom.2019.01.072. |
| [8] |
WU F, LI Q, CHEN L, et al. Use of Ce to reinforce the interface of Ni-rich LiNi0.83Co0.1Mn0.07O2 cathode materials for lithium-ion batteries under high operating voltage[J].
CHEMSUSCHEM, 2019, 12: 935–943. DOI: 10.1002/cssc.201802304. |
| [9] |
LIU W, OH P, LIU X, et al. Nickel-rich layered lithium transition-metal oxide for high-energy lithium-ion batteries[J].
Angewandte Chemie-International Edition, 2015, 54(15): 4440–4457. DOI: 10.1002/anie.201409262. |
| [10] |
LIANG L, DU K, PENG Z, et al. Co-precipitation synthesis of Ni0.6Co0.2Mn0.2(ОH)2 precursor and characterization of LiNi0.6Co0.2Mn0.2O2, cathode material for secondary lithium batteries[J].
Electrochimica Acta, 2014, 130: 82–89. DOI: 10.1016/j.electacta.2014.02.100. |
| [11] |
KIM T, PARK J, CHANG S K, et al. The current move of lithium ion batteries towards the next phase[J].
Advanced Energy Materials, 2012, 7(2): 860–872. |
| [12] |
肖建伟, 刘良彬, 符泽卫, 等. 单晶LiNixCoyMn1-x-yO2三元正极材料研究进展[J].
电池工业, 2017, 21(2): 51–54.
|
| [13] |
KIM J, LEE H, CHA H, et al. Prospect and reality of Ni-rich cathode for commercialization[J]. Advanced Energy Materials, 2017: 1702028.
|
| [14] |
YUE P, WANG Z, LI X, et al. The enhanced electrochemical performance of LiNi0.6Co0.2Mn0.2O2 cathode materials by low temperature fluorine substitution[J].
Electrochimica Acta, 2013, 95: 112–118. DOI: 10.1016/j.electacta.2013.02.037. |
| [15] |
NOH H J, YOUN S J, YOON C S, et al. Comparison of thestructural and electrochemical properties of layered Li[NixCoyMnz]O2(x=1/3, 0.5, 0.6, 0.7, 0.8 and 0.85) cathode material for lithium-ion batteries[J].
Journal Power Sources, 2003, 233(1): 121–130. DOI: 10.1016/j.jpowsour.2013.01.063. |
| [16] |
唐爱东, 黄可龙. 合成温度对六方Li-Ni-Co-Mn-O固溶体结构和性能的影响[J].
金属学报, 2005, 41(12): 1280–1284.
|
| [17] |
LlN Y K, LU C H. Preparation and electrochemical properties of layer-structured LiNi1/3Co1/3Mn1/3-yAlyO2[J].
Journal Power Sources, 2009, 189: 353–358. DOI: 10.1016/j.jpowsour.2008.08.072. |
| [18] |
LOVE C T, JOHANNES M D, SWIDER-LYONS K. Thermal stability of delithiated Al-substituted Li(Ni1/3Co1/3Mn1/3)O2 cathodes[J].
ECS Transactions, 2010, 25: 231–240. |
| [19] |
WANG M, CHEN Y B, WU F, et al. Characterization of yttrium substituted LiNi0.33Mn0.33Co0.33O2 cathode material for lithium secondary cells[J].
Elect Rochimica Acta, 2010, 55(28): 8815–8820. DOI: 10.1016/j.electacta.2010.08.022. |
| [20] |
CHIO J M, MANTHIRAM A. Role of chemical and structural stabilities on the electrochemical properties of layered LiNi1/3Co1/3Mn1/3O2 cathodes[J].
Journal of The Electrochemical Society, 2005, 152: 1714–1718. DOI: 10.1149/1.1954927. |
| [21] |
IDEMOTO Y, MATSYI T. Thermodynamic stability, crystal structure, and cathodic performance of LixNi1/3Co1/3Mn1/3O2, depend on the synthetic process and Li content[J].
Diffusion & Reactions, 2008, 179(l7/18): 625–635. DOI: 10.1016/j.ssi.2008.03.024. |
| [22] |
邱世涛, 钟盛文, 李婷婷, 等. Cu掺杂LiNi0.6Co0.2Mn0.2O2的电化学性能[J].
有色金属科学与工程, 2018, 9(5): 21–25.
|
| [23] |
彭弯弯, 徐唱, 李之锋, 等. 面密度和压实密度对锂离子电池快充性能的影响[J].
有色金属科学与工程, 2017, 8(3): 69–73.
|
 2020, Vol. 11
2020, Vol. 11


