| Lewis酸型固体酸催化剂Ce-Ag-PW的制备、表征及催化酯化反应合成生物柴油性能研究 |
生物柴油,作为一种绿色、可生物降解、无毒性的新型可再生能源, 已经引起了世界的广泛关注[1-5]。当前,世界各国纷纷根据各自国家适合种植油料作物的特点,选择不同油料来合成生物柴油,如美国盛产大豆主要以其为原料[6];日本因土地等因素限制,则主要以回收的废弃食用油脂为原料[7]。我国是一个人口大国,每年要消耗约1600万t可食用植物油,约有10%的食用油在使用后被废弃。因此,我国每年产生近160万t的废弃植物油脂[8]。基于该现状,以废弃植物油为原料将是一种不错的选择。然而,要实现废弃油脂为原料生产生物柴油,合成一种能适应于其中含有的复杂成分且能在反应过程中保持高催化活性和稳定性的催化剂非常关键。
本研究尝试采用杂多酸(HPA)为催化剂来合成生物柴油,其是一种环境友好的固体酸催化剂,现已广泛用于酸催化的均相液相反应[9-12]。当前,已有一些研究报道:HPA对动植物油脂(由多种脂肪酸甘油酯构成的混合物)与甲醇经酯交换反应或游离脂肪酸(Free Fatty Acid, FFA)与甲醇经酯化反应合成生物柴油均具有高催化活性[13-15]。以HPA为催化剂合成生物柴油时,主要是使用具有Keggin结构的12系列HPA(分子通式为HnAB12O40·xH2O),如十二硅钨酸、十二磷钨酸和十二磷钼酸等,当前的研究更多偏向于选择十二磷钨酸(HPW)[14]。
HPW通常以液态存在或者固态存在,且均呈现出极强的Brönsted酸性。因而,它极易溶解于极性溶剂,使得在反应结束后难以将其从反应液中分离并循环使用;同时,Brönsted酸位活性中心易与水发生水合反应,从而导致该类催化剂易在富含水的反应介质环境中失去催化活性。近期,本课题组以HPW为基体,通过溶胶凝胶法对其进行了La3+改性作用,合成了固体酸催化剂LaPW12O40/SiO2,并发现其在用于催化以油酸和甲醇为反应物经酯化反应合成生物柴油时具有最高催化活性和稳定性[16]。这是由于La3+具有独特的价电子构型5d1,是一个很好的电子受体,而O原子有一个孤对电子。因此,O和La之间很容易形成配位键。在这过程中,La3+强吸电子作用对Lewis酸位的形成起到促进作用。从而有效避免了HPW催化剂的酸性活性位以Brönsted酸位为主,而易在富含水的反应介质中发生水合作用而降低,甚至失去催化活性的现象发生。由于Ce3+的价电子构型为4f1,相比于La3+,其更容易与O原子形成配位键,从而在催化剂中产生更多的Lewis酸位。然而,Ce3+改性HPW,只是增加其中的Lewis酸位数量,并不能使Brönsted酸位转变为Lewis酸位。考虑到Ag+可置换HPW中的质子,如与Ce3+协同改性HPW,则可使其由Brönsted酸型催化剂转化为Lewis酸型催化剂。
基于上述分析,本研究拟通过稀土Ce3+和Ag+对HPW进行协同改性作用,通过配位成键形成稀土缺位杂多酸配合物,合成一种Lewis酸型催化剂Ce-Ag-PW。通过XRD,FT-IR,SEM,TEM,TG,NH3-TPD,Py-IR,XPS等表征手段对合成的催化剂的物理化学性能进行了表征分析,并以油酸和甲醇为反应物,对Ce-Ag-PW的催化活性和稳定性进行了研究。
1 实验部分 1.1 试剂与仪器试剂:磷钨酸(99%,AR,国药集团化学试剂有限公司),六水合硝酸铈(99.9%,AR,成都艾科达化学试剂有限公司),硝酸银(99.9%,AR,成都艾科达化学试剂有限公司),甲醇(99%,AR,西陇科学股份有限公司),油酸(99%,AR,西陇化工股份有限公司),油酸甲酯(99%,GC,成都艾科达化学试剂有限公司)。
仪器:数控超声波清洗器(KQ-S00DE,昆山市超声仪器有限公司),集热式磁力加热搅拌器(DF-101S,金坛市白塔新宝仪器厂),电子天平(AR223CN,奥豪斯仪器有限公司),电热恒温干燥箱(DHG-9036A,上海精宏实验设备有限公司),循环水式真空泵(SHZ-D(Ⅲ),巩义市予华仪器有限责任公司),气相色谱仪(Agilent 7820A型,美国安捷伦公司)。
1.2 催化剂制备Ce-Ag-PW制备:①在一个50 mL的烧杯中分别加入2 g HPW和10 mL去离子水,用磁力搅拌器搅拌均匀,得到A溶液;②另取一个50 mL的烧杯,分别加入0.1 g硝酸银、0.1 g硝酸铈和10 mL去离子水,搅拌均匀,得到B溶液;③将B溶液逐滴滴加到A溶液中,可观察到溶液由无色变为橙色;④将混合后的溶液放入超声洗涤器中,超声作用30 min,随后移入干燥箱中,并设置温度为80 ℃,直至将溶液蒸发干;⑤所得到的固体物在空气氛围中于120 ℃下煅烧4 h,冷却至室温后用研钵研碎,即得到催化剂Ce-Ag-PW。
1.3 催化剂表征通过TEM(Tecnai G2 F20,美国菲达康有限责任公司)和SEM(FEI-MLA650F场发射扫描电子显微镜,美国FEI公司)对HPW和Ce-Ag-PW催化剂的形貌结构进行了观察;采用XRD(D8 ADVANCE,德国Bruker公司)对HPW和Ce-Ag-PW催化剂的晶型结构进行表征分析,采用Cu Kα为辐射源,管电压40 kV,入射波长λ为0.154 44 nm,管电流40 mA,扫描速度为4°/min,扫描范围5°~90°;通过傅里叶变换红外光谱仪(Magna-IR 750,美国尼高力公司),对HPW和Ce-Ag-PW催化剂的表面官能团结构进行了分析。使用吡啶吸附法对Ce-Ag-PW催化剂的酸性活性位类型进行了分析;采用热重分析仪(Q500,美国TA公司)对HPW和Ce-Ag-PW催化剂的热稳定性进行了分析,测试温度范围为室温到800 ℃,升温速率10 ℃/min;采用多功能自动化程序升温化学吸附仪(ChemiSorb 2720,美国麦克公司)分析了HPW和Ce-Ag-PW催化剂的酸性活性位强度;通过XPS能谱仪(Thermo Scientific Escalab 250Xi,美国赛默飞世科技公司)对Ce-Ag-PW催化剂价键类型进行分析,采用单色Al Kα(hv=1486.6 eV),功率150 W,500 μm束斑。
1.4 催化活性测试以油酸与甲醇为反应物,通过考察不同反应参数条件下油酸转化率的差异,对合成的Ce-Ag-PW催化剂的活性和稳定性进行了测试。反应参数条件如下:反应时间(1~6 h)、反应温度(50~70 ℃)、醇油物质量比(6: 1~18: 1)、催化剂占反应物总质量之比(0.5%~3%)。
油酸与甲醇的酯化反应在250 mL的三口烧瓶中进行,反应装置如图 1所示。实验过程如下:首先,按照一定物质量比,将油酸与甲醇加入到干燥的三口烧瓶中;然后,加入一定质量的Ce-Ag-PW催化剂。在一特定的反应温度下,磁力搅拌并且冷凝回流,每间隔一小时取一次样;最后,将反应产物置于干燥箱中,在90 ℃下加热30 min,蒸发掉未反应的甲醇和反应过程中产生的少量水分。并进一步通过一次性注射器和过滤头除去试样中残留的催化剂,得到提纯后的试样。以甲醇为溶剂,通过5 mL的容量瓶对不同反应时间得到的产物进行定容。通过气相色谱,获得油酸的转化率。
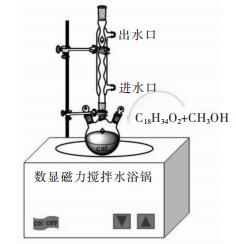 |
| 图 1 油酸与甲醇酯化反应装置简图 Fig. 1 Diagram of esterification unit for oleic acid and methanol |
1.5 油酸甲酯含量测定
采用气相色谱法,以高纯度的油酸甲酯为标样,选择外标法对其进行线性拟合得到标准曲线。仪器条件:色谱柱DB-5(30 m×0.25 mm×0.25 μm);程序升温,分两个阶段:初始温度为40 ℃,以20 ℃/min升温到150 ℃,然后再以4 ℃/min升温到250 ℃。以高纯氮气为载气,柱流速度2 mL/min,柱流量20 mL/min;氢气流量30 mL/min,空气流量400 mL/min;尾吹气流量25 mL/min;FID检测器温度250 ℃;进样口温度250 ℃;分流比20: 1;进样量1 μL。
2 结果与讨论 2.1 催化剂表征结果纯HPW与制备的Ce-Ag-PW催化剂的XRD图谱如图 2所示:纯HPW的杂多阴离子结构在2θ角为10.7°,21.1°,25.4°,28.2°,31.8°,35.9°处分别出现了6个特征峰,以上特征峰与立方晶系H3PW12O40·6H2O(JCPDS 00-050-0304)标准卡片对比基本一致,归属于杂多阴离子的体心立方二级结构[16]。Ce-Ag-PW同样也在2θ值为10.2°、19.6°、24.7°、30.3°处出现了相应的特征峰值。然而,从图 2可以发现:Ce-Ag-PW的XRD谱图中出现的特征峰,整体向着小角度的方向移动。之前,文献[17-18]报道了类似的实验结果,并尝试解释该现象的发生是由于用于改性HPW的金属离子与氢质子发生了交换。因此,这可能是Ag+与HPW中的氢质子发生了交换,由于Ag+比H+的体积大,随着Ag+的加入而使HPW晶格中的轴长度变短,导致单晶胞收缩。由上述分析结果,可以初步判断Ag+与HPW中的H+发生了交换。
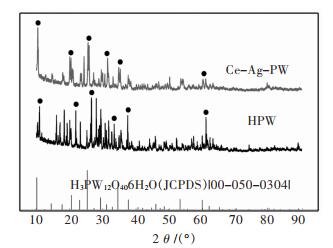 |
| 图 2 HPW和Ce-Ag-PW催化剂的XRD图谱 Fig. 2 XRD patterns of HPW and Ce-Ag-PW catalysts |
为了进一步确定Ce3+和Ag+对HPW改性前后,表面官能团结构是否发生了变化,采用傅里叶红外光谱对HPW和Ce-Ag-PW催化剂进行了表征,结果如图 3所示。
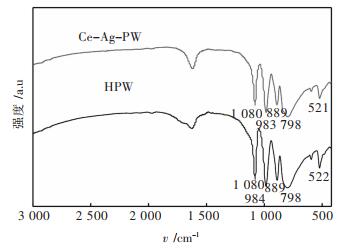 |
| 图 3 HPW和Ce-Ag-PW催化剂的红外光谱 Fig. 3 FTIR spectra of HPW and Ce-Ag-PW catalyst |
由图 3可观察到:Ce-Ag-PW的红外光谱图与纯HPW相似。与HPW相对应的4个杂多阴离子结构特征峰分别出现在1 080、984、889、798 cm-1位置处。以上红外特征峰分别归属于PO4中心四面体中P-O键的伸缩振动、在表面的W=O终端键、八面体中W-Oa-W键桥接的棱角共享伸缩振动、八面体的边缘共享的W-Ob-W键的伸缩振动[19-22]。然而,与Ce-Ag-PW催化剂相对应的特征峰,分别出现在1 080、983、889 cm-1和798 cm-1处,以上变化可能是由于Ag+与Ce3+对HPW的改性作用。此外,HPW和Ce-Ag-PW催化剂均在521 cm-1处出现了对应于O-P-O键伸缩振动的特征峰。因此,Ce-Ag-PW中的杂多阴离子结构并没有被破坏,仍保持着HPW的结构特征。
从扫描电镜和透射电镜可以观察HPW和Ce-Ag-PW催化剂的表面形貌,结果如图 4所示。由图 4(a)、图 4(b)可观察到,相比于纯HPW团聚在一起且为不规则的大块状结构,Ce-Ag-PW出现了分散度良好的立体状结构。同时,由图 4(c)的透射电镜图也可发现,Ce-Ag呈不规则颗粒状且均匀分散在HPW中。
 |
| 图 4 (a)HPW和(b)Ce-Ag-PW催化剂的扫描电镜图和(c)Ce-Ag-PW的透射电镜像 Fig. 4 SEM image of (a) HPW and (b) Ce-Ag-PW and (c)TEM image of Ce-Ag-PW |
对Ce-Ag-PW催化剂的热稳定性进行了热重分析,结果如图 5所示。从图 5可以发现:Ce-Ag-PW催化剂在551 ℃以后质量保持稳定。它的第1个失重平台出现在28~112 ℃,质量损失了0.93%,主要原于表面吸附水损失所导致;第2个失重平台出现在112~300 ℃,质量损失了3.3%,由于该催化剂结晶水损失所导致;第3个失重平台出现在370~600 ℃,质量损失了0.6%,其他研究者也报道了类似的结果[23-24],这可能是Ce3+和Ag+在高温条件下从磷钨杂多阴离子基体中解离出来所致。
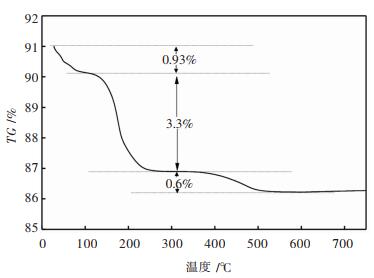 |
| 图 5 Ce-Ag-PW催化剂的热重分析 Fig. 5 TG analysis of Ce-Ag-PW catalyst |
采用氨程序升温脱附对HPW和Ce-Ag-PW催化剂的酸性活性位强度进行了测定,结果如图 6所示。由图 6可知:HPW和Ce-Ag-PW均在100~200 ℃及500~600 ℃处出现了一个分别对应于弱酸位和强酸位的脱附峰。与HPW不同的是,Ce-Ag-PW在300~400 ℃处还出现了一个对应于中强度酸性位的脱附峰。由上述可知:Ce-Ag-PW催化剂的酸性活性位强度要弱于HPW。
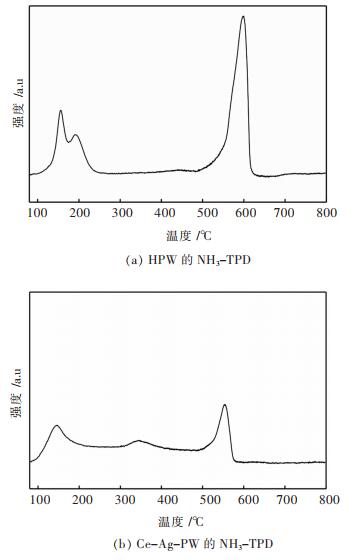 |
| 图 6 HPW和催化剂Ce-Ag-PW的NH3-TPD Fig. 6 NH3-TPD profiles of HPW and Ce-Ag-PW catalyst |
为了进一步证明催化剂Ce-Ag-PW中的Lewis酸性位和Brönsted酸性位类型的存在,采用吡啶吸附法对催化剂进行了分析,分析结果如图 7所示。由图 7可知:Ce-Ag-PW催化剂在1 450 cm-1和1 540 cm-1处别出现了一个归属于Lewis酸性活性位和Brönsted酸性活性位的特征吸收峰[25-26],由此说明Ce-Ag-PW是一种双酸位类型的混合固体酸催化剂。此外,从图 7可知,在波数为1 450 cm-1处出现的特征峰的强度要远强于1 540 cm-1处出现的特征峰,由此表明Ce-Ag-PW是以Lewis酸性位为主的固体酸催化剂,这将有助于其在含水反应介质环境中保持高催化稳定性。
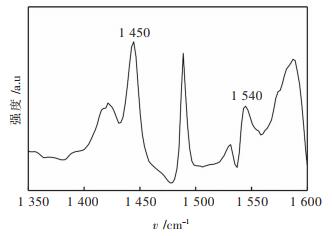 |
| 图 7 Ce-Ag-PW催化剂的吡啶吸附光谱 Fig. 7 Pyridine adsorption IR spectra of Ce-Ag-PW catalyst |
图 8所示为Ce-Ag-PW催化剂X射线光电子能谱图,分别测得W4f,O1s,P2p,Ag3d,Ce3d的窄扫描谱图,用以确定该催化剂中各元素之间形成的价键类型。
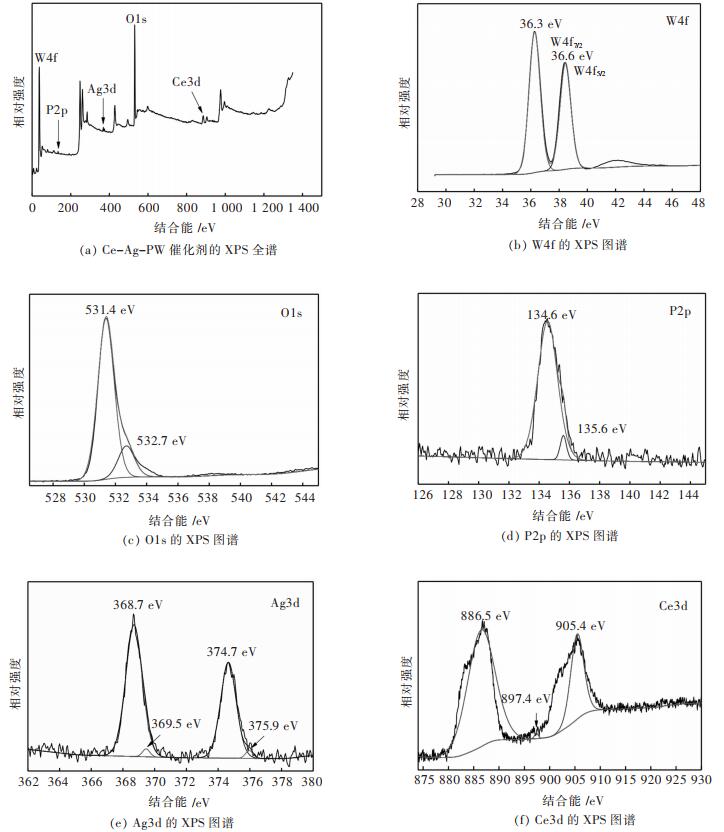 |
| 图 8 Ce-Ag-PW催化剂的XPS光谱图 Fig. 8 XPS spectra of Ce-Ag-PW catalyst |
图 8(a)是Ce-Ag-PW的X射线光电子全谱图。图 8(b)为W4f的窄扫描谱图,显示的两个特征峰结合能为36.3 eV和38.6 eV,分别对应于W4f7/2 和W4f5/2的吸收振动峰,这与W6+的氧化态有关[27]。图 8(c)为O1s的窄扫描谱图,分别在结合能为531.4 eV和532.7 eV处出现了两个特征峰,分别对应了存在于W-O-W和W-O-P中的氧。图 8(d)为P2p的窄扫描谱图,分别在结合能为134.6 eV和135.6 eV处出现了两个特征峰,主要是由于自旋轨道的分离所致。图 8(e)为Ag3d的窄扫描谱图,由图 8(e)可知,在368.7、369.5、374.7、375.9 eV处分别出现了4个特征峰,结合能为368.7 eV与银离子有关,在369.5 eV处的峰强度较低。表明:Ag+所处的化学环境比银原子所处的环境更具正电性[28]。图 8(f)为Ce3d的窄扫描谱图,分别在结合能为886.5、897.4、905.5 eV处出现了3个对应于Ce3d的特征峰,由此表明它是以CeO2(Ce4+)氧化物形式存在[29]。这可能是由于Ce3+吸电子后发生的转变,该转变有利于Lewis酸位的形成。结合以上分析结果可知:Ce3+和Ag+成功地掺杂到HPW中。
2.2 催化剂催化酯化性能分析 2.2.1 催化剂活性比较为了检测固体酸Ce-Ag-PW催化剂催化活性,以油酸和甲醇为反应原料进行了实验研究,并与HPW和空白实验(不添加任何催化剂)结果进行了比较。反应条件如下:甲醇与油酸摩尔比为14: 1,反应温度为65 ℃,催化剂(HPW或Ce-Ag-PW)占总物质质量比为2%。反应结果由图 9可知:Ce-Ag-PW催化活性最高,且当反应时间达到6 h时,油酸转化率高达91%。相比于HPW,Ce-Ag-PW催化剂具有更高催化活性的原因可能是Ce3+和Ag+的加入改变了HPW的热稳定性和酸性位类型。主要因为Lewis酸性位数量的增加,减少催化剂活性中心的损失,从而提高了催化活性。结果表明:该催化剂较好的反应时间为6 h。
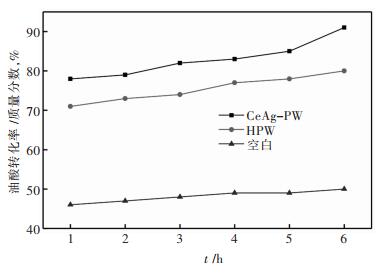 |
| 图 9 HPW、Ce-Ag-PW和无催化剂添加时对油酸转化率的影响 Fig. 9 Effects of HPW, Ce-Ag-PW and blank test on the conversion of oleic acid |
2.2.2 催化剂用量对Ce-Ag-PW催化活性的影响
通过研究不同比列的催化剂质量比对其活性的影响,文中使用催化剂量占反应物总质量范围(0.5%、1%、1.5%、2%、2.5%、3%),甲醇与油酸的摩尔比为14: 1、反应温度为65 ℃、反应时间为6 h。反应结果如图 10所示:油酸转化率随着催化剂用量的增加有着明显的提高。当催化剂用量达到2%时,生物柴油的转化率可达到90%。这一实验结果是由于随着催化剂量的增加,相应的Lewis酸性活性位点也随之增加。然而,随着催化剂量增加到2.5%和3%时,油酸转化率反而有所降低。因此,催化剂占反应物总质量2%可作为适宜的催化剂用量。
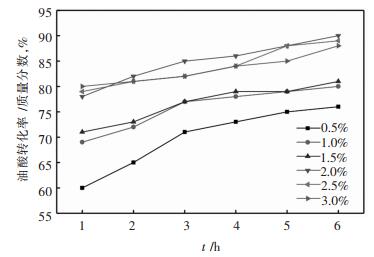 |
| 图 10 Ce-Ag-PW催化剂用量对油酸转化率的影响 Fig. 10 Effects of catalyst amount of Ce-Ag-PW on the conversion of oleic acid |
2.2.3 醇油摩尔比对Ce-Ag-PW催化活性的影响
油醇摩尔比是影响酯化反应效率的一个重要因素,在以下反应条件进行了酯化反应研究:反应温度65 ℃、催化剂用量2%、反应时间6 h,甲醇与油酸物质的量比为6: 1~18: 1,反应结果如图 11所示。可以明显发现当甲醇与油酸的物质的量比从6: 1增加到14: 1时,油酸的转化率可显著提高。然而,当醇油物质的量比继续增加到16: 1时,油酸转化率没有明显提高,反而略有下降。本课题组之前的研究报道曾解释该现象的出现是由于当甲醇过量时,Ce-Ag-PW固体酸活性位将主要被甲醇占据,使油酸与Lewis酸活性位点的接触几率减少,从而导致油酸转化率降低[30-31]。此外,进一步增加醇油摩尔比到18: 1时,油酸的转化率与醇油摩尔比为14: 1时的转化率相当,因此,醇油物质的量比为14: 1可作为适宜的体系反应物物质的量比。
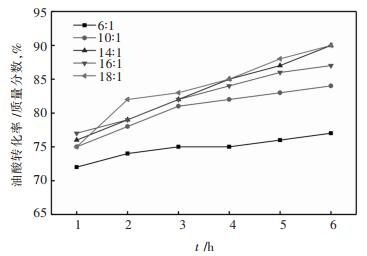 |
| 图 11 甲醇与油酸物质的量比对油酸转化率的影响 Fig. 11 Effects of molar ratio of oleic acid and methanol on the conversion of oleic acid |
2.2.4 反应温度对Ce-Ag-PW催化活性的影响
酯化反应是一个可逆的吸热反应,随着温度的升高,反应向着正反应方向进行,有利于油酸甲酯的生成。在以下反应条件下,针对反应温度对油酸转化率的影响进行了实验研究:反应温度(50、55、60、65、70 ℃),醇油摩尔比为14: 1、催化剂用量为反应物总质量2%、反应时间6 h,结果如图 12所示。由图 12可知:当反应温度50 ℃增加到65 ℃时,油酸的转化率从81%增加到90.2%。然而,随着反应温度继续增加到70 ℃时,油酸转化率略有下降,这主要是因为在标准大气压力下, 甲醇的沸点为64.7 ℃,当反应温度超过甲醇的沸点温度时,将导致更多甲醇蒸发所致[32]。由此,可得出较适宜的反应温度为65 ℃。
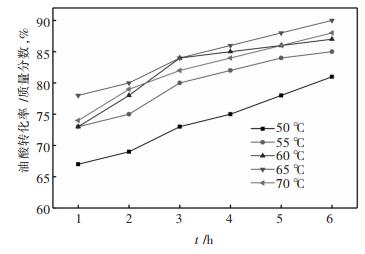 |
| 图 12 反应温度对油酸转化率的影响 Fig. 12 Effects of reaction temperature on the conversion of oleic acid |
2.3 催化剂的可重用性
催化剂的重复使用稳定性在工业催化中至关重要。经以上实验结果得出较好的反应参数(反应温度65 ℃、催化剂占反应物总质量的2%、油醇摩尔比1: 14、反应时间6 h)作为Ce-Ag-PW固体酸催化剂反应条件测试其重复使用稳定性,反应结果如图 13所示。由图 13可知:Ce-Ag-PW固体酸催化剂在经过4次循环使用后,油酸的转化率仍可达到80.5%,由此表明合成的Ce-Ag-PW固体酸催化剂,具有可重复使用性。
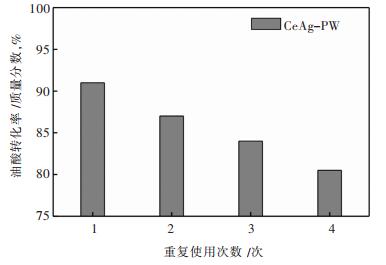 |
| 图 13 Ce-Ag-PW催化剂在酯化反应中的可重复性研究 Fig. 13 Reusability study of Ce-Ag-PW catalysts in esterification |
3 结论
H3PW12O40经稀土Ce3+和Ag+双金属协同改性后,制备而成了一种以Lewis酸性活性位为主的Ce-Ag-PW催化剂。以油酸和甲醇为反应物合成生物柴油为例,对Ce-Ag-PW催化剂的活性和稳定性进行了研究,得出以下结论:
1)通过对Ce-Ag-PW、HPW和空白实验(不添加任何催化剂)结果进行了比较。结果表明,Ce-Ag-PW具有较高的催化活性,该催化剂在以下较优条件(甲醇与油酸的物质的量比为14:1、催化剂用量为反应物总质量的2%、反应温度为65 ℃、反应时间6 h)用于油酸催化酯化反应,油酸转化率可高达91%。固体酸催化剂在经过4次循环使用后,油酸的转化率仍可达到80.5%。Ce-Ag-PW催化剂是一种具有高催化活性和稳定性的以Lewis酸性活性位为主的固体酸催化剂。
2)Ce-Ag-PW的高催化活性和稳定性可归因于以下几点:①Ag+可置换HPW中的质子氢,形成Lewis酸性位;②Ce3+的价电子构型为4f1,是一个很好的受电子体,易于与O原子形成配位键,协同Ag+改性作用能产生更多的Lewis酸位;③在酯化反应过程中,Brönsted酸位易与水发生水合反应而使催化活性受到阻碍。而Lewis酸位的形成将有助于克服水合反应现象的发生。
| [1] |
SU Y J, ZHANG P D, SU Y Q. An overview of biofuels policies and industrialization in the major biofuel producing countries[J].
Renewable and Sustainable Energy Reviews, 2015, 50: 991–1003. DOI: 10.1016/j.rser.2015.04.032. |
| [2] |
HAY J X W, WU T Y, JUAN J C, et al. Biohydrogen production through photo fermentation or dark fermentation using waste as a substrate: Overview, economics, and future prospects of hydrogen usage[J].
Biofuels Bioprod Biorefin, 2013, 7: 334–352. DOI: 10.1002/bbb.1403. |
| [3] |
YANG J X, GUO X L, ZUO Y S. Development of biodiesel industry in China: Upon the terms of production and consumption[J].
Renewable and Sustainable Energy Reviews, 2016, 54: 318–330. DOI: 10.1016/j.rser.2015.10.035. |
| [4] |
YANG Y, TONG C F, WEI Q B, et al. Life Cycle analysis of greenhouse gas and PM2.5 emissions from restaurant waste oil used for biodiesel production in China[J].
BioEnergy Research, 2017, 10(1): 199–207. |
| [5] |
KALAM M A, MASJUKI H H, JAYED M H, et al. Emission and performance characteristics of an indirect ignition diesel engine fuelled with waste cooking oil[J].
Energy, 2011, 36(1): 397–402. |
| [6] |
CANDICE S F, MICHELE E C, MARIA S A M, et al. Dry washing in biodiesel purification: a comparative study of adsorbents[J].
Journal of the Brazilian Chemical Society, 2011, 22(3): 558–563. DOI: 10.1590/S0103-50532011000300021. |
| [7] |
PIZARRO A V, PARK E Y. Lipase-catalyzed production of biodiesel fuel from vegetable oils contained in waste activated bleaching earth[J].
Process Biochemistry, 2003, 38(7): 1077–1082. DOI: 10.1016/S0032-9592(02)00241-8. |
| [8] |
XU Y J, LI G X, SUN Z Y. Development of biodiesel industry in China: Upon the terms of production and consumption[J].
Renewable Sustainable Energy Reviews, 2016, 54: 318–330. DOI: 10.1016/j.rser.2015.10.035. |
| [9] |
GUI M M, LEE K T, BHATIA S. Feasibility of edible oil vs. non-edible oil vs. waste edible oil as biodiesel feedstock[J].
Energy, 2008, 33: 1646–1653. DOI: 10.1016/j.energy.2008.06.002. |
| [10] |
SHUIT S H, YEE K F, LEE K T, et al. Evolution towards the utilisation of functionalised carbon nanotubes as a new generation catalyst support in biodiesel production: an overview[J].
Rayal Society of Chemistry, 2013, 3: 9070–9094. |
| [11] |
ZHOU Y J, NIU S L, LI J. Activity of the carbon-based heterogeneous acid catalyst derived from bamboo in esterification of oleic acid with ethanol[J].
Energy Conversion and Management, 2016, 114: 188–196. DOI: 10.1016/j.enconman.2016.02.027. |
| [12] |
WU L P, HU X, WANG S, et al. Acid-treatment of bio-oil in methanol: The distinct catalytic behaviours of a mineral acid catalyst and a solid acid catalyst[J].
Fuel, 2018, 212: 412–421. DOI: 10.1016/j.fuel.2017.10.049. |
| [13] |
SHU Q, ZHANG Q, XU G H, et al. Preparation of biodiesel using s-MWCNT catalysts and the coupling of reaction and separation[J].
Food Bioprod. Process, 2009, 87: 164–170. DOI: 10.1016/j.fbp.2009.01.004. |
| [14] |
MELERO J A, MORALES G, IGLESIAS J, et al. Rational optimization of reaction conditions for the one-pot transformation of furfural to γ-valerolactone over Zr-Al-Beta zeolite: toward the efficient utilization of biomass[J].
Ind. Eng. Chem. Res, 2018, 57(35): 11592–11599. |
| [15] |
GUAN Q Q, SHANG H, LIU J, et al. Biodiesel from transesterification at low temperature by AlCl3 catalysis in ethanol and carbon dioxide as cosolvent: Process, mechanism and application[J].
Appl. Energy, 2016, 164: 380–386. |
| [16] |
舒庆, 唐国强, 刘峰生, 等. 新型Brönsted-Lewis酸性催化剂LaPW12O40/SiO2制备及其在催化酯化反应合成生物柴油中的应用[J].
燃料化学学报, 2017, 45: 939–949.
DOI: 10.3969/j.issn.0253-2409.2017.08.006.
|
| [17] |
ZHU S H, GAO X Q, DONG F, et al. Design of a highly active silver-exchanged phosphotungstic acid catalyst for glycerol esterification with acetic acid[J].
Catal, 2013, 306: 155–163. DOI: 10.1016/j.jcat.2013.06.026. |
| [18] |
KUMAR C R, JAGADEESWARAIAH K, PRASAD P S S, et al. Samarium-exchanged heteropoly tungstate: an efficient solid acid catalyst for the synthesis of glycerol carbonate from glycerol and benzylation of anisole[J].
Chem Cat Chem, 2012, 4: 1360–1367. |
| [19] |
ZHANG D Y, DUAN M H, YAO X H, et al. Preparation of a novel cellulose-based immobilized heteropoly acid system and its application on the biodiesel production[J].
Fuel, 2016, 172: 293–300. DOI: 10.1016/j.fuel.2015.12.020. |
| [20] |
REN Y S, LIU B, ZHANG Z H. Silver-exchanged heteropolyacid catalyst (Ag1H2PW): An efficient heterogeneous catalyst for the synthesis of 5-ethoxymethyl furfural from 5-hydroxymethyl furfural and fructose[J].
Ind. Eng. Chem, 2015, 21: 1127–1131. DOI: 10.1016/j.jiec.2014.05.024. |
| [21] |
舒庆, 侯小鹏, 刘峰生, 等. 稀土镧改性磷钨杂多酸盐催化油酸与甲醇酯化反应合成生物柴油活性研究[J].
有色金属科学与工程, 2016, 7(3): 131–136.
|
| [22] |
KUMAR C R, JAGADEESWARAIAH K, SAI P P S, et al. Samarium-exchanged heteropoly tungstate: An efficient solid acid catalyst for synthesis of glycerol carbonate from glycerol and benzylation of anisole[J].
Chem Cat Chem, 2012, 4: 1360–1367. |
| [23] |
GAWADE A B, TIWARI M S, YADAY G D. Biobased green process: selective hydrogenation of 5-Hydroxymethylfurfural to 2, 5-dimethyl furan under mild conditions using Pd-Cs2.5H0.5PW12O40/K-10 clay[J].
ACS Sustainable Chem. Eng, 2016, 4: 4113–4123. DOI: 10.1021/acssuschemeng.6b00426. |
| [24] |
TIWARI M S, YADAY G D. Kinetics of friedel crafts benzoylation of veratrole with benzoic anhydride using Cs2.5H0.5PW12O40/K-10 solid acid catalyst[J].
Chem. Eng. J, 2015, 266: 64–73. DOI: 10.1016/j.cej.2014.12.043. |
| [25] |
CAMPOSECO R, CASTILLO S, MEJIA-CENTENO I, et al. Behavior of Lewis and Brönsted surface acidity featured by Ag, Au, Ce, La, Fe, Mn, Pd, Pt, V2O5 and WO3 decorated on protonated titanate nanotubes[J].
Microporous and Mesoporous Materials, 2016, 236: 235–243. DOI: 10.1016/j.micromeso.2016.08.033. |
| [26] |
SONG D Y, AN S, SUN Y N, et al. Efficient conversion of levulinic acid or furfuryl alcohol into alkyl levulinates catalyzed by heteropoly acid and ZrO2 bifunctionalized organosilica nanotubes[J].
Journal of Catalysis, 2016, 333: 184–199. DOI: 10.1016/j.jcat.2015.10.018. |
| [27] |
XU L L, LI W, HU J, et al. Transesterification of soybean oil to biodiesel catalyzed by mesostructured Ta2O5-based hybrid catalysts functionalized by both alkyl-bridged organosilica moieties and Keggin-type heteropoly acid[J].
Mater. Chem, 2009, 19: 8571–8579. DOI: 10.1039/b910694d. |
| [28] |
VENKATESWARA R K T, SAIPRASAD P S, LINGAIAH N. ChemInform abstract: solvent-free hydration of alkynes over a heterogeneous silver exchanged silicotungstic acid catalyst[J].
Green Chem, 2012, 14: 1507–1514. |
| [29] |
WANG J X, WANG A Q, XING Y L, et al. Synthesis, characterization and properties of Ce-modified S2O82-/ZnAl2O4 solid acid catalysts[J].
RSC Adv, 2015, 5: 105908–105916. DOI: 10.1039/C5RA21409B. |
| [30] |
CHAVEANGHONG S, SMITH S M, OOPATHUM C, et al. Fatty acid methyl ester (FAME) production from soybean oil under ambient conditions using strontium loaded bovine bone[J].
Renewable Energy, 2017, 109: 480–486. |
| [31] |
舒庆, 侯小鹏, 唐国强, 等. 氟离子与磺化反应改性多壁纳米碳管催化剂的制备、表征及催化酯化反应合成油酸甲酯性能[J].
无机化学学报, 2016, 10(32): 1791–1801.
|
| [32] |
SHU Q, ZOU W Q, HE J F, et al. Preparation of the F-SO42-/MWCNTs catalyst and kinetic studies of the biodiesel production via esterification reaction of oleic acid and methanol[J].
Renewable Energy, 2019, 135: 836–845. DOI: 10.1016/j.renene.2018.12.067. |
 2020, Vol. 11
2020, Vol. 11


