| 锰元素对铜镍合金电化学性能的影响 |
在海洋环境中, 铜镍合金是一种非常重要的商业合金。90Cu-10Ni在海水中表现出优异的耐腐蚀性能, 在船舶热交换管等不同的海洋工程用管道中得到广泛应用[1, 2]。铜镍合金在整个铜、镍组分中无限固溶, 形成单一的固溶体[3]。镍、铁等合金元素被认为是通过改变表面腐蚀产物层来改善合金的耐蚀性能[4, 5]。铜镍合金能够拥有优异的耐蚀性能, 主要归功于腐蚀过程中合金表面能够生成具有保护性的产物膜[6-8]。这种产物膜为双层结构, 外层为铜的羟基化合物Cu2(OH)3Cl组成, 内层为致密的氧化亚铜[7-9]。有研究证明氧化亚铜中掺杂了镍和铁, 占据由阳离子空位, 因此提高了铜镍合金的耐蚀性能[10-12]。尽管铜镍合金在海洋工程中得到了广泛应用, 但Mn元素作为铜镍合金的主要成分之一, Mn含量的变化对铜镍合金腐蚀行为的影响尚未得到充分的研究, 尤其是对电化学行为的研究较少.
通过利用极化曲线和交流阻抗谱等不同的电化学手段对不同锰含量的铜镍合金在3.5 %NaCl溶液中的电化学行为进行了研究, 分析Mn含量的变化对铜镍合金电化学性能的影响.
1 实验与材料以纯铜(99.9 %)、纯镍(99.9 %)、纯铁(99.9 %)、纯锰(99.9 %)(均为质量分数)为原料, 采用真空熔炼炉炼制了不同Mn含量的Cu-Ni合金, 试样的检测成分如表 1所列。将铸锭在电阻炉中加热至920 ℃, 保温3 h, 热轧至2.6 mm。之后在720 ℃保温1 h进行固溶处理, 之后进行水冷处理.
| 表 1 铜镍合金的化学成分(质量分数, %) Table 1 Chemical compositions of copper-nickel alloy(mass fraction, %) |
 |
| 点击放大 |
电化学实验样品为10 mm×10 mm方形小块, 背面用铜导线焊接后用环氧树脂密封。待环氧树脂凝固后, 将工作表面先用砂纸逐级机械研磨至2000#, 再用颗粒度为0.5 μm进行抛光, 将试样最后用去离子水冲洗表面后备用。实验所用溶液为去离子水和分析纯试剂配制的浓度为3.5 %NaCl溶液.
电化学实验在CHI660E电化学工作站上进行。在装有配制好的电解质溶液的敞口烧杯中, 以Pt片作为辅助电极, 饱和甘汞电极(SCE)作为参比电极, 对电极进行开路电位测量, 极化曲线测试和阻抗谱测试。开路电位测试时间为400 s。极化曲线测试的扫描速率为1 mV/s, 扫描范围从-0.5 V扫描至0.1 V。阻抗测试前先测开路电位, 当开路电位稳定后, 以开路电位值为起始电压进行测试, 阻抗测试采用10 mV的交流电压扰动信号, 扫描范围为100 kHz至0.01 Hz.
2 结果与讨论 2.1 合金组织图 1、图 2所示分别为不同Mn含量铜镍合金的显微组织及面扫描成分分析。其中图 1(b)~1(f)、图 2(b)~2(f)分别为合金未经侵蚀的背散射像及相应的面扫描结果。从图 1(a)、图 2(a)中两种锰含量的样品均发现较多的退火孪晶, 并且随着Mn含量的升高, 晶粒尺寸略有减小。文献[13-14]研究认为Mn元素的添加对一些合金起到细化晶粒的作用。Mn对晶粒的细化作用并不局限于合金的凝固过程, 还有很大可能性在于热轧协助破碎变形组织及后续退火过程中阻止晶粒长大[14]。通过对元素分布图的分析, 发现Mn含量低的1#合金元素分布较为均匀, Mn含量高的2#合金中Mn元素有轻微的富集, 均匀性较1#合金略差, 这对合金的耐蚀性能会产生较大的影响.
 |
| 图 1 1#铜镍合金(0.53 %Mn)的组织及元素分布 Fig. 1 Microstructures and element distribution of sample 1# copper-Nichel alloy (0.53 %Mn) |
 |
| 图 2 2#铜镍合金(1.19 %Mn)的组织及元素分布 Fig. 2 Microstructures and element distribution of sample 2# copper-Nichel alloy (1.19 %Mn) |
2.2 开位电路测试
图 3所示为不同Mn含量铜镍合金的开位电路测量结果。开位电路表征了材料热力学趋势的大小, 电位值越负, 说明材料具有更高的腐蚀倾向。从图 3中可以发现铜镍合金在腐蚀初期开路电位随着腐蚀时间的延长逐渐负移, 说明铜镍合金在腐蚀初期的腐蚀倾向增大[15]。这是由于在腐蚀初期, 合金表面尚未完全生成具有保护性的腐蚀产物, 基体直接与溶液相接触, 在Cl-的作用下, 基体开始发生溶解, 致使开位电路下降[16]。Mn含量低的1#样品的开路电位正于2#样品。由于铜镍无限固溶, 形成单一的α相, Mn的添加量升高, 在合金中形成中间化合物[17], 使得基体开位电路负移, 腐蚀倾向增大。随着腐蚀时间的延长, 合金的表面形成具有保护性作用的腐蚀产物层, 阻碍基体与溶液直接接触, 使得铜镍合金开位电路正移。之后Cl-吸附在表面, 腐蚀产物层被侵蚀破坏, 开位电路开始负移。腐蚀7 d后, 2#样品的开位电路正于1#样品, 说明腐蚀7 d后的1#样品形成的腐蚀产物层较2#样品形成的腐蚀产物层具有更高的腐蚀倾向.
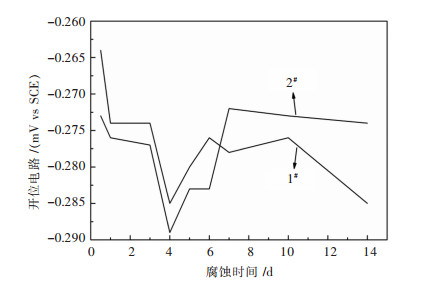 |
| 图 3 不同Mn含量铜镍合金在3.5 %NaCl溶液中的开路电位 Fig. 3 Open-circuit potentials of copper-nickel alloys with different Mn contents in 3.5 %NaCl solution |
2.3 电化学交流阻抗测试
为了更好地了解Mn含量对铜镍合金电化学性能的影响, 根据图 3的开路电位变化, 对腐蚀3 d、7 d、14 d后的样品进行阻抗谱测试, 结果如图 4所示。从腐蚀3 d的Nyquist图和Bode图中可以发现, 此时1#、2#样品的容抗弧半径相近, 1#半径略大于2#; 随着腐蚀时间的延长, 1#样品的阻抗弧半径及总阻抗模值与2#样品的差距加大。一般认为, 交流阻抗谱高频区容抗弧反映了电荷转移反应, 低频区容抗弧则反映电荷或物质通过腐蚀产物层的传输过程, 容抗弧半径越小, 表明合金表面转移电阻小, 反映合金耐腐蚀性能越差[18, 19].
 |
| 图 4 不同Mn含量铜镍合金在3.5 %NaCl溶液中浸泡不同时间的Nyquist图(a~c)和Bode图(d~e) Fig. 4 The Nyquist diagram(a~c) and Bode diagram(d~e) for different time with different Mn contents in 3.5 % NaCl solution |
图 5所示为铜镍合金在3.5 %NaCl溶液中腐蚀不同时间后的等效电路图。其中Rs为溶液电阻, Rct为电荷转移电阻, Rf1和Rf2分别为膜电阻, Q1, Q2, Q3为常相位角元件(CPE)。考虑到表面膜层的不均匀性, 利用常相位角元件替代理想电容。利用Zsimpwin软件根据等效电路图对腐蚀不同时间后的阻抗谱进行拟合, 拟合结果如表 2所列, 表 2中用Rtotal表示为膜层总电阻, 使用式(1)计算各电阻值的和得到[16]。拟合效果用卡方值χ2进行判定, 从表 2中发现, χ2的值均为10-4数量级, 说明该等效电路具有非常好的拟合效果。腐蚀初期, 1#样品的Rtotal略大于2#, 随着时间的延长, 两者的Rtotal差距明显, 说明浸泡到一定时间后, 低Mn含量有助于生成稳定性和耐蚀性更好的腐蚀产物膜.

|
(1) |
 |
| 图 5 铜镍合金在3.5 %NaCl中浸泡不同时间后的等效电路 Fig. 5 Equivalent circuit diagram of copper-nickel alloys immersed in 3.5 %NaCl for different time |
| 表 2 铜镍合金在3.5 %NaCl中浸泡不同时间后的阻抗拟合值 Table 2 Impedance fitting values of copper-nickel alloys immersed in 3.5 %NaCl for different time |
 |
| 点击放大 |
2.4 极化曲线测试
图 6所示分别为含有不同Mn含量的样品在3.5 %NaCl溶液中腐蚀3 d、7 d、14 d后所测得的极化曲线, 利用Tafel外推法对极化曲线进行处理[20, 21], 表 3所列为极化曲线拟合后所得的自腐蚀电流密度和自腐蚀电位值。从图 6和表 3可以发现铜镍合金的自腐蚀电位在腐蚀初期负移, 这是由于阳极在合金表面吸附的Cl-的作用下发生溶解, 形成可溶性氯化物, 表现为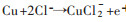
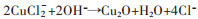
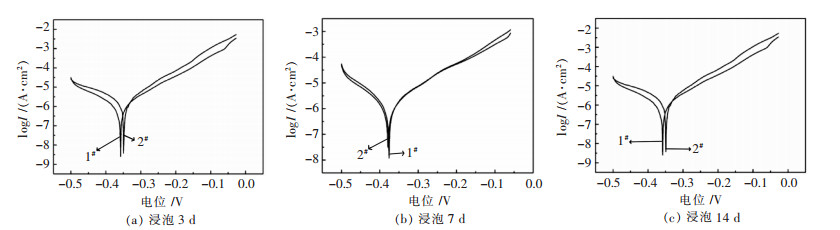 |
| 图 6 铜镍合金在3.5 %NaCl中浸泡不同时间后的极化曲线. Fig. 6 Polarization curves of copper-nickel alloys after immersion in 3.5 %NaCl for different time |
| 表 3 铜镍合金在3.5 %NaCl中浸泡不同时间后的自腐蚀电流密度和自腐蚀电位 Table 3 Self-corrosion current density and self-corrosion potential of copper-nickel alloy after immersed in 3.5 %NaCl for different time |
 |
| 点击放大 |
自腐蚀电流密度是评价材料耐蚀性能的重要参数, 自腐蚀电流密度越小, 材料的耐蚀性能越优良[18]。从表 3可以发现, 1#样品的自腐蚀电流密度在整个腐蚀周期中都是大于2#样品的自腐蚀电流密度, 说明1#样品在腐蚀过程中生成的腐蚀产物膜较2#样品更具保护性, 使得1#样品的耐蚀能力强于2#样品, 进一步证实了图 2的结果.
3 结论1) 在腐蚀初期, Mn含量为0.53 %的1#铜镍合金样品正于Mn含量为1.19 %的2#铜镍合金样品开位电路。随着时间延长, 1#样品开路电位逐渐负于2#样品.
2) Mn含量低的样品合金表面生成的腐蚀产物膜较Mn含量高的样品具有更好的耐蚀性, 低Mn含量有利于提高铜镍合金的耐腐蚀性能。在铜镍合金中提高Mn含量的添加量会减小样品的容抗弧半径, 并且随着时间的延长, 半径的减小量会越明显.
| [1] |
赵月红, 林乐耘, 崔大为. 铜镍合金在我国实海海域的局部腐蚀[J].
中国有色金属学报, 2005(11): 140–148.
|
| [2] |
林乐耘, 刘少峰, 刘增才, 等. 铜镍合金海水腐蚀的表面与界面特征研究[J].
腐蚀科学与防护技术, 1999(1): 37–43.
DOI: 10.3969/j.issn.1002-6495.1999.01.005.
|
| [3] |
徐时清, 王焕平.
材料科学基础[M]. 上海: 上海交通大学出版社, 2015.
|
| [4] |
POPPLEWELL J M, HART R J, FORD J A. The effect of iron on the corrosion characteristics of 90-10 cupro nickel in quiescent 3.4%NaCl solution[J].
Corrosion Science, 1973, 13(4): 295–298. DOI: 10.1016/0010-938X(73)90007-3. |
| [5] |
BADAWY W A, ISMAIL K M, FATHI A M. The influence of the copper/nickel ratio on the electrochemical behavior of Cu–Ni alloys in acidic sulfate solutions[J].
Journal of Alloys and Compounds, 2009, 484(1/2): 365–370. |
| [6] |
林乐耘, 雷廷权, 朱小龙. 70Cu-30Ni合金海水腐蚀产物膜形成过程[J].
金属学报, 1997, 33(12): 1256–1261.
|
| [7] |
MA A L, JIANG S L, ZHENG Y G, et al. Corrosion product film formed on the 90/10 copper–nickel tube in natural seawater:Composition/structure and formation mechanism[J].
Corrosion Science, 2015, 91: 245–261. DOI: 10.1016/j.corsci.2014.11.028. |
| [8] |
ZHU X, LEI T. Characteristics and formation of corrosion product films of 70Cu–30Ni alloy in seawater[J].
Corrosion Science, 2002, 44(1): 67–79. DOI: 10.1016/S0010-938X(01)00041-5. |
| [9] |
BECCARIA A M, WANG Y Z, POGGI G. Study of passive film formation on Cu–Ni 70/30 alloy in seawater at high temperature[J].
Surface & Interface Analysis, 1994, 21(21): 442–446. |
| [10] |
BADAWY W A, ISMAIL K M, FATHI A M. Effect of Ni content on the corrosion behavior of Cu–Ni alloys in neutral chloride solutions[J].
Electrochimica Acta, 2005, 50(18): 3603–3608. DOI: 10.1016/j.electacta.2004.12.030. |
| [11] |
PEASON C. Role of Iron in the Inhibition of Corrosion of Marine Heat Exchangers — A Review[J].
British Corrosion Journal, 1972, 7(2): 8. |
| [12] |
RAO B V A, Kumar K C, Hebalkar N Y. X-ray photoelectron spectroscopy depth-profiling analysis of surface films formed on Cu–Ni (90/10) alloy in seawater in the absence and presence of 1, 2, 3-benzotriazole[J].
Thin Solid Films, 2014, 556(4): 337–344. |
| [13] |
高宝东, 千东范, 刘雅秀. 锰对Cu-Zn-Al形状记忆合金的影响[J].
稀有金属, 1993(6): 405–409.
|
| [14] |
张新明, 陈健美, 邓运来, 等. Mg-Gd-Y-(Mn, Zr)合金的显微组织和力学性能[J].
中国有色金属学报, 2006, 16(2): 219–227.
DOI: 10.3321/j.issn:1004-0609.2006.02.004.
|
| [15] |
李晓孟, 国秀花, 张彦敏, 等. 人工海水冲刷时间对B10管电化学性能影响的研究[J].
材料研究与应用, 2016, 10(1): 53–56.
DOI: 10.3969/j.issn.1673-9981.2016.01.011.
|
| [16] |
EKERENAM O O, MA A, ZHENG Y, et al. Electrochemical Behavior of Three 90Cu-10Ni Tubes from Different Manufacturers After Immersion in 3.5% NaCl Solution[J].
Journal of Materials Engineering & Performance, 2017, 26(4): 1701–1716. |
| [17] |
P G K.
Phase Diagrams Ternary Nickel Alloys[M]. India: Indian Institute of Metals, 1990.
|
| [18] |
杨少华, 刘增威, 林明, 等. 7075铝合金在不同pH值NaCl溶液中的腐蚀行为[J].
有色金属科学与工程, 2017, 8(4): 7–11.
|
| [19] |
林向飞, 康巍, 李红英. 硼和稀土对铝阴极板耐腐蚀性能的影响[J].
有色金属科学与工程, 2017, 8(3): 42–47.
|
| [20] |
SHI Z, LIU M, Atrens A. Measurement of the corrosion rate of magnesium alloys using Tafel extrapolation[J].
Corrosion Science, 2010, 52(2): 579–588. DOI: 10.1016/j.corsci.2009.10.016. |
| [21] |
吴茂永, 田继强, 曹立新, 等. 钨铝合金在不同NaCl溶液中的电化学腐蚀行为研究[J].
腐蚀科学与防护技术, 2015, 27(1): 25–30.
|
| [22] |
曹楚南.
腐蚀电化学原理[M]. 3版. 北京: 化学工业出版社, 2015: 25-30.
|
| [23] |
马爱利. 海水管路用B10合金腐蚀机制、晶界工程及腐蚀产物膜研究[D]. 中国科学院大学, 2014.
|
 2018, Vol. 9
2018, Vol. 9


