| 烧结温度对LiNi0.8Co0.15Al0.05O2结构和电化学性能的影响 |
b. 江西理工大学,江西省动力电池及其材料重点实验室,江西 赣州 341000
b. Jiangxi Key Laboratory of Power Battery and Materials, Jiangxi University of Science and Technology, Ganzhou 341000, China
锂离子电池因比容量高、工作电压宽和安全性好被广泛应用于电动汽车及数码设备.产业化锂离子电池负极材料比容量已达350 mAh/g[1],正在研发的硅碳负极也突破600 mAh/g, 而商业化正极材料LiCoO2比容量140 mAh/g、三元材料如:LiNi1/3Mn1/3Co1/3O2[2]、LiNi0.5Mn0.3Co0.2O2、LiNi0.6Mn0.3Co0.1O2[3]比容量只有150 mAh/g左右[4],LiNiO2材料的比容量在185~220 mAh/g,然而LiNiO2材料结构不稳定[5],电化学反应生成的Ni4+具有强氧化性,易与电解液发生副反应,导致容量衰减[6].低容量正极材料已经影响了锂离子电池能量密度的提升,研发高容量正极材料是当务之急.
研究发现LiNiO2掺杂金属离子锰[7]、钴[8]、铝[9-10]等对其电化学性能有所改善.在这些掺杂中, 发现通过掺杂适量的铝和钴制备的LiNi0.8Co0.15Al0.05O2材料实际比容量在180 mAh/g以上[11-12],掺杂Al3+和Co3+不仅稳定结构,增强循环性能,掺杂铝的LiNi0.8Co0.15Al0.05O2材料稳定性比掺杂锰的LiNi0.7Co0.15Mn0.15O2材料更优异[13],地壳中铝含量丰富,因而LiNi0.8Co0.15Al0.05O2被认为是最有前景的正极材料之一[14].但是LiNi0.8Co0.15Al0.05O2相对LiCoO2仍有不足,在合成过程中也存在一些问题,比如镍、钴、铝的氢氧化物在水溶液中离子积常数相差甚远[15-16],前驱体金属离子含量分布不一致,镍离子错位和氧化难度大,且很难合成理想态的晶体结构,三价镍氧化过程中易与电解液生产副产物降低电池性能.合适的烧结温度对提升材料性能和降低生产成本有利,较优烧结温度的确定对LiNi0.8Co0.15Al0.05O2材料产业化发展有重大意义.Qiu等[17]采用固相法合成LiNi0.8Co0.15Al0.05O2烧结温度对其性能的影响,发现750℃能获得纯的六方相,0.2 C倍率、2.75~4.3 V首次放电比容量194 mAh/g,1 C倍率性能优于700℃和800℃; Xie等[18]利用共沉淀法在800℃氧气气氛下获得的材料在3.0~4.3 V、0.1 C首次比容量203.1 mAh/g,1 C循环200次后保持率为93 %; 刘城[19]实验发现650℃、900℃烧结后的材料均出现杂相,在750℃下获得性能较优的材料有182.1 mAh/g的首次放电比容量,800℃和850℃颗粒形貌严重偏离球型状形貌.
正极材料的结构对其电化学性能影响甚大,大多数文献在报道温度对结构性能的研究时,温度变化大,未能具体确定较优烧结温度.根据上述文献报道可以预判:LiNi0.8Co0.15Al0.05O2材料的较优烧结温度在750~800℃.但是相关文献对此温度区间的烧结实验报道较少, 通过缩小LiNi0.8Co0.15Al0.05O2的烧结温度区间进行改进,研究烧结温度对其结构和电化学性能的影响, 探讨LiNi0.8Co0.15Al0.05O2材料的较优烧结工艺, 得到电化学性能优异的正极材料,对基础研究数据进行补充, 期望促进正极材料尽快批量生产.
1 实验过程选用氢氧化物共沉淀法将NiSO4·6H2O、CoSO4·7H2O、Al2(SO4)3·18H2O按镍:钴:铝原子量=0.8:0.15:0.05的摩尔比溶于去离子水溶液,与适量浓度的NaOH+NH3·H2O溶液同时逐渐滴入以去离子水为底液的密闭反应釜内,控制反应pH=10.5±0.2,通氮气保护、加热反应24 h,静止12 h后除去上清液,150℃干燥48 h获得D50=10.45 μm的Ni0.8Co0.15Al0.05(OH)2前驱体.将Ni0.8Co0.15Al0.05(OH)2前驱体和LiOH·H2O(过量8 %,指质量分数)按摩尔比称量,在玛瑙罐内用酒精湿混6 h后,65℃去除酒精后干混1 h,在氧气气氛下从室温以2℃/min的速率升至500℃保温6 h后、以2℃/min分别升至740℃、760℃、780℃、800℃、820℃条件下保温18 h, 自然降至室温.
1.1 结构、形貌表征不同温度烧结获取的材料采用X射线衍射仪(XRD,日本理学MiniFlex 600,Cu靶,Kα射线,测试电压40 kV,电流15 mA)分析正极材料结构, 扫描速度10 °/min,扫描范围10 °~80 °.样品形貌采用德国ZEISS产EVO/MA10型扫描电镜表征.
1.2 电化学性能测试干燥后的LiNi0.8Co0.15Al0.05O2、导电炭黑(SP)、黏结剂(PVDF)按质量比92:3:5,在有机溶剂(NMP)中混合均匀后,涂覆在铝箔上获得60 μm厚的正极片,单质锂为负极,在氩气手套箱内组装成CR2032型纽扣电池.LiNi0.8Co0.15Al0.05O2为正极,裁剪成35 cm×3.5 cm石墨为负极裁剪成39 cm× 3.8 cm制成软包.
电池采用新威测试系统,在25℃、2.75~4.2 V、0.1 C(1 C=180 mA/g)化成一周,0.5 C循环5次后充电至3.9 V测试交流阻抗.软包电池在0.1 C化成后,0.5 C循环100次.
2 实验结果分析与讨论 2.1 烧结温度对LiNi0.8Co0.15Al0.05O2晶体结构的影响图 1所示为在不同烧结温度(740 ℃、760 ℃、780℃、800℃、820℃)下合成的LiNi0.8Co0.15Al0.05O2材料XRD谱图.LiNi0.8Co0.15Al0.05O2中的原子按ABCABC排列方式紧密堆积而成,锂占据层状结构的3a、金属离子占据3b、氧占据6c位置[20].从XRD谱图看,5个不同烧结温度的材料峰位置基本一致,没有发生偏移现象,均符合α-NaFeO2型六方层状结构特征,(006)和(102)、(108)和(110)峰分裂明显,表明层状结构发育完好,740 ℃~820 ℃温度适合LiNi0.8Co0.15Al0.05O2晶体材料的生长,资料显示I(003)/I(104)峰强比大于1.2时,表明Li+(半径为74pm)空位被Ni2+(半径为70pm)占用程度低[21-22].5种温度制备的材料其I(003)/I(104)峰强比均大于1.4,其中780℃条件下制备的材料峰强度最高,表明780 ℃和18 h条件下合成出的材料Ni2+/Li+占用程度低,Li+损失量少,Ni2+到Ni3+的氧化率高,层状结构最完整.表 1是材料的晶胞参数计算值,c值和a值出现细微变化,c/a值均大于4.9, 表明阳离子混排情况少,且在780 ℃出现最高值,说明该温度下材料晶型结构最接近理想状态,过渡金属离子和锂离子排列有序度好.
 |
| 图 1 不同烧结温度下合成的LiNi0.8Co0.15Al0.05O2XRD谱 Fig. 1 XRD patterns of LiNi0.8Co0.15Al0.05O2under different sintering temperatures |
| 表 1 不同烧结温度下合成的LiNi0.8Co0.15Al0.05O2晶胞参数计算值 Table 1 Lattice parameters of LiNi0.8Co0.15Al0.05O2 prepared by different sintering temperatures |
 |
| 点击放大 |
2.2 烧结温度对LiNi0.8Co0.15Al0.05O2颗粒形貌和粒度影响
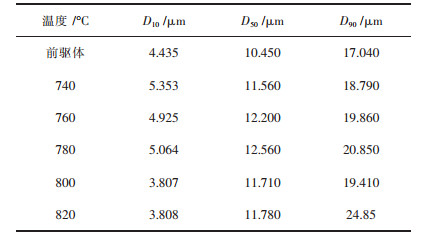
图 2所示为样品的SEM图, 表 2所列为烧结后颗粒粒径数据.图 2可以判断五组样品颗粒外形类似于球型, 随着烧结温度上升,颗粒逐渐长大,780 ℃的一次颗粒连接较紧密,温度高于780 ℃后一次颗粒接触过于致密, 致密的一次颗粒会降低锂离子通道与电解液接触面积, 阻碍锂离子的扩散.在820 ℃二次颗粒团聚导致粒径异常增大, 颗粒呈现多边形,球形度下降进一步影响材料性能.
 |
| 图 2 LiNi0.8Co0.15Al0.05O2颗粒SEM像 Fig. 2 SEM images of iNi0.8Co0.15Al0.05O2 |
| 表 2 不同烧结温度下合成的LiNi0.8Co0.15Al0.05O2颗粒粒径 Table 2 LiNi0.8Co0.15Al0.05O2 particle size synthesized at different sintering temperatures |
 |
| 点击放大 |
2.3 烧结温度对LiNi0.8Co0.15Al0.05O2电化学性能影响 2.3.1 循环伏安测试
为了研究不同温度制备的材料电化学可逆性,在2.5~4.6 V电压区间、以0.1 mV/s的扫描速率对纽扣电池进行循环伏安测试.图 3所示是不同烧结温度材料的循环伏安测试结果,5种温度下制备的材料曲线峰型相似,Ni的价态变化过程反映了材料可逆程度,体现在峰电流的变化,图 3中出现3组氧化还原峰对,在3.7~3.8 V附近发生H1→M相转变,对应的还原峰在3.6~3.7 V; 在4.0 V附近发生M→H2转变,对应的还原峰在3.95V附近; 在4.2 V附近对应H2→H3相转变,其还原峰在4.15 V附近.循环伏安曲线中的氧化、还原电位差可以说明电极极化程度,差值越小,极化越小.780 ℃材料峰面积最大,氧化峰、还原峰强度电压差值最小,为0.07 V,760℃和820℃材料的电压差为0.09 V,740 ℃和800 ℃材料电压差值均超过0.14 V,说明在780 ℃条件下烧结18 h的材料电池极化电压小,电池可逆性最好,结构最为稳定.
 |
| 图 3 不同烧结温度材料的循环伏安测试 Fig. 3 Cyclic voltammetry curve of LiNi0.8Co0.15Al0.05O2 |
2.3.2 充放电测试
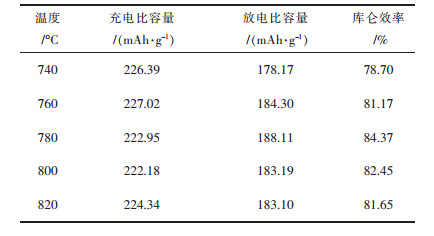
图 4所示为在室温下、2.75~4.2 V以0.1 C(1 C=180 mAh/g)倍率对软包电池进行首次充放电激活锂离子电池.由于烧结温差小,5种材料的首次充放电曲线基本重合,但仍然存在差距.表 3可以看出:740 ℃下烧结的材料放电比容量178.18 mAh/g,760 ℃下烧结的材料放电比容量184.30 mAh/g,780 ℃下烧结的材料放电比容量188.11 mAh/g为最高值,800 ℃下烧结的材料放电比容量183.19 mAh/g,820 ℃下烧结的材料放电比容量183.10 mAh/g; 在740 ℃、760 ℃、780 ℃、800 ℃、820 ℃下平均库伦效率分别是78.70%、81.17%、84.37%、82.45%、81.65%,数据呈现先上升后下降规律.
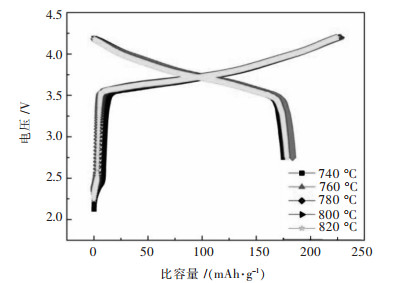 |
| 图 4 不同烧结温度下合成的LiNi0.8Co0.15Al0.05O2在2.75~4.2 V和0.1 C倍率首次充放电 Fig. 4 Initial cycle curves of LiNi0.8Co0.15Al0.05O2 (2.75~4.2 V & 0.1 C) |
| 表 3 不同烧结温度下合成的LiNi0.8Co0.15Al0.05O2在2.75~4.2 V和0.1 C倍率化成 Table 3 Initial cycle data of LiNi0.8Co0.15Al0.05O2 (2.75~4.2 V & 0.1 C) |
 |
| 点击放大 |
对化成的软包电池以0.2 C倍率进行充电,不同倍率放电.图 5显示不同温度材料的倍率性能测试结果,从图 5曲线分析,随着倍率增大,材料的比容量逐渐下降.在0.1、0.2、0.5、1、2、5 C放电最后回到0.2 C倍率放电,图 6显示780 ℃样品比容量分别是185.32、175.42、168.56、161.73、154.17、151.05、184.04 mAh/g,在相同放电倍率下,比容量高于其他温度制备的材料.图 6是烧结材料LiNi0.8Co0.15Al0.05O2为正极、石墨材料为负极制成软包电池,在0.1 C倍率激活后在0.5 C、2.75~4.2 V循环100次曲线图,780 ℃材料保持率88.55%,高于其他温度制备的材料.在740~820 ℃的温度区间内,细小温度差对LiNi0.8Co0.15Al0.05O2电池性能产生重要影响,740 ℃的低温使颗粒发育不够完善,820 ℃的高温使一次颗粒间距收缩导致二次颗粒过于致密, 降低了正极材料与电解液接触面积,二者均影响锂离子扩散系数,780 ℃时LiNi0.8Co0.15Al0.05O2材料一次颗粒和二次颗粒球形度最好, 各级颗粒间距适当,锂离子扩散系数最大,结构最稳定,因而其容量保持率最好.
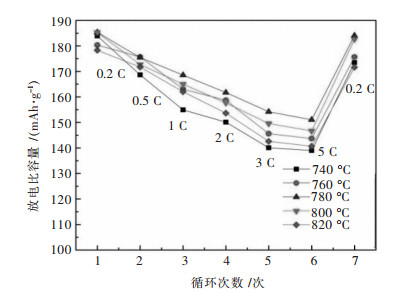 |
| 图 5 不同烧结温度下合成的LiNi0.8Co0.15Al0.05O2倍率测试 Fig. 5 Rate capacity of LiNi0.8Co0.15Al0.05O2cycled at |
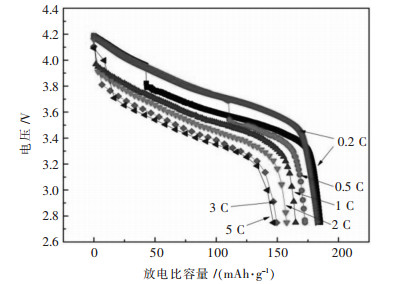 |
| 图 6 780 ℃材料不同倍率测试结果 Fig. 6 Rate capacity of 780 ℃cycled atdifferent rate different sintering temperatures |
对化成的软包电池以0.2 C倍率进行充电,不同倍率放电.图 5所示为不同温度材料的倍率性能测试结果,从图 5曲线分析,随着倍率增大,材料的比容量逐渐下降.在0.1、0.2、0.5、1、2、5 C放电最后回到0.2 C倍率放电,图 6所示为780 ℃样品不同倍率比容量分别是185.32、175.42、168.56、161.73、154.17、151.05、184.04 mAh/g,在相同放电倍率下,比容量高于其他温度制备的材料.图 7是烧结材料LiNi0.8Co0.15Al0.05O2为正极、石墨材料为负极制成软包电池,0.1 C激活后在0.5 C、2.75~4.2 V循环100次曲线图,780 ℃材料保持率88.55 %,高于其他温度制备的材料.在740~820 ℃的温度区间内,细小温度差对LiNi0.8Co0.15Al0.05O2电池性能产生重要影响,740 ℃的低温使晶格发育不够完善,820 ℃的高温使材料孔隙结构收缩,二者均影响锂离子扩散系数,780 ℃的温度刚好促使LiNi0.8Co0.15Al0.05O2材料孔隙通道最畅通,锂离子扩散系数最大,结构最稳定,因而其容量保持率最好.
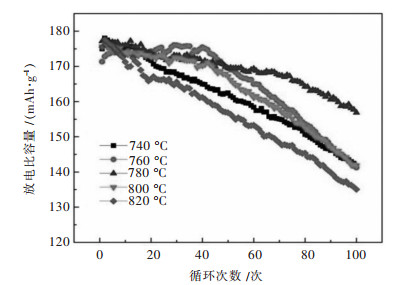 |
| 图 7 不同烧结温度下合成的LiNi0.8Co0.15Al0.05O2循环测试 Fig. 7 Cycle performance curves of LiNi0.8Co0.15Al0.05O2 |
3 结论
1)通过共沉淀法制备Ni0.8Co0.15Al0.05(OH)2前驱体,利用固相法在不同烧结温度下获得LiNi0.8Co0.15Al0.05O2正极材料,XRD和电化学数据显示,780 ℃材料性能最好,2.75~4.2 V电压区间、0.1 C倍率首次比容量188.11 mAh/g,0.5 C循环100次容量保持率88.55%.
2)实验结果对前人相关文献报道可以得出总结性结论:LiNi0.8Co0.15Al0.05O2在740~820 ℃之间烧结能获得结构优异的正极材料.温度变化对LiNi0.8Co0.15Al0.05O2材料有很大影响,在工业生产和科学研究中适当调整烧结温度,能够制备出性能最优异的电池材料.
| [1] |
刘柏男, 徐泉, 褚赓, 等. 锂离子电池高容量硅碳负极材料研究进展[J].
储能科学与技术, 2016, 5(4): 417–421.
|
| [2] |
赖江洪, 钟盛文, 郭进康, 等. LiNi1/3Co1/3Mn1/3O2正极材料的合成与性能[J].
有色金属科学与工程, 2017, 8(4): 68–72.
|
| [3] |
吕庆文, 尹从岭, 钟盛文, 等. LiNi0.6Co0.1Mn0.3O2正极材料的合成与性能[J].
有色金属科学与工程, 2016, 7(4): 50–54.
|
| [4] |
CHO Y H, JANG YOON J, et al. Thermal stability of charged LiNi0.5Co0.2Mn0.3O2, cathode for Li-ion batteries investigated by synchrotron based in situ X-ray diffraction[J].
Journal of Alloys & Compounds, 2013, 562(562): 219–223. |
| [5] |
CHONG S Y, UN W, YUNG S T, et al. Structural stability of LiNiO2 cycled above 4.2 V[J].
Acs Energy Letters, 2017, 2(5): 1150–1155. DOI: 10.1021/acsenergylett.7b00304. |
| [6] |
MURALI NBABU K V, BABU K E, et al. Structural and morphological characterization of Mg doped LiNiO2 cathode materials for Lithium-Ion Batteries[J].
Chemical Science Transcations, 2015, 4(4): 1031–1036. |
| [7] |
KIM Y. First principles investigation of the structure and stability of LiNiO2, doped with Co and Mn[J].
Journal of Materials Science, 2012, 47(21): 7558–7563. DOI: 10.1007/s10853-012-6299-0. |
| [8] |
ZHONG S, LAI M, YAO W, et al. Synthesis and electrochemical properties of LiNi0.8CoxMn0.2-xO2, positive-electrode material for lithium-ion batteries[J].
Electrochimica Acta, 2016, 212: 343–351. DOI: 10.1016/j.electacta.2016.07.040. |
| [9] |
KO H S, KIM J H, WANG J, et al. Co/Ti co-substituted layered LiNiO2 prepared using a concentration gradient method as an effective cathode material for Li-ion batteries[J].
Journal of Power Sources, 2017, 372: 107–115. DOI: 10.1016/j.jpowsour.2017.10.021. |
| [10] |
华政. 锂离子电池LiNi0. 8Co0. 15Al0. 05O2正极材料的合成与改性研究[D]. 昆明: 昆明理工大学, 2017.
http://www.cqvip.com/QK/71651X/201604/669384057.html |
| [11] |
SONG C, WANG W, PENG H, et al. Improving the electrochemical performance of LiNi0.8Co0.15Al0.05O2 in lithium ion batteries by LiAlO2 surface modification[J].
Applied Sciences, 2018, 8(3): 378. DOI: 10.3390/app8030378. |
| [12] |
GRENIER A, LIU H, WIADEREK K M, et al. Reaction heterogeneity in LiNi0.8Co0.15Al0.05O2 induced by surface layer[J].
Chemistry of Materials, 2017, 29(17): 7345–7352. DOI: 10.1021/acs.chemmater.7b02236. |
| [13] |
LI W, LIU X, CELIO H, et al. Mn versus Al in layered oxide cathodes in lithium-ion batteries: A comprehensive evaluation on long-term cycle ability[J].
Advanced Energy Materials, 2018, 170: 3154. |
| [14] |
WU N, WU H, YUAN W, et al. Facile synthesis of one-dimensional LiNi0.80Co0.15Al0.05O2 microrods as advanced cathode materials for lithium ion batteries[J].
Journal of Materials Chemistry A, 2015, 3(26): 13648–13652. DOI: 10.1039/C5TA02767E. |
| [15] |
LIANG M, SONG D, ZHANG H, et al. Improved performances of LiNi0.80Co0.15Al0.05O2 material employing NaAlO2 as a new aluminium source[J].
Acs Appl Mater Interfaces, 2017, 9: 38567–38574. DOI: 10.1021/acsami.7b12306. |
| [16] |
YU J., CARBO N NANOTUBE S. Coating on LiNi0.80Co0.15Al0.05O2 as cathode materials for lithium battery[J].
International Journal of Electrochemical Science, 2017, 12(12): 11892–11903. |
| [17] |
QIU Z, ZHANG Y, DONG P, et al. A facile method for synthesis of LiNi0.80Co0.15Al0.05O2, cathode material[J].
Journal of Materials Science Materials in Electronics, 2017, 28(24): 1–7. |
| [18] |
XIE H, DU K, HU G, et al. Synthesis of LiNi0.80Co0.15Al0.05O2 with 5-sulfosalicylic acid as a chelating agent and its electrochemical properties[J].
Journal of Materials Chemistry A, 2015, 3(40): 20236–20243. DOI: 10.1039/C5TA05266A. |
| [19] |
刘城. 高镍层状结构LiNi0. 80Co0. 15Al0. 05O2正极材料的合成与性能研究[D]. 天津: 天津理工大学, 2016.
|
| [20] |
ROBERT R, BUNZLI C, Berg E J, et al. Activation mechanism of LiNi0.80Co0.15Al0.05O2: surface and bulk operando electrochemical, differential electrochemical mass spectrometry, and X- ray diffraction analyses[J].
Chemistry of Materials, 2015, 27(2): 526–536. DOI: 10.1021/cm503833b. |
| [21] |
CHEN Y, LI P, ZHAO S, et al. Influence of integrated microstructure on the performance of LiNi0.80Co0.15Al0.05O2 as a cathodic material for lithium ion batteries[J].
Rsc Advances, 2017, 7(46): 29233–29239. DOI: 10.1039/C7RA04206J. |
| [22] |
SONG C, WANG W, PENG H, et al. Improving the electrochemical performance of LiNi0.80Co0.15Al0.05O2 in lithium ion batteries by LiAlO2 surface modification[J].
Applied Sciences, 2018, 8(3): 378. DOI: 10.3390/app8030378. |
 2018, Vol. 9
2018, Vol. 9


