| 钨冶炼渣中铁、锰浸出工艺研究 |
钨金属所具备的高强度、高硬度、导电性、导热性等优点使其在工业中得到了较为广泛应用,主要表现在化工,金属合金、电子器件等方面,常被称为“工业味精[1-3]”.根据2015年美国地质局的调查报告显示,我国钨矿资源储存量为190万t,大约占全球总量的60%[4].我国过去几十年钨矿资源的开发利用及即将到来的工业化4.0[5, 6],都体现了钨矿战略地位越来越重要,而随之而带来的问题也越来越突出:国内品位较高黑钨矿的大量减少,生产将目光聚焦在品位较低的白钨矿,钨冶炼渣的产生势必会大量增加.据文献[7]报道每生产1 t WO3≥65%的钨精矿,大约要产生0.8 t的钨冶炼渣.钨冶炼渣中含有的大量有价金属和可回收石料,如果随意填埋或堆弃,不但会造成环境的污染,还会对身体健康造成危害[8, 9],钨冶炼渣的回收利用主要有3个方面:①新型材料的制备[10-13];②有价金属的回收[14-17];③石料的回收利用[18-20].目前,各国对环境的担忧促进了电池三元材料的开发与利用,作为新能源材料,其具备优良优点[21-23]:高比容量、安全性能、循环性能,而且成本价格相对较低.在未来,锂电池具备广阔的发展前景[24, 25],电池级硫酸锰作为三元材料的主要合成原料将同样受到重用.钨矿种类不同伴生元素不同,往往含有较多的Fe、Mn、Ca等元素,从钨冶炼渣中回收Mn将会产生可观的经济效益.
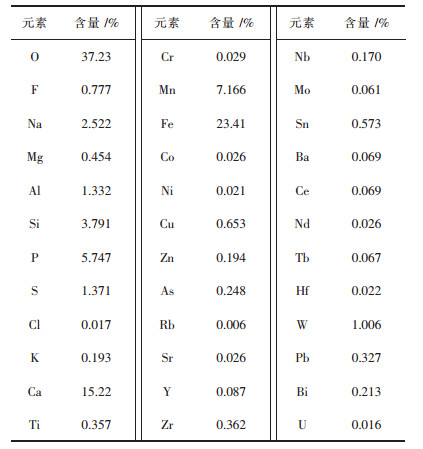
1 实验材料与方法 1.1 实验原料实验原料:实验所用的原料来源于赣州某厂的废旧钨冶炼渣,经105 ℃条件下鼓风干燥箱干燥24 h,然后碾磨过孔径为0.15 mm的筛子,再次干燥,放入干燥皿中备用.经过XRF、XRD、SEM检测,结果见表 1、图 1、图 2.
| 表 1 钨冶炼渣化学成分含量 Table 1 Chemical composition of tungsten smelting slag |
 |
| 点击放大 |
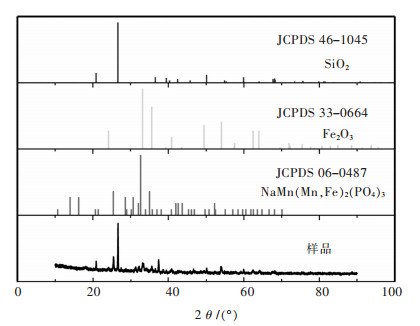 |
| 图 1 钨冶炼渣的XRD谱 Fig. 1 XRD pattern of tungsten smelting slag |
 |
| 图 2 钨冶炼渣的电镜扫描像 Fig. 2 SEM image of tungsten smelting slag |
1.2 实验试剂和设备
实验试剂:浓硫酸(AR西陇科学股份有限公司)、浓硝酸(AR西陇科学股份有限公司)、去离子水(实验室自制).
实验设备:分析天平(FA224上海舜宇恒平科学仪器有限公司)、电热恒温鼓风干燥箱(DH-9073BS-Ⅲ上海新苗医疗器械制造有限公司)、循环水式真空泵(SHZ-D(Ⅲ)巩义市予华仪器有限责任公司)、集热式恒温磁力搅拌器(HH江苏金坛市亿通电子有限公司)、原子吸收光谱分析仪(TAS-990北京普析通用仪器有限责任公司)、pH计(PHS-3E上海仪电科学仪器股份有限公司).
1.3 钨冶炼渣的酸浸出工艺如图 3所示:电子天平称取10.00 g备用钨冶炼渣,加入到圆底烧瓶中,然后按固液比1:6加入60 g质量分数25%的硫酸,放入水浴温度80 ℃的恒温水浴锅中,转速设定为中速[6]、90 min后,停止反应,取出、静置、冷却、抽滤等操作,转移到250 mL的容量瓶,用硝酸(1+9)定容.由于反应加入的硫酸用量是过量的,pH测定显示浸出液的酸度在0以下,酸性仍然较强,所以实验进行浸出液的二次循环利用.二次浸出同样按照上面的条件浸出新鲜钨冶炼渣.
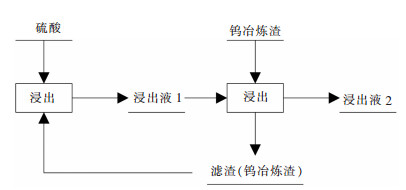 |
| 图 3 硫酸浸出钨冶炼渣工艺流程 Fig. 3 Flowchart of sulfuric acid leaching tungsten smelting slag |
1.4 分析方法-标线的绘制
锰、铁离子的浓度测量采用火焰原子吸收分光光度法,此方法参照GB11911-89进行实验操作.
锰标准曲线的绘制:用移液管移取25 mg/L的锰标准液0.00 mL、0.50 mL、1.00 mL、1.50 mL、2.00 mL、2.50 mL、3.00 mL于50mL容量瓶中,加入硝酸(1+9)定容.选择合适的火焰原子吸收仪器预热30 min,于279.5 nm测量并绘制锰的标准曲线见图 4.
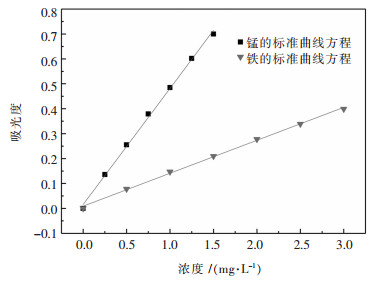 |
| 图 4 火焰原子吸收标准方程 Fig. 4 Flame atomic absorption standard equation |
铁标准曲线的绘制:用移液管移取25 mg/L的铁标准液0.00 mL、1.00 mL、2.00 mL、3.00 mL、4.00 mL、5.00 mL、6.00 mL于50 mL容量瓶中,加入硝酸(1+9)定容.选择合适的火焰原子吸收条件预热30 min,于248.3 nm测量并绘制铁的标准曲线见图 4.
标准曲线方程分别见式(1)、式(2):
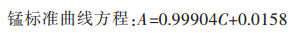
|
(1) |
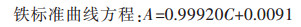
|
(2) |
线性相关系数R2分别为0.999 02、0.999 24.式(1)、式(2)中:A为溶液的吸光度;C为溶液铁、锰的浓度(mg/L).
2 结果与讨论 2.1 原料表征分析从表 1可以看出:钨冶炼渣中主要含有7.166% Mn、15.22% Ca、23.41% Fe以及含有少量的1.332% Al、1.006% W等元素. XRD图 1中分析得出,钨冶炼渣中吸收峰最强为SiO2,虽然Si元素的含量不多,SiO2的晶体结构较好,所以吸收峰较强,而且SiO2不与硫酸反应,所以浸出时二氧化硅依旧保留在浸出渣中.另外,还可以得出含有铁、锰的主要化合物为Fe2O3和NaMn(Mn, Fe)2(PO4)3这2种物质,在酸浸条件下反应比较容易.钨冶炼渣的扫描电镜为图 2(a)~图 2(d)分别为不同倍数下的扫描电镜图,可以看出:颗粒大小十分不均匀,部分较大的颗粒表面负载有小颗粒矿物质,有些非常小的针尖似的晶状物质夹杂在矿物颗粒里面.
2.2 浸出实验研究钨冶炼渣的处理方法较多,就酸浸来说一般选用3种酸:盐酸、硫酸和磷酸.通过XRF的元素分析可知,钨冶炼渣的主要成分含有Ca、Mn、Fe、O、P、Si等元素,为了在实验中不引入其它杂质,且能够使钙留在滤渣中,实验选择硫酸作为浸出剂.硫酸浸出滤渣较盐酸多,但在浸出液中不会存在大量钙离子,为以后的净化除杂制备电池级硫酸锰提供便利,另外产生的滤渣因其中含有较多的钙可以作为建筑材料加以利用.磷酸会引入磷酸根,所以不适合作为钨冶炼渣的浸出剂.
实验进行了硫酸浸出钨冶炼渣条件优化:分别考察了反应温度、酸浓度、时间、固液比和反应次数对铁、锰2种离子浸出率的影响.
2.2.1 反应温度对铁、锰浸出率的影响考察反应温度对铁、锰浸出率的影响:设定固液比1:5(g/g)、酸浓度25%(g/g)、时间为2 h,转速调整在中速,探讨温度对实验的影响.
取钨冶炼渣10 g,按照上述设定条件进行实验,温度设定在50 ℃、60 ℃、70 ℃、80 ℃、90 ℃进行.结果如图 5所示.
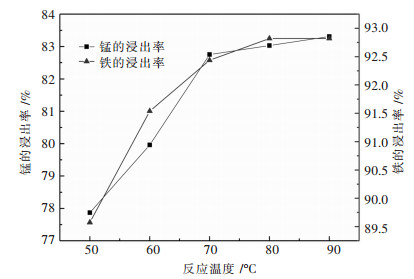 |
| 图 5 反应温度对铁、锰浸出率的影响 Fig. 5 Effect of reaction temperature on leaching of iron and manganese |
由图 5可知,铁、锰的浸出率随着温度的增加而增高.在50~70 ℃之间,浸出率增加最快,70~90 ℃之间,浸出率趋于平缓.从数据来看:温度在80 ℃时,锰的浸出率较50 ℃时多6.63%.这可能是因为钨冶炼渣中含有铁、锰的化合物与硫酸反应较为容易,温度偏低时反应也较为顺利,随着温度升高,溶液中的分子运动加剧,增加了溶液中分子的碰撞次数,而且活化分子含量相对增多,对铁、锰的浸出率有一定的提高作用,作用明显不如开始提高显著.从图 5中可以看出,为避免能量的浪费,较优温度为80 ℃.
2.2.2 酸浓度对铁、锰浸出率的影响取钨冶炼渣10 g,温度设定在80 ℃,其它条件设定不变,改变酸浓度,依次为10%、15%、20%、25%、30%(g/g)进行实验研究,结果如图 6所示.
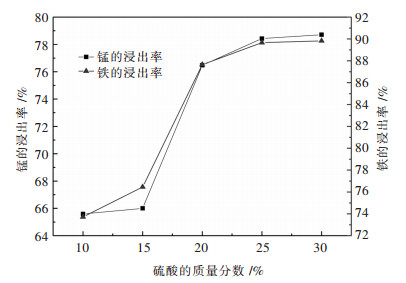 |
| 图 6 硫酸锰质量分数对铁、锰浸出率的影响 Fig. 6 Effect of manganese sulfate mass fraction on the leaching of iron and manganese |
由图 6可知,铁、锰浸出率随着硫酸浓度的增大而增大.整个范围内,铁、锰浸出率在10%~25%之间,浸出率的趋势增加较快,随后增加趋势趋于平稳.硫酸浓度为25%较10%锰的浸出率提升约19%.这可能是因为硫酸浓度低时,酸的量太少,导致反应无法全面进行,酸浓度的增加提高了溶液中H+,搅拌能够为H+带来更多反应机会,释放更多的铁、锰进入浸出液中.随后铁、锰的浸出率到了顶值,这是因为酸的用量供大于求,酸已经完全和有效物质反应完全.从图 6中可以看出,为避免设备的腐蚀,较优硫酸质量分数条件为25%.
2.2.3 反应时间对铁、锰浸出率的影响取钨冶炼渣10 g,温度设定在80 ℃,酸浓度设定在25%,其它条件设定不变,改变时间,依次为10 min、20 min、30 min、60 min、90 min、120min进行实验研究,结果如图 7所示.
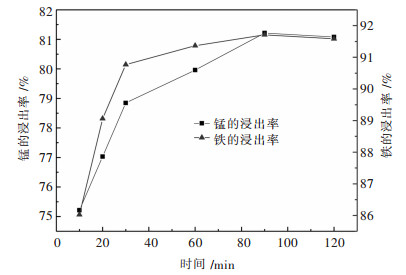 |
| 图 7 反应时间对铁、锰浸出率的影响 Fig. 7 Effect of reaction time on leaching of iron and manganese |
由图 7可知,整体上铁、锰浸出率随着时间的增加而增大.时间在10~60 min,浸出率增加幅度较大,60~120 min增加量趋于平稳,于90 min达到最大值.这可能是因为开始反应时间较短,造成反应不够充分,随着反应时间的延长,在90 min得到充分反应达到最大,随后略微降低,这是由于反应温度较高,溶液蒸发较快,溶液量的减少限制了离子活动,少量离子吸附于浸出渣中.从图 7中可以看出,较优反应时间为90 min.
2.2.4 固液比(g/g)对铁、锰浸出率的影响取钨冶炼渣10 g,温度为80 ℃,酸浓度为25%,实验时间为90 min,固液比依次为1:3、1:4、1:5、1:6、1:7进行试验研究,结果如图 8所示.
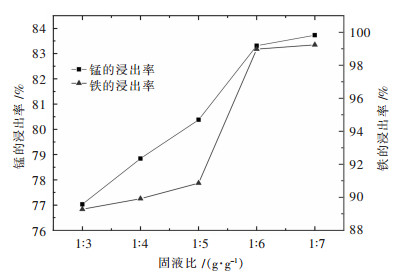 |
| 图 8 固液比对铁、锰浸出率的影响 Fig. 8 Effect of solid-liquid ratio on the leaching of iron and manganese |
由图 8可知,铁、锰浸出率随着固液比的增加而增大,在整个范围内,铁、锰浸出率先增大后趋于平稳,在1:3~1:6之间,浸出率增加幅度较大,随后增加率趋于平稳.这是因为投放初时酸容量整体较小,而且当固液比较小时,会造成溶液与原料不能够充分接触,反应的铁、锰无法顺利进入到溶液中,反应不彻底.随着固液比的增大固液充分接触,反应速率加快,并且酸容量的增大,提高了离子的扩散速度,使铁、锰离子较容易进入浸出液中.当固液比从1:6继续增大时,虽然铁、锰的浸出率有所增加,但是并没有增加很多,反而浪费了很多酸.从图 8中可以看出,较优固液比为1:6.
2.2.5 浸出次数对铁、锰浸出率的影响为了证明硫酸溶液与钨冶炼渣反应后是否彻底,实验在上述较优条件下,考察了浸出次数对浸出率的影响,如图 9所示.
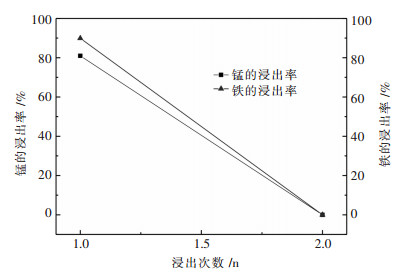 |
| 图 9 浸出次数比对铁、锰浸出率的影响 Fig. 9 Effect of leaching times on the leaching rate of iron and manganese |
由图 9可知,在实验中对钨冶炼浸出渣又进行了一次上述较优条件下的浸出研究,其结果表明铁、锰在较优条件下被硫酸溶液一次浸出完全,并未在浸出渣中残留可浸出的铁、锰化合物.
2.2.6 硫酸浸出液的循环浸出硫酸与钨冶炼渣在较优条件下反应,浸出液中酸度依旧较高(pH无法显示测量),经过计算滤液浓度大约为2.3 mol/L.实验研究了利用浸出液对新鲜钨冶炼渣的二次浸出实验,结果表明:在较优条件下,称取10 g钨冶炼渣反应,得到浸出液52.91 g(稍微润洗),然后向浸出液中加入8.82 g钨冶炼渣,反应完全后,测定铁、锰的浸出量分别为3.045 g和0.832 5 g,分别提高了大约50%和38%.铁浸出率提高的百分比大于锰浸出率提高的百分比,可能是因为酸与钨冶炼渣反应时铁化合物与硫酸反应活化能较低,反应较先发生.在化合物反应方面,铁的化合物较锰的化合物更活泼.
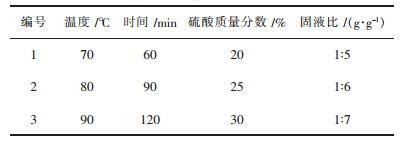
2.2.7 钨冶炼渣浸出工艺正交实验为节约成本,以反应温度(℃)、时间(min)、硫酸质量分数(%)、固液比(g/g)对铁、锰的浸出量影响为因素,选择较优条件附近的3个数据作为水平,设计L9(3)4的正交实验,结果如表 2、表 3、表 4.
| 表 2 正交实验水平因素表 Table 2 Orthogonal experiment level factor table |
 |
| 点击放大 |
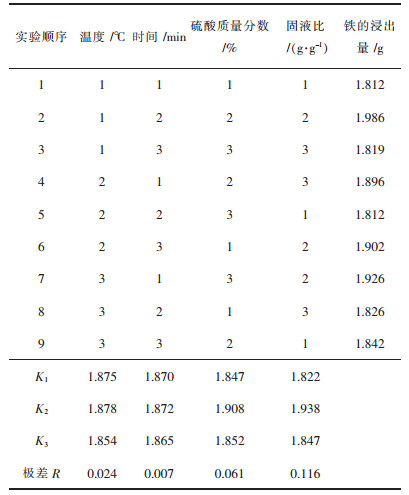
| 表 3 正交实验结果及直观分析(铁浸出量) Table 3 Orthogonal experimental results and visual analysis (iron leaching amount) |
 |
| 点击放大 |
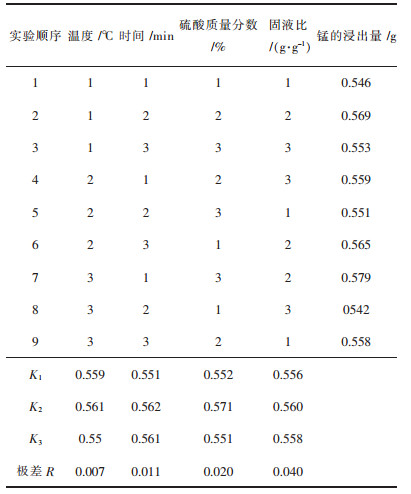
| 表 4 正交实验结果及直观分析(锰浸出量) Table 4 Orthogonal experimental results and visual analysis (manganese leaching amount) |
 |
| 点击放大 |
正交实验表 3、表 4的结果分析:从铁的浸出率来看极差R,固液比的极差值最大、其次为质量分数,极差大小代表了对浸出量的影响的大小,即对铁的浸出率的影响大小是固液比>质量分数>反应温度>反应时间.从锰浸出量的极差R来看,对锰的浸出量影响条件顺序为:固液比>反应时间>质量分数>反应温度,不管从那个条件来看,固液比对铁、锰浸出量影响都是最大的.从铁、锰的极差数值差别可以看出数值差别并不是很大,这可能是因为铁、锰化合物活化能较低,反应较快.为了能够最大程度地浸出锰,实验选定较优条件:固液比为1:6,反应时间为90 min,质量分数为25%,温度为80 ℃.
2.3 铁、锰浸出过程动力学钨冶炼渣在低质量分数稀酸浸出时基本不溶解,另外从扫描电镜也可以看出大部分颗粒呈球形状态,所以可以用缩核模型[26]进行动力学分析,液-固浸出动力学中有2种控制步骤分别为化学反应为控制步骤、通过产物层的扩散为控制步骤.控制性质的改变决定了速率方程的不同.
当浸出受化学反应为主导时,速率方程如式(3),当受产物层扩散为主导时,方程如式(4).
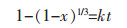
|
(3) |
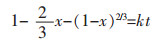
|
(4) |
式(3)、式(4)中:x为浸出率,k代表方程斜率.
将温度80 ℃、不同时间条件下所得到的锰、铁浸出率分别代入式(3)和式(4),通过计算得到公式(4)较符合线性回归关系,即铁、锰浸出关系受到产物层扩散为控制步骤,线性回归见图 10.
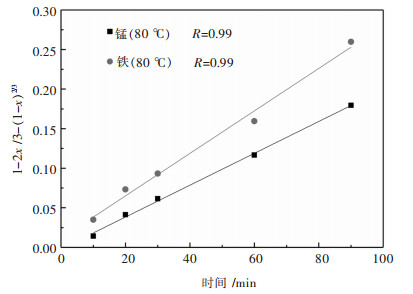 |
| 图 10 产物层扩散控制时铁、锰浸出动力学曲线 Fig. 10 Leaching kinetics of iron and manganese during product layer control |
如图 10所示,线性回归方程相关度R较高,符合产物层控制动力学方程.这可能是因为利用硫酸浸出钨冶炼渣时,其中的硫酸根与钙离子发生反应生产硫酸钙沉淀覆盖在矿物表面,形成了牢固高扩散阻力层,阻碍了反应的进行.另外铁的浸出动力学曲线斜率较高,说明铁更容易浸出,循环浸出率的提高差别也可以验证这一点.
3 结论1)通过对原料的表征:XRF分析得到原料中主要含有Fe、Mn、Ca、O 4种元素、少量重金属离子及非金属离子;XRD表征得出含有铁、锰主要化合物为Fe2O3、NaMn(Mn, Fe)2(PO4)3;SEM形貌分析得出颗粒大小不均匀,大颗粒表面吸附少量小颗粒物质,并且少量针状晶体物质夹杂在矿物中.
2)通过对钨冶炼渣浸出工艺研究,得到了浸出实验的较优条件:温度为80 ℃、硫酸的质量分数为25%、时间为90 min、固液比为1:6.铁、锰在较优条件下可以被硫酸溶液一次性完全浸出可反应的铁、锰化合物.硫酸浸出液的循环浸出实验可以使浸出溶液中铁、锰的浸出率大约提高50%和38%,达到3.0 g和0.83 g.通过计算得到铁、锰的浸出动力学较符合产物层的扩散为控制步骤,铁浸出速率较锰高.
| [1] |
JI N, ZHANG T, ZHENG M, et al. Direct catalytic conversion of cellulose into ethylene glycol using nickel-promoted tungsten carbide catalysts[J].
Angewandte Chemie, 2008, 47(44): 8510–8513. DOI: 10.1002/anie.v47:44. |
| [2] |
LIM S H N, ISIDORSSON J, SUN L, et al. Modeling of optical and energy performance of tungsten-oxide-based electrochromic windows including their intermediate states[J].
Solar Energy Materials & Solar Cells, 2013, 108(108): 129–135. |
| [3] |
WANG Y, SONG S, MARAGOU V, et al. High surface area tungsten carbide microspheres as effective Pt catalyst support for oxygen reduction reaction[J].
Applied Catalysis B Environmental, 2009, 89(1/2): 223–228. |
| [4] |
金属百科. 钨资源分布和产量. http://baike.asianmetal.cn/metal/w/resources&production.shtml, 2016. 10. 23/2018. 4. 3
|
| [5] |
佚名. 再工业化-工业化4.0时代的新思路[J].
智慧工厂, 2016(9): 39–40.
|
| [6] |
贠天一. 工业4.0-工业化的第四阶段[J].
中国战略新兴产业, 2015(2): 44–46.
|
| [7] |
闫升. 钨矿浸出渣制备电子级硫酸锰[D]. 长沙: 中南大学, 2014.
http://cdmd.cnki.com.cn/Article/CDMD-10533-1014406282.htm |
| [8] |
陈沛云, 冯秀娟. 钨尾矿农田重金属空间分布特征研究[J].
安徽农业科学, 2011, 39(23): 14039–14040.
DOI: 10.3969/j.issn.0517-6611.2011.23.057.
|
| [9] |
赵武, 霍成立, 刘明珠, 等. 有色金属尾矿综合利用的研究进展[J].
中国资源综合利用, 2011, 29(3): 24–28.
DOI: 10.3969/j.issn.1008-9500.2011.03.004.
|
| [10] |
焦向科, 罗仙平, 李佳, 等. 钨尾矿预处理制备矿物聚合材料[J].
硅酸盐通报, 2015, 34(12): 3610–3616.
|
| [11] |
卢安贤, 吴婷, 刘涛涌, 等. 一种以钨尾矿为主要原料的高强度陶瓷及其制备方法: CN104496433A[P]. 2015-10-01.
|
| [12] |
朱刚雄, 王海. 钨尾矿在水泥胶砂中的应用[J].
矿产保护与利用, 2017(5): 82–86.
|
| [13] |
司加保, 李琳, 黄震. 用钨尾矿制备水泥混合材实验[J].
现代矿业, 2016(7): 222–225.
DOI: 10.3969/j.issn.1674-6082.2016.07.077.
|
| [14] |
何桂春, 肖策环. 江西某钨尾矿浮选实验[J].
有色金属科学与工程, 2015, 6(6): 82–87.
|
| [15] |
戴艳阳, 钟晖, 钟海云. 钨渣回收制备四氧化三锰新工艺[J].
中国有色金属学报, 2012, 22(4): 1242–1247.
|
| [16] |
杨秀丽, 王晓辉, 向仕彪, 等. 盐酸法富集钨渣中的钽和铌[J].
中国有色金属学报, 2013(3): 873–881.
|
| [17] |
卢友中. 选冶联合工艺从钨尾矿及细泥中回收钨的实验研究[J].
江西理工大学学报, 2009, 30(3): 70–73.
|
| [18] |
房朝军, 冯其明, 欧乐明, 等. 某钨尾矿综合回收低品位萤石浮选实验研究[J].
有色金属科学与工程, 2014(2): 72–76.
|
| [19] |
艾光华, 李继福, 邬海滨, 等. 从某黑白钨尾矿中回收萤石的实验研究[J].
非金属矿, 2016, 39(3): 33–35.
DOI: 10.3969/j.issn.1000-8098.2016.03.011.
|
| [20] |
吴师金, 陈军, 黄六老. 江西大余某钨锡尾矿云母、长石和石英分离研究[J].
现代矿业, 2017(11): 135–137.
DOI: 10.3969/j.issn.1674-6082.2017.11.037.
|
| [21] |
王丰, 刘成士, 曹利娜, 等. 三元正极材料LixNiyCo2Mn2-x-y-zO2的研究现状[J].
电池, 2016, 46(2): 109–112.
DOI: 10.3969/j.issn.1001-1579.2016.02.014.
|
| [22] |
YABUUCHI N, OHZUKU T. Novel lithium insertion material of LiCo3Ni3Mn3O2, for advanced lithium-ion batteries[J].
Journal of Power Sources, 2003, 119/120/121(6): 171–174. |
| [23] |
MURALIGANTH T, STROUKOFF K R, MANTHIRAM A. Microwave-solvothermal synthesis of nanostructured Li2MSO4/C(M: Mn and Fe) cathodes for lithium-ion batteries[J].
Cheminform, 2010, 22(20): 5754–5761. |
| [24] |
JIN E M, JIN B, JEON Y S, et al. Electrochemical properties of LiMn2O4 for lithium polymer battery[J].
Journal of Power Sources, 2009, 189(1): 620–623. DOI: 10.1016/j.jpowsour.2008.09.102. |
| [25] |
DING Y L, XIE J, CAO G S, et al. Single-crystalline LiMn2O4 nanotubes synthesized via template-engaged reaction as cathodes for high-power lithium ion batteries[J].
Advanced Functional Materials, 2011, 21(2): 348–355. DOI: 10.1002/adfm.201001448. |
| [26] |
郭钟群, 金解放, 王观石, 等. 风化壳淋积稀土矿浸取动力学基础理论研究[J].
有色金属科学与工程, 2017, 8(5): 127–132.
|
 2018, Vol. 9
2018, Vol. 9


