| 离子型稀土矿土壤对铜的吸附解吸特性 |
b. 江西理工大学, 资源与环境工程学院,江西 赣州 341000
b. School of Resources and Environment Engineering, Jiangxi University of Science and Technology, Ganzhou 341000, China
稀土由于其独特的物理化学性质而被广泛应用于各领域,尤其在“高”、“精”、“尖”产业领域发挥着重要作用[1-3].稀土开采过程中,由于工艺落后、管理不善、环保意识淡薄等导致土壤受重金属污染[4-7].Cu虽然是生物必需的微量元素,许多生理过程都有Cu参与,但又是环境污染的主要重金属之一,因具有隐蔽、难降解、移动性差等特性,可通过大气、水体或食物链进入人体,危害人体健康[8-9].目前,土壤中Cu污染事件进入高发期和多发期,引起了社会和学术界的广泛关注,成为土壤环境污染和预防研究的重点.
吸附-解吸特征是土壤的重要特征之一[10-12],影响重金属在土壤中的形态转化、迁移和归趋,因此研究土壤重金属的吸附解吸在生态环境领域具有重要的意义.重金属在土壤中的吸附解吸与重金属种类、土壤性质及环境条件有关,国内外学者对土壤的吸附-解吸行为已经进行了系统的研究,但是针对离子型稀土矿区土壤重金属吸附-解吸的研究较少报道,只是局限于对矿区土壤重金属的调查[13].刘胜洪等[14]对广东省稀土废弃矿的调查表明,Zn、Pb、Mn的含量偏高,Pb的含量高达(532.6±80.2) mg/kg,且3种重金属含量远远超过中国土壤背景值.滕达等[15]对冕宁县稀土尾矿区土壤中的重金属进行调査,结果表明,Pb、Zn的污染非常严重且含量范围分别为1 193~5 077 mg/kg、38~239 mg/kg.对此,选择原矿、尾矿土为研究对象,采用振荡平衡法,对Cu的吸附-解吸过程进行详细研究,以期为矿区土壤重金属污染评价、土壤修复提供科学依据和基础数据.
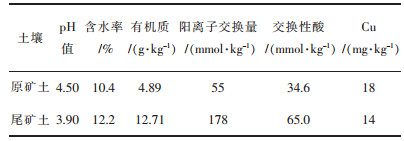
1 材料与方法 1.1 供试土壤供试土壤采自赣州市龙南县足洞矿区的原矿土与尾矿土,采样深度为0~20 cm表层土.土样放阴凉处自然风干,去除杂物,过0.25 mm筛后保存在聚乙烯塑料袋中备用.土壤的理化性质见表 1.
| 表 1 土壤的基本理化性质 Table 1 Basic physical and chemical properties of soil |
 |
| 点击放大 |
1.2 实验方法 1.2.1 吸附-解吸等温实验
吸附、解吸采用一次平衡法.称取0.200 g土壤于50 mL塑料离心管中,分别加入20 mL不同浓度5 mg/L、10 mg/L、20 mg/L、30 mg/L、40 mg/L、50 mg/L、60 mg/L的Cu溶液,温度恒定在25 ℃,转速为160 r/min,恒温平衡24 h后,以5 000 r/min速度离心10 min,上清液用0.45 μm水系滤膜过滤,用原子吸收分光光度法测Cu浓度.剩余残渣用于解吸试验,向离心管中加入0.01 mmol/L EDTA溶液20 mL进行解吸,其余步骤同吸附试验.
1.2.2 吸附动力学实验称取2.500 g土壤于500 mL锥形瓶中,加入10 mg/L的Cu溶液250 mL.在25 ℃条件下恒温振荡,原矿土分别在5 min、15 min、30 min、40 min、50 min、90 min、120 min、130 min、150 min取样;尾矿土分别在5 min、10 min、15 min、40 min、60 min、80 min、100 min、120 min、140 min取样.以5 000 r/min速度离心10 min,上清液用0.45 μm水系滤膜过滤,用原子吸收分光光度法测Cu浓度.
1.3 数据计算 1.3.1 吸附量或解吸量计算根据Cu的初始浓度与平衡浓度之差计算吸附量或解吸量,方程如下:
| $ Q_e = \frac{{(C_0-C_e)V}}{m} $ | (1) |
式(1)中:Qe为单位质量土壤吸附或解吸重金属的量,mg/kg;C0为重金属的初始浓度,mg/L;Ce为重金属的平衡浓度,mg/L;V为溶液的体积,mL;m为土壤的质量,g.
1.3.2 重金属在土壤中模型拟合1) 等温吸附模型
| $ {\rm{Langmuir模型:}}Q_e = \frac{{bQC_e}}{{1 + bC_e}} $ | (2) |
| $ {\rm{Freundlich模型:}}Q_e = {K_F}C_e^{1/n} $ | (3) |
| $ {\rm{Temkin模型:}}Q_e = A{\rm{ln}}{C_e} + B $ | (4) |
式(2)、式(3)、式(4)中:Qe为吸附平衡时重金属的吸附量,mg/g;Q为重金属的最大吸附量,mg/g;Ce为吸附平衡时溶液中重金属的浓度,mg/L;b为与结合强度有关的常数,L/mg;KF为表征吸附表面强度的指标,L/mg;1/n为各向异性指数;A、B为常数,分别与最大吸附量和吸附能有关.
2) 动力学模型
准一级吸附动力学模型:
| $ \log({Q_e}-{Q_t}) = \log {Q_e}-\frac{{{K_1}t}}{{2.303}} $ | (5) |
| $ {\rm{准二级吸附动力学模型:}}\frac{t}{{{Q_t}}} = \frac{1}{{{K_2}Q_e^2}} + \frac{t}{{{Q_e}}} $ | (6) |
| $ {\rm{Elovich模型:}}{Q_t} = A + {K_t}\ln t $ | (7) |
式(5)、式(6)、式(7)中:Qe是平衡时溶质在单位质量吸附剂上的吸附量,mg/g;Qt是t时刻溶质在单位质量吸附剂上的吸附量,mg/g;K1、K2是准一级、二级吸附动力学速率常数,min-1;t是反应时间,min;Kt是反应速率常数,mg·g·min-0.5;A为扩散速率常数,mg/g.
2 结果与讨论 2.1 Cu在土壤中的等温吸附原矿、尾矿土对Cu的吸附等温线如图 1、图 2所示.吸附等温线根据离原点最近曲线斜率的变化分为4大类,分别为“L”、“H”、“C”、“S”型[16-17].由图 1、图 2可知,原矿、尾矿土对Cu的吸附等温线均属于“L”型,属于单分子层吸附.原矿、尾矿土对Cu的吸附量均随着Cu浓度的增加而增大.当平衡浓度较低时,2种土壤对Cu的吸附量均随Cu浓度的增加而快速增加;随着平衡浓度的提高,2种土壤对Cu的吸附量增加幅度逐渐趋缓.研究表明,低浓度Cu首先与土壤的高能吸附位点结合,此时土壤对Cu的亲和力较大能快速被吸附.随着处理浓度的增加,与土壤的高能吸附位点结合呈现饱和后才依次与低能吸附位点结合,随着吸附剂中的吸附位被覆盖,吸附质分子越来越难撞到表面吸附位上,从而使土壤中Cu浓度与溶液中Cu浓度形成动态平衡[18-19].
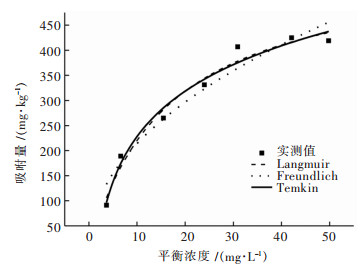 |
| 图 1 Cu在原矿土中的吸附等温线 Fig. 1 Adsorption isotherms of Cu in ore soil |
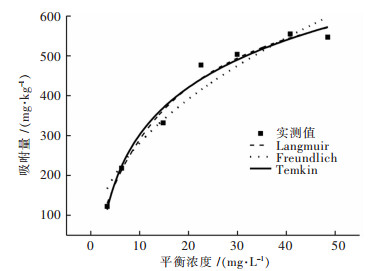 |
| 图 2 Cu在尾矿土中的吸附等温线 Fig. 2 Adsorption isotherms of Cu in tailings soil |
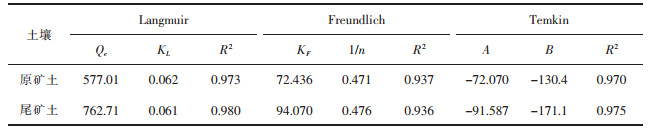
为了更好地解释原矿、尾矿土对Cu的吸附机理,选用Langmuir、Freundlich、Temkin模型对Cu等温吸附数据进行拟合(表 2).
| 表 2 Cu在土壤中等温吸附方程的拟合参数 Table 2 Fitting parameters of Cu in soil isothermal adsorption equation |
 |
| 点击放大 |
结果表明,Langmuir、Frundlich、Temkin模型可较好的拟合Cu在原矿、尾矿土中的等温吸附,相关系数R2均大于0.93,其中Langmuir模型拟合效果最好. Langmuir模型是基于吸附剂表面均匀且同向、吸附是单分子层吸附、存在最大吸附量3种假设基础上建立的[20].其中,KL表示吸附亲和力,值越小,亲和力越大;最大吸附量Qe表征土壤对重金属的吸附容量的指标[21].根据拟合结果可知,原矿、尾矿土对Cu的最大吸附量分别为577.01 mg/kg、762.71 mg/kg,说明尾矿土对Cu的吸附能力大于原矿土.这可能与有机质含量有关,有机质影响土壤颗粒对重金属的吸附能力,因其具有多种含氧功能团,如羧基、羟基、酮基等, 容易与金属离子形成稳定的络合、螯合产物,故有机质含量较高者对重金属有较大的吸附容量,这与前人的研究结果一致[22].胡宁静等[23]采用性质接近的乌黄土和青紫泥为试验土壤,用30 %H2O2去除有机质后对Pb进行吸附实验.结果表明,去除有机质后2种土壤对Pb的吸附量明显降低,说明有机质含量高对重金属的吸附量大.
2.2 Cu在土壤中的动力学吸附原矿、尾矿土对Cu的吸附量随时间的变化情况如图 3、图 4所示.从图 3、图 4中可以看出,2种土壤对Cu的吸附分为2个阶段,第1阶段为快速吸附阶段,反应速度很快,几乎呈直线上升;第2阶段为慢速吸附阶段,吸附曲线缓慢增加,之后变得十分平缓.原矿土对Cu的吸附在0~40 min内是快速吸附阶段,Cu的吸附量占总吸附量的85.44 %,在40~150 min内属于慢速吸附阶段;尾矿土对Cu的吸附在0~15 min内是快速吸附阶段,Cu的吸附量占总吸附量的89.58 %,在15~140 min内属于慢速吸附阶段.一般认为快速吸附阶段主要由化学反应和表面扩散机制决定的,而慢速吸附阶段主要与重金属离子向无机矿物和有机质的微孔扩散、表面沉淀现象有关.不同土壤吸附不同重金属时,对吸附过程划分情况不同.宋凤敏等[24]研究黄褐土与水稻沙田土对Mn和Ni的吸附动力学试验表明,吸附分为3个阶段,第1个阶段是慢速吸附,吸附量增加较慢;第2个阶段是快速吸附,吸附量增加较快;第3个阶段是慢速吸附,吸附量增加缓慢.任力洁等[25]研究湖库周边土壤对Pb的吸附动力学试验表明,吸附分为2个阶段,快速吸附阶段在0~60 min内,吸附量占吸附总量的96.83 %,60~1 440 min内是慢速吸附阶段.
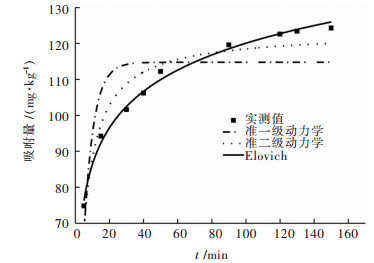 |
| 图 3 Cu在原矿土中的动力学方程拟合 Fig. 3 Kinetic equation fitting of Cu in ore soil |
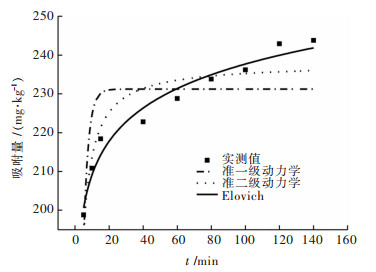 |
| 图 4 Cu在尾矿土中的动力学方程拟合 Fig. 4 Kinetic equation fitting of Cu in tailings soil |
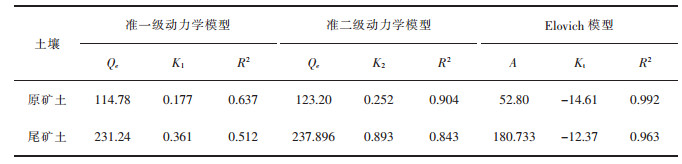
为了研究Cu在原矿、尾矿土上吸附速率变化的规律,用准一级动力学、准二级动力学、Elovich模型对Cu吸附动力学进行拟合(表 3).结果表明,Elovich模型描述Cu的吸附过程,可以明确的表达Cu在颗粒内的扩散机制,其R2分别为0.992、0.963;准二级动力学模型拟合效果次之,其R2分别为0.904、0.843;准一级动力学模型拟合效果最差.说明Elovich模型更适合描述原矿、尾矿土对Cu的吸附动力学过程. Elovich方程中,A值代表吸附速率的快慢,值越大吸附速率越快,尾矿土的A值大于原矿土,表明尾矿土吸附Cu的速率大于原矿土.从图 3、图 4可知,原矿土和尾矿土对Cu的最大吸附量分别为124.30 mg/kg、243.80 mg/kg.另外,通过准二级动力学方程拟合的Qe值(123.2 mg/kg、237.896 mg/kg)与实测值较接近.
| 表 3 Cu在土壤中的吸附动力学参数 Table 3 Adsorption kinetics parameters of Cu in soil |
 |
| 点击放大 |
2.3 Cu在土壤中的解吸特性
图 5所示为Cu在原矿、尾矿土上的解吸量随解吸平衡浓度的变化情况.研究采用EDTA作为解吸剂.从图 5中可以看出,随着平衡浓度的增加,Cu在原矿、尾矿土的解吸量持续增大.总体来说,原矿土和尾矿土的解吸量远远大于其吸附量,说明这2种土壤对Cu的吸附不存在滞后现象,被吸附的Cu易被解吸.研究表明,酸性条件下有利于重金属离子的解吸,原矿土(pH为4.5)、尾矿土(pH为3.9)是酸性的,故易发生解吸.对比研究发现Cu在尾矿土中的吸附量Qe大于原矿土,说明尾矿土对Cu的亲和力大于原矿土,故Cu在原矿土中较易发生解吸.另外,EDTA作为解吸剂本身含有Na对Cu有直接置换能力,另一方面,EDTA是很强的螯合剂,能将部分与土壤紧密吸附的或被其他螯合剂螯合的Cu解吸出来[26].EDTA不仅可以解吸被吸附的Cu,也能溶解不溶性的金属化合物;EDTA能活化土壤中的Cu,使残渣态的Cu转化为较易解吸的其他形态[27].因此,EDTA被用作土壤重金属修复的螯合剂.
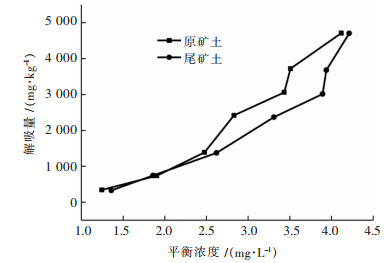 |
| 图 5 Cu在原矿、尾矿土中的解吸量 Fig. 5 Desorption of Cu in the ore and tailings soil |
2.4 Cu在土壤中的解吸特性与吸附作用的关系
原矿、尾矿土对Cu的解吸量与吸附量的关系如图 6所示.从图 6中可以看出,Cu在原矿土和尾矿土中的解吸曲线是向上弯曲的,解吸量随Cu的吸附量的增加而增加,但解吸过程并不是吸附过程的逆过程.当低吸附区域时,解吸量较小,在高吸附区域时,解吸量较大.主要原因是,当Cu浓度较低时,土壤对Cu的吸附主要以专性吸附为主,Cu占据着高能结合位点,解吸剂很难将其置换下来.达到一定饱和度后,专性吸附位点减少,此时主要以非专性吸附为主,土壤对Cu的吸附势降低,被土壤吸附的Cu稳定性也降低,故易于解吸,解吸量也随之增加[28].
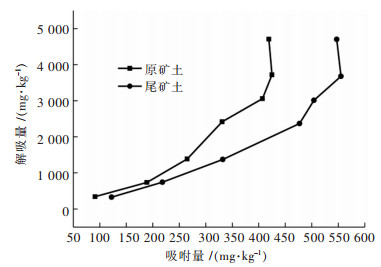 |
| 图 6 Cu在原矿土、尾矿土中的吸附量-解吸量关系 Fig. 6 Relationship between adsorption and desorption of Cu in ore and tailings soil |
土壤中重金属的解吸过程与吸附行为密切相关.为了进一步了解原矿土和尾矿土中Cu的解吸量与吸附量的关系,对2种土壤中Cu解吸量随吸附量的变化进行模拟,发现二次幂函数模拟效果最好.
| $ {\rm{原矿土:}}Y = 0.030{X^2}-4.561X + 511.5\;\;{R^2} = 0.927 $ | (8) |
| $ {\rm{尾矿土:}}Y = 0.021{X^2}-6.076X + 887.3\;\;{R^2} = 0.929 $ | (9) |
式(8)、式(9)中:Y为Cu的解吸量,mg/kg,X为解吸前Cu的吸附量,mg/kg.
从上述方程可以看出,Cu的解吸量随吸附量的增加而增加,并呈现极显著的幂函数关系.解吸量较高的原因可能与原矿土和尾矿土中的砂粒相关,土壤砂粒含量高,土壤的结构性就差,与重金属结合后形成的产物稳定性较低,故易发生解吸[29].解吸能力的大小,直接影响着地下水、土壤溶液以及生物吸收重金属的多少.因此,通过研究Cu的解吸行为,可以预测土壤环境中Cu的迁移和归宿,为重金属污染土壤的修复、治理提供有价值的参考.
3 结论1) 原矿土、尾矿土对Cu的吸附过程可以用Langmuir、Freundlich、Temkin模型进行拟合. Langmuir模型拟合效果最好,其相关系数R2分别为0.973、0.980.尾矿土对Cu的吸附量大于原矿土,这可能与有机质含量有关,有机质含量较高者对重金属有较大的吸附容量,这与前人的研究结果一致.
2) 原矿土、尾矿土对Cu的吸附包括快速吸附、慢速吸附2个过程.原矿土对Cu的吸附在0~40 min内是快速吸附阶段,Cu的吸附量占总吸附量的85.44 %;尾矿土对Cu的吸附在0~15 min内是快速吸附阶段,Cu的吸附量占总吸附量的89.58 %.
3) Cu在原矿土、尾矿土上的解吸量随解吸平衡浓度的增加而增大.尾矿土对Cu的吸附量Qe大于原矿土,说明尾矿土对Cu的亲和力大于原矿土,故原矿土较易发生解吸.对原矿、尾矿土中Cu解吸量随吸附量的变化进行模拟,发现二次幂函数模拟效果最好,且解吸量也随吸附量的增加而增加.
| [1] |
肖子捷, 刘祖文, 张念. 离子型稀土采选工艺环境影响分析与控制技术[J].
稀土, 2014, 35(6): 56–61.
|
| [2] |
吴迪, 钱贵霞. 中国稀土产业经济研究现状与发展趋势分析[J].
稀土, 2014, 35(5): 104–112.
|
| [3] |
池汝安, 田君, 罗仙平, 等. 风化壳淋积型稀土矿的基础研究[J].
有色金属科学与工程, 2012, 3(4): 1–13.
|
| [4] |
中华人民共和国国务院新闻办公室. 中国的稀土状况与政策[J].
中国金属通报, 2012(24): 20–24.
|
| [5] |
王友生, 侯晓龙, 吴鹏飞, 等. 长汀稀土矿废弃地土壤重金属污染特征及其评价[J].
安全与环境学报, 2014, 14(4): 259–262.
|
| [6] |
邹国良, 吴一丁, 蔡嗣经. 离子型稀土矿浸取工艺对资源、环境的影响[J].
有色金属科学与工程, 2014, 5(2): 100–106.
|
| [7] |
温春辉, 刘祖文, 张念, 等. 模拟酸雨对赣南稀土矿淋滤实验研究[J].
有色金属科学与工程, 2016, 7(3): 113–117.
|
| [8] |
李淑敏, 李红, 孙丹峰, 等. 北京耕作土壤4种重金属空间分布的网络特征分析[J].
农业工程学报, 2012, 28(23): 208–215.
|
| [9] |
周建军, 周桔, 冯仁国. 我国土壤重金属污染现状及治理战略[J].
中国科学院院刊, 2014, 29(3): 315–320.
|
| [10] |
ARIAS M, PéREZNOVO C, OSORIO F, et al. Adsorption and desorption of copper and zinc in the surface layer of acid soils[J].
Journal of Colloid & Interface Science, 2005, 288(1): 21–29. |
| [11] |
JANG A, SEO Y, BISHOP P L. The removal of heavy metals in urban runoff by sorption on mulch[J].
Environmental Pollution, 2005, 133(1): 117–127. DOI: 10.1016/j.envpol.2004.05.020. |
| [12] |
MARKIEWICZ-PATKOWSKA J, HURSTHOUSE A, PRZYBYLA-KIJ H. The interaction of heavy metals with urban soils: sorption behaviour of Cd, Cu, Cr, Pb and Zn with a typical mixed brownfield deposit[J].
Environment International, 2005, 31(4): 513–517. DOI: 10.1016/j.envint.2004.09.004. |
| [13] |
缪鑫, 李兆君, 龙健, 等. 不同类型土壤对汞和砷的吸附解吸特征研究[J].
核农学报, 2012, 26(3): 552–557.
|
| [14] |
刘胜洪, 张雅君, 杨妙贤, 等. 稀土尾矿区土壤重金属污染与优势植物累积特征[J].
生态环境学报, 2014, 23(6): 1042–1045.
|
| [15] |
滕达. 四川省冕宁县牦牛坪稀土尾矿区植物修复研究[D]. 成都: 成都理工大学, 2009.
|
| [16] |
LIMOUSIN G, GAUDET J P, CHARLET L, et al. Sorption isotherms: A review on physical bases, modeling and measurement[J].
Applied Geochemistry, 2007, 22(2): 249–275. DOI: 10.1016/j.apgeochem.2006.09.010. |
| [17] |
HINZ C. Description of sorption data with isotherm equations[J].
Geoderma, 2001, 99(3/4): 225–243. |
| [18] |
黄冠星, 王莹, 刘景涛, 等. 污灌土壤对铅的吸附和解吸特性[J].
吉林大学学报(地球科学版), 2012, 42(1): 220–225.
|
| [19] |
SINEGANI A A S, ARAKI H M. The effects of soil properties and temperature on the adsorption isotherms of lead on some temperate and semiarid surface soils of Iran[J].
Environmental Chemistry Letters, 2010, 8(2): 129–137. DOI: 10.1007/s10311-009-0199-9. |
| [20] |
刘晶晶. Pb(Ⅱ)、Cu(Ⅱ)、Cd(Ⅱ)在黄土上竞争吸附及解吸特性研究[D]. 杭州: 浙江大学, 2014.
|
| [21] |
LU S G, XU Q F. Competitive adsorption of Cd, Cu, Pb and Zn by different soils of Eastern China[J].
Environmental Geology, 2009, 57(3): 685–693. DOI: 10.1007/s00254-008-1347-4. |
| [22] |
李仁英, 周志高, 岳海燕, 等. 水溶性有机质对南京城郊菜地土壤Pb吸附解吸行为的影响[J].
农业环境科学学报, 2011, 30(5): 867–873.
|
| [23] |
胡宁静, 骆永明, 中宋静. 长江三角洲地区典型土壤对镉的吸附及其与有机质、pH和温度的关系[J].
土壤学报, 2007, 44(3): 437–443.
DOI: 10.11766/trxb200601100309. |
| [24] |
宋凤敏, 张兴昌, 葛红光, 等. 黄褐土与水稻田沙土对Mn(Ⅱ)和Ni(Ⅱ)的吸附[J].
水土保持学报, 2017, 31(1): 265–271.
|
| [25] |
任力洁, 马秀兰, 边炜涛, 等. 湖库底泥对重金属Pb吸附特性的研究[J].
水土保持学报, 2016, 30(5): 255–260.
|
| [26] |
许超, 夏北城, 林颖. EDTA和柠檬酸对污染土壤中重金属的解吸动力学及其形态的影响[J].
水土保持学报, 2009, 23(4): 146–151.
|
| [27] |
陈志良, 雷国建, 赵述华, 等. EDTA、茶皂素及其混剂对土壤中Pb、Zn的解吸效果[J].
环境化学, 2014(8): 1314–1320.
DOI: 10.7524/j.issn.0254-6108.2014.08.012. |
| [28] |
刘铮, 白英, 刘琴, 等. 熟污泥改性黄土对铜的吸附解吸特征[J].
中国环境科学, 2014, 34(9): 2306–2312.
|
| [29] |
房莉, 余健, 张彩峰, 等. 不同土地利用方式土壤对铜、镉离子的吸附解吸特征[J].
中国生态农业学报, 2013, 21(10): 1257–1263.
|
 2018, Vol. 9
2018, Vol. 9


