| 原位观察电子束辐照条件下SUS316L钢中辐照肿胀行为 |
b. 北京科技大学钢铁冶金新技术国家重点实验室,北京 100083
b. State Key Laboratory of Advanced Metallurgy, University of Science and Technology Beijing, Beijing 100083, China
随着核反应堆服役时间不断增长,功率不断增大,堆中包壳和结构材料用奥氏体不锈钢的辐照肿胀问题日益凸显[1-5].辐照肿胀是由材料内空位聚集形成空洞所引起,会使材料体积发生膨胀,造成紧固件断裂,危害反应堆安全.现有的抑制肿胀方法有冷加工和添加合金元素[6-8],但研究表明,经这2种方法处理的奥氏体不锈钢所能经受的辐照剂量无法超过100 dpa[9-10],远未达到先进核反应堆对奥氏体不锈钢性能的要求.
核反应堆是相对封闭的高危环境,无法原位观察反应堆中奥氏体不锈钢的辐照肿胀行为[11].奥氏体不锈钢在核反应堆中应用广泛,其服役温度也相对较宽,如压水堆中工作温度约为300 ℃[12],而快堆中工作温度却在500 ℃左右[13].利用超高压电子显微镜,Sekio等[14]对奥氏体不锈钢在450 ℃下的辐照肿胀行为进行原位观察.考虑到工作温度不同,奥氏体不锈钢在核反应堆中的辐照肿胀行为必然也存在差异,因此,有必要对奥氏体不锈钢在其他温度下的辐照肿胀行为进行系统原位观察和分析.
以SUS316L奥氏体不锈钢为研究对象,原位观察其在300~500 ℃区间内电子辐照过程中的辐照肿胀行为,对比分析不同辐照温度下空洞形核及长大的差异,为预测不同工作温度下奥氏体不锈钢辐照肿胀情况提供实验依据.
1 材料及方法本研究所用材料为SUS316L奥氏体不锈钢,其化学成分如表 1所示.
| 表1 SUS316L奥氏体不锈钢化学成分/(质量分数,%) Table 1 Chemical composition of SUS316L austenitic stainless steel /(mass fraction, %) |
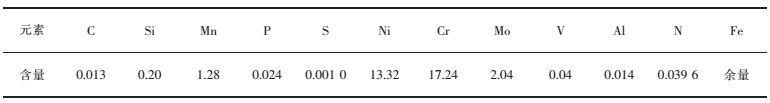 |
| 点击放大 |
利用超高压电子显微镜 (型号为JEOL,JEM-ARM1300) 对直径为3 mm的透射电镜薄膜试样进行电子束辐照.辐照电压1 250 kV,辐照剂量3.6 dpa (30 min),辐照温度分别为300 ℃、350 ℃、400 ℃、450 ℃和500 ℃.辐照过程中,对辐照区形貌进行原位观察.辐照完成后,利用透射电镜 (Tecnai G2 F20) 观察辐照后空洞分布,并利用Image-pro plus软件对空洞尺寸进行测量统计.
2 结果及讨论 2.1 电子束辐照条件下辐照区形貌变化电子束辐照过程中,试样内不断引入过饱和点缺陷,即空位和间隙原子[15-16].为趋于能量平衡,这些过饱和点缺陷会不断扩散迁移,聚集形成位错环、空洞等二次缺陷[17-18].以500 ℃电子束辐照过程中原位观察辐照区形貌变化为例,如图 1所示.辐照前由于取向差异,晶界两侧视场衬度不同,但并无点缺陷簇、位错环等缺陷组织 (图 1(a)).辐照5 min后,晶界附近产生大量点缺陷簇,而且越靠近晶界,点缺陷簇的密度越高 (见图 1(b)).受晶界的尾闾作用[19],辐照引入的过饱和点缺陷不断向晶界扩散,导致晶界附近点缺陷相互聚集几率增加,点缺陷簇密度也随之增大.随着辐照时间增长,形成点缺陷簇和位错环的区域也不断增大.辐照30 min后,整个辐照区都可以明显观察到点缺陷簇 (如图 1(d)).
 |
| 图 1 500 ℃电子辐照下辐照区形貌 Fig. 1 Micrographs of irradiated area under electron irradiation at 500 ℃ |
电子束辐照条件下,不仅有点缺陷簇形成,还可以观察到位错环.利用透射电镜对辐照30 min后的位错环形貌进行观察,如图 2所示.同样以500 ℃为例,可以看出电子束辐照30 min后,试样内形成形态不一的位错环,尺寸也不尽相同,所观察到的最大尺寸将近300 nm.
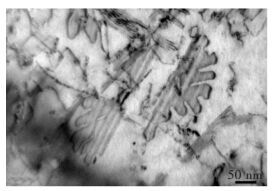 |
| 图 2 500 ℃电子束辐照后位错环形貌 Fig. 2 Loops formed after electron irradiation at 500 ℃ |
2.2 不同温度下空洞的演变
除了点缺陷簇及位错环外,辐照引入的过饱和空位还可聚集形成空洞.空洞的产生可分为形核和长大2个过程[20-21].即辐照引入的过饱和空位先相互聚集形成空洞核心,然后空洞核不断吸收空位而长大.
对500 ℃电子辐照条件下空洞的产生及演变进行原位观察,如图 3所示.辐照前,晶界两侧并无空洞 (图 3(a)).当辐照5 min,辐照剂量达到0.6 dpa时,晶界附近已有少量小尺寸空洞形成 (见图 3(b)),空洞在此辐照剂量下已完成形核;随着辐照时间不断增加,空洞数量和尺寸不断增大;辐照30 min时 (辐照剂量为3.6 dpa),辐照区内清晰可见大量尺寸较大的空洞 (见图 3(d)).
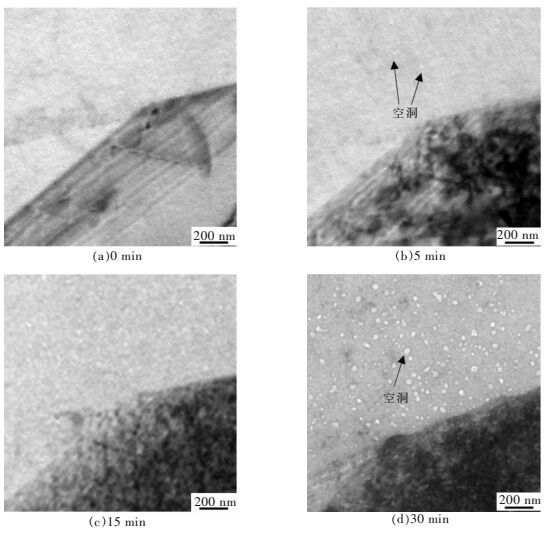 |
| 图 3 500 ℃电子辐照过程中空洞的演变过程 Fig. 3 Void evolution under electron irradiation at 500 ℃ |
450 ℃、400 ℃、350 ℃及300 ℃电子辐照条件下空洞的演变分别如图 4、图 5、图 6和图 7所示.这4种辐照温度下样品内也都有空洞生成,但空洞的产生时间及尺寸却存在较大差异.450 ℃时,电子辐照5 min后,晶界附近有少量小尺寸空洞形成 (如图 4(b)),表明此时的空洞也已完成形核.但随着辐照温度降低,空位扩散能力下降,导致空洞形核所需时间增加.400 ℃时,电子辐照10 min后晶界附近仍未观察到空洞,15 min后晶界附近出现少量小尺寸空洞;而350 ℃和300 ℃下分别辐照15 min和25 min后才观察到空洞.另外,随着温度降低,空洞尺寸也在逐渐下降.300 ℃时,即使辐照30 min,晶界附近也只能观察到一些尺寸非常小的空洞.
 |
| 图 4 450 ℃电子辐照过程中空洞的产生及演变过程 Fig. 4 Void evolution under electron irradiation at 450 ℃ |
 |
| 图 5 400 ℃电子辐照过程中空洞的产生及演变过程 Fig. 5 Void evolution under electron irradiation at 400 ℃ |
 |
| 图 6 350 ℃电子辐照过程中空洞的产生及演变过程 Fig. 6 Void evolution under electron irradiation at 350 ℃ |
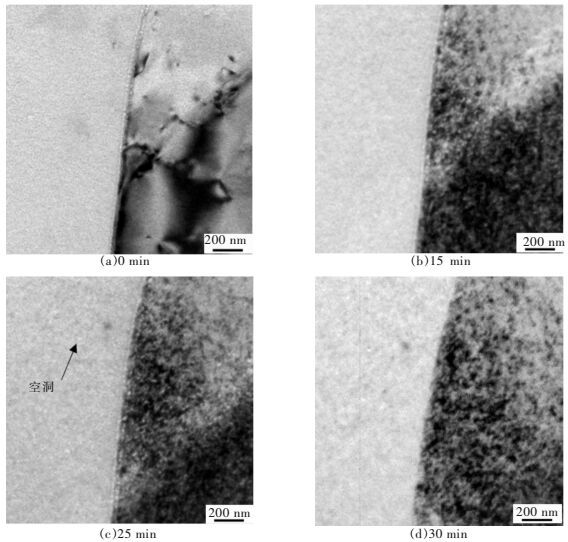 |
| 图 7 300 ℃电子辐照过程中空洞的产生及演变过程 Fig. 7 Void evolution under electron irradiation at 300 ℃ |
利用透射电镜对辐照30 min后的空洞形貌进行观察,如图 8所示.对比图 8(a)~图 8(d)可知,在300~500 ℃范围内,辐照温度越高,空洞尺寸越大,这与原位观察的结果相符.经统计300 ℃、350 ℃、400 ℃、450 ℃和500 ℃时,空洞的平均尺寸分别为3.6 nm、5.5 nm、7.9 nm、13.3 nm和14.5 nm.
 |
| 图 8 不同温度下电子辐照30 min后空洞形貌 Fig. 8 Void micrographs after 30 min electron irradiation at different temperatures |
对比300~500 ℃区间内电子辐照过程中空洞的演变情况 (图 3~图 7) 可知,450 ℃和500 ℃时,空洞形核所需时间最短;同时,这2种温度下空洞尺寸也远大于其他温度 (见图 8).空洞是空位在三维空间通过扩散而聚集形成的体缺陷.空位的扩散能力随温度增加而增加,因而在本研究中,高温下 (如≥450 ℃),空位具有较高扩散能力,易于聚集形成空洞核心并促进空洞长大.低温下 (如≤400 ℃),空位扩散能力相对较低,因而空洞形核所需时间增长,空洞长大也受到了限制.因此,通过降低奥氏体不锈钢中空位扩散能力,可以抑制空洞长大,减小辐照肿胀.
3 结论1) 300~500 ℃区间内,3.6 dpa辐照剂量以内,随着电子辐照时间增长,辐照区内点缺陷簇的数量不断增加,尺寸也不断增大.位错环呈现不同形貌,最大尺寸可达300 nm左右.
2) 300~500 ℃区间内,经30 min电子辐照,试样内都有空洞形成.随着辐照温度升高,空洞尺寸不断增大,450 ℃和500 ℃时尺寸最大,分别为13.3 nm和14.5 nm.该研究结果可为不同工作环境下奥氏体不锈钢中辐照肿胀情况的评估提供实验依据.
| [1] |
LIJINSKY W, EPSTEIN S S. Nitrosamines as environmental carcinogens[J].
Nature, 1970, 225: 21–23. DOI: 10.1038/225021a0. |
| [2] |
MIRVISH S S. Role of N-nitroso compounds (NOC) and N-nitrosation in etiology of gastric, esophageal, nasopharyngeal and bladder cancer and contribution to cancer of known exposures to NOC[J].
Cancer Letters, 1995, 93(1): 17–48. DOI: 10.1016/0304-3835(95)03786-V. |
| [3] |
CHEN H Q, WU Y, ZHANG Y Y, et al. Determination of chromium (Ⅲ) in aqueous solution using CePO4: Tb3+nanocrystals in a fluorescence resonance energy transfer system[J].
Biological and Chemical Luminescence, 2014, 29(6): 642–648. DOI: 10.1002/bio.2599. |
| [4] |
VILIAN A, CHEN S M, KWAK C H. Immobilization of hemoglobin on functionalized multi-walled carbon nanotubes-poly-l-histidine-zinc oxide nanocomposites toward the detection of bromate and H2O2[J].
Sensors and Actuators B (Chemical), 2016, 224: 607–617. DOI: 10.1016/j.snb.2015.10.099. |
| [5] |
ZHANG Y Y, BAI X Y, WANG X M, et al. Highly sensitive graphene Pt nanocomposites amperometric biosensor and its application in living cell H2O2 detection[J].
Analytical Chemistry, 2014, 86: 9459–9465. DOI: 10.1021/ac5009699. |
| [6] |
LIU J Y, WANG X H, WANG T S, et al. Functionalization of monolithic and porous three-dimensional graphene by one-step chitosan electrode position for enzymatic biosensor[J].
ACS Applied. Material Interfaces, 2014(6): 1997–2002. |
| [7] |
AKHAVAN O, GHADERI E, RAHIGHI R. Toward single-DNA electrochemical biosensing by grapheme nanowalls[J].
ACS NANO, 2012, 6(4): 2904–2916. DOI: 10.1021/nn300261t. |
| [8] |
GAI S L, LI C X, YANG P P, et al. Recent progress in rare earth micro/nanocrystals: soft chemical synthesis, luminescent properties, and biomedical applications[J].
Chemical Reviews, 2014, 114(4): 2343–2389. DOI: 10.1021/cr4001594. |
| [9] |
ZHANG S, LI B Q, SHENG Q L, et al. Electrochemical sensor for sensitive determination of nitrite based on the CuS-MWCNT nanocomposites[J].
Journal of Electroanalytical Chemistry, 2016, 769: 118–123. DOI: 10.1016/j.jelechem.2016.03.025. |
| [10] | 郑冬云, 张倩倩, 刘晓军, 等. 基于PVN-GO复合膜的亚硝酸盐电化学传感器[J]. 传感器与微系统, 2014, 33(12): 60–63. |
| [11] | 李扬, 彭本遵, 弓瑾, 等. 基于血红蛋白、血红素的亚硝酸盐传感器的构建[J]. 化学通报, 2014, 77(3): 255–259. |
| [12] | 韩瑞芳, 曹艳萍, 王若珩, 等. Nano-Au/复合壳聚糖@纳米碳修饰金电极检测亚硝酸盐[J]. 化学传感器, 2015, 35(1): 57–61. |
| [13] |
CANBAY E, SAHIN B, KIRAN M, et al. MWCNT-cysteamine-Nafion modified gold electrode based on myoglobin for determination of hydrogen peroxide and nitrite[J].
Bioelectrochemistry, 2015, 101: 126–131. DOI: 10.1016/j.bioelechem.2014.09.001. |
| [14] | 魏龙福, 余长林. 石墨烯/半导体复合光催化剂的研究进展[J]. 有色金属科学与工程, 2013, 4(3): 34–39. |
| [15] | 朱辰杰, 洪瑞金, 温和瑞. 石墨烯掺杂氧化锡薄膜的结构与光学性能的研究[J]. 有色金属科学与工程, 2012, 3(6): 13–16. |
| [16] | 于浩, 王毅, 简选, 等. 电化学方法制备石墨烯修饰电极在亚硝酸根检测中的应用[J]. 江西师范大学学报 (自然科学版), 2013, 37(1): 79–83. |
| [17] | 王小萍, 刘娇, 龚晨晨, 等. 石墨烯碳糊电极的制备及其性能研究[J]. 应用化工, 2014, 43(7): 1196–1199. |
| [18] |
WU X, TIAN F, WANG W X, et al. Fabrication of highly fluorescent graphene quantum dots using L-glutamic acid for in vitro/in vivo imaging and sensing[J].
Journal of Materials Chemistry C, 2013(1): 4676–4684. |
| [19] |
ZHANG M, BAI L L, SHANG W H, et al. Facile synthesis of water-soluble, highly fluorescent graphene quantum dots as a robust biological label for stem cells[J].
Journal of Materials Chemistry, 2012, 22: 7461–7467. DOI: 10.1039/c2jm16835a. |
| [20] |
LIU J Q, HE X X, WANG K M, et al. A highly sensitive electro chemiluminescence assay for protein kinase based on double-quenching of graphene quantum dots by G-quad-ruplex-hemin and gold nanoparticles[J].
Biosensors and Bioelectronics, 2015, 70: 54–60. DOI: 10.1016/j.bios.2015.03.026. |
| [21] |
HUMMERS WS, OFFEMAN RE. Preparation of graphitic oxide[J].
Journal of American Chemical Society, 1958, 80(60): 1339. |
| [22] |
ZHANG P, ZHUO Y, CHANG Y Y, et al. Electro chemiluminescent grapheme quantum dots as a sensing platform: adual amplification for microRNA assay[J].
Analytical Chemistry, 2015, 87(20): 10385–10391. DOI: 10.1021/acs.analchem.5b02495. |
| [23] |
STOBINSKI L, LESIAK B, MALOLEPSZY A, et al. Graphene oxide and reduced graphene oxide studied by the XRD, TEM and electron spectroscopy methods[J].
Journal of Electron Spectroscopy and Related Phenomena, 2014, 195: 145–154. DOI: 10.1016/j.elspec.2014.07.003. |
| [24] |
ZHANG M, BAI L L, SHANG W H, et al. Facile synthesis of water-soluble, highly fluorescent graphene quantum dots as a robust biological label for stem cells[J].
Journal of Materials Chemistry, 2012, 22: 7461–7467. DOI: 10.1039/c2jm16835a. |
| [25] |
BAI J, WU L P, WANG X J, et al. Hemoglobin-graphene modified carbon fiber microelectrode for direct electrochemistry and electrochemical H2O2sensing[J].
Electrochimica Acta, 2015, 185: 142–147. DOI: 10.1016/j.electacta.2015.10.100. |
 2017, Vol. 8
2017, Vol. 8


