| 活性炭负载铁盐去除水中高氯酸盐 |
高氯酸盐是一种有毒的含氧无机污染物,其对人体的典型危害是影响甲状腺功能,干扰人体正常新陈代谢[1],特别是对婴幼儿的神经系统和大脑组织发育产生不可逆危害,易造成智力缺陷[2],因此,开展去除高氯酸盐的研究具有重大意义.高氯酸根离子(ClO4-)为一个四面体结构,一个氯离子被4个氧原子围在中间,高氯酸盐易溶于水,物化性质非常稳定,难以降解,易随水流动而迁移扩散[3-4].水体中的高氯酸盐主要来源于军火厂、火柴厂、烟花厂等企业生产的含有大量ClO4-的废渣、废水的排放[5].USEPA在安全饮用水法案(SDWA)规定高氯酸盐浓度限值为24.5 mg/L[6].
去除高氯酸盐的方法有:生物膜法、吸附法[7]、离子交换法[8]、还原法[9]、微生物法[10]等.吸附法由于方法简单,成本较低,反应完全等优点被广泛运用于去除水体污染物[11];活性炭具有表面积大,吸附能力强的特点;由于它表面既存在疏水性结构又含有由官能团形成的亲水性结构,所以能有效去除污染物.但因为活性炭为非极性物质,对极性无机物离子吸附较弱[12].因此对活性炭进行有针对性的改性为一个重要研究方向.本研究采用浸润法将5种铁盐负载在颗粒活性炭上制备新型复合材料(GAC-Fe)来吸附水中的ClO4-,研究在不同条件下其对ClO4-的去除效果和吸附等温,并研究了反应的吸附动力学及对高氯酸盐的去除机理.
1 实验 1.1 实验材料与仪器设备选用杭州碳素公司生产的活性炭(GAC),水全部来至超纯水机(Millipore-Q)出水;高氯酸钾(KClO4)、氯化铁(FeCl3)、氯化亚铁(FeCl2)、硫酸亚铁(FeSO4)、硫酸铁(Fe2(SO4)3)、硝酸铁(Fe(NO3)3)、氢氧化钠(NaOH)、浓盐酸(HCl)等均为分析纯,均购自国药集团化学试剂有限公司.电子天平(AL204);恒温搅拌器;pH计(FE20K);电热恒温鼓风烘箱(DHG-9146);恒温振荡器(HZQ-X300C);单联立式万用电炉(DK-98);离子色谱(ICS-1000);傅立叶红外光谱仪(Nicolet5700);X射线衍射仪(D8 Advance型).
1.2 实验方法 1.2.1 制备复合材料1) 活性炭预处理:将颗粒活性炭和蒸馏水混合于电炉上煮沸10 min,然后再用蒸馏水冲洗干净,于110 ℃烘箱中烘干至恒重备用,标号为GAC.
2) 分别称取5 g的GAC放入5个小烧杯中,再分别取FeCl2,FeSO4,FeCl3,Fe2(SO4)3,Fe2(NO3)35种铁盐各0.1 mmol加入这5个小烧杯中,分别加入50 mL超纯水均匀搅拌后用锡纸密封后放入110℃的电热恒温鼓风烘箱中浸润24 h,确保浸润完全.
3) 取出浸润后的材料通过超纯水冲洗多次直至水清澈,放入110 oC烘箱中干燥5 h后,取出复合材料存于塑料封袋里,并分别标记为GAC-FeCl2、GAC-FeSO4、GAC-FeCl3、GAC-Fe2(SO4)3、GAC-Fe2(NO3)3备用.
1.2.2 铁含量测定在5个烧杯中盛入100 mL超纯水,分别放入0.1 g备用的复合材料,通过2 mol/L HCl来调制pH值约为1.5,放入恒定25 ℃的摇床(150 r/min)振荡24 h, 之后的溶液取样过0.22 μm微孔滤膜,通过ICP-OES测出铁离子含量.
1.2.3 GAC和GAC-Fe材料对去除ClO4-影响因素的实验去除ClO4-的实验均在250 mL磨口细颈瓶中进行;吸附等温实验将0.1 g的GAC、GAC-FeCl2、GAC-FeSO4、GAC-FeCl3、GAC-Fe2(SO4)3、GAC-Fe(NO3)3分别加入到100 mL的ClO4-溶液的细口瓶中,控制初始浓度为0.1 mmol/L、0.15 mmol/L、0.2 mmol/L、0.25 mmol/L、0.3 mmo/L;选出最好的复合材料进一步做后续分析.pH实验为向100 mL的ClO4-溶液中加入0.1 g材料,控制溶液ClO4-浓度为0.1 mmol/L.动力学实验将0.2 g的GAC、GAC-FeCl3分别加入到浓度为0.1 mmol/L,体积为200 mL的ClO4-溶液的细口瓶中,在不同时间、间隔取样;放入恒定25 ℃的摇床(150 r/min)振荡24 h,反应之后的溶液取样过0.22 μm微孔滤膜,采用ICP-1000测出ClO4-的浓度.
1.2.4 材料表征分析对材料GAC和GAC-FeCl3进行XRD和FTIR表征,并对吸附的材料GAC-FeCl3进行FTIR表征获得相关衍射图,从而分析材料的表面结构、成分和形态.
1.2.5 相关计算公式铁含量计算公式:
| $ {\rm{Fe\% = }}\frac{{{M_{{\rm{Fe}}}}}}{M} \times 100\% $ | (1) |
吸附平衡容量的公式:
| $ {q_{\rm{e}}} = \frac{{({C_{\rm{0}}} - {C_e})V}}{M} $ | (2) |
吸附率计算公式:
| $ R = \frac{{{C_0}{\rm{-}}{C_e}}}{{{C_0}}} \times 100\% $ | (3) |
其中,M为投入吸附剂的质量,g;MFe为铁质量,g;Fe%为铁含量;Co为初始浓度,mg/L;Ce为平衡时浓度,mg/L;V为废水溶液体积,L;qe为平衡吸附容量,mg/g;R为吸附率.
2 结果与讨论 2.1 铁盐种类对复合材料的铁含量影响通过计算公式和铁离子含量的测定算出复合材料GAC-FeCl2的铁含量为8.46 %,GAC-FeSO4为9.87 %,GAC-FeCl3为9.22 %,GAC-Fe2(SO4)3为9.93 %,GAC-Fe2(NO3)3为12.84 %;可以看出5种复合材料的含铁量相差不大,其中复合材料GAC-Fe2(NO3)3的含铁量最高,为12.84 %;材料GAC-FeCl2的含铁量最低,为8.46 %;活性炭负载三价铁盐的复合材料普遍比负载亚铁盐的铁含量更多,原因是三价铁离子易与水结合生成羟基铁,更易负载在颗粒活性碳上[13],从而铁含量增多.
2.2 吸附等温线图 1为材料GAC和复合材料GAC-Fe对ClO4-的吸附等温线实验.
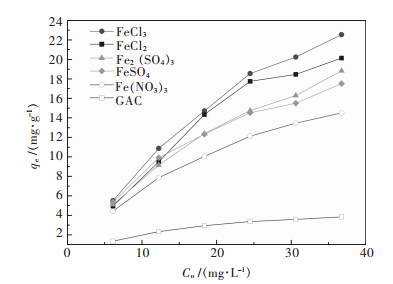 |
| 图 1 GAC与GAC-Fe对ClO4-的吸附等温线 Fig. 1 Adsorption isotherm of GAC and GAC-Fe on ClO4- |
由图 1可以看出,经改性后的活性炭对ClO4-的吸附能力远优于GAC, 且可以看出GAC-FeCl2、GAC-FeCl3对于去除ClO4-的去除效果更好,原因可能是其他3种阴离子的干扰;卢宁等[14]研究表明活性炭吸附高氯酸盐过程中,阴离子SO42-和NO3-的存在对吸附ClO4-均有较大的影响;而Cl-能改善GAC表面的化学性质,使水合氧化铁更易负载在GAC上,形成更多官能团,增强吸附能力.SO42-、NO3-与ClO4-存在竞争吸附,占据了复合材料表面的大量吸附点位,从而导致其对高氯酸盐的去除效率明显降低.GAC-FeCl2和GAC-FeCl3结果相比,可能由于GAC-FeCl2的铁含量较少,影响其去除高氯酸根的效果.实验采用Freundlich模型和Langmuir模型对结果进行拟合[15];Freundlich模型能够描述吸附剂表面非均匀的吸附行为,Langmuir模型能够描述吸附剂表面均一的单分子层的吸附行为[16].它们方程式分别用式(4),式(5)来表示:
| $ {{\rm{q}}_e} = {k_F}{C_e}\frac{1}{n} $ | (4) |
| $ {{\rm{q}}_e} = \frac{{{q_{{\rm{max}}}}{k_L}{C_e}}}{{1 + {k_L}{C_e}}} $ | (5) |
qe为平衡吸附容量,mg/g;Ce为平衡时浓度,mg/L;qmax为最大吸附容量,mg/g;kF为吸附系数;kL为平衡吸附有关常数;n为常数.吸附等温实验拟合结果如表 1.
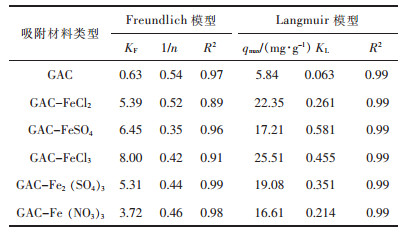
| 表1 GAC和GAC-Fe吸附ClO4-等温线拟合参数表 Table 1 Langmuir and Freundlich constants of GAC and GAC-Fe adsorb ClO4- |
 |
| 点击放大 |
由表 1可以看出,通过Langmuir模型能够更好地拟合复合材料对去除ClO4-的吸附等温效果,相关系数R2基本优于Freundlich模型拟合.1/n在0.1~0.5之间,说明GAC-Fe吸附剂容易吸附ClO4-;比较复合材料最大吸附容量qmax能够得出,复合材料GAC-FeCl3对ClO4-吸附能力最强,为25.51 mg/g;GAC-Fe(NO3)3的吸附力最弱;比较最大吸附能力可知,复合材料GAC-Fe2(SO4)3、GAC-FeSO4的吸附能力没有随铁含量的增多而增强,并且相对于GAC-FeCl3有所降低,原因可能是过多的铁拥堵在GAC表面,影响材料吸附ClO4-的效果[17];因此可知,GAC-FeCl3为去除ClO4-的最佳复合材料.Xu等[18]研究表明吸附剂去除水中ClO4-主要通过静电吸附和离子交换,更加符合单分子层吸附;综合比较,Langmuir模型能更好地描述复合材料GAC-Fe对水中ClO4-的吸附等温过程,复合材料GAC-FeCl3对ClO4-去除效果最好,采用复合材料GAC-FeCl3进行后续实验研究.
2.3 初始pH值的影响pH值的变化是影响活性炭吸附ClO4-的一个重要因素,主要表现在影响吸附质表面的分布形态、官能团及电性性质.通过对吸附质调节不同的pH值研究去除水中ClO4-的效果,结果见图 2.
图 2所示为不同pH条件下GAC-FeCl3对ClO4-的去除效果,由图 2中能够看出,复合材料GAC-FeCl3去除水中ClO4-时,在中性pH=5~7的条件下去除效果最好;在酸性条件下略差;在碱性环境下急剧下降.在酸性条件下(pH < 4)去除效果较好,原因可能是由于H+的作用,附着在活性炭的水合氧化铁以FeOH+的形式存在[19],通过静电吸附作用吸附高氯酸根离子.当溶液为碱性时(pH > 8)去除率明显下降,原因是OH-与ClO4-的竞争吸附,与活性炭亲和力更强的OH-占据了更多的吸附位[20],并且Fe3+与OH-形成沉淀随pH值增大而增多,从而附着在活性炭表面,影响电子传导,阻碍吸附剂吸附,导致降低去除效率[21],溶液的初始pH值对去除效果具有较大影响.
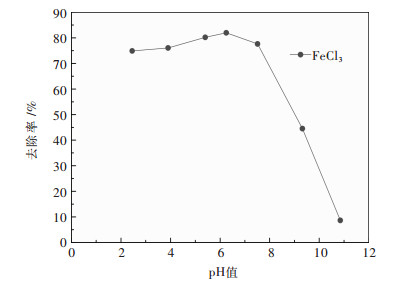 |
| 图 2 初始pH值对GAC-FeCl3去除ClO4-的影响 Fig. 2 Effect of initial pH on ClO4- reduction by GAC-FeCl3 |
2.4 吸附动力学
吸附动力学主要研究吸附质在吸附过程中随时间变化达到一个吸附平衡的过程,用于测定吸附过程中物质转移及物理化学反应的速率控制步骤,并利用动力学模型对结果拟合[22];材料GAC与GAC-FeCl3对ClO4-的吸附容量随时间的变化关系如图 3所示.
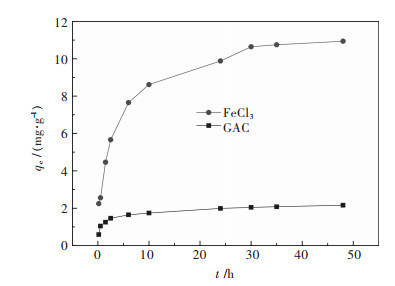 |
| 图 3 高氯酸盐的吸附容量随时间的变化 Fig. 3 Adsorption quantity of perchlorate with the time |
高氯酸根溶液的初始pH值为4.51,初始浓度为0.1 mmol/L.由图 3能够看出GAC经过10 h左右差不多就达到平衡,反应经过48 h吸附率仅仅2 mg/g左右.经改性后的复合材料吸附效果大大增加,GAC-FeCl3在10 h内,随时间的递增快速增加,原因是吸附开始时吸附剂与ClO4-能够充分接触;在10 h至35 h时间段,增加速率比较慢,原因为活性炭上的位点已经被逐渐占据,越来越少;GAC-FeCl3在35 h后吸附就基本平衡,是由于参与吸附的活性炭位点基本达到饱和状态.材料GAC、GAC-FeCl3吸附饱和量分为2.17 mg/g;10.94 mg/g.
准一级吸附动力学:
| $ {\rm{lg}}({q_e}-{q_t}) = \lg {q_e}-\frac{{{k_1}}}{{2.303}}t $ | (6) |
准二级吸附动力学:
| $ \frac{{\rm{t}}}{{{q_t}}} = \frac{1}{{{k_2}{q_e}^2}} + \frac{t}{{{q_e}}} $ | (7) |
其中t为吸附时间,h;qe为平衡吸附容量,mg/g;qt为吸附剂在t时刻吸附容量,mg/g;k1为准一级动力学吸附速率常数;k2为准二级动力学吸附速率常数.
实验结果用准一级动力学和准二级动力学模拟;相关参数见表 2.
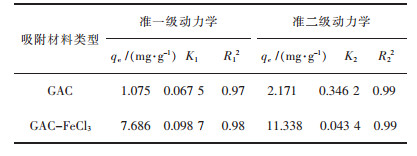
| 表2 GAC和GAC-FeCl3去除ClO4-的拟合反应速率方程式参数 Table 2 Two kinds of Lagergren models constants for ClO4- adsorption by GAC and GAC-FeCl3 |
 |
| 点击放大 |
由表 2吸附动力学拟合结果可知,材料GAC和GAC-FeCl3准二级动力学相关系数(R2 > 0.99)大于准一级动力学,并且复合材料GAC-FeCl3吸附容量qe(11.338 mg/g)与实际qe(10.94 mg/g)更加接近,误差更小,因此准二级动力学模型能可以更好的描述吸附材料对ClO4-的吸附,说明吸附过程中发生了物理-化学吸附作用.
2.5 材料的表征并讨论吸附机理1) 材料XRD表征.图 4所示为GAC、GAC-FeCl3的XRD衍射图谱,分析可知材料a、b在2θ=23°~26°之间均有不定型炭的衍射峰,并且衍射峰的强度逐渐减弱,原因是活性炭被酸碱预处理及制备过程中的搅拌作用下使活性炭内部孔径部分坍塌,导致活性炭的结晶度降低[23].图 4中材料a在2θ=20.88°、36.72°、43.54°、50.68°、64.5°处是SiO2的特征峰;与材料a相比,材料b在2θ=32.02°、35.4°、36.28°、43.33°处增添了水合氧化铁的特征峰,表明活性炭负载铁成功;但由于峰强比较弱,只能够在次相检索中检出,说明活性炭负载的铁主要是非晶体型.材料结构通过XDR无法确定,所以样品还需要通过FTIR进一步分析.
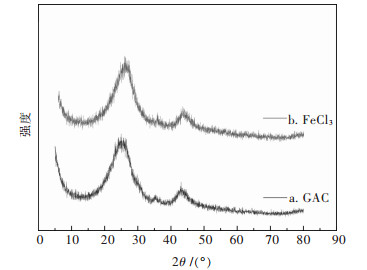 |
| 图 4 GAC和GAC-FeCl3的XRD谱 Fig. 4 XRD pattern of GAC and GAC-FeCl3 |
2) 材料FTIR表征分析.图 5所示为GAC、GAC-FeCl3吸附前及吸附ClO4-后的FTIR衍射图谱,图 5可知,材料GAC在波数1112.74 cm-1处为C-O伸缩振动峰,1542.79 cm-1处为H-C-H变形振动峰,1562.08~1591.01 cm-1处为水的H-O-H弯曲振动峰,在3135.73~3153.16 cm-1处出现宽且强的特征谱带,为水分子O-H伸缩振动峰.与GAC相比,复合材料GAC-FeCl3在3135.73~3153.16 cm-1处的峰透过率增强了,原因是负载的铁化合物的O-H伸缩振动引起的;2915.88 cm-1、2850.31 cm-1处为C-H弯曲振动峰,波数为1118.52 cm-1处多出了一个明显的特征峰,通过特征谱带分析可知,此处为Fe-OH特征峰,波数为1031.74 cm-1处有一个Si-O-Si伸缩振动峰,850~1064 cm-1处为Si-O键引发的宽且强的伸缩振动带,在619.04 cm-1、798.39 cm-1处有一个明显特征峰,对比标准红外光谱图集,此处是FeOOH相应的Fe-O伸缩振动峰.对比分析复合材料GAC-FeCl3吸附ClO4-前后的FTIR图谱可知,吸附后复合材料GAC-FeCl3在波数3149.23 cm-1、1587.15 cm-1、1400.08 cm-1处的O-H的伸缩振动峰峰高均有一定程度降低,619.04 cm-1、798.39 cm-1处FeOOH相应的Fe-O伸缩振动峰有所减弱,873.6 cm-1、701.97 cm-1处为Cl-O伸缩振动峰,表明ClO4-与复合材料GAC-FeCl3上的FeOOH结合发生吸附反应.由上可知,改性后的材料含有FeOOH官能团,同时含有丰富的羟基官能团.复合材料的吸附机理是水和氧化铁中的羟基铁带正电荷与高氯酸根发生静电吸附和吸附剂与高氯酸根之间的化学作用.
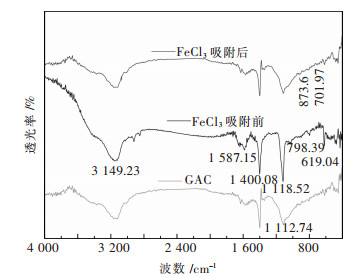 |
| 图 5 GAC、GAC-FeCl3的FTIR谱 Fig. 5 FTIR pattern of GAC and GAC-FeCl3 |
3 结论
1) 采用浸润法以颗粒活性炭为负载制备的新型复合材料(GAC-Fe),实验结果表明改性后活性炭对ClO4-的去除效果大大加强,表征结果表明活性炭成功负载了铁化合物,主要是由于活性炭上负载的FeOOH和ClO4-结合发生吸附反应,其中活性炭负载FeCl3对ClO4-的去除效果最佳,去除率高达97 %,相比于GAC高出75 %.
2) 初始pH值不同对去除水中ClO4-影响研究结果表明,ClO4-的去除效果在偏弱酸性和中性条件下较好,当pH > 8时,随着pH的升高,去除效果迅速下降.
3) 吸附等温实验拟合结果表明Langmuir模型(R2 > 0.99)能够更好地描述材料GAC和GAC-FeCl3对去除水中ClO4-的吸附等温过程;吸附动力学实验表明准二级动力学方程(R2 > 0.99)能更好的描述材料GAC和GAC-FeCl3对去除水中ClO4-的反应过程.
| [1] | 谢杰, 杨志泉, 陈兵, 等.硫自养菌降解还原高氯酸盐的优化控制研究[J]. 水处理技术,2012,38 (6):33–35. |
| [2] | 于佳, 唐玄乐, 刘家仁, 等.高氯酸盐对人体健康影响的研究进展[J]. 环境与健康杂志,2008,25 (7):648–650. |
| [3] | 谢永洪, 杨坪, 熊杰, 等.高氯酸盐分析方法研究进展[J]. 四川环境,2014,33 (3):140–147. |
| [4] |
KANNAN K, PRAAMSMA M L, OLDI J F, et al. Occurrence of perchlorate in drinking water, groundwater, surface water and human saliva from India[J].
ChemospHere, 2009,76 (1):22–26. DOI: 10.1016/j.chemosphere.2009.02.054. |
| [5] |
LV L, XIE Y H, LIU G M, et al. Removal of perchlorate from aqueous solution by cross-linked Fe(III)-chitosan complex[J].
Journal of Environmental Sciences, 2014,26 (4):792–800. DOI: 10.1016/S1001-0742(13)60519-7. |
| [6] |
DASGUPTA P K, DYKE J V, KIRK A B, et al. Perchlorate in the United States. Analysis of relative source contributions to the food chain[J].
Environmental Science & Technology, 2006,40 (21):6608–6614. |
| [7] | 彭银仙, 吴春笃, 宁德刚, 等.高氯酸盐去除方法研究进展[J]. 环境科学与工程,2009,32 (2):87–90. |
| [8] | 王东霜, 张向东, 陈云嫩, 等.无机盐改性麦糟在低浓度含砷水中的吸附性能研究[J]. 有色金属科学与工程,2013,4 (6):69–72. |
| [9] |
VELLANKI B P, BATCHELOR B. Perchlorate reduction by the sulfite ultraviolet light advanced reduction process[J].
Journal of hazardous materials, 2013,262 (15):348–356. |
| [10] | 冯杲, 王倩, 张媛媛, 等.微生物法去除高氯酸盐的研究进展[J]. 河北工业科技,2014,31 (6):519–524. |
| [11] | 吴春笃, 窦金亮, 许小红, 等.椰壳基活性炭吸附高氯酸盐污染物的研究[J]. 工业安全与环保,2012,38 (5):15–17. |
| [12] | 顾雪琼, 陈维芳.改性活性炭对饮用水中铬酸盐的去除特性研究[J]. 水资源与水工程学报,2011,22 (2):20–24. |
| [13] | 唐敏康, 陈苹, 许建红, 等.Fe(Ⅱ)-H2O2不同温度浸润改性活性炭吸附去除水中砷(V)[J]. 有色金属科学与工程,2014,5 (4):66–70. |
| [14] | 卢宁, 高乃云, 黄鑫, 等.水中高氯酸根的颗粒活性炭吸附过程及影响因素分析[J]. 环境科学,2008,29 (6):1572–1577. |
| [15] | 肖卫红, 张青梅, 尤翔宇, 等.镁铝水滑石的合成及其对VO3-的吸附特性[J]. 有色金属科学与工程,2015,6 (4):37–40. |
| [16] | 姚淑华, 刘丹, 石中亮, 等.粉煤灰/水合氧化铁复合吸附剂去除水中磷(V)[J]. 辽宁工程技术大学学报(自然科学版),2010,29 (1):151–154. |
| [17] | 唐敏康, 肖爱红, 许建红, 等.活性炭负载亚铁离子去除水中溴酸盐研究[J]. 水处理技术,2015 (5):58–62. |
| [18] |
XU J H, GAO N Y, DENG Y, et al. Perchlorate removal by granular activated carbon coated with cetyltrimethy lammo-nium chloride[J].
Desalination, 2011,275 (1/2/3):87–92. DOI: 10.1016/j.desal.2011.02.036. |
| [19] | 许建红, 高乃云, 唐玉霖, 等.浅析水合氧化铁的研究进展[J]. 水处理技术,2011,9 (28):26–30. |
| [20] | 吴云海, 李斌, 冯仕训, 等.活性炭对废水中Cr(Ⅵ)、As(Ⅲ)的吸附[J]. 化工环保,2010,30 (2):108–112. |
| [21] |
LV L, XIE Y H, LIU G M, et al. Removal of perchlorate from aqueous solution by cross-linked Fe(III)-chitosan complex[J].
Journal of Environmental Sciences, 2014,26 (4):792–800. DOI: 10.1016/S1001-0742(13)60519-7. |
| [22] | 卢辛成, 蒋剑春, 孙康, 等.活性炭对汞离子的吸附动力学研究[J]. 生物质化学工程,2014,48 (2):1–7. |
| [23] |
LING X F, LI J S, ZHU W, et al. Synthesis of nanoscale zero—valent iron/ordered mesoporous carbon for adsorption and synergistic reduction of nitrobenzene[J].
ChemospHere, 2012,87 (6):655–660. DOI: 10.1016/j.chemosphere.2012.02.002. |
 2016, Vol. 7
2016, Vol. 7


