| (NH4)3PO4-NH3·H2O-H2O体系中磷酸铵溶解度研究 |
2. 崇义章源钨业有限公司, 江西 赣州 341300
2. Chongyi Zhangyuan Tungsten Co., Ltd, Chongyi 341300, China
随着我国黑钨矿资源的逐渐枯竭,白钨矿成为钨冶炼的主要原料[1-4].现行白钨矿的冶炼工艺为:白钨矿苛性钠分解-离子交换-蒸发结晶仲钨酸铵(APT)[5-7].离子交换过程中,溶液由钠盐体系转变为铵盐体系,交后液为大量含钠离子的碱性废水,直接排放会造成严重的环境污染[8].此外,负载钨的树脂采用高浓度的NH4Cl作为解吸剂,APT结晶母液中含有大量的氯离子难以处理[9-12].我国白钨冶炼大都采用碱分解-离子交换工艺,除部分企业废水能够达标排放外,大部分企业依然存在废水超标排放、污染严重的问题:全国年排放废水2400万m3、烧碱4.16万t、氨氮3.16万t、废水排放pH值高达13(超国标1万倍),氨氮400 mg/L(超国标27倍).根据国家环境保护部2008年3月发布的新规,钨冶炼为一类元素排放废水,强制执行零排放要求.针对现行白钨矿冶炼工艺不能实现闭路循环和零排放,难以达到国家环保要求的现状,江西理工大学开发了白钨矿铵盐不变体系冶炼技术,即采用磷酸铵和液氨作为白钨矿的浸出剂,一步得到粗钨酸铵溶液[13-14].由于该工艺取消了离子交换过程,因此浸出剂磷酸铵中的钾、钠等杂质离子会直接进入钨酸铵溶液中.钾和钠的化学性质非常活泼,在后续蒸发结晶过程中,它们很容易在APT中析出,造成APT产品中钾、钠含量超标[15].根据国家0级品APT标准(GB/T 10116-2007),APT中钾、钠的含量必须低于10-5 g/g.APT,因此,在浸出之前有必要对浸出剂磷酸铵进行精制提纯.
探索实验发现,磷酸铵的溶解度受氨水浓度和温度的影响很大.因此,在(NH4)3PO4-NH3·H2O-H2O系中,控制一定的工艺条件,便有可能使得磷酸铵结晶析出,而钾、钠等杂质离子留在结晶母液中,从而实现浸出剂磷酸铵的提纯.目前,有人只测定了磷酸铵在水中的溶解度数据[16],但是对磷酸铵在NH3·H2O-H2O系中的溶解度研究还未见报导.因此,我们测定了磷酸铵在氨水溶液中的溶解度数据,并绘制了不同温度下(NH4)3PO4-NH3·H2O-H2O三元体系相图,以期为磷酸铵的提纯提供一定的理论指导.
1 实验 1.1 化学试剂测定磷酸铵溶解度实验中,所用试剂磷酸铵、氨水及分析试剂均为分析纯,所用水为去离子水.氨溶析结晶法从磷酸铵溶液除去钾、钠实验中,所用的磷酸铵为工业级.
1.2 分析测试方法采用电感耦合等离子体原子发射光谱法(ICP)测定样品中钾、钠的含量.采用磷钼黄分光光度法测定溶液中的磷浓度[17].溶液试样加入一定量的EDTA溶液,再用硫酸-硫酸铍混合液沉淀磷,然后用过量氨水中和并洗涤沉淀,并用热硝酸溶解沉淀,以钒酸铵-钼酸铵为显色剂,于分光光度计波长为420nm处测其吸光度.该方法测试磷的误差能够控制在2%以内.磷的分析标准曲线如下图 2所示.
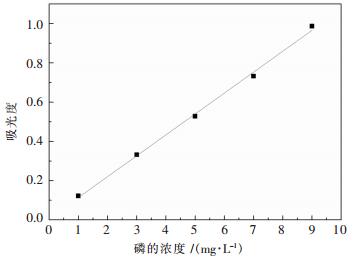 |
| 图 1 分光光度法测试磷的标准曲线 Fig. 1 The standard curve of phosphorus determination by spectrophotometry method |
采用酸碱滴定法测定溶液中的氨浓度[17].量取一定体积的试液于250ml三角瓶中,加入中性水至30ml体积,滴加1~2滴酚酞指示剂,用盐酸标准溶液(1.0N)滴定至红色为终点.根据盐酸标准溶液的加入体积计算出溶液中氨的浓度.该方法测定氨浓度误差可控制在2%以内.采用差减法测定溶液水的含量,并用波美比重计测定溶液的密度.
1.3 实验方法测定(NH4)3PO4-NH3·H2O-H2O三元体系中磷酸铵溶解度时,将预先配置成不同浓度的氨水倒入带搅拌装备的密闭容器中,然后再分别加入足量的磷酸铵,水浴加热并精确控制实验温度,隔一定时间取样,分析溶液中的磷和氨的浓度,当溶液中磷和氨的浓度在2 h内保持不变时,即认为溶解达到平衡.静置20 min使固液相分层,然后迅速取少许上清液进行分析测定(取样过程中温度保持恒定).从工业磷酸铵中氨溶析结晶法除去钾、钠时,5份等体积且成分相同的溶液加入三井烧瓶并置于恒温震荡水浴锅中,初始温度设定为60 ℃,再往5个三井烧瓶中分别鼓入氨气1、2、4、6、8分钟,然后密封三井烧瓶,并调节温度至20 ℃下震荡4 h,然后快速分离结晶固体和溶液,分析溶液中磷以及钾、钠的含量,并计算出磷酸铵结晶率和钾、钠的去除率.
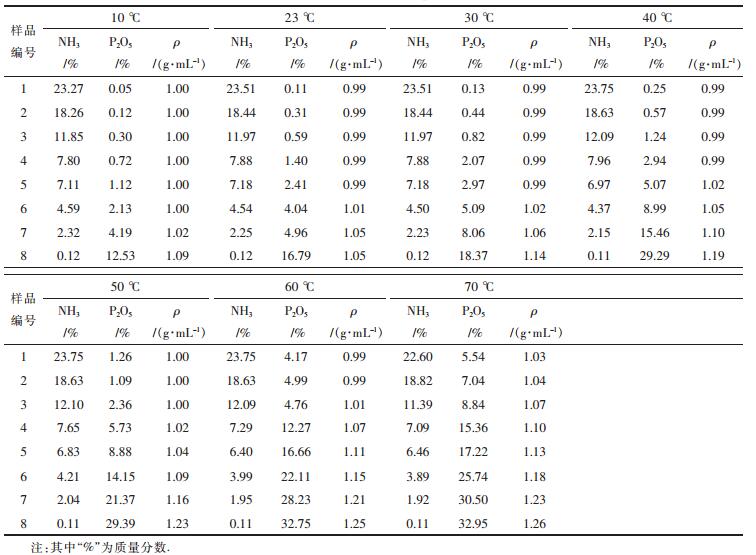
2 结果与讨论 2.1 (NH4)3PO4-NH3·H2O-H2O体系中磷酸铵溶解度的测定在不同温度条件下,实验测定了磷酸铵在氨水中的溶解度数据,结果如表 1所示.
| 表1 不同温度下(NH4)3PO4-NH3·H2O-H2O体系平衡时磷酸铵溶解度 Table 1 Ammonium phosphate solubility of equilibria in ternary system (NH4)3PO4-NH3·H2O-H2O system at different temperature |
 |
| 点击放大 |
从图 2可以看出,磷酸铵的溶解度受温度和氨水浓度的影响很大.随着体系温度的降低以及氨水浓度的升高,磷酸铵溶解度显著降低.对比图 2和图 3可知,当溶液温度相同时,磷酸铵在氨水溶液的溶解度比在纯水中的溶解度大大降低.为了更好的分析磷酸铵的溶解度规律,将本实验的数据经过换算处理后得到(NH4)3PO4-NH3·H2O-H2O系的溶解平衡曲线图,如图 4.
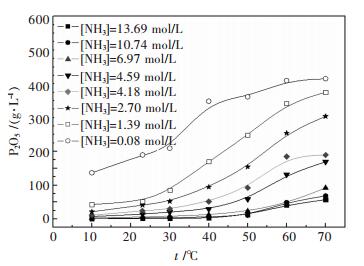 |
| 图 2 温度和氨水浓度对磷酸铵溶解度的影响 Fig. 2 Effect of temperature and ammonia concentration on solubility of ammonium phosphate in ammonia solution |
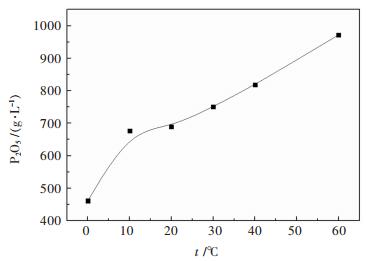 |
| 图 3 (NH4)2HPO4在水中的溶解度曲线 Fig. 3 The curve of (NH4)2HPO4 solubility in water |
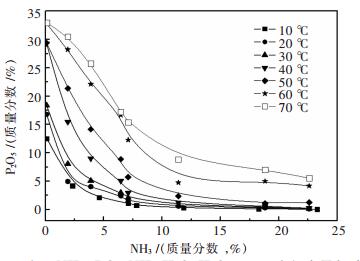 |
| 图 4 (NH4)3PO4-NH3·H2O-H2O三元系中氨含量与磷含量的关系 Fig. 4 Relationship between ammonia content and phosphorus content of the ternary (NH4)3PO4-NH3•H2O-H2O system |
实验分别测定了温度为10 ℃、23 ℃、30 ℃、40 ℃、50 ℃、60 ℃、70 ℃时,(NH4)3PO4-NH3·H2O-H2O体系中磷酸铵的溶解度数据.从图 4可知,在测定温度范围内,磷酸铵的溶解度随氨水浓度变化的规律大致相似.当氨水含量小于8%时,磷酸铵溶解度随着氨水浓度的增大而急剧下降,而当氨水含量大于8%后,磷酸铵溶解度下降的趋势逐渐变缓.当氨水浓度相同时,溶液温度越低则磷酸铵的溶解度也越低.如当氨水浓度为6.97 mol/L、温度为70 ℃时,溶液中[P2O5]=91.97 g/L、温度为10℃时,溶液中[P2O5]=2.98 g/L.溶液温度下降,磷酸铵的溶解度也随之下降,这符合化合物溶解度的一般规律.溶液中氨水浓度越高,由式(1)可知,则氨水电离出来的NH4+浓度相应增大.根据同离子效应可知,如式(2)和式(4)所示,溶液中NH4+浓度增大则会抑制磷酸铵的溶解,容易达到过饱和从溶液中结晶析出.此外,温度越低,氨气在溶液中的溶解度越大,从而氨的溶析效应也就越大,这也会使得磷酸铵的溶解度降低.
| $ \text{N}{{\text{H}}_{3}}\cdot {{\text{H}}_{2}}\text{O}\rightleftarrows \text{NH}_{4}^{+}+\text{O}{{\text{H}}^{-}} $ | (1) |
| $ {{\left( \text{N}{{\text{H}}_{4}} \right)}_{2}}\text{HP}{{\text{O}}_{4}}+\text{NH}_{4}^{+}+\text{O}{{\text{H}}^{-}}\rightleftarrows {{\left( \text{N}{{\text{H}}_{4}} \right)}_{3}}\text{P}{{\text{O}}_{4}}+{{\text{H}}_{2}}\text{O} $ | (2) |
| $ 2\text{NH}_{4}^{+}+\text{NH}_{4}^{3-}+{{\text{H}}_{2}}\text{O}\rightleftarrows {{\left( \text{N}{{\text{H}}_{4}} \right)}_{2}}\text{HP}{{\text{O}}_{4}}+\text{O}{{\text{H}}^{-}} $ | (3) |
| $ 3\text{NH}_{4}^{+}+\text{PO}{{\text{4}}^{3-}}\rightleftarrows {{\left( \text{N}{{\text{H}}_{4}} \right)}_{3}}\text{P}{{\text{O}}_{4}} $ | (4) |
以上分析可知,实践中可以通过控制溶液温度和氨浓度来实现工业磷酸铵的提纯.例如,当温度为60 ℃、氨浓度为0.08 mol/L时,磷酸铵溶液中[P2O5]=409.41 g/L,降低溶液温度至10 ℃以及提高溶液中氨浓度至2.7 mol/L时,磷酸铵溶液中[P2O5]=21.34 g/L,磷酸铵结晶率高达94.78%.该工艺条件,在实际操作中很容易实现.此外,工业上常采用浓缩结晶的方法对无机盐进行提纯.从图 3可知,在(NH4)2HPO4-H2O系中,溶液温度60℃时,(NH4)2HPO4的溶解度为97.20 g,降低温度至10℃时,(NH4)2HPO4的溶解度为42.90 g,结晶率仅为55.86%.若要获得97.48%的结晶率,则需要进一步将溶液体积蒸发浓缩至原来体积的57.56%.对比上述两种方法可知,在(NH4)3PO4-NH3·H2O-H2O系中,通过调整溶液温度和氨浓度使得磷酸铵结晶析出比浓缩结晶法更为简便,具有节能、降低成本的优点.
2.2 磷酸铵结晶率对钾、钠去除效果的影响实验过程中,往含有钾、钠的磷酸铵溶液中冲入氨气,使得磷酸铵结晶析出,而钾、钠等杂质留在结晶母液中,从而达到净化提纯磷酸铵的目的.溶液中初始P2O5浓度为392.24 g/L, 钾和钠的浓度分别为4.90 mg/L、26.75 mg/L.实验结果如图 5所示.
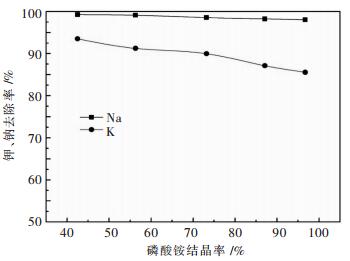 |
| 图 5 磷酸铵结晶率与钾钠去除率的关系 Fig. 5 Effect of ammonium phosphate crystallization ratio on the removal ratio of potassium and sodium ion |
从图 5可知,随着磷酸铵结晶率的增大,钾、钠的去除率缓慢下降.但同时我们发现,即使当磷酸铵结晶率高达96.65%时,钾、钠的除去率仍然分别为85.56%和98.03%.由此可见,氨溶析结晶法除去磷酸铵溶液中的钾、钠效果非常好,可以同时保证得到较高的磷酸铵结晶率和钾、钠除去率,而且操作过程简单可行.实践中,可采用该方法对工业磷酸铵进行提纯,然后再用提纯后的磷酸铵用作白钨矿的浸出剂.
3 结论1)分别测定了温度为10-70 ℃时,(NH4)3PO4-NH3·H2O-H2O体系磷酸铵溶解平衡曲线图.结果表明:磷酸铵溶解度与温度及氨水浓度关系密切.当氨水含量小于8%时,磷酸铵的溶解度随氨水含量的增加而急剧下降,当氨水含量为8%~24%时,磷酸铵的溶解度随氨水含量的增加而下降的趋势变缓.
2)浸出剂磷酸铵中含有一定的钾、钠杂质时,可以通过降温冷却和提高溶液中氨浓度相结合的方法除去钾、钠,净化提纯磷酸铵.该法与浓缩结晶法相比,具有节能和降低生产成本的优势.
| [1] |
ILHAN S, KALPAKLI A O, KAHRUMAN C, et al. The investigation of dissolution behavior of gangue materials during the dissolution of scheelite concentrate in oxalic acid solution[J].
Hydrometallurgy, 2013,136 :15–26. DOI: 10.1016/j.hydromet.2013.02.013. |
| [2] |
KALPAKLI A O, ILHAN S, KAHRUMAN C, et al. Dissolution behavior of calcium tungstate in oxalic acid solutions[J].
Hydrometallurgy, 2012,121 . |
| [3] |
ZHANG W J, LI J T, ZHAO Z W. Leaching kinetics of scheelite with nitric acid and phosphoric acid[J].
International Journal of Refractory Metals and Hard Materials, 2015,52 :78–84. DOI: 10.1016/j.ijrmhm.2015.05.017. |
| [4] | 万林生, 赵立夫, 李红超.崇义章源钨业APT绿色冶炼的技术进步和发展[J]. 中国钨业,2012,27 (1):47–49. |
| [5] | 李义兵, 刘开忠, 张大增.钨冶炼工业工艺及装备述评[J]. 稀有金属与硬质合金,2015,43 (3):1–4. |
| [6] |
ZHAO Z W, LI J T, WANG S B, et al. Extracting tungsten from scheelite concentrate with caustic soda by autoclaving process[J].
Hydrometallurgy, 2011,108 :152–156. DOI: 10.1016/j.hydromet.2011.03.004. |
| [7] | 邓声华, 黄泽辉, 赵立夫, 等.高杂质含量钨酸钠溶液净化试验[J]. 中国钨业,2015,30 (5):64–67. |
| [8] |
ZHAO Z W, HU F, HU Y J, et al. Adsorption behaviour of WO42-onto 201×7 resin in highly concentrated tungstate solutions[J].
International Journal of Refractory Metals and Hard Materials, 2010,28 (5):633–637. DOI: 10.1016/j.ijrmhm.2010.04.005. |
| [9] |
WANG Y L, YANG S H, LI H. Studies on the leaching of tungsten from composite barite-scheelite concentrate[J].
International Journal of Refractory Metals and Hard Materials, 2016,54 :284–288. DOI: 10.1016/j.ijrmhm.2015.07.020. |
| [10] |
GAO Z Y, SUN W, HU Y H. New insights into the dodecylamine adsorption on scheelite and calcite:An adsorption model[J].
Minerals Engineering, 2015,79 :54–61. DOI: 10.1016/j.mineng.2015.05.011. |
| [11] | 张英, 胡岳华, 王毓华, 等.硅酸钠对含钙矿物浮选行为的影响及作用机理[J]. 中国有色金属学报,2014,24 (9):2366–2372. |
| [12] | 曹才放, 赵中伟, 刘旭恒, 等.硅酸钠分解白钨矿的热力学研究[J]. 中国有色金属学报,2012,22 (9):2636–2641. |
| [13] | 万林生, 赵立夫, 黄泽辉, 等.一种铵盐分解白钨矿的方法:中国专利, 102154547 B[p].2011-03-14. http://industry.wanfangdata.com.cn/yj/Detail/Patent?id=Patent_CN201310218994.X |
| [14] | 中国有色治金编辑部."白钨矿铵盐不变体系闭路冶炼工艺"通过省级鉴定达国际领先水平[J]. 中国有色冶金,2011,40 (4):86. |
| [15] | 李洪桂, 羊建高, 李昆. 钨冶金学[M]. 长沙: 中南大学出版社 , 2010 : 235 -238. |
| [16] | SPEIGHT J G. Lange's handbook of chemistry[M]. Sixteenth Edition: New York:McGraw-Hill Press , 2005 : 326 . |
| [17] | 北京矿冶研究总院分析室编. 矿石及有色金属分析手册[M]. 冶金工业出版社 , 1990 . |
 2016, Vol. 7
2016, Vol. 7


