| 广东某低品位铜矿石细菌浸出研究 |
近年来,富矿、易处理矿资源日益减少,环保要求不断提高,利用微生物浸出贫矿、废矿以及难采、难选、难冶矿石中有用金属的技术显示出了独特的优越性.目前全世界已有约50 个采用生物冶金浸出铜矿石的工业应用实例,尤其是针对低品位次生硫化矿和氧化矿,生物冶金的应用实现了广泛推广[1-12].广东某矿山有大约50 万t 低品位难选铜矿石,铜金属量预计为2 500~3 000 t,矿石中铜的赋存状态复杂,仅通过物理选矿很难有效回收矿石中的铜.针对该矿山存在的问题,开展了低品位铜矿石的生物浸出试验研究,为实现该难选铜矿石的高效利用提供技术指导.
1 材料与方法 1.1 矿石性质试验所用矿石来自广东某铜矿露采场,矿石多元素分析结果见表 1,铜物相分析结果见表 2.矿石中铜含量为0.505 %,其中水溶铜和自由氧化铜占总铜的23.30 %,结合氧化铜占总铜的11.07 %,次生硫化铜占总铜的56.31 %,原生硫化铜占总铜的9.32 %.本次浸出试验所用矿石的磨矿细度为≤0.074 mm 占80 %.
| 表1 原矿多元素化学分析结果/% Table 1 Analysis results of multi-elements of crude ore /% |
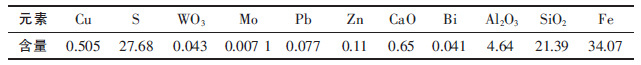 |
| 点击放大 |
| 表2 原矿铜物相分析结果/% Table 2 Analysis results of copper phase of crude ore /% |
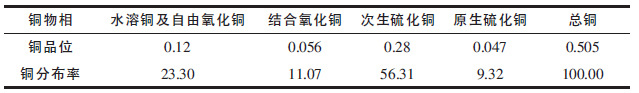 |
| 点击放大 |
1.2 菌种与培养基
试验所用菌种为从某硫化矿山中分离获得的氧化亚铁硫杆菌GZY-1 菌株,该菌株是对铁、硫具有氧化特性的细菌混合培养物[13].
本试验采用改进的9K 培养基[13]:(NH4)2SO4 3 g,KCl 0.1 g,K2HPO4 0.5 g,MgSO4·7H2O 0.5 g,Ca(NO3)2 0.01 g,蒸馏水1000 mL,FeSO4·7H2O 44.5 g,pH 值为1.5~2.0.
GZY-1 菌株在低品位铜矿石含量为1 %(W/V)的液体培养基中驯化培养,用细菌处于对数生长期的培养液进行低品位铜矿石的浸出试验.
1.3 试验方法在HZQ-C 型恒温振荡器中,采用摇瓶浸出法研究低品位铜矿石的细菌浸出效果.本试验按照矿浆浓度分为3 组,30 个容量为250 mL 的锥形瓶中分别装入100 mL 细菌处于对数生长期的9K 液体培养基,第1 组10 个锥形瓶中分别加入10 g 矿样,第2 组10 个锥形瓶中分别加入15 g 矿样,第3 组10 个锥形瓶中分别加入20 g 矿样,在30 ℃、200 r/min 条件下摇瓶浸出矿石中的铜.浸出24 h 后,每天从3 组锥形瓶中各取出1 瓶,分别测定矿浆的pH 值和氧化还原电位.矿浆固液分离后,测定浸矿液中的细菌浓度,分析检测浸矿液中的铜离子浓度.浸出残渣经过洗涤、烘干、制样后,分析残渣中铜的含量,计算矿石中铜的浸出率.
1.4 试验仪器设备常州澳华生产的HZQ-C 型恒温振荡器;上海精科生产的PHS-3C 型pH 计,雷磁E-201-C pH 复合电极,501 型氧化还原电极,232-01 参比电极; 上海成光生产的XSP-2XC 型生物显微镜;常熟双杰生产的JJ1000 型电子天平.
2 结果与讨论 2.1 摇瓶浸出条件下矿石中铜的浸出效果在温度30 ℃、转速200 r/min、矿浆起始pH 值1.85 的浸出条件下进行了3 组不同矿浆浓度的细菌浸出试验,浸出时间为10 d,试验结果见图 1.
 |
| 图 1 浸矿过程中铜浸出率的变化 Fig. 1 Change of copper leaching rate in process of leaching |
从图 1 可以看到,在3 组不同矿浆浓度下矿石中铜的浸出率分别达到97.72 %、92.42 %、87.66 %,表明GZY-1 菌株培养液可以高效浸出该低品位铜矿石中的铜.分析浸矿曲线可以发现,在浸出起始阶段,随着浸出时间的延长,矿石中铜的浸出率不断提高,但达到一定的浸出率后不再增加.第1 组100 mL 培养液浸出10 g 矿石,浸出5 d,矿石中铜的浸出率达到97.56 %,延长浸出时间,矿石中铜的浸出率不再增大;第2 组100 mL 培养液浸出15 g 矿石,浸出7 d,矿石中铜的浸出率达到91.45 %,延长浸出时间,矿石中铜的浸出率不再明显增大; 第3 组100 mL 培养液浸出20 g 矿石,浸出9 d,矿石中铜的浸出率达到87.66 %,继续延长浸出时间,矿石中铜的浸出率也不再明显增加.
2.2 浸矿过程中细菌浓度的变化本试验采用细菌处于对数生长期的培养液摇瓶浸出低品位铜矿石,在矿石浸出过程中,浸矿液中细菌浓度的变化见图 2.
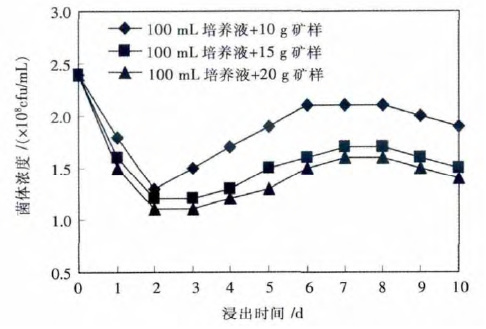 |
| 图 2 浸矿过程中细菌浓度的变化 Fig. 2 Change of bacterial concentration in process of leaching |
从图 2 可以看出,本次浸矿试验使用的细菌培养液的菌体浓度为2.4×108 cfu/mL,在3 组不同矿浆浓度的矿石浸出过程中,浸矿液中的细菌浓度是不断变化的,先降低,后升高,然后再慢慢降低.浸出前期浸矿液中菌体浓度降低的原因有二:一是矿浆中快速运动的矿石固体颗粒会对细菌体产生摩擦、挤压和剪切作用,造成菌体损失和死亡;二是部分细菌体会吸附在固体矿物表面,造成浸矿液中菌体浓度降低.浸矿过程中,随着矿石中硫化物的不断氧化,矿浆中的细菌浓度会不断升高,但当浸出液中的各种金属离子累积到一定的数量时,细菌的氧化活性就会受到抑制,浸矿液中的细菌浓度就会相应有所降低.
2.3 浸矿过程中矿浆体系pH 值的变化在细菌浸矿过程中,矿石中硫化矿的细菌氧化会产生硫酸,而氧化铜矿的溶解浸出会消耗硫酸,其它钙镁等氧化物的溶解也会消耗硫酸,以上反应过程会导致矿浆pH 值发生变化,本次试验的变化结果见图 3.
 |
| 图 3 浸矿过程中pH 值的变化 Fig. 3 Change of pH value in process of leaching |
从图 3 可以看出,低品位铜矿石细菌浸出过程中,矿浆体系的pH 值不断变化.3 组不同矿浆浓度的浸出试验中,矿浆pH 值的变化趋势相似,在浸出过程中,矿浆pH 值先不断升高,从1.85 升高到2.35左右,然后慢慢降低到2.0 左右.分析原因,是由于本次试验浸出的矿石是低品位氧化铜-硫化铜混合矿石,在浸出过程中2 种不同类型的反应会影响矿浆体系的pH 值变化.第1 类是矿石中的可溶性氧化铜矿物和细菌培养液中的硫酸发生溶解反应生成硫酸铜,该反应会消耗硫酸,造成浸矿体系的pH 值升高;第2类是矿石中的硫化铜、硫化铁等硫化矿物的细菌氧化反应,该类反应会产生硫酸,造成浸矿体系的pH 值降低.在浸出前期,主要是矿石中氧化矿物的硫酸溶解反应,造成矿浆体系中酸度下降,pH 值升高;随着矿浆体系细菌浓度的不断增大,细菌氧化活性的不断提高,矿石中的硫化物不断被细菌氧化,产生过量的硫酸,使得矿浆体系的酸度增大,pH 值下降.
2.4 浸矿过程中矿浆体系氧化还原电位的变化细菌浸矿过程中,由于细菌对矿石中硫化物特别是硫化铁矿物的氧化、Fe3+对硫化物的氧化,以及细菌对Fe2+的氧化,使得浸矿体系中的Fe3+和Fe2+浓度不断产生变化,造成浸矿过程中矿浆体系的氧化还原电位发生变化,本次试验的变化结果见图 4.
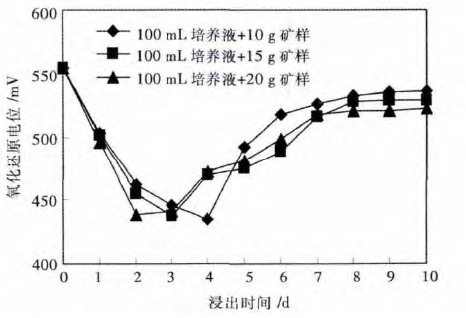 |
| 图 4 浸矿过程中氧化还原电位的变化 Fig. 4 Change of redox potential in process of leaching |
从图 4 可以看出,低品位铜矿石细菌浸出过程中,矿浆体系的氧化还原电位是发生变化的.3 组浸出试验中,矿浆的氧化还原电位先降低,从起始的554 mV 降低到435~438 mV,然后再升高到522~536 mV.原因是由于本次试验采用细菌处于对数生长期的9 K 培养液浸出矿石,该培养液中Fe3+离子浓度接近9 g/L,而Fe2+浓度不足0.2 g/L,[Fe3+]/[Fe2+]比值大,所以浸矿液的起始氧化还原电位较高,达到554 mV.在浸出前期,由于Fe3+对硫化物特别是硫化铁矿物的氧化反应,造成矿浆体系中Fe3+离子浓度降低,Fe2+离子浓度大幅升高,造成矿浆体系的氧化还原电位降低.然后随着矿浆体系中细菌浓度的不断增大,细菌氧化活性的不断提高,溶液中的Fe2+会被细菌快速氧化为Fe3+,[Fe3+]/[Fe2+] 比值会变大并稳定在一个较高的水平,矿浆体系中的氧化还原电位也会相应升高到522~536 mV,并在一定时间内保持稳定.
2.5 细菌浸铜机理分析由于本次试验浸出矿石类型为低品位氧化铜-硫化铜混合矿石,涉及到3 种类型的浸出反应:一是氧化铜矿物的硫酸直接浸出[14-15];二是硫化铜矿物的细菌直接浸出[16-17];三是硫化铜矿物的间接浸出[18-19].
可溶性氧化铜矿物硫酸直接浸出反应式:
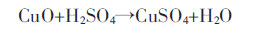
|
硫化铜矿物细菌直接浸出反应式如下:
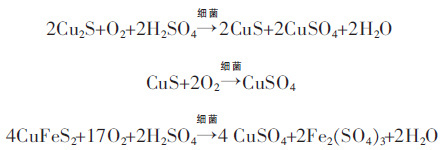
|
硫化铜矿物间接浸出反应:
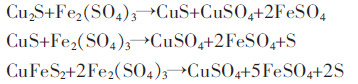
|
另外,该矿石浸出过程中还有以下细菌氧化反应[19]:
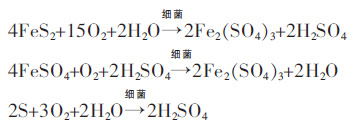
|
1)在温度30 ℃、转速200 r/min 、起始pH 值1.85、矿石磨矿细度为≤0.074 mm 占80 %的条件下,采用氧化亚铁硫杆菌GZY-1 菌株培养液搅拌浸出广东某低品位难选氧化铜-硫化铜混合矿石,在3 组不同矿浆浓度下,浸出10 d,矿石中铜的浸出率分别达到97.72 %、92.42 %、87.66 %.结果表明该低品位铜矿石中的铜矿物可以被GZY-1 菌株培养液高效浸出.
2)细菌培养液搅拌浸铜过程中,由于发生多种生物、化学反应,矿浆中的细菌浓度、pH 值、氧化还原电位产生变化.细菌浓度在浸出前期会有所降低,然后不断升高,浸出后期又会有所降低;pH 值在浸出前期会有所升高,然后随着细菌对硫化矿物的氧化,不断产生硫酸,导致矿浆体系的pH 值降低;氧化还原电位在浸出前期会有所降低,然后随着矿浆中 Fe2+被细菌快速氧化为Fe3+,矿浆体系的氧化还原电位相应升高,并在一定时间内保持稳定.
3)本次试验采用氧化亚铁硫杆菌氧化浸出低品位氧化铜-硫化铜混合矿石,浸铜机理涉及到3 种类型的反应:一是可溶性氧化铜矿物的硫酸直接浸出;二是硫化铜矿物的细菌直接浸出; 三是硫化铜矿物的间接浸出.
| [1] | 曾伟民, 邱冠周. 硫化铜矿生物堆浸研究进展[J]. 金属矿山, 2010, 410(8): 102–107. |
| [2] | 邹平, 杨家明, 周兴龙, 等. 嗜热嗜酸菌生物浸出低品位原生硫化铜矿[J]. 有色金属, 2003, 55(2): 21–24. |
| [3] | 施利特WJ. 美国肯尼柯特铜业公司百万吨级试验堆浸—— 一种有效的浸出方案(第1部分)[J]. 国外金属矿选矿, 2006, 43(11): 4–10. |
| [4] | 施利特WJ. 美国肯尼柯特铜业公司百万吨级试验堆浸 —— 一种有效的浸出方案(第2部分)[J]. 国外金属矿选矿, 2006, 43(12): 12–18. |
| [5] | 熊英, 胡建平, 林滨兰, 等. 硫化铜矿微生物浸出-溶剂萃取-结晶硫酸铜[J]. 湿法冶金, 2002, 21(1): 28–31. |
| [6] | 柳建设, 夏海波, 王海东. 低品位硫化铜矿细菌浸出[J]. 中国有色金属学报, 2000, 14(2): 286–290. |
| [7] | 陈世馆. 生物浸出及其在有色冶金中的应用[J]. 上海有色金属, 2000, 21(3): 137–146. |
| [8] |
Darezereshki E, Schaffie M, Lotfalian M., et al. Use of mesophilic and thermophilic bacteria for the improvement of copper extraction from a low-grade ore[J].
International Journal of Minerals, Metallurgy and Materials, 2011, 18(2): 138–143. DOI: 10.1007/s12613-011-0413-1. |
| [9] | 刘美林, 臧宏, 周成英, 等. 嗜温菌、中等嗜热菌、嗜热菌分段浸出原生硫化铜矿表外矿万吨级工业堆浸试验[J]. 湿法冶金, 2012, 31(6): 357–362. |
| [10] | 伍赠玲, 赖晓康, 邹来昌, 等. 低品位次生硫化铜矿生物柱浸试验研究[J]. 湿法冶金, 2014, 33(6): 424–428. |
| [11] | 白静, 温建康, 黄松涛, 等. 不同成矿条件下黄铜矿微生物浸出研究概况[J]. 稀有金属, 2012, 36(4): 644–650. |
| [12] | 潘嘉芬, 盛桂华. 氧化亚铁硫杆菌浸出贫铜矿中的铜离子试验研究[J]. 矿业研究与开发, 2013, 33(5): 47–50. |
| [13] | 周吉奎, 钮因健. 微生物浸出低品位铜矿的研究[J]. 中国有色冶金, 2006, 6(3): 24–27. |
| [14] | 严佳龙, 王洪江, 吴爱祥, 等. 羊拉铜矿氧化铜矿柱浸扩大试验研究[J]. 矿冶工程, 2011, 31(2): 79–82. |
| [15] | 李辉, 胡重, 刘岩. 刚果(金)氧化铜矿硫酸浸出的研究[J]. 有色矿冶, 2014, 30(2): 35–38. |
| [16] | 卢贯能, 莫镇华, 罗汉金, 等. 常温浸矿菌对高砷铜精矿浸出机理的研究[J]. 矿冶工程, 2012, 32(3): 82–85. |
| [17] | 吴健辉. 紫金山低品位铜矿生物堆浸模拟研究[J]. 有色金属(冶炼部分), 2015(2): 1–4. |
| [18] | 周吉奎, 钮因健. 硫化矿生物冶金研究进展[J]. 金属矿山, 2005, 346(4): 24–30. |
| [19] | 童雄. 微生物浸矿的理论与实践[M]. 北京: 冶金工业出版社 , 1997. |
 2015, Vol. 6
2015, Vol. 6

