| 大颗粒氧化钆的沉淀法合成及其合成条件控制的研究 |
氧化钆作为一种重要的稀土氧化物,已被广泛应用于催化剂、陶瓷和光学玻璃、荧光材料[1]以及核工业材料.随着工业科学技术的发展,氧化钆的应用将有广阔的市场前景,同时对稀土氧化的形貌及粒度有了更高的要求.例如,喷涂材料要求稀土氧化物粒度在10μm以上[2],而陶瓷用稀土氧化物的要求其粒度甚至大于100μm [3],熔盐电解制备单质金属用的氧化物,为达到节能降耗、提高电解效率和环保目的,则希望选用砂状形貌的氧化物,如砂状稀土氧化物,氧化钆、氧化钕和氧化钇;以及电解铝使用的砂状氧化铝[4].目前对于稀土氧化物的研究主要集中在微米级以下,而对大颗粒稀土氧化物的研究却很少报道,尤其是氧化钆.制备特殊形貌的稀土氧化物大都采用液相法,其中又以沉淀法[5]最为广泛和实用.沉淀法制备稀土氧化物的使用的沉淀剂很多,有NH4HCO3[6]、NH4HCO3和氨水[7]、氨水[8]、尿素[9]及草酸[10]等.本文以早期工业生产用的草酸为沉淀剂,合成了大颗粒及砂状形貌的氧化钆.
1 实验原料:氧化钆,99.9 %;草酸,分析纯;浓盐酸,分析纯;去离子水,自制.
设备:集热式磁力加热搅拌器;循环水真空泵;电子天平;马尔文激光粒度分析仪,型号2000;比表面积分析仪,型号ASAP2020;场发射扫描电镜,型号为MI3401474.
实验过程:配制一定浓度的草酸和氯化钆溶液,将草酸缓慢滴入到已加热到设定温度的氯化钆溶液中,待沉淀完全,陈化,将沉淀用去离子水和酒精各洗涤过滤3次,经100 ℃干燥12 h,最后高温灼烧,即可制得目标产物.
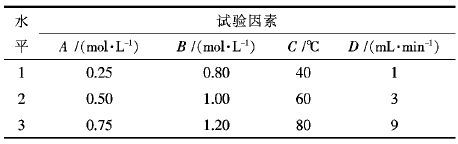
针对草酸沉淀稀土反应快、草酸盐溶解度低,且影响沉淀因素众多特点,笔者采用正交方式进行实验影响因素的分析.选择稀土料液起始浓度、草酸浓度、反应沉淀温度、滴加速率为正交试验的影响因素.每因素取3水平.正交试验因素和具体水平见表 1,其中A代表氯化钆起始浓度;B代表草酸浓度;C代表沉淀温度;D代表草酸滴加速率.
| 表1 正交试验与水平表 Table 1 Orthogonal test level |
 |
| 点击放大 |
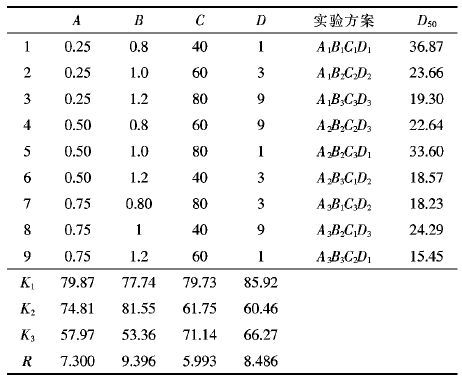
具体正交试验方案与粒径统计结果见表 2.
| 表2 正交试验方案与对应中心粒径结果 Table 2 Result of orthogonal test program and the corresponding median particle size |
 |
| 点击放大 |
2 结果与分析
从表 2正交实验方案和粒径统计可以得知,氯化钆起始浓度、草酸浓度、沉淀温度及滴加速率对实验最终产物的粒径影响大小:草酸浓度B>滴加速率D>氯化钆起始浓度A>沉淀温度C.由于以上几个因素的水平数跨度偏大,未能全面反映各个制备条件对最终产物粒度大小的影响效果,以及陈化时间和灼烧温度对最终产物粒径的影响未研究.因此,笔者再选择前3个影响因素及陈化时间、灼烧温度做单因素实验研究.
2.1 草酸浓度对Gd2O3粒径的影响草酸作为传统工业生产稀土氧化物用的沉淀剂,现仍然大量应用于稀土粉体材料的研究.在用草酸作为沉淀剂的研究中,稀土氧化物的粒径与前驱体稀土草酸盐的粒径大小成正比[11],而稀土草酸盐粒径大小与沉淀剂草酸浓度、沉淀温度、原料浓度等有密切关系[12].固定氯化钆起始浓度0.25 mol/L,沉淀温度60 ℃;滴速3 mL/min;陈化时间10 h;灼烧温度900 ℃不变.控制草酸浓度为0.6 mol/L,0.8 mol/L,1.0 mol/L,1.2 mol/L,1.4 mol/L进行试验,并对最终的 产物做粒度分析.
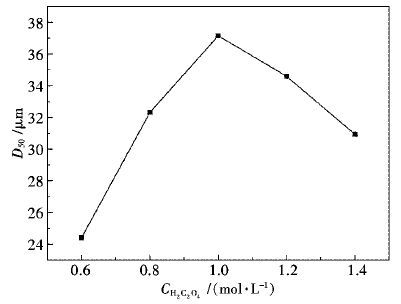 |
| 图 1 草酸浓度与氧化钆D50的关系 Fig. 1 Diagram of relationship between oxalic acid concentration and D50 of Gd2O3 |
从图 1可以得知,Gd2O3的中心粒径D50随着沉淀剂草酸浓度的增大,呈现先增大后减小趋势,且在草酸浓度为1.0 mol/L时,D50达到最大值37.15μm.原因是,当草酸浓度在0.6~1.0 mol/L范围内,反应瞬间生成大量的稀土草酸盐晶粒,且尺寸非常小,极易团聚成小颗粒,而团聚后小颗粒粒径仍较小,易二次团聚,且随着草酸浓度的增大,团聚效果越明显.而当草酸浓度达到1.0 mol/L后,由于草酸浓度过大,初次形成的晶粒变大,一次团聚后,无法再二次团聚,即出现Gd2O3的D50逐渐变小现象.
2.2 滴加速度对Gd2O3粒径的影响沉淀剂滴加速率也是影响稀土草酸盐沉淀物粒度大小的重要因素之一,柳召刚等[13]在用草酸沉淀法制备CeO2的实验中,就报道了沉淀剂滴加速率对CeO2颗粒粒度的影响,结果表明,要获得细颗粒的CeO2,滴加速率宜控制在6 mL/min.固定氯化钆起始浓度0.25 mol/L,沉淀温度60 ℃;陈化时间10 h;灼烧温度900 ℃;草酸浓度1 mol/L不变.控制草酸滴加速率为1 mL/min,3 mL/min, 6 mL/min,9 mL/min,12 mL/min,实验结果见图 2.
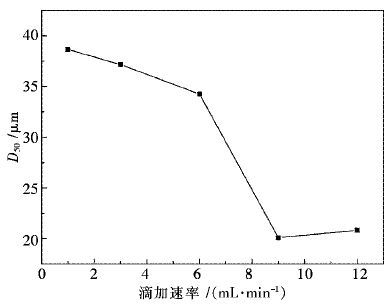 |
| 图 2 草酸滴加速率与氧化钆D50的关系 Fig. 2 Diagram of relationship between oxalic acid addition rate and D50 of Gd2O3 |
从图 2可以得知,Gd2O3的D50与滴加速率大致呈反比关系.原因是,在一定浓度范围内,草酸滴加速率大,容易造成浓度梯度存在,以至于局部反应生成晶粒存在较长的时间差; 这大大增加了核长大的作用,则形成晶粒的变大且极不均匀,晶粒表面能减小而导致团聚作用减弱,而颗粒粒径变小;随着滴速的增加此现象越严重,所以颗粒粒度逐渐较小.但是,速率不宜过小,过小易导致化学反应过慢,以至于晶核长大占据主导而出现粒度不均匀.若要制备大颗粒的Gd2O3,沉淀剂滴加速率宜控制为1~3 mL/min之间.
2.3 氯化钆起始浓度对Gd2O3粒径的影响氯化钆作为反应原料,将直接与草酸反应形成稀土草酸盐沉淀.固定沉淀温度60 ℃;陈化时间10 h;灼烧温度800 ℃;草酸浓度0.80 mol/L;草酸滴加速率3 mL/min不变.控制氯化钆起始浓度为0.10 mol/L,0.30 mol/L,0.50 mol/L,0.70 mol/L,0.90 mol/L,实验结果见图 3.
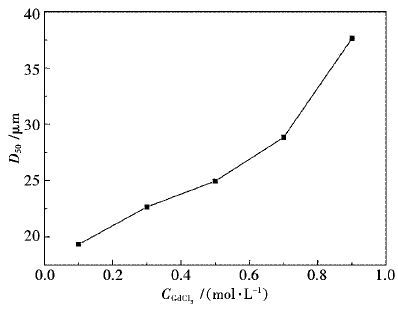 |
| 图 3 氯化钆起始浓度与氧化钆D50的关系 Fig. 3 Diagram of relationship between the initial concentration of GdCl3 and D50 of Gd2O3 |
从图 3可以得知,当氯化钆起始浓度在0.10~0.90 mol/L范围时,Gd2O3的D50与氯化钆起始浓度大致成正比关系,氯化钆起始浓度由0.75 mol/L变为0.90 mol/L时,粒径变化增大最多,且D50最大值能达到37.64μm.原因是,随着氯化钆起始浓度增大,化学反应形核速率越大,而形核作用和核长大作用存在相对竞争关系,因此削弱了核长大作用;所以随着其浓度的不断增大,反应形核数急剧增多,团聚现象就越明显,即颗粒粒径随着氯化钆起始浓度增大而增大.
2.4 陈化条件对Gd2O3粒径和形貌的影响陈化是指反应完全的沉淀微粒在一定温度、一定振荡频率条件下的反应母液中进行物理化学反应的过程.事实上,由于存在粒度不同的颗粒,母液对小晶粒未达到饱和状态,母液对大颗粒已经达到饱和,所以小晶粒在溶解与结晶动态趋于平衡过程中,小晶粒溶解,而大颗粒在这个过程中粒径变大,表面变光滑规整.由此可见,陈化过程是沉淀法制备大颗粒的关键因素之一.
如图 4为陈化时间与最终产物的中心粒径D50的关系图.其他具体条件如下:固定沉淀温度60 ℃;灼烧温度900 ℃;草酸浓度1.0 mol/L;草酸滴加速率3 mL/min;氯化钆起始浓度0.30 mol/L不变;控制陈化时间为0 h,5 h,10 h,15 h,20 h,25 h,30 h.
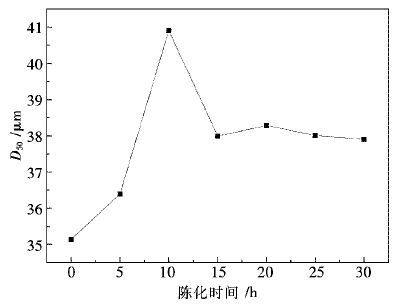 |
| 图 4 陈化时间与氧化钆D50的关系 Fig. 4 Diagram of relationship between aging time and D50 of Gd2O3 |
如图 5为沉淀温度60 ℃;灼烧温度900 ℃;草酸浓度1.0 mol/L;草酸滴加速率3 mL/min;氯化钆起始浓度0.30 mol/L;陈化时间10 h,振荡处理和未振荡处理的SEM图.从图 5(a)可以得知,经振荡陈化的氧化钆大都为规则的棱柱状,粒度也相对均匀,几乎不存在微小颗粒.从图 5(b)可以得知,除了大量的柱状颗粒外,还有大量微小颗粒,且小颗粒附着在柱状大颗粒上.综合图 4和图 5可以得知,随着陈化时间增长及附加振荡处理,确实有助于溶液内部大颗粒变规整、小颗粒溶解.因此,陈化过程,适当延长陈化时间和附加振荡作用,对形成粒度均匀,相貌规整的大颗粒是十分必要的.
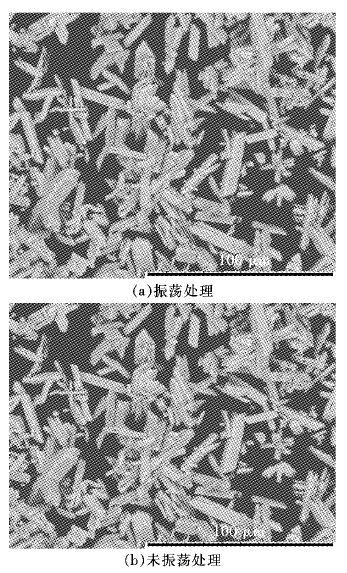 |
| 图 5 不同陈化处理条件的SEM图 Fig. 5 SEM image of different aging treatment conditions |
2.5 灼烧温度对Gd2O3粒径的影响
固定沉淀温度60 ℃;振荡陈化时间10 h;草酸浓度1.0 mo/L;草酸滴加速率3 mL/min;氯化钆起始浓度0.10 mol/L不变;灼烧温度为750 ℃,800 ℃,850 ℃,900 ℃,950 ℃;粒径分析结果见图 6.
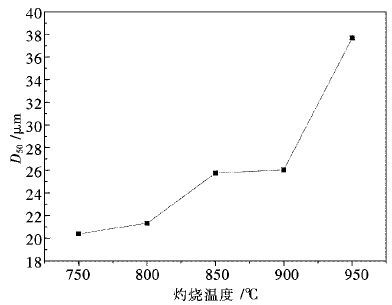 |
| 图 6 灼烧温度与氧化钆D50的关系 Fig. 6 Diagram of relation between the firing temperature and D50 of Gd2O3 |
从图 6可以看出,随着灼烧温度的升高,最终产物氧化钆D50呈增大趋势,最大可以达到D50为37.65μm.在低于900 ℃范围时,粒径增大趋势小,当温度超过900 ℃时,氧化钆的D50迅速增大.这是因为,在灼烧温度接近850 ℃时,氧化钆已经分解完全,晶型也已完整;当温度继续升高,颗粒开始板结,即颗粒粒度迅速变大.所以灼烧温度应控制在850~900℃间.实验结果也与史卫东等[14]人报道的制备大颗粒氧化物所需灼烧温度相吻合.
2.6 大颗粒氧化钆的合成根据正交试验结果,以及对焙烧温度、草酸浓度、氯化钆起始浓度、滴加速率、沉淀温度与Gd2O3的粒径的关系的总结.选择氯化钆起始浓度0.9 mol/L、草酸浓度1 mol/L、滴加速率1 mL/min、沉淀温度60~70 ℃、振荡陈化时间10 h、灼烧温度900 ℃,即能制备D50为38.93μm的大颗粒Gd2O3.大颗粒Gd2O3的SEM如图 7,不规则的大颗粒粒度总体分布均匀,每个大颗粒是由几个微米的类球形小颗粒团聚而成.
 |
| 图 7 大颗粒Gd2O3的SEM图 Fig. 7 SEM image of larger particles Gd2O3 |
2.7 砂状氧化钆合成的探究
当前,用于熔盐电解制备稀土金属或者合金的稀土氧化物大都是几个微米的小颗粒,而其中存在粉体流动性差以及扬尘损失的问题,现仍然没有解决.而砂状稀土氧化物拥有大比表面积、粒度分布均匀、流动性好和易溶解的特点[15],正好能克服上述存在的问题,既可以减小损耗、改善电解过程的传质,提高电解效率,又环保[16].
图 8是正交试验组8号所制备Gd2O3的SEM图,放大倍数5 000.具体实验制备条件为:草酸浓度0.8 mol/L;草酸滴加速率3 mL/min;氯化钆起始浓度0.75 mol/L;沉淀温度80 ℃;振荡陈化时间10 h;灼烧温度900 ℃.
 |
| 图 8 砂状Gd2O3的SEM图 Fig. 8 SEM image of sand shaped Gd2O3 |
从图 8可以得知,颗粒为20μm左右,呈现类球形,并由大量粒径在1μm左右的小颗粒松散团聚而成,中间存在大量孔隙.此外,测得比表面积为6.0010 m2/g.测得粒径相关数据D50=18.57μm,D10=9.99μm ,D90=29.49μm,而粉体粒度分布好坏可由离散度:
离散度=(D90-D10)/D50
来衡量[17].由离散度为1.05可知,制备的Gd2O3颗粒粒度分布窄.根据上述对正交试验组7号所制备的氧化钆的形貌、粒径分布及比表面积的分析,可知实验所制备的氧化钆大致符合砂状氧化物对形貌的要求.
3 结论1) 确定了制备粒度分布均匀且中心粒径D50为39μm的大颗粒Gd2O3的实验制备条件:氯化钆起始浓度0.9 mol/L、草酸浓度1 mol/L、滴加速率1 mL/min、沉淀温度60~70 ℃、振荡陈化时间10 h、灼烧温度900 ℃.
2) 根据制备条件:草酸浓度0.8 mol/L、草酸滴加速率3 mL/min、氯化钆浓度0.75 mol/L、沉淀温度80 ℃、振荡陈化时间10 h、灼烧温度900 ℃,可制备中心粒径D50为18.57μm,比表面积为6.0010 m2/g,形貌大致符合砂状稀土氧化物要求的Gd2O3.对今后砂状稀土氧化物的研究提供实验依据.
| [1] |
Bi H F, Li X. Self-assembled columnar structure Gd2O3:Eu3+:solvothermal synthesis and luminescence properties[J].
Integrated Ferroelectrics, 2012, 135(1): 119–124. DOI: 10.1080/10584587.2012.685421. |
| [2] | 马莹, 李莉娜, 王宝荣. 草酸沉淀法制备大颗粒氧化钇工艺研究[J]. 稀有金属, 2010, 34(6): 950–953. |
| [3] | 高玮, 古宏晨. 稀土草酸盐沉淀过程中颗粒大小的控制[J]. 稀土, 2000, 21(2): 11–13. |
| [4] |
Fadda M B, Dessi M R, Rinaldi A, et al. sandy alumina as substrate for economic and highly efficient immobilization of beta-glucosidase[J].
Biotechnology and bioengineering, 1989, 33(6): 777–779. DOI: 10.1002/(ISSN)1097-0290. |
| [5] |
Ravi K S, Ranjana G. Synthesis of nanocrystalline CuO-ZnO mixed oxide powder by a homogeneous precipitation method[J].
Ceramics International, 2014, 40(7): 10744–10749. |
| [6] | 李梅, 刘召刚, 胡艳宏, 等. 碳酸氢铵沉淀法制备大颗粒稀土氧化物的研究[J]. 稀有金属, 2007, 31(5): 717–720. |
| [7] | 王士智, 赵永志, 郝先库. 大颗粒氧化钆的制备及物理性能研究[J]. 稀土, 2014, 35(2): 63–67. |
| [8] | 潘艳.掺杂氧化钇纳米功能材料的制备及其光学性能的研究[D].北京:中国科学院研究生院,2010. |
| [9] | 秦海明.尿素沉淀法Y2O3纳米粉体微结构调控机制及其在YAG透明陶瓷制备中的应用[D].济南:山东大学,2013. |
| [10] | 周筱桐, 肖汉宁, 刘井雄. 草酸沉淀法制备稀土抛光粉其其抛光性能[J]. 机械工程材料, 2014, 38(8): 57–60. |
| [11] | 赵小山, 冯江传. 稀土草酸盐的溶解度与稀土氧化物粒径之间的关系及粒度控制[J]. 稀有金属, 2003, 27(1): 167–169. |
| [12] | 王觅堂.草酸铈沉淀过程中团聚行为的研究[D].包头:内蒙古科技大学,2005. |
| [13] | 柳召刚, 李梅, 史振学. 草酸沉淀法制备超细氧化铈的研究[J]. 中国稀土学报, 2008, 26(5): 666–670. |
| [14] | 史卫东,肖睿,朱荣华.大颗粒稀土氧化物的制备方法:中国,ZL200610040818.1[P].2008-06-11. |
| [15] | 曾青云, 帅庚未, 张勇. 微波外场对液相合成砂状氧化钇前驱体形貌的影响[J]. 有色金属科学与工程, 2014, 5(3): 28–31. |
| [16] | 李程文, 周康根, 姜科涛, 等. 晶种法处理含氟废水与氟化钙沉淀砂状化研究[J]. 环境科学与技术, 2011, 34(5): 157–160. |
| [17] | 张福根.粒度测量基础理论与研究论文集[M].4版.广州:珠海欧美克仪器有限公司:2007,10. |
 2016, Vol. 6
2016, Vol. 6

