| 锌冶炼中浸渣锌还原浸出行为研究 |
2. 国家重金属污染防治工程技术研究中心,长沙 410083
2. Chinese National Engineering Research Center for Control & Treatment of Heavy Metal Pollution, 410083, Changsha,China
锌是应用广泛的有色金属,目前世界上超过80 %的金属锌采用湿法冶炼工艺,即锌精矿焙烧-浸出-净化-电积流程[1-2].铁原子半径与锌相近,常以配位体形式置换闪锌矿中部分锌而进入晶格中,锌精矿中伴生铁有的甚至高达20%以上[3].在锌精矿高温氧化焙烧时,部分锌与铁生成稳定性极强的具有尖晶石结构的铁酸锌,在中性浸出工序难以被浸出,导致约10 %~20 %的锌以铁酸盐形式进入渣中,降低了锌浸出率[4-6].
锌浸出渣的处理包括火法处理和湿法处理工艺.火法处理包括常用的回转窑挥发、烟化法等方法,将渣中锌元素还原挥发,以氧化锌粉形式回收,但此法存在污染严重,能源及资源消耗高等缺点[7-8].湿法处理工艺,包括热酸浸出黄钾铁矾法,热酸浸出针铁矿法以及热酸浸出赤铁矿法等,锌浸出率高,但存在着流程长,操作复杂,设备腐蚀严重及沉铁渣难以利用等缺点[9-11].
近年来,许多研究人员开展了铁酸锌强化浸出研究.中浸渣经机械活化后可增强中浸渣反应活性,锌浸出率有较大幅度提高[12-13].另外,有研究人员采用微波加热和超声强化浸出方法,降低了浸出酸度[14-15].浸出技术正逐渐转变为在低酸条件下(<1 mol/L)通过添加某种强化浸取剂及辅助强化手段,达到降低成本,便于操作,获取高浸出率的目的.目前,氧化还原浸出、络合浸出、选择性浸出已成为研究的重点[16-18].
本文以湿法炼锌中浸渣为研究对象,以Zn和Fe的浸出率为评价指标,研究了不同类型还原剂对渣中铁酸锌还原浸出效果,筛选出高性能还原剂,考察还原剂浓度、时间、初始酸度、温度及液固比等因素对浸出率的影响,探讨其浸出过程锌物相转变过程.
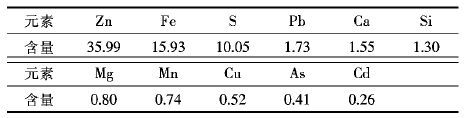
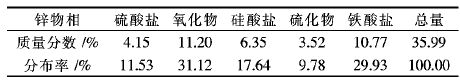
1 试验 1.1 试验原料还原浸出试验所用中浸渣来源于湖南某大型铅锌冶炼厂.中浸渣经105 ℃烘干,振磨后干燥保存.如图 1所示,其粒径主要分布在1.19~14.38 μm范围内.其化学成分如表 1 所示,锌物相分析结果见表 2.中浸渣XRD衍射图如图 2所示,中浸渣中锌主要以铁酸盐和氧化物形式存在,其次为硫酸盐、硅酸盐及硫化物等物相,而铁酸盐是制约中性浸出条件下锌浸出率提高的关键.
| 表1 中浸渣化学成分 Table 1 Chemical composition of zinc neutral leaching residue |
 |
| 点击放大 |
| 表2 中浸渣中锌的物相分析结果 Table 2 Phase composition of zinc in zinc neutral leaching residue |
 |
| 点击放大 |
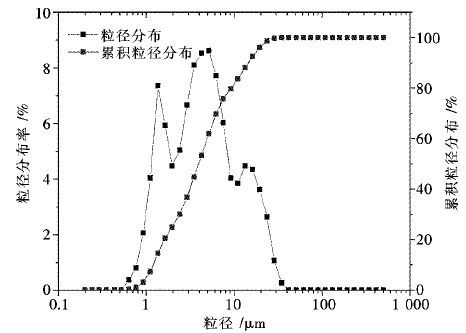 |
| 图 1 中浸渣粒径分布图 Fig. 1 Particle size distribution of zinc neutral leaching residue |
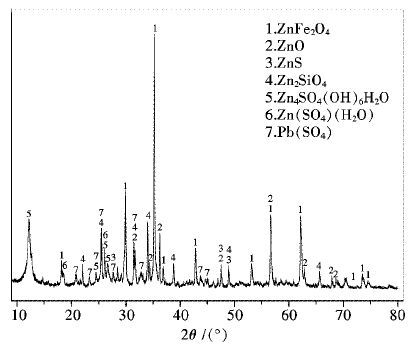 |
| 图 2 中浸渣XRD衍射图 Fig. 2 The XRD pattern of zinc neutral leaching residue |
1.2 试验方法
采用单因素实验方法,研究了还原剂种类及用量、温度、硫酸初始浓度、时间、以及液固比等因素对锌浸出率的影响.实验在恒温水浴控温的六联搅拌机上进行,温度误差1℃.采用电感等离子发射光谱法(ICP-AES)测定浸出液中Zn、Fe浓度,浸出率按式(1) 计算.浸出渣洗净,在105 ℃烘干24 h后,干燥保存,供XRD及SEM-EDS分析.在研究温度对渣中锌和铁浸出率的影响时,当温度高于水的沸点时,采用高压釜作为实验研究设备.
| $\eta {\rm{ = }}\frac{{C \times V}}{{{\rm{m}} \times {\rm{wt\% }}}} \times 100{\rm{\% }}$ | (1) |
式(1) 中,η为元素浸出率,%;C代表浸出液中元素的质量浓度,g/L;V为浸出液体积,L;m表示渣的用量,g;wt%代表元素在渣中的百分含量,%.
2 实验结果与讨论 2.1 还原剂的筛选固定硫酸初始浓度为80 g/L,温度95 ℃,液固比10 mL/g,时间120 min和搅拌速度400 r/min.还原剂用量按与渣中含铁量摩尔比1:1~1.2:1添加,考察采用不同还原剂时Zn、Fe的浸出效率.结果如图 3所示.
图 3表明,在该固定条件下不添加还原剂时Zn和Fe浸出率分别为57.1 %和2.6 %,浸出的锌物相大部分为是氧化物、硫酸盐和硅酸盐,锌的铁酸盐及硫化物未能溶出,留存于渣中.当在浸出过程中添加还原剂,Zn、Fe浸出率大幅提高,以亚硫酸钠和硫代硫酸钠为还原剂时,Zn浸出率分别提高到88.71 %和80.49 %,Fe浸出率分别为71.35 %和35.15 %;当以硫脲和硫酸肼为还原剂时,Zn浸出率分别达到了89.65 %和92.97 %,而Fe浸出率为81.19 %和89.14 %.可见,添加还原剂有利于强化渣中铁酸锌浸出,提高了锌和铁的浸出率.通过以上对比,硫酸肼对铁酸锌还原浸出效果最好,因此选择硫酸肼作为本实验还原剂.反应式如下所示.
| $\text{MeO }\!\!\cdot\!\!\text{ F}{{\text{e}}_{\text{2}}}{{\text{O}}_{\text{3}}}\text{+8}{{\text{H}}^{\text{+}}}\text{M}{{\text{e}}^{\text{2+}}}\text{+2F}{{\text{e}}^{\text{3+}}}\text{+4}{{\text{H}}_{\text{2}}}\text{O}$ | (2) |
| ${{\text{N}}_{\text{2}}}{{\text{H}}_{\text{5}}}^{\text{+}}\text{+F}{{\text{e}}^{\text{3+}}}\text{N}{{\text{H}}_{\text{4}}}^{\text{+}}\text{+1/2}{{\text{N}}_{\text{2}}}\uparrow \text{+}{{\text{H}}^{\text{+}}}\text{+F}{{\text{e}}^{\text{2+}}}$ | (3) |
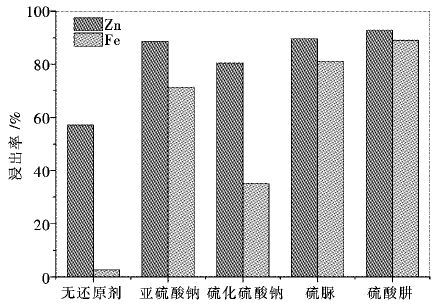 |
| 图 3 不同还原剂对中浸渣中铁酸锌的浸出效果 Fig. 3 The metal extraction efficiency of zinc neutral leaching residue at different reductants |
2.2 硫酸肼浓度对浸出效果的影响
固定搅拌速度400 r/min,温度95 ℃,硫酸初始浓度80 g/L,液固比10 mL/g,时间120 min,考察了不同硫酸肼浓度对Zn、Fe浸出率的影响.硫酸肼添加量按与渣中含铁量摩尔比0.8~1.2:1添加,结果如图 4所示.结果表明,Zn浸出率在研究的硫酸肼浓度范围内均可达90 %以上;当硫酸肼初始浓度为33.3 g/L时,Zn浸出率达95.53 %,进一步增加硫酸肼初始浓度对Zn浸出率提升较小;Fe浸出率总体上随硫酸肼初始浓度增加而提高,随着硫酸肼初始浓度从29.6 g/L增加到40.7 g/L,Fe浸出率从82.86 %提高到97.3 %.为优化中浸渣中铁酸锌还原浸出工艺参数,选定后续实验硫酸肼初始浓度为33.3 g/L.
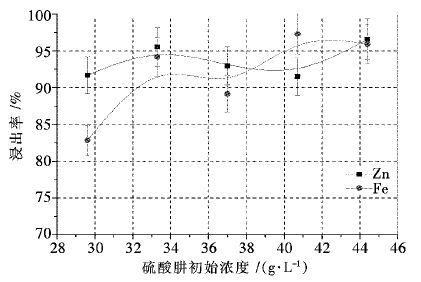 |
| 图 4 硫酸肼浓度对锌和铁浸出率的影响 Fig. 4 Effect of hydrazine sulfate concentration on metals extraction from zinc neutral leaching residue |
2.3 时间对浸出效果的影响
固定搅拌速度400 r/min,温度95℃,硫酸肼初始浓度33.3 g/L,硫酸浓度80 g/L,液固比10 mL/g,考察了不同浸出时间下Zn、Fe浸出率,结果如图 5所示.根据图 5,延长浸出时间有利于锌和铁浸出率提高.在该条件下浸出30 min,91.25 %的锌和76.9 %的铁被浸出,到120 min时Zn、Fe浸出率分别提高到了95.83 %和94.19 %,进一步延长浸出时间,Zn、Fe浸出无显著提高,此后实验浸出时间固定为120 min.
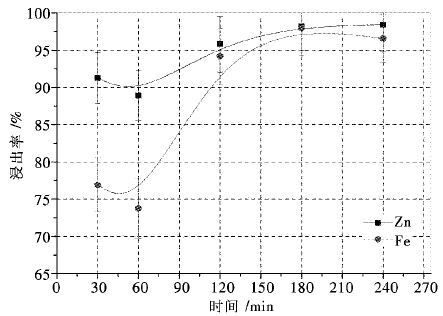 |
| 图 5 时间对锌和铁浸出率的影响 Fig. 5 Effect of leaching time on metals extraction from zinc neutral leaching residue |
2.4 硫酸浓度对浸出效果的影响
固定搅拌速度400 r/min,温度95 ℃,硫酸肼初始浓度33.3 g/L,液固比10 mL/g,浸出时间120 min,考察了不同硫酸初始浓度对Zn、Fe浸出率的影响.根据图 6,随着硫酸浓度的增加,Zn、Fe浸出率随之提高.当硫酸浓度为35 g/L,锌浸出率达73.52 %,但主要是硫酸盐,氧化物以及硅酸盐等锌的易溶态,而难溶铁酸锌依然存在于渣中,因此铁浸出率很低,只有4.71 %的铁浸出.可见,当H+严重不足时,即使存在还原剂,铁酸锌仍难以溶解.当硫酸初始浓度进一步提高到65 g/L时,Zn浸出率接近90 %,而Fe浸出率也增加到了70.62 %.硫酸初始浓度升至95 g/L时,Zn、Fe浸出率均在95 %以上;可见,硫酸初始酸度对中浸渣中铁酸锌分解有重要影响,但硫酸初始浓度过大对设备腐蚀加重.而在本实验研究中,当硫酸初始浓度为80 g/L时,Zn、Fe浸出率均在90 %以上,故选取80 g/L为后续实验固定参数.
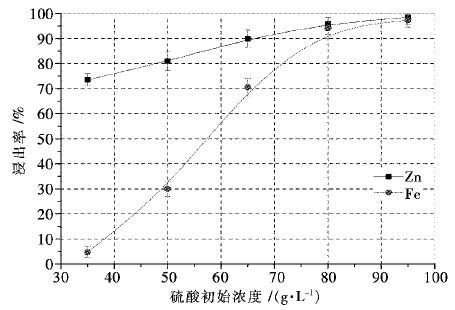 |
| 图 6 硫酸浓度对锌和铁浸出率的影响 Fig. 6 Effect of sulfuric acid concentration on metals extraction from zinc neutral leaching residue |
2.5 温度对浸出效果的影响
固定搅拌速度400 r/min,硫酸肼初始浓度33.3 g/L,硫酸初始浓度80 g/L,液固比10 mL/g,浸出时间120 min,考察了温度对Zn、Fe浸出率的影响,结果如图 7所示.当浸出温度从55 ℃提高到95 ℃时,锌的浸出率从69.08 %提高到95.83 %;铁浸出率从25.11 %提高到94.19 %,温度进一步升高到110 ℃ 时,锌和铁的浸出率无明显变化.可见温度对锌和铁浸出有重大影响,提高温度有利于锌和铁浸出率的提高,然而过高的温度不仅增加操作难度,而且导致高能量消耗,因此在保证金属浸出率前提下,浸出温度宜控制在水沸点以下,所以选定温度95 ℃为后续实验操作温度.
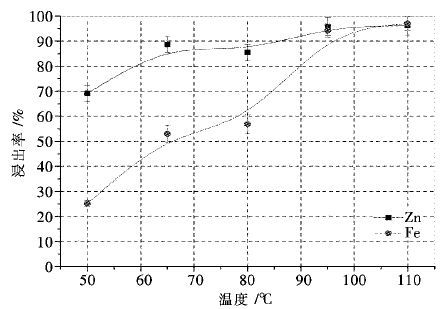 |
| 图 7 温度对锌和铁浸出率的影响 Fig. 7 Effect of leaching temperature on metals extraction from zinc neutral leaching residue |
2.6 液固比对浸出效果的影响
固定搅拌速度400 r/min,硫酸肼初始浓度33.3 g/L,硫酸初始浓度80 g/L,温度95 ℃,浸出时间120 min,考察了液固比对Zn、Fe浸出率的影响.结果如图 8所示,Zn、Fe浸出率随液固比的增加而增加,这主要归因于反应物硫酸和硫酸肼量的增加.当液固比为7 mL/g时,Zn、Fe浸出率分别达到79.74 %和48.65 %,随着液固比增加到10 mL/g,Zn、Fe浸出率分别提高到95.83 %和94.19 %,进一步增加浸出液固比对Zn、Fe浸出率影响不大.
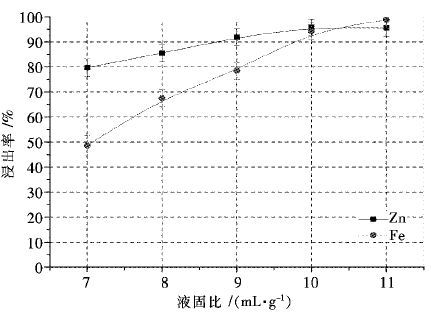 |
| 图 8 液固比对锌和铁浸出率的影响 Fig. 8 Effect of Liquid-Solid Ratio on metals extraction from zinc neutral leaching residue |
2.7 浸出过程物相转变
图 9为不同温度下铁酸锌-水系的电位-pH图,从图 9中可以看出在酸性条件下ZnFe2O4的浸出物相转变由铁酸锌分解为Fe2O3和Zn2+,再分解为Fe3+;在还原条件下,Fe2O3分解为Fe2+,而且Fe2+与Zn2+有着较大稳定共存区域,使得能够在较低的酸度条件下实现铁酸锌的分解,以提高锌的浸出率.温度升高使得Fe2+与Zn2+的pH稳定区域缩小,需要更高酸度以保证铁酸锌浸出率,同时Fe2+与Zn2+的稳定共存区域氧化还原电位升高,为酸性条件下Zn、Fe还原浸出创造了有利条件,通过添加还原剂控制体系氧化还原电位,在适当酸度条件下即可保证铁酸锌的浸出.
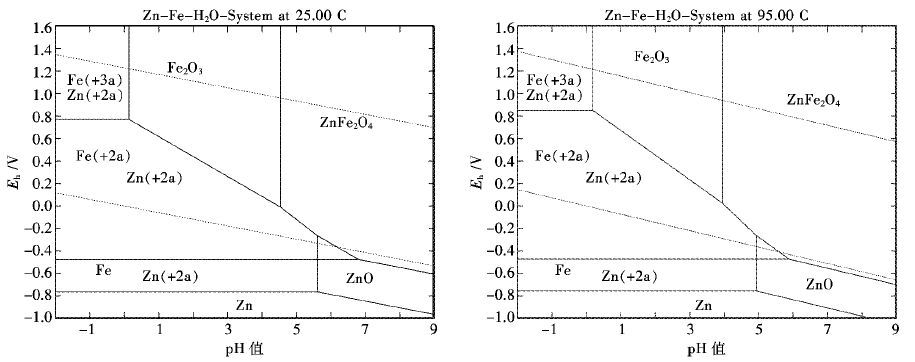 |
| 图 9 ZnFe2O4-H2O系不同温度下电位-pH图(HSC5.0) Fig. 9 The Eh-pH diagram of ZnFe2O4-H2O system at different temperatures |
图 10为不同浸出时间下中浸渣还原浸出渣XRD衍射图,从图 10中可以看出,浸出30 min后,未检测出锌的硫酸盐、氧化物及硅酸盐等易溶态及硫化物的特征峰,而主要是铁酸锌衍射峰,表明浸出初始阶段主要是锌易溶态及硫化物溶出.随着浸出时间延长,渣中铁酸锌衍射特征峰峰强逐渐减弱,峰型逐渐变宽,直至浸出120 min后铁酸锌衍射特征峰基本消失,表明在该条件下,浸出120 min后铁酸锌即可被大部分浸出.渣中硫酸铅衍射峰逐渐增强,同时浸出过程中生成了硫酸锌肼的复盐((N2H5)2Zn(SO4)2),这解释了当硫酸肼浓度增加到33.3 g/L以后,进一步增加硫酸肼浓度,锌浸出率反而稍有下降,因此要控制硫酸肼的添加量.
浸出过程中,新物相的生成很可能包裹在颗粒表面,导致颗粒与浸出剂接触面积减小,不利于浸出的进行.图 11为中浸渣浸出渣的SEM-EDS图,图 11中所示颗粒(a)经能谱分析主要成分为PbSO4及少量含硅杂质,颗粒(b)经能谱鉴定,其主要含有Zn、Si、Cu、Fe以及Pb等元素,为多物相的团聚颗粒,无疑增加了浸出难度,因此渣在浸出前必须进行磨样处理,使浸取物裸露,与浸提剂充分接触.
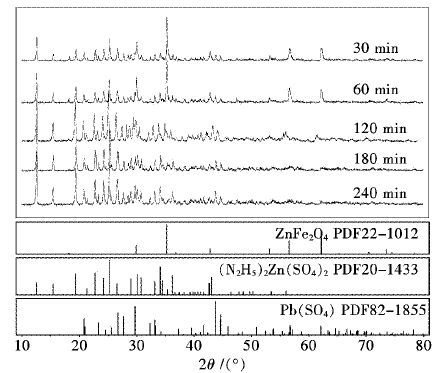 |
| 图 10 不同浸出时间下中浸渣还原浸出渣XRD衍射图 Fig. 10 The XRD pattern of residue leached at different time |
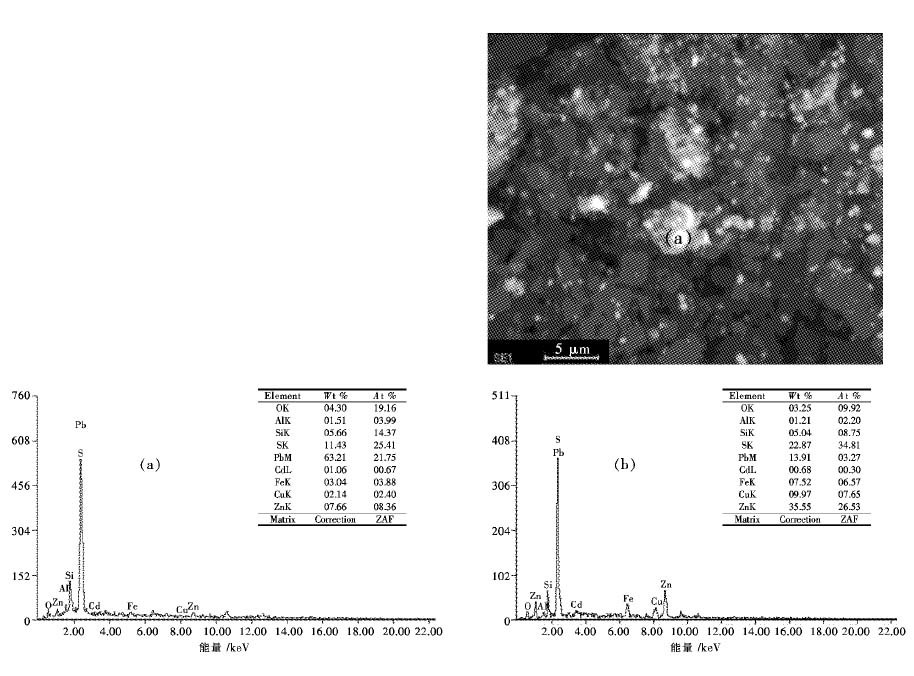 |
| 图 11 中浸渣浸出渣SEM-EDS图 Fig. 11 SEM-EDS analyses of leaching residue from zinc neutral leaching residue |
3 结论
1) 通过对比不同类型还原剂对中浸渣中铁酸锌浸出效果,筛选出硫酸肼作为还原强化浸出中浸渣的还原剂.研究了硫酸肼浓度、浸出时间、硫酸浓度、温度及液固比等因素对浸出效率影响.通过添加还原剂硫酸肼,实现渣中铁酸锌能在较低酸度条件下浸出.
2) 通过单因素试验优化获得了最佳的工艺参数.中浸渣在初始硫酸浓度80 g/L,硫酸肼浓度33.3 g/L,温度95℃,液固比10 mL/g及400 r/min条件下浸出120 min,锌和铁的浸出率分别达到了95.83 %和94.19 %.
3) 渣中锌的硫酸盐、氧化物以及硅酸盐等易溶态容易被浸出,反应初始阶段就被溶出;铁酸锌浸出比较缓慢,在反应120 min后大部分被溶出,浸出渣中主要存在物相为硫酸铅(PbSO4)和硫酸锌肼复盐((N2H5)2Zn(SO4)2).因此要控制硫酸肼的添加量.
| [1] | 蒋继穆. 我国铅锌冶炼现状与持续发展[J]. 中国有色金属学报, 2004, 14(F1): 52–62. |
| [2] | 何静, 罗超, 唐谟堂, 等. 采用铅黄铁矾去除硫酸体系中的铁[J]. 中国有色金属学报, 2012(10): 2890–2895. |
| [3] | 阙绍娟. 高铁锌焙砂浸出试验研究[D].南宁:广西大学矿物加工工程, 2010. |
| [4] | 施友富, 蒋开喜, 王海北. 采用加压浸出工艺优化传统湿法炼锌流程研究[J]. 有色金属(冶炼部分), 2012(5): 11–14. |
| [5] | 彭海良. 常规湿法炼锌中铁酸锌的行为研究[J]. 湖南有色金属, 2004(5): 20–22. |
| [6] | 柴立元, 李青竹, 李密, 等. 锌冶炼污染物减排与治理技术及理论基础研究进展[J]. 有色金属科学与工程, 2013, 4(4): 1–10. |
| [7] | 王福生, 车欣. 浸锌渣综合利用现状及发展趋势[J]. 天津化工, 2010, 24(3): 1–3. |
| [8] | 张向阳, 王吉坤, 巨佳, 等. 氧压酸浸处理锌焙砂中浸渣的新工艺研究[J]. 中国材料进展, 2012, 31(8): 52–56. |
| [9] | 周廷熙, 王吉坤. 高铁硫化锌精矿冶炼工艺研究进展[J]. 中国有色冶金, 2006, 35(1): 13–17. |
| [10] | 孙德堃. 国内外锌冶炼技术的新进展[J]. 中国有色冶金, 2004, 33(3): 1–4. |
| [11] | 谢冰. 湿法炼锌工艺过程除铁技术的发展[J]. 矿冶工程, 2012, 32(2): 100–102. |
| [12] | 张凡, 马启坤, 刘韬. 中浸渣的机械活化浸出工艺研究[J]. 云南冶金, 2002, 31(4): 33–37. |
| [13] | Yao J,Li X, Pan L, et al. Kinetics of leaching zinc and indium from indium-bearing zinc ferrite mechanically activated by tumbling mill[Z]. Society for Mining, Metallurgy,and Exploration, Inc, 2013:30, 45. |
| [14] |
Zhang L, Mo J, Li X, et al. A Kinetic Study of Indium Leaching from Indium-Bearing Zinc Ferrite Under Microwave Heating[J].
Metallurgical and Materials Transactions B-Process Metallurgy and Materials Processing Science, 2013, 44(6): 1329–1336. DOI: 10.1007/s11663-013-9930-9. |
| [15] |
Xin W, Srinivasakannan C, Xin-hui D, et al. Leaching kinetics of zinc residues augmented with ultrasound[J].
Separation and Purification Technology, 2013, 115: 66–72. DOI: 10.1016/j.seppur.2013.04.043. |
| [16] | 彭建蓉, 王吉坤, 杨大锦, 等. 高铟高铁硫化锌精矿加压浸出溶液铁的还原研究[J]. 有色金属(冶炼部分), 2007(4): 2–4. |
| [17] |
Langová Š, Leško J, Matsek D. Selective leaching of zinc from zinc ferrite with hydrochloric acid[J].
Hydrometallurgy, 1995(3/4): 179–182. |
| [18] |
Wu X, Wu S, Qin W, et al. Reductive leaching of gallium from zinc residue[J].
Hydrometallurgy, 2012, 113/114: 195–199. DOI: 10.1016/j.hydromet.2011.11.016. |
 2016, Vol. 6
2016, Vol. 6


