| 高砷碱式碳酸铜硫酸浸出研究 |
2011年,我国有色金属工业“十二五”科技发展规划中,已将有色金属资源循环与再生金属回收利用技术列为重大专项,其中铜的二次资源回收受到重点关注.在铜的冶金过程中会产生大量的铜砷二次资源,如铜火法冶炼时会产出含铜砷渣和铜冶炼烟灰;铜电解精炼时,产出黑铜泥;硫化钠沉淀铜冶炼废水后产出硫化砷渣.国内外冶金科研工作者对铜砷二次资源的回收,进行了大量研究.冯泽民[1]对含铜砷渣制备砷酸铜进行了研究,含铜砷渣经硫酸浸出、萃取除铁、氧化、沉淀,得到砷酸铜,产品符合新西兰标准.刘启武[2]对黑铜泥制备砷酸铜进行了研究,黑铜泥分别经硫酸浸出铜砷,氢氧化钠浸出砷后,将所得酸浸液和碱浸液混合,制备出砷酸铜.目前,随着环保要求的日益严格,将减少砷酸铜作为木材防腐剂的使用,因此,需要考虑以其他形式将铜砷回收.唐仁衡[3]发现黑铜泥经通氧碱浸、苛化、酸分解、还原结晶后,可以制备纯度99.6 %的As2O3.但是工艺流程复杂.蒋开喜等[4]对硫化砷渣进行加压硫酸氧浸,铜砷铼浸出率均达到95 %以上,浸出液经SO2还原、冷却结晶后得到粗As2O3,粗As2O3经重溶精制后得到纯As2O3;SO2还原后液经萃取提铼后,萃余液蒸发结晶回收硫酸铜.该流程虽能实现硫化砷渣的综合回收,但工艺流程过长.郑雅杰等[5]对硫化砷渣采用碱浸、氧化脱硫、二氧化硫还原制备As2O3.该流程碱无法再生,工业上成本较高.董四禄[6]对硫化砷渣采用常压硫酸高铁浸出,硫化砷渣经2段浸出后,浸出液经SO2还原、冷冻结晶,可制备高纯度的As2O3;浸渣采用盐酸浸出,铁粉置换,制备纯度96.60 %的海绵铋.但该法流程长,需要定期补充硫酸高铁.欧阳辉[7]采用硫酸铜置换法,硫化砷渣经硫酸铜置换、氧化、还原结晶、铜浸出,可制得纯度大于99.5 %的As2O3.但该法工艺流程长.硫化砷渣的回收方法还有氯化铜焙烧法、碱焙烧法、硝酸浸出法、砷酸浸出法、三氧化二砷溶解度法[4].上述方法均存在着有价成分浸出率低,经济上不合理,因此,无法大规模推广.李利丽[8]对铜冶炼烟灰中有价成分综合回收进行了研究,铜冶炼烟灰采用两段水浸法,浸出铜锌铟镉砷,铅铋留在浸出渣中,浸出液采用置换法,生产海绵铜、海绵镉、海绵铟、七水硫酸锌,浸出渣采用鼓风炉还原熔炼,生产1#电解铅、1#精铋和贫冰铜.但该法流程复杂,返料多,工业上应用困难.郝士涛[9]对铜冶炼烟灰中有价成分综合回收进行了研究,铜冶炼烟灰经苛性钠和硫化钠体系常温浸出脱砷,浸渣经两级逆流通氧酸浸后,铜浸出率94.66 %,锌浸出率99.06 %.该法回收流程较长.罗毛遂[10]对铜冶炼烟灰中有价成分综合回收进行了研究,铜冶炼烟灰经还原焙烧、硫酸浸出后,焙烧渣可作为炼铜原料,浸出渣可作为铅铋回收原料.但该法未对其他有价成分进行回收.曹应科[11]对铜冶炼烟灰中锌的回收进行了研究,铜冶炼烟灰采用硫酸化焙烧、水浸,可制备七水硫酸锌.但是该法易造成有价成分砷的分散,不利于砷的回收.铜冶炼烟灰的回收方法除上述方法外,还有稀酸浸出-还原熔炼法、浸出-萃取法、浸出-碳铵转化法[9].但上述方法都无法对铜冶炼烟灰中有价成分进行综合回收.
该高砷粗碱式碳酸铜是某公司以碱式碳酸铜作为铜电解液的沉砷剂,从铜电解液中净化脱砷后,得到的高砷粗碱式碳酸铜.高砷碱式碳酸铜中含有无机剧毒物质亚砷酸铜、无机有毒物质砷酸铜.亚砷酸铜会对人体肝肾造成伤害,严重可致死,并对环境造成污染.砷酸铜是一种无机有毒物质,损害人体肝脏,严重可致肝癌,同时造成土壤污染[12-15].砷酸铜的用途是作为木材防腐剂使用[16-17].高砷碱式碳酸铜的堆存,占用工业用地,造成土地资源浪费,其含有的重金属在土壤中迁移,造成土壤污染.目前,对该铜砷二次资源,工业上采取低价出售的方式,造成企业经济上一定的损失.对该废料中有价成分进行回收,一方面消除废料堆存带来的环境污染,另一方面达到变废为宝的目的,增加企业效益.
前期探索实验采用NaOH浸出高砷碱式碳酸铜,希望浸出砷的同时,铜留在渣中,实验结果是砷浸出率非常不理想,由于物料中存在着钙,钙和砷酸根离子会生成砷酸钙沉淀,导致砷无法有效浸出;探索实验继续改用氨水浸出,希望络合浸出铜,但实验结果很不理想,铜砷都无法有效浸出.采用HCl或HNO3浸出时,物料中含有大量杂质元素钙,大量消耗浸出剂HCl和HNO3,恶化操作环境,也会给后续处理增加困难.因此,综合考虑,确定采用硫酸浸出.由于碱式碳酸铜中含有Cl-,浸出铜砷的同时可以抑止银的浸出,银保留在酸浸渣中,达到有价成分铜砷和银分离的目的.以搅拌速度、硫酸浓度、反应时间、反应温度、液固比作为考察因素,考察对铜、砷浸出率的影响.
1 实验 1.1 原料碱式碳酸铜在105 ℃下干燥4 h后,细磨至≤0.074 mm,碱式碳酸铜主要元素含量如表 1所示,XRD物相分析结果如图 1所示.
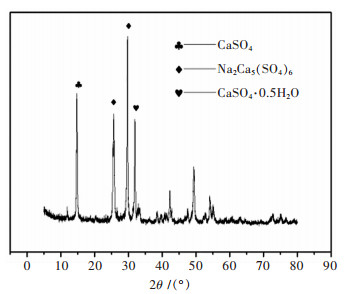 |
| 图 1 原料XRD谱 Fig. 1 XRD pattern of raw material |
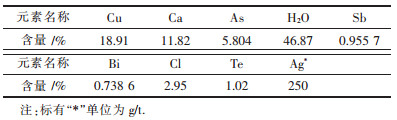
| 表1 碱式碳酸铜化学成分 Table 1 Chemical analysis of basic copper carbonate |
 |
| 点击放大 |
粗碱式碳酸铜中铜可能以碱式碳酸铜、砷酸铜和亚砷酸铜形式存在,砷可能以砷酸铜和亚砷酸铜形式存在,铋可能以氯氧铋形式存在.碱式碳酸铜中铜含量为18.91 %,银含量为200 g/t,该二次资源具有良好的回收价值.XRD分析数据表明该原料主要是由硫酸钙组成,这可能是由于铜化合物以无定形态存在,导致衍射峰被硫酸钙的衍射峰掩盖.
主要试剂有硫酸(分析纯),超纯水.
1.2 仪器设备试验仪器设备有:DF-I集热式磁力加热搅拌器(金坛市荣华仪器制造有限公司);JHS-2/60恒速数显搅拌机(杭州仪表电机有限公司);DZF-6050型真空干燥箱(上海精宏实验设备有限公司);SHZ-D(III)循环水式真空泵(杭州瑞佳精密科学仪器有限公司).
1.3 实验方法及流程高砷碱式碳酸铜的酸浸实验在1 L烧杯中进行.将一定体积并配好浓度的稀硫酸倒入烧杯,放置在恒温水浴箱中,升温加热,待恒温水浴箱加热至设定温度后,将称量好的物料,加入到烧杯中,开始以设定的速度搅拌,同时开始计时,反应至设定的时间后,用抽滤装置抽滤分离固液.滤渣用少量蒸馏水洗涤3次后,洗水转入浸出液,将滤渣放置烘箱中,在105 ℃下干燥4 h后称重;浸出液稀释后分析铜砷含量,计算Cu、As的浸出率.
1.4 分析方法铜砷的分析均采用ICP-MS仪器分析.
2 实验结果与讨论 2.1 基本原理 |
| 图 2 Cu-As-H2O系电位-pH图 Fig. 2 Potential-pH diagram of Cu-As-H2O system |
由图 2可知,在较高的电位下,-1<pH<2.6时,铜和砷分别以Cu2+和H3AsO4形式进入溶液.7.1<pH<11.6时,铜以CuO形式留在渣中,砷以HAsO42-或AsO43-形式进入溶液.因此,可以采用酸同时浸出铜砷,或用碱浸出砷,铜留在渣中,达到分离铜砷的目的.
物质在酸性条件下,浸出的难易可用标准平衡状态下的pHΘ表示,以Cu3(AsO4)2形式[19]存在的砷酸铜在25 ℃下的pHΘ为1.918,100 ℃下的pHΘ为1.32,这说明砷酸铜在高温高酸下易于浸出,反应需要在高温高酸度条件下进行.
浸出时主要发生的反应为:
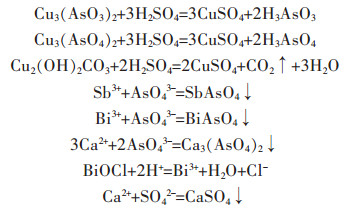
|
浸出条件为:物料用量50 g,在硫酸用量1 mol/L、反应时间1.5 h、反应温度60 ℃、液固比6:1(硫酸体积与物料质量之比,单位为mL/g,下同)的条件下,考察搅拌速度对铜砷浸出率的影响,结果如图 3所示.
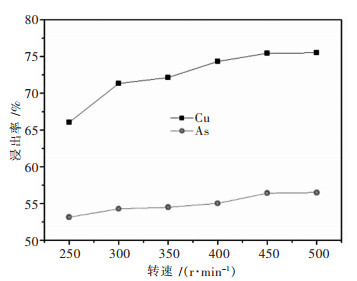 |
| 图 3 转速对铜砷浸出率的影响 Fig. 3 Effect of stirring speed on copper and arsenic extraction |
由图 3可知,转速的变化对铜浸出率和砷浸出率影响类似.铜砷浸出率随着转速的增大而明显增加,转速由250 r/min增加到450 r/min时,铜浸出率由66.02 %增加到75.45 %,砷浸出率由53.14 %缓慢地增加到56.41 %;继续增大转速,铜砷浸出率增幅不大.这是由于转速过低时,硫酸同物料颗粒两相间接触面积较小,会导致浸出反应的不完全,因而铜砷浸出率稍低;继续增大转速,两相间接触面积增大,反应进行的比较完全,相应的增大铜砷浸出率.搅拌速度达到一定后,进一步增大转速,浸出率的增加不明显,这是由于转速增加到一定程度后,扩散层厚度将不会减小,即不能进一步的增加浸出率.由于转速过低不能有效浸出铜砷,转速增加又会增加能耗,综合考虑,合适的转速为400 r/min.
2.3 硫酸浓度对铜砷浸出率的影响浸出条件为:物料用量50 g,在反应时间为2 h、液固比6:1、反应温度70 ℃、转速400 r/min的条件下,考察硫酸浓度对铜砷浸出率的影响.结果如图 4所示.
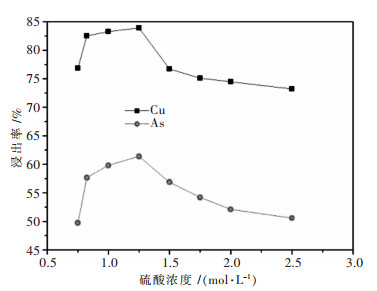 |
| 图 4 硫酸浓度对铜砷浸出率的影响 Fig. 4 Effect of concentration of sulfuric acid on copper and arsenic extraction |
由图 4可知,随着硫酸浓度增大,铜砷浸出率也随之明显增大.硫酸浓度由0.75 mol/L变化到1.25 mol/L时,铜浸出率由76.87 %增加到83.90 %,砷浸出率由49.74 %增加到61.38 %.继续增大浓度,铜砷浸出率反而有所下降.硫酸浓度由1.25 mol/L增加到2.5 mol/L时,铜浸出率由83.90 %减小到73.22 %,砷浸出率由61.38 %减小到50.57 %.硫酸浓度增大,理论上铜砷浸出率都应增加,但在实验中,随着硫酸浓度增大,铜砷浸出率反而降低,这可能是由于生成物中含有硫酸钙,硫酸钙存在着如下所示的电离平衡:
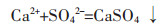
|
硫酸浓度较低时,生成的硫酸钙沉淀不足于形成固体产物膜包裹原料颗粒;继续增大硫酸浓度时,平衡向右移动,生成的硫酸钙沉淀增多,硫酸钙会形成固体产物膜包裹原料颗粒,阻止浸出反应的继续进行,宏观表现为铜砷浸出率都下降;硫酸浓度增大时,同时增大溶液的黏度,导致过滤困难,经济上增加成本.综合考虑,合适的硫酸浓度为1 mol/L.
2.4 反应时间对铜砷浸出率的影响浸出条件为:物料用量50 g,在硫酸浓度1 mol/L、液固比6:1、反应温度70 ℃、转速400 r/min的条件下,考察浸出时间对铜砷浸出率的影响,结果如图 5所示.
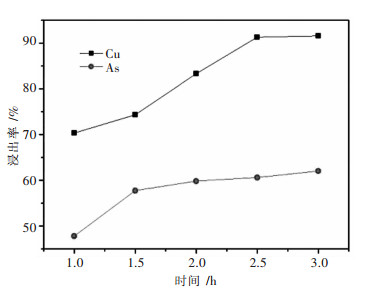 |
| 图 5 反应时间对铜砷浸出率的影响 Fig. 5 Effect of reaction time on copper and arsenic extraction |
由图 5可知,在一定的反应条件下,随着反应时间的提高,铜砷浸出率升高.反应时间由1 h增加到2.5 h时,铜浸出率由70.35 %迅速增加到91.30 %,砷浸出率由47.78 %迅速增加到60.58 %.继续增加反应时间,铜砷浸出率增幅不大,说明铜砷的浸出反应已达平衡.由于反应时间过长,将会延长生产周期,反应时间过短,将会降低金属的浸出率,因此,合适的浸出时间为2.5 h.
2.5 反应温度对铜砷浸出率的影响浸出条件为:物料用量50 g,在硫酸浓度1 mol/L、液固比6:1、反应时间1.5 h、转速400 r/min的条件下,考察反应温度对铜砷浸出率的影响,结果如图 6所示.
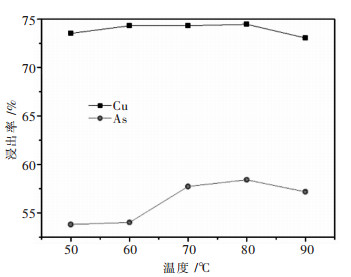 |
| 图 6 反应温度对铜砷浸出率的影响 Fig. 6 Effect of reaction temperature on copper and arsenic extraction |
由图 6可知,铜浸出率随温度变化并不明显,温度由50 ℃增大到80 ℃时,铜浸出率由73.52 %增加到74.46 %,继续增大温度,铜浸出率略微下降.砷浸出率随温度的增加而增加,温度由60 ℃增加到80 ℃时,砷浸出率由54.01 %增加到58.41 %,继续增加温度,砷浸出率略微下降.高温下,铜砷浸出率略微下降,这是由于温度过高时,溶液蒸发过快,导致铜砷浸出率下降.综合考虑能耗和溶液蒸发,合适的反应温度取为60 ℃.
2.6 液固比对铜砷浸出率的影响浸出条件为:物料用量50 g,在硫酸浓度1 mol/L、浸出温度60 ℃、浸出时间1.5 h、转速400 r/min的条件下,考察液固比对铜砷浸出率的影响.结果如图 7所示.
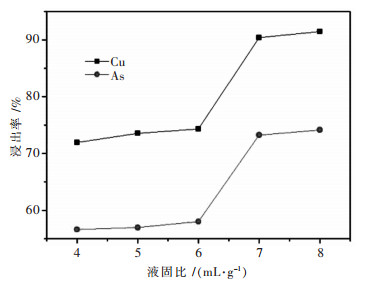 |
| 图 7 液固比对铜砷浸出率的影响 Fig. 7 Effect of liquid-to-solid ratio on copper and arsenic extraction |
由图 7可知,液固比由4增加到6时,铜砷浸出率增幅不大,当液固比由6增加到7时,铜砷浸出率急剧的增加,铜浸出率由74.31 %增加到90.4 %,砷浸出率由58.01 %急剧增加到73.25 %.继续增大液固比,铜砷浸出率变化不大.这是因为液固比较小的时候,会造成溶液黏度过大,不利于传质过程的进行,因而导致铜砷浸出率较小,随着液固比增大,溶液黏度降低,有利于传质过程的进行,从而使铜砷浸出率均增大.由于增大液固比,硫酸用量增加,废水量也增大,增加后续工艺处理浸出液的难度.因此,合适的液固比取为7:1.
2.7 浸出液和浸渣成分分析高砷碱式碳酸铜经硫酸浸出后,浸出液主要化学成分如表 2所示.
| 表2 浸出液化学成分 Table 2 Chemical analysis of leachate |
 |
| 点击放大 |
浸出液可以采用SO2还原浸出液中的As,制备As2O3,除As后的溶液可以送至铜电解工序进行电解回收铜[20-21].
浸出渣主要化学成分如表 3所示,浸出渣的XRD图谱如图 8所示.
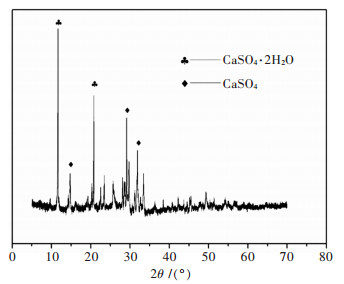 |
| 图 8 硫酸浸渣XRD谱 Fig. 8 XRD pattern of leach residue |
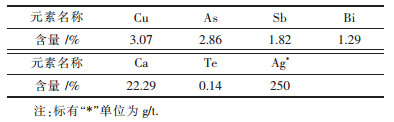
| 表3 浸出渣化学成分 Table 3 Chemical analysis of leach residue |
 |
| 点击放大 |
浸出渣XRD图谱表明浸出渣的主要成分是硫酸钙.浸渣中银含量250 g/t,银富集了1.25倍,目前工业上认为含Ag 100~120 g/t原矿便具有工业开采价值,浸出渣中银含量是工业开采量的2倍,具有一定回收价值,因此,浸出渣可作为提银原料.
3 结论实验以硫酸作为浸出剂,浸出高砷碱式碳酸铜中的铜和砷,银留在酸浸渣中,银富集了1.25倍.最佳浸出条件为:反应温度60 ℃、反应时间2.5 h、硫酸浓度1 mol/L、液固比7:1、转速400 r/min.在较佳条件下,铜浸出率91.50 %,砷浸出率74.15 %.
| [1] | 冯泽民.含铜砷渣制备砷酸铜工艺研究[D].兰州:兰州大学, 2009. http://cdmd.cnki.com.cn/Article/CDMD-10730-2010016720.htm |
| [2] | 刘启武.黑铜泥综合利用技术研究[D].兰州:兰州理工大学, 2011. http://cdmd.cnki.com.cn/Article/CDMD-10731-1011133663.htm |
| [3] | 唐仁衡.由黑铜泥制备砷酸铜工艺及理论研究[D].长沙:中南工业大学, 2000. |
| [4] | 蒋开喜, 王海北, 王玉芳, 等. 铜冶炼过程中硫化砷渣综合利用技术[J]. 有色金属科学与工程, 2014, 5(5): 13–17. |
| [5] | 郑雅杰, 刘万宇, 白猛, 等. 采用硫化砷渣制备三氧化二砷工艺[J]. 中南大学学报(自然科学版), 2008(6): 1157–1163. |
| [6] | 董四禄. 湿法处理硫化砷渣研究[J]. 硫酸工业, 1994(5): 3–8. |
| [7] | 欧阳辉. 贵溪冶炼厂亚砷酸工艺综述[J]. 有色金属(冶炼部分), 1999(4): 10–12. |
| [8] | 李利丽. 铜冶炼高砷烟灰综合处理流程研究[J]. 中国金属通报, 2011, 19: 42–43. |
| [9] | 郝士涛.铜冶炼烟灰碱浸脱砷预处理及有价金属综合回收[D].赣州:江西理工大学, 2012. http://cdmd.cnki.com.cn/Article/CDMD-10407-1012506981.htm |
| [10] | 罗毛遂. 沈冶铜烟灰处理方法的探讨[J]. 有色科技, 1989(3): 1–29. |
| [11] | 曹应科. 从铜冶炼砷烟灰中回收铟[J]. 湖南有色金属, 2005(1): 5–8. |
| [12] |
Tony S S, Pant K K. Solidification/stabilization of arsenic containing solid waste using portland cement, fly ash and polymeric materials[J].
Journal of Hazardous Materials, 2005, 122(2): 123–131. |
| [13] |
Leist M, Casey R J, Caridi D. Management of arsenic:Problems and prospects[J].
Journal of Hazardous Materials, 2000(B76): 125–138. |
| [14] |
Palfy P, Vircikova E, Molnar L. Processing of arsenic waste by precipitation and solidification[J].
Waste Management, 1999(19): 55–59. |
| [15] |
Tang M T. The arsenic harm and protection measurement in nonferrous industry in China[J].
Hunan Nonferrous Metals (in Chinese), 1989, 5(2): 42–44. |
| [16] |
Emile H, Hashmonai D, Yosef E, et al. Suicide by ingestion of a CCA wood preservative 11 selected topics:Toxicology is coordinated by Kenneth Kulig, MD, of Denver, Colorado[J].
Journal of Emergency Medicine, 2000, 19(2): 159–163. DOI: 10.1016/S0736-4679(00)00202-X. |
| [17] |
Robert M L. An alternative to arsenic disposal :Wood preservation[J].
The Journeal of The Minerals, Metals & Materials society, 1999, 51(9): 34. |
| [18] | 谢海云.高砷硫化铜精矿细菌浸出及砷的综合利用工艺及理论研究[D].昆明:昆明理工大学, 2008. http://cdmd.cnki.com.cn/Article/CDMD-10674-2008112616.htm |
| [19] | 钟竹前, 梅光贵. 化学位图在湿法冶金和废水净化中的应用[M]. 长沙: 中南工业大学出版社 , 1986. |
| [20] | 周文科. SO2还原法净化铜电解液工艺研究[D].长沙:中南大学, 2011. |
| [21] | 崔涛.高砷脱铜电解液的净化与回用研究[D].长沙:中南大学, 2012. http://cdmd.cnki.com.cn/Article/CDMD-10533-1012477211.htm |
 2015, Vol. 6
2015, Vol. 6


