| 钨钼混配型杂多酸盐催化剂上酯化反应条件的优化研究 |
乙酸正丁酯是一种用途广泛的重要化工原料,因具有扩散性能好的特点而常用于食用香精中;与醇、酮、酯等大多数常用的有机溶剂均具有良好的溶解性能,是一种性能优良的有机溶剂;与塑料、橡胶均具有较好的相容性,可作为增塑剂.除此之外,在涂料、食品、医药和印染等行业也具有重要的使用价值.因此,其在国内外都存在着巨大的市场需求[1-6].迄今为止,合成乙酸正丁酯所使用的催化剂主要是浓硫酸,这主要是因为浓硫酸具有以下优势:能以分子的形态参与化学反应,保证了催化剂与反应液的充分接触,有利于反应的进行;催化活性高,可使反应在低温下有效进行.然而,以浓硫酸作为通过酯化反应合成乙酸正丁酯的催化剂,仍然存在着一些问题:如催化选择性较差,副产品多;生产过程中产生了较多的工业三废,容易污染环境;对设备带来了较为严重的腐蚀问题,需定期对设备进行检修和维护;容易与原料和产物形成均相体系,后处理繁杂;工艺上采用的是间歇反应过程,不利于实现连续化生产要求.
近年来,随着人们的环保意识的提高,以及环保立法的要求不断增强,开发和研究环境友好型催化剂来代替浓硫酸已经成为了必然趋势.其中,具有催化效果好、催化稳定性高、易分离、无污染和可循环使用等优势的固体酸也成为了研究的热点[7-10].杂多酸是一种具有广泛应用前景的绿色固体酸催化剂,其通常是由杂原子(如Si、P、Co、Fe)和多原子(如W、Mo、V、Ta、Nb)按一定的结构通过氧原子配位桥联组成的一类含氧多酸.目前,已报道的可用于催化酯化反应的杂多酸催化剂主要有硅钨酸(H4SiW12O40)、磷钨酸(H3PW12O40)、硅钼酸(H4SiMo12O40)和磷钼酸(H3PMo12O40)[11-15].但是,杂多酸是一种强Brönsted酸催化剂,极易溶解在极性溶剂中,形成均匀的液相反应体系,这对其的分离与回收带来了困难.另外,其比表面积较小( < 10 m2/g),因而限制了它的实际应用.相比于杂多酸,杂多酸盐具有较大的表面积(50~200 m2/g),不溶于水,易从反应液中分离循环使用,且其比表面积和酸性可通过改变金属阳离子与杂多阴离子的比例和类型来进行调节.因此,杂多酸盐已经引起了研究者的广泛关注.并且,也有研究报道了其在应用于催化酯化反应时,具有较好的催化性能[16-19].
本研究采用硝酸酸化与乙醚萃取法相结合的方式,合成了一种钨钼混配型杂多酸盐催化剂(Na4SiMoW12O40·xH2O),并以正丁醇和乙酸为反应物,研究了所制备的钨钼混配型杂多酸盐在催化酯化反应时的活性和稳定性.通过正交试验[L9(3)4]对影响乙酸正丁酯收率的关键影响参数进行了优化,包括催化剂与反应物的质量比,反应时间和温度,以及正丁醇与乙酸的摩尔比.
1 实验 1.1 试剂实验所用试剂:正丁醇(CH3(CH2)3OH, 分析纯, ≥99.5 %),乙酸(CH3COOH, 99.5 %),钨酸钠(Na2WO4·2H2O, 分析纯)和钼酸钠(Na2MoO4·2H2O,分析纯),硅酸钠(Na2SiO3·9H2O,分析纯, 99.5 %),乙醚((C2H5)2O,分析纯),硝酸(HNO3,分析纯)和氢氧化钠(NaOH,分析纯),无色酚酞溶液,实验用水均为蒸馏水.
1.2 仪器与测试在PW2424型X射线荧光分析仪(荷兰帕纳科公司)上进行了所合成的钨钼混配型杂多酸盐催化剂样品的元素分析.通过STA409 C/3/F型热重及差热分析仪(德国NETZSCH公司),对催化剂样品的热重(TGA)曲线进行了测定,测试时所使用的气氛为氮气;通过Nicolet 6700型傅立叶变换红外光谱仪,对催化剂样品的红外光谱(FTIR)图进行了测定.
1.3 钨钼混配型杂多酸盐的制备钨钼混配型杂多酸盐的制备过程如下:①分别将8.248 gNa2WO4·2H2O和6.047 gNa2MoO4·2H2O溶于250 mL蒸馏水中,均配成0.1 mol/L的溶液.然后:按照体积比为12:1的比例,将以上2种配好的溶液倒入烧杯,并在烧杯中加入Na2SiO3·9H2O,搅拌使之溶解,用H2SO4调整溶液pH值为3,于敞口容器中煮沸1 h,通过分液漏斗向混合液中逐滴加入HNO3,直至无沉淀生成为止,停止加热;②将混合液倒入布氏漏斗中,趁热对其抽滤,而实现沉淀物的分离.待滤液冷却至室温后,倾入分液漏斗中,并加入大量的乙醚洗涤,直至有醚合物生成;③分出下层醚合物,并于44~55 ℃水中除净乙醚,静置3 d,直至有淡黄色晶体析出.将产品放入恒温干燥箱烘干,即得产品钨钼混配型杂多酸盐催化剂(Na4SiMoW12O40·xH2O),其制备原理如反应方程式(1)所示:
| $ \text{SiO}_{\text{3}}^{\text{2-}}\text{+12WO}_{\text{4}}^{\text{2-}}\text{+MnO}_{\text{4}}^{\text{2-}}\text{+3O}{{\text{H}}^{\text{+}}}\to \text{SiMo}{{\text{W}}_{\text{12}}}\text{O}_{\text{40}}^{\text{4-}}\text{+15}{{\text{H}}_{\text{2}}}\text{O} $ | (1) |
在一套自搭的低温常压实验装置中,对钨钼混配型杂多酸盐催化乙酸与正丁醇酯化反应的性能进行了研究.反应过程如下:在已连接好机械搅拌装置、冷凝回流管和温度计的250 mL三口烧瓶中,按照既定的比例先加入反应物乙酸和正丁醇,开始加热.待加热至所预先设定的反应温度后,再加入混配型杂多酸盐催化剂,开始搅拌和反应计时.反应条件如下:反应温度(50~100 ℃)、催化剂/反应物质量比为(0.1 wt%~4.0 wt%)和反应时间(30~180 min)、正丁醇与乙酸摩尔比(0.5:1~4:1).酯化反应转化率分析过程如下:在固定的时间间隔内,连续取样分析,并根据分析的结果来计算乙酸的酸值而确定其转化率.
基于国标GB/T5530-2005中所介绍的方法,对反应物的酸值进行了测定.测定过程如下:首先,准确称取1 g已经过预处理后的样品,注入锥形瓶中.然后,按照体积比为1:1的方式在锥形瓶中加入10 mL乙醚-乙醇混合液.最后,通过0.1 mol/L KOH标准溶液对样品进行滴定,以酚酞为指示剂来确定滴定的终点.另外,考虑到乙醚-乙醇混合液将会消耗一部分KOH标准溶液,需要做一个空白试验,除不加样品外,其余操作同上,记录空白试验中KOH的用量,来排除乙醚-乙醇混合液的影响.除此之外,样品中还残留着一部分正丁醇,由于在常温和滴定时间很短的情况下,正丁醇与KOH几乎不发生反应,可忽略.
样品的酸值计算如式(2)所示:
| $ SV\text{=}\frac{56.1\times \left( {{V}_{2}}-{{V}_{1}} \right)\times C}{m} $ | (2) |
式(2)中:SV:酸值(mg KOH/g油脂);V1:空白试样所消耗的KOH标准溶液的体积,mL;V2:试样所消耗的KOH标准溶液的体积,mL;C:氢氧化钾浓度,0.1 mol/L;m:试样的质量,g.
通过对初始反应物的酸值及在相同反应时间间隔内所取的一系列样品的酸值进行测定,可计算得到乙酸在不同反应时间的转化率.通过对不同反应时间、反应温度、催化剂/反应物质量比、正丁醇与乙酸摩尔比的乙酸转化率进行比较分析,即可获知钨钼混配型杂多酸盐催化剂具有最佳活性的反应参数条件.乙酸转化率计算公式如式(3)所示:
| $ Y=\frac{S{{V}_{0}}-S{{V}_{\text{t}}}}{S{{V}_{0}}}\times 100% $ | (3) |
式(3)中:Y:转化率,wt%;SVO:原料乙酸的初始酸值;SVt:反应时间为t时所取样品的酸值.
2 结果与讨论 2.1 催化剂表征结果利用X射线荧光光谱分析仪对产物进行了元素分析,分析结果:Na2O、MoO3、WO3、SiO2的质量百分含量分别为20.034 0、4.458 6、52.633 0、21.956 4.由元素分析结果,经计算后可知:钨钼的摩尔比为11.804 8,可近似看作12:1,符合理论值,由此可知所合成的产品为钨钼混配型杂多酸盐催化剂(Na4SiMoW12O40·xH2O).利用傅利叶红外光谱仪对产物进行了官能团结构分析,分析结果如图 1所示.
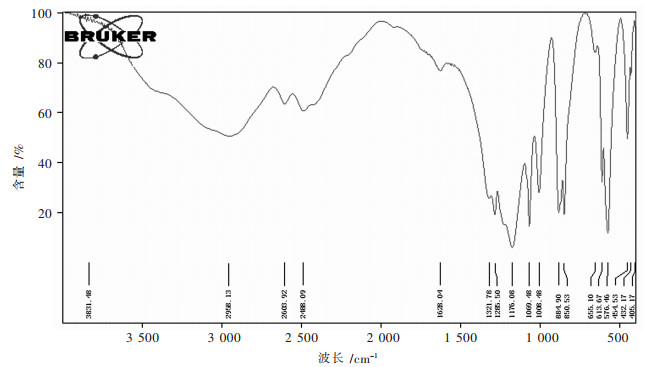 |
| 图 1 钨钼混配型杂多酸盐催化剂的红外光谱分析图 |
图 1中850 cm-1处的吸收峰对应于Mo-O-Mo键,884 cm-1处出现的特征吸收峰对应于Si-O键,1 008 cm-1处出现的特征吸收峰对应于Mo-O键,1 096 cm-1处出现的特征吸收峰对应于W-O键,1 629 cm-1处出现的特征吸收峰对应于杂多酸盐表面,由于化学吸附的水中的-OH的弯曲振动,在3 000 cm-1到3 500 cm-1之间的区域出现的宽且强的特征吸收峰,为活性位-OH的特征吸收峰,对应为Brönsted酸位.红外光谱的分析结果,进一步证明了所合成的产品为钨钼混配型杂多酸盐催化剂(Na4SiMoW12O40·xH2O).并且,由于高密度Brönsted酸位的存在,可预期该钨钼混配型杂多酸盐在催化酯化反应时,将具有高催化活性.
由于热稳定性是决定催化剂使用价值的一项重要指标.因此,利用热重分析仪对产物进行了热稳定性分析,结果如图 2所示.
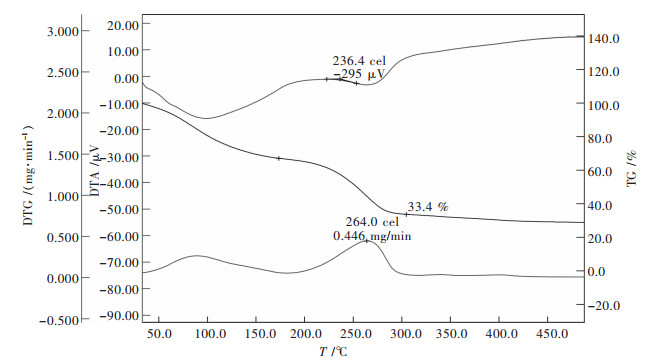 |
| 图 2 钨钼混配型杂多酸盐催化剂的热重分析图 |
通过对TG、DTA和DTG曲线进行分析,可知钨钼混配型杂多酸盐催化剂在受热时的失重过程分为2个阶段:第一阶段为30~120 ℃,该阶段所失去的是催化剂中容易脱除的吸附水及结晶水,TG曲线质量损失很大,DTA曲线出现了一个吸收峰(吸热峰),DTG曲线出现了一个失重速率峰.第二阶段为200~280 ℃,该阶段所失去的是催化剂中与杂多阴离子结合比较紧密的水,并伴随着杂多阴离子的分解.同样,DTA曲线也出现了一个吸收峰(吸热峰),DTG曲线出现了一个失重速率峰.同时,从图 2还可以看出:至300~450 ℃,催化剂不再失重,TG曲线上出现了很长的一段平台,说明所合成的钨钼混配型杂多酸盐催化剂具有较好的热稳定性.
2.2 催化活性研究结果 2.2.1 反应时间对钨钼混配型杂多酸盐催化活性的影响当乙酸与正丁醇摩尔比为2:1(乙酸加入量为0.167 mol),钨钼混配型杂多酸盐催化剂用量为0.4 g,反应温度为90 ℃时,进行了反应时间的变化对乙酸转化率大小的影响研究,结果如图 3所示.由图 3可知:催化剂的催化性能较好,能在短时间提升反应转化率.当反应时间为120 min时,乙酸转化率达到93.24 %.随着反应时间增加,转化率也随之提高,但是增加速度明显减缓.乙酸与正丁醇的酯化反应为一个可逆反应过程,当在一定反应条件下达到化学反应平衡后,即使反应时间增加,不会打破固有的动态平衡状态,也不能提高产物的产率.故当反应时间达到120 min时,酯化反应转化率基本不再增加,说明该反应已经达到平衡.由此可知:120 min为最佳反应时间.
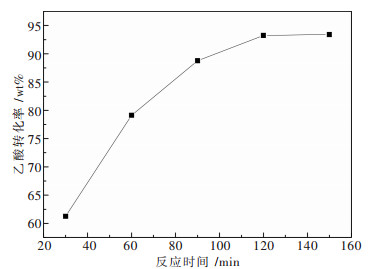 |
| 图 3 酯化率随反应时间的变化规律 |
2.2.2 反应温度对钨钼混配型杂多酸盐催化活性的影响
由于酯化反应为吸热反应过程,因而酯化程度的大小与反应温度关系密切.对不同反应温度对酯化率的影响进行了考察,反应条件如下:杂多酸用量为0.4 g,醇酸摩尔比为2:1(乙酸加入量为0.167 mol),反应时间为120 min,结果如图 4所示.由图 4可知:当反应温度在50 ℃时,乙酸转化率为58.06 %,随着反应温度的提高,转化率也随之提高,当温度到达90 ℃时,乙酸转化率高达93.24 %.进一步提高反应温度至100 ℃,这时的乙酸转化率与90 ℃的反应转化率基本相当.从节能的角度考虑,最佳反应温度为90 ℃.
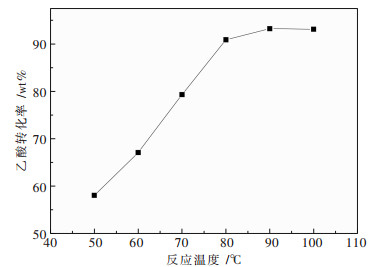 |
| 图 4 酯化率随反应温度的变化规律 |
2.2.3 催化剂用量对钨钼混配型杂多酸盐催化活性的影响
催化剂用量对催化反应活性起着非常重要的作用,考察了不同催化剂用量对酯化率的影响(0.1 %,0.5 %,1.0 %,2.0 %,4.0 %均为反应物总质量的百分比).反应条件如下:反应温度为90 ℃,反应时间为120 min,醇酸摩尔比为2:1(乙酸加入量为0.167 mol),反应结果如图 5所示.由图 5可知:当催化剂质量不高于2 %时,随着催化剂质量的增加,其酯化反应转化率也不断升高,这应该是由于随着催化剂的质量增加,其提供的活性酸中心数量也在增加,从而增加了反应物中活性酸中心浓度,在单位时间内反应物与其的有效接触增多,有利于酯化反应的进行,使酯化率提高.当催化剂质量占反应物总质量的2 %时,此时酯化率最高,达到了96.70 %.当催化剂质量继续增加到4 %时,酯化反应转化率反而下降到89.73 %,同时反应混合液的颜色由无色透明变为带略微的黄色,应该是产生了一定量的副产物导致.综合考虑,催化剂用量占反应物质量的2 %时,较为适宜.
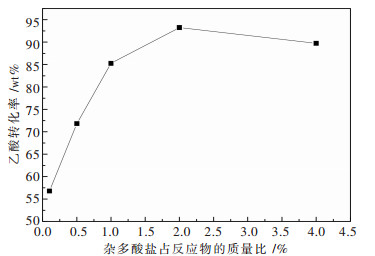 |
| 图 5 酯化率随杂多酸盐占反应物质量分数的变化规律 |
2.2.4 醇酸摩尔比对钨钼混配型杂多酸盐催化活性的影响
根据酯化反应的反应原理当醇酸摩尔比为1:1,即n(乙酸):n(正丁醇)=1:1时即可完全反应,但由于酯化反应的平衡常数比较小,若按上述比例反应,酯化反应进行得不完全.从化学平衡的角度来看,增加反应物量能使平衡向正方向进行,即增加乙酸或正丁醇的量应该均能达到此效果.分别考察了乙酸过量和正丁醇过量对酯化反应程度影响的情况.反应条件如下:杂多酸盐用量为0.4 g,反应温度为90 ℃,反应时间为120 min.实验结果如图 6所示.图 6中结果表明:在考察范围内,随着正丁醇与乙酸摩尔比从4:1下降到2:1,酯化率上升;进一步从2:1下降到1:2,酯化率下降.但是,当乙酸过量和正丁醇过量的比例相同时,正丁醇过量时的酯化反应转化率要远高于乙酸过量时的转化率,如醇酸摩尔比为2:1和1:2时的乙酸转化率分别为93.24 %和53.87 %.这可能是因为正丁醇在酯化反应中起到带水剂的作用,能及时地分离出反应产生的水,促使反应朝正方向进行,结果是酯化率提高.当乙酸过量时,随着乙酸量的增加而反应转化率降低,这可能是过量的乙酸降低了乙酸与杂多酸形成的较低活化能的中间络合物的浓度,导致不利于酯化反应的进行,结果是酯化率较低.并且,某种反应物大量过量时,催化剂的大量活性位将被该种过量的反应物占据,而不利于反应的进行.因此,最佳醇酸摩尔比为2:1.
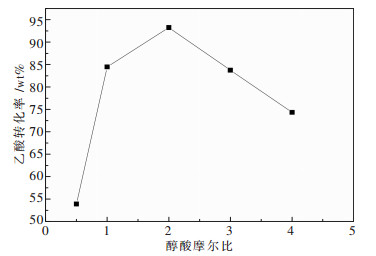 |
| 图 6 酯化率随醇酸摩尔比的变化规律 |
2.3 L9(34)正交实验结果及分析
对于多因素试验,正交试验设计是简单常用的一种试验设计方法,通过正交试验[L9(3)4]对影响乙酸正丁酯收率的关键影响参数进行了优化,包括以下4个因素:反应时间(A)和反应温度(B),钼钨混配型杂多酸盐催化剂占反应物质量分数(C),以及正丁醇与乙酸的摩尔比(D),如表 1所示.钼钨混配型杂多酸盐催化正丁醇与乙酸酯化反应的正交试验结果如表 2所示.
| 表1 正交实验选用的因素与水平 |
 |
| 点击放大 |
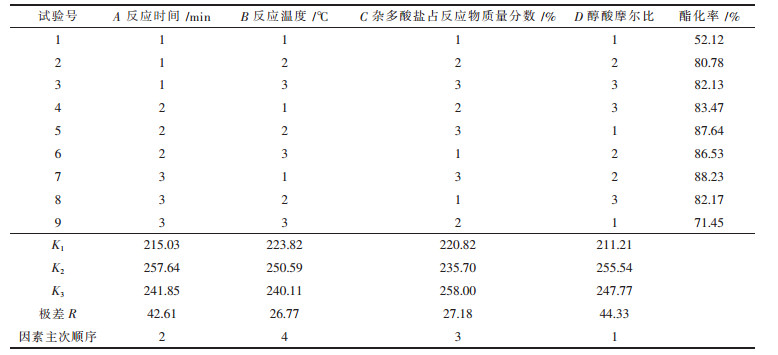
| 表2 钨钼混配型杂多酸盐催化酯化反应的正交试验结果 |
 |
| 点击放大 |
由极差数据R可见,各因素对酯化反应的影响依次为D>A>C>B,即醇酸摩尔比>反应时间>钨钼混配型杂多酸盐催化剂占反应物质量分数>反应温度,综合单因素和经济成本等方面考虑,最佳工艺条件为A2B2C2D2。
2.4 钨钼混配型杂多酸催化稳定性与再生杂多酸盐除了有催化效率高的特点,还具有重复利用的优点.因此,对钨钼混配型杂多酸盐催化乙酸和正丁醇酯化反应的稳定性进行了考察.反应条件如下:醇酸摩尔比为2:1,反应温度为90 ℃,催化剂用量为0.4 g,反应时间为120 min.在以上实验条件下连续重复反应4次.每次反应结束后,经简单过滤分离出杂多酸盐催化剂,分离出来的催化剂用无水正丁醇多次洗涤,并在烘箱中于100 ℃的条件下干燥120 min,之后再进行下一次酯化反应研究.由实验结果可知:制备出的钨钼混配型杂多酸盐催化剂对酯化反应有较好的可重复使用性.催化活性虽然逐次下降,但都能使反应转化率达到85 %以上.失活的原因可能是随着杂多酸盐催化剂的多次使用,活性组分有所丢失,导致乙酸转化率下降.
由于钨钼混配型杂多酸盐催化剂出现了活性下降的情况,而尝试通过一些方法来恢复其活性.基于对该催化剂失活原因的假设(活性组分逐渐丢失所造成),尝试将催化活性下降的钨钼混配型杂多酸盐放置于用于合成新鲜催化剂的浸渍液中重新浸渍,并通过干燥、焙烧等处理来恢复其活性.然后,将已经通过再生处理后的杂多酸盐再次应用于催化乙酸与正丁醇的酯化反应,反应条件如下:醇酸摩尔比为2:1,反应温度为90 ℃,催化剂用量为2 %,反应时间120min.反应结束后,酯化反应转化率达到92.14 %.由此可见:钨钼混配型杂多酸盐催化剂具有再生简单和可循环使用等优点,是一种理想的可用于高效催化合成乙酸正丁酯的绿色环保型催化剂.
3 结论研究制备了一种钨钼混配型杂多酸盐催化剂(Na4SiMoW12O40·xH2O),通过多种表征手段对合成的催化剂进行了分析,并通过正交试验[L9(3)4]对影响乙酸正丁酯收率的关键影响参数进行了优化.结果表明:当反应时间为120 min,反应温度为90 ℃,催化剂用量为0.4 g,醇酸摩尔比为2:1,酯化率效果最好,达到93.24 wt%.另外,合成的钨钼混配型杂多酸盐催化剂可回收并循环使用,是一种绿色环保型催化剂.
| [1] |
Tian H, Huang Z X, Qiu T, et al. Reactive distillation for producing n-butyl acetate: Experiment and simulation[J].
Chinese Journal of Chemical Engineering, 2012, 20(5): 980–987. DOI: 10.1016/S1004-9541(12)60426-1. |
| [2] |
Liu K, Tong Z F, Liu L, et al. Separation of organic compounds from water by pervaporation in the production of n-butyl acetate via esterification by reactive distillation[J].
Journal of Membrane Science, 2005, 256(1/2): 193–201. |
| [3] |
Chen L, Yin P, Hu Y C, et al. Optimization of production conditions of n-butyl acetate over NaY supported organophosphonic acid catalyst using response surface methodology[J].
Journal of the Taiwan Institute of Chemical Engineers, 2011, 42(5): 768–774. DOI: 10.1016/j.jtice.2011.02.001. |
| [4] |
He J, Xu B Y, Zhang W J, et al. Experimental study and process simulation of n-butyl acetate produced by transesterification in a catalytic distillation column[J].
Chemical Engineering and Processing:Process Intensification, 2010, 49(1): 132–137. DOI: 10.1016/j.cep.2009.12.004. |
| [5] |
Arpornwichanop A, Koomsup K, Kiatkittipong W, et al. Production of n-butyl acetate from dilute acetic acid and n-butanol using different reactive distillation systems: Economic analysis[J].
Journal of the Taiwan Institute of Chemical Engineers, 2009, 40(1): 21–28. DOI: 10.1016/j.jtice.2008.07.009. |
| [6] |
Martins A B, Graebin N G, Lorenzoni A S G, et al. Rapid and high yields of synthesis of butyl acetate catalyzed by Novozym 435: Reaction optimization by response surface methodology[J].
Process Biochemistry, 2011, 46(12): 2311–2316. DOI: 10.1016/j.procbio.2011.09.011. |
| [7] |
Song S H, Park D R, Woo S Y, et al. Direct preparation of dichloropropanol from glycerol and hydrochloric acid gas using heteropolyacid (HPA) catalyst by heterogeneous gas phase reaction[J].
Journal of Industrial and Engineering Chemistry, 2010, 16(5): 662–665. DOI: 10.1016/j.jiec.2010.05.012. |
| [8] |
Badday A S, Abdullah A Z, Lee K T. Optimization of biodiesel production process from Jatropha oil using supported heteropolyacid catalyst and assisted by ultrasonic energy[J].
Renewable Energy, 2013, 50: 427–432. DOI: 10.1016/j.renene.2012.07.013. |
| [9] |
Bashir A D, Akshya K S, Praveen P, et al. Heteropolyacid-clay nano-composite as a novel heterogeneous catalyst for the synthesis of 2, 3-dihydroquinazolinones[J].
Journal of Industrial and Engineering Chemistry, 2013, 19(2): 407–412. DOI: 10.1016/j.jiec.2012.08.027. |
| [10] |
Leng Y, Zhao P P, Zhang M J, et al. Amino functionalized bipyridine-heteropolyacid ionic hybrid: A recyclable catalyst for solvent-free oxidation of benzyl alcohol with H2O2[J].
Journal of Molecular Catalysis A: Chemical, 2012, 358: 67–72. DOI: 10.1016/j.molcata.2012.02.012. |
| [11] |
Zhao J, Guan H Y, Shi W, et al. A Brønsted-Lewis-surfactant-combined heteropolyacid as an environmental benign catalyst for esterification reaction[J].
Catalysis Communications, 2012, 20: 103–106. DOI: 10.1016/j.catcom.2012.01.014. |
| [12] |
Dilek V, Timur D, Gulsen D. Ethylene and diethyl-ether production by dehydration reaction of ethanol over different heteropolyacid catalysts[J].
Chemical Engineering Science, 2007, 62(18/19/20): 5349–5352. |
| [13] |
Choi J H, Kang T H, Song J H, et al. Redox behavior and oxidation catalysis of HnXW12O40(X=Co2+, B3+, Si4+, and P5+) Keggin heteropolyacid catalysts[J].
Catalysis Communications, 2014, 43: 155–158. DOI: 10.1016/j.catcom.2013.09.015. |
| [14] | 赵忠奎, 李总石, 王桂茹, 等. 杂多酸催化剂及其在精细化学品合成中的应用[J]. 化学进展, 2004, 16: 620–630. |
| [15] | 舒庆, 刘宝, 巢志聪, 等. 硅钨杂多酸制备、表征及催化油酸酯化反应合成生物柴油活性研究[J]. 有色金属科学与工程, 2013, 4(2): 19–24. |
| [16] |
Li K X, Chen L, Wang H L, et al. Heteropolyacid salts as self-separation and recyclable catalysts for transesterification of trimethylolpropane[J].
Applied Catalysis A: General, 2011, 392(1/2): 233–237. |
| [17] |
Li W Y, Zong Y X, Wang J K, et al. Sulfonated poly (4-vinylpyridine) heteropolyacid salts: A reusable green solid catalyst for Mannich reaction[J].
Chinese Chemical Letters, 2014, 25(4): 575–578. DOI: 10.1016/j.cclet.2013.11.022. |
| [18] |
Leng Y, Wang J, Zhu D R, et al. Sulfonated organic heteropolyacid salts: Recyclable green solid catalysts for esterifications[J].
Journal of Molecular Catalysis A: Chemical, 2009, 313(1/2): 1–6. |
| [19] |
Mansilla D S, Torviso M R, Alesso E N, et al. Synthesis and characterization of copper and aluminum salts of H3PMo12O40 for their use as catalysts in the eco-friendly synthesis of chromanes[J].
Applied Catalysis A: General, 1994, 375(2): 196–204. |
 2014, Vol. 5
2014, Vol. 5

