| 浸矿微生物与矿物相互作用的研究方法与技术 |
富矿资源由于不断地开发利用而日趋贫乏,高效合理地开发利用低品位难处理金属矿产资源已经成为热点.生物冶金由于低成本、低能耗、少污染成为了处理低品位矿物的有效方法[1-2].矿物生物浸出时,金属离子是在浸矿微生物-矿物相互作用过程中溶出的[3-4].因此,为了获得较高的金属浸出率,研究浸矿微生物-矿物相互作用显得尤为重要.
微生物与矿物表面的相互作用依赖于若干物理和生化参数.研究显示微生物通过各种方法吸附在矿物表面:站液层的分泌,蛋白结合受体,化学吸附,静电、疏水性相互作用,使用多糖-蛋白质复合物或借助于菌毛吸附[5-8],因此,微生物与矿物相互作用受两者表面性质的影响.对于微生物与矿物相互作用研究中表面性质的表征来说,确定微生物种类、矿物类型、 溶液环境等都很重要[9-10].因而,通过各种方法来表征作用体系的性质,有助于加深对微生物与矿物相互作用的理解.微生物与矿物之间实验分不开的复杂的物理化学相互作用使两者之间相互作用的研究有一定难度.
随着研究的不断发展与深入,各种物理的、化学的方法以及仪器分析的技术逐步地应用于相互作用领域.目前,微生物与矿物相互作用既可以从宏观角度分析,也可以从分子或原子的微观角度来分析.微观和宏观层面分析的结合使相互作用机制的探讨更加深入,并将微生物与矿物相互作用的研究推向了新的高度. 本文总结了浸矿微生物一矿物相互作用的主要研究方法和技术,以便使这些方法技术进一步从不同视角和尺度来研究生物冶金的机理与过程.
1 经典物理化学方法浸矿微生物-矿物相互作用涉及到物理、化学等各方面的机理.定性定量描述微生物吸附到矿物表面的机理包括表面热力学方法、 经典DLVO 及扩展DLVO 理论、等温吸附模型和微量热技术等.
1.1 表面热力学方法热力学方法通过比较浸矿微生物与矿物相互作用前后界面自由能的变化来解释吸附[11-13],吸附的总自由能表述为[13]:
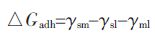
|
其中,γsm,γsl 和γml 分别为矿物与浸矿微生物,矿物与溶液及浸矿微生物与溶液的界面自由能. 当△Gadh 小于0,浸矿微生物容易吸附到矿物的表面.反之,则不易发生吸附.
GU Guo-hua 等[14] 应用热力学方法计算Acidithiobacillus ferrooxidans 在黄铁矿表面吸附的自由能,发现其吸附自由能为正值,无法解释Acidithiobacillus ferrooxidans 在黄铁矿表面的吸附现象.P.K. Sharma 等[13] 使用表面热力学方法来预测Paenibacillus polymyxa 在黄铜矿和黄铁矿表面的吸附行为. 热力学方法表明Paenibacillus polymyxa 和2 种矿物之间存在着范德华引力和酸碱作用斥力,细菌与矿物表面之间的吸附自由能都是正值,也就是说细菌不能吸附到矿物表面,但这与实验结果相反.A. Vilinska 和K. Hanumantha Rao[15]用表面热力学方法预测Leptospirillum ferrooxidans 在黄铁矿和黄铜矿表面的吸附情况,结果表明细菌与2 种矿物表面之间存在范德华引力和酸碱作用引力,两者之间的吸附自由能为负值,即Leptospirillum ferrooxidans 可以吸附到黄铜矿或者黄铁矿表面.表面热力学方法是对假定为可逆吸附的平衡过程的一种描述,但是忽视了静电相互作用及吸附自由能和距离之间的关系.当微生物与矿物之间的酸碱作用为引力或者范德华引力大于酸碱作用斥力时,热力学方法预测微生物可以吸附到矿物表面.相反则不能.因此,表面热力学方法不能完全解释吸附动力学特征,甚至还会出现与细菌吸附的实际测定数据不相符的结果.
1.2 经典DLVO 及扩展DLVO 理论经典DLVO 理论包括范德华力和静电力[12-13, 16],相互作用的总能量(Gtotal)等于范德华力能(GLW)和静电力作用能(GEL)之和,即:Gtotal(H)=GLW(H)+GEL(H). 这里H 为微生物与矿物表面的距离.范德华相互作用是浓缩状态下的分子或者表面的微小引力,它包括永久偶极子之间、永久偶极子与感生偶极子之间及感生偶极子之间的引力,它通过测定微生物及矿物的接触角来计算,因而,通过接触角数据可以直观地表现亲疏水性.静电作用是由于两界面之间的双电层相互作用产生的,Zeta 电位是连续相与附着在分散粒子上的流体稳定层之间的电势差,它可以表征分散粒子在连续相中表面所带的电荷性质及电荷量,因此,测量Zeta 电位在确定微生物与矿物之间的静电相互作用中变得很重要.DLVO 理论的缺陷是,只考虑到微生物细胞与矿物表面间的长程范德华力势能和静电力势能的相互作用.实际上,二者间还存在诸如疏水力、 氢键等作用力.后来,Van Oss 等[12-13]将酸碱相互作用加入经典DLVO 理论中.酸碱作用能(GAB)依赖于在溶液中极性部分的电子供体和电子受体之间的相互作用.因此,浸矿微生物与矿物之间的作用势能曲线被描述为范德华力、静电力和酸碱作用力关于作用距离(H)的一种平衡:Gtotal(H)=GLW(H)+GEL(H)+GAB(H).
GU Guo-hua 等[14] 通过扩展DLVO 理论建立的范德华力、疏水相互作用和静电作用自由能与作用距离(H)之间的势能曲线准确地预言了Acidithiobacil-lus ferrooxidans 在黄铁矿表面的吸附现象.Mohsen F arahat 等[17]利用扩展DLVO 理论来评估Ferroplasma acidiphilum 在黄铁矿表面的吸附情况,根据扩展DLVO 理论,在研究的所有pH 条件下,细菌矿物总的相互作用能主要由静电能贡献,其次是酸碱相互作用能和范德华能.酸碱相互作用比静电相互作用和范德华相互作用影响大,但是酸碱相互作用是短程的,相互作用面必须足够近.扩展DLVO 理论可以解释所有pH 条件下Ferroplasma acidiphilum-黄铁矿的吸附行为.
1.3 等温吸附模型吸附等温曲线是指在一定温度下微生物在矿物表面的吸附达到平衡时,微生物在两相中浓度之间的关系曲线.根据吸附实验获取的数据,拟合它们间的关系,其拟合参数能概括吸附量、吸附强度和吸附状态等特性.Langmuir 方程和Freundlich 方程己经广泛应用于浸矿微生物吸附到矿物表面的模拟中,且能很好地拟合浸矿微生物在矿物表面吸附的实验数据[18-19]. Langmuir 方程用于微生物-矿物吸附必须提出假设:吸附必须是单层的,均匀的,且吸附的细胞之间无相互作用.Freundlich 方程用于微生物一矿物吸附时不容易区分是单层吸附还是多层吸附,主要看细菌在矿物表面的覆盖度.LeXian Xia 等[20]测定了Acidithiobacillus ferrooxidans ATCC 23270 吸附到黄铜矿上的数量,并且利用Langmuir 和Freundlich 方程对吸附数据进行了模拟.2 个方程模拟的相关系数都超过了0.9,说明细菌吸附到矿物表面是一个涉及到Langmuir 和Freundlich 特性的很复杂的过程.S.N.Tan 等[21] 观察了Acidithiobacillus ferrooxidans 吸附到黄铜矿以及黄铁矿表面的行为,并对吸附数据进行了假一级动力学和Langmuir 方程的模拟,实验结果表明细菌吸附受底物疏水性质的影响,由调节趋化性的化学感应系统控制的Acidithiobacillus ferrooxidans 的活性位点,来应对细菌-矿物的初始接触.
1.4 微量热技术等温滴定微量热法是微量热测定方法中较常用的一种.等温滴定微量热法通过高灵敏度、高自动化的微量量热仪连续准确地监测和记录量热变化[22-23].Xingmin Rong 等[24] 利用等温滴定微量热仪(ITC) 和傅立叶红外光谱仪(FTIR)鉴定Pseudomonas putida 在针铁矿上的吸附,在pH 低于针铁矿等电点时,大量的细菌吸附到针铁矿上.ITC 的实验结果表明细菌吸附到针铁矿上是放热反应,吸附焰随着pH 和电解质浓度的提高而提高. 等温滴定微量热法通过自动记录反应的热功率(P)随时间(t)变化的曲线[25-26],对P-t曲线与基线之间的峰面积进行积分,就得到反应焰变(△H),进一步可以求出一系列反应动力学参数,如恼变、自由能变等,并且还可以获得反应的结合位点数.等温滴定微量热法既可以研究液相、固相、气相反应及两相间的反应,也可以长时间地监测缓慢的反应过程.Thore Rohwerder 等[27]用等温滴定微量热法,分批测定化能无机营养型的浸矿细菌Acidithiobacillus ferrooxidans 单菌,Leptospirillum ferrooxidans 单菌及Leptospirillum ferrooxidans 和Acidithiobacillus thiooxidans 混菌分别氧化黄铁矿的反应能. 实验表明,对比Acidithiobacillus ferrooxidans 单菌或者Acidithiobacillus thiooxidans 单菌,Leptospirillum ferrooxidans 具有更高的能量储存效率,利用等温滴定微量热测定方法,可以定量矿物的浸出速率.朱建裕等[28]以细菌胞外聚合物的3 种模拟成分葡萄糖、甘露糖和半肮氨酸与黄铁矿相互作用,通过等温滴定微量热技术,考察了它们与黄铁矿表面相互作用的反应热情况,半肮氨酸与黄铁矿的吸附和气体-固体吸附过程相似,符合langmuir 单层吸附模型,而葡萄糖和甘露糖为多层吸附. 实验结果证明胞外聚合物(EPS) 介导细菌吸附到硫化矿上,并与其发生反应导致矿物表面化学成分的改变.
2 表面成分检测方法 2.1 X 射线衍射法(X-ray diffraction,XRD)X 射线衍射仪能够定性定量分析大部分金属和非金属粉末样品[29-30],具有测量精确和样品制备简单等特点.夏乐先等[31]利用X 射线衍射和扫描电子显微镜/能谱(SEM/EDX)来分析Acidithiobacillus ferriooxidans 与Acidithiobacillus thiooxidans 分别及共同浸出闪辞矿.XRD 确定了太高的三价铁离子由于形成黄饵铁矶而降低了辞离子的溶解.另外,通过XRD、SEM 和EDX 分析无菌条件下,或者只有Acidithiobacillus ferrioox-idans 条件下,浸出闪辞矿的残基,表明存在于矿渣表面的硫层阻碍了矿物的浸出,Acidithiobacillus thioox-idans 浸出的矿渣表面没有硫层.2 种细菌在共同浸出闪辞矿过程中展现了不同的功能.Hui Liu 等[32] 通过XRD 和FTIR 分析Acidithiobacillus ferrooxidans 与黄铁矿相互作用30 d 后的矿渣表明黄饵铁矶的形成及无硫层的存在,这说明此种浸出情况下,阻碍矿物浸出的是黄饵铁矶钝化层.
2.2 傅立叶变换红外光谱法(Fourier transform infrared spectroscopy,FTIR)傅立叶变换红外光谱仪能够定性定量分析样品,可以分析样品表面的官能团,具有分辨率高、重现性好、 测定光谱范围宽等优点[33-35].Santhiy 等[36]用FTIR 分析发现Acidithiobacillus ferrooxidans 吸附在方铅矿及闪辞矿表面时,3 383cm-1 的吸收峰和1 453cm-1 的吸收峰因为吸附过程中氢键的作用发生偏移.Meng耶ue Diao 等[37]结合FTIR 与SEM 分析证明细菌Acidithiobacil-lus thiooxidans 和Leptospirillum ferrooxidans 表面成分及表面附属物的不同,导致了在AFM 测量细菌与黄铁矿相互作用过程中缩回曲线的差异.CHEN Ming-lian 等[38]通过TIR 分析Acidithiobacillus fer-rooxidans 和Acidithiobacillus caldus 分别与黄铜矿相互作用后的样品,与Acidithiobacillus ferrooxidans 相互作用后的黄铜矿比与Acidithiobacillus caldus 相互作用后的黄铜矿变化明显,将这2 种样品与纯黄铜矿样品的红外光谱进行比较得知:细胞吸附到了黄铜矿表面,结合吸附试验,Acidithiobacillus ferrooxi- dans 比Acidithiobacillus caldus 吸附到黄铜矿表面的量多.
2.3 拉曼光谱法(Raman spectra)拉曼光谱仪可用于分子结构研究的分析,它能提供简单快速、可重复、无损伤的定性定量分析,无需样品准备[39-41].R.H. Lara 等[42]使用拉曼光谱来分析评估在黄铁矿电极表面的硫化合物的状态,被Acidithiobacillus thiooxidans 氧化的矿物颗粒样品的拉曼光谱,证实了在酸性条件下黄铁矿的腐蚀过程中元素硫的形成、 稳定和渐进式的结晶.P.K. Sharma 等[43]利用TIR 和拉曼光谱,揭示了硫或黄铁矿培养的Acidithiobacillus ferrooxidans 菌比硫酸亚铁培养的Acidithiobacillus ferrooxidans 菌的表面蛋白含量更高,这表明在不同的生长条件下细菌合成蛋白成分的差异,导致了细菌表面电荷的不同.
2.4 X-射线光电子能谱法(X-ray photoelectron spectroscopyIXPS)X 射线光电子能谱,根据光电子的结合能定性定量分析物质的元素种类及化学形态[44-47],在研究微生物对矿物的溶解过程中起到独特的作用.Åke Sand- ström 等[48] 结合XRD 和XPS 来研究65 ℃的2 个不同的还原电位条件下,极端嗜热微生物Sulfolobus metallicus 浸出及化学浸出黄铜矿所得的矿渣,在这2 种情况下黄铜矿的浸出,均比在较低的氧化还原电位时有较大地提高,这也导致了大量元素硫的形成,但是在化学浸出时提高的特别明显.高的氧化还原电位伴随着黄饵铁矶的生成,而生物浸出可以将硫完全氧化成硫酸.因此,黄铜矿浸出的钝化层是黄饵铁矶. Keiko Sasaki 等[49] 利用XPS 分析有无CE 透析膜存在时,Acidithiobacillus caldus 与黄铜矿相互作用过程中硫的形成和消失,实验表明2 种情况下黄铜矿表面均形成了一硫化合物和元素硫,并且细菌直接与矿物接触更有助于中间化合物的溶解和铜的浸出.
2.5 X-射线吸收近边结构光谱法(X-ray absorption near-edge structure spectroscopyIXANES)X-射线吸收近边结构光谱能,能够获得吸收X射线的原子周围的配位原子种类、键长、配位数等电子和几何的局部结构参数[50-52],该技术具有可进行元素分辨,对吸收原子的周围局域结构和化学环境敏感等优势.Huan He 等[53] 结合XANES、SEM 和XRD 来研究极端嗜热微生物Acidianus manzaensis 与黄铜矿相互作用过程中硫形态的变化.SEM 表明细胞吸附到黄铜矿上,相互作用20 d 后矿物表面被许多絮状物覆盖.XRD 指出矿渣主要成分是黄铜矿和黄饵铁矶,同时XANES 证明Acidianus manzaensis 与黄铜矿相互作用的钝化层主要是黄饵铁矶. 光谱形貌分析表明:铜蓝是黄铜矿生物浸出过程中的中间硫化合物.
3 微观形貌探测技术 3.1 电子显微镜技术(Electron microscopeIEM)电子显微镜采用电子束和电磁透镜来成像,从而使其分辨率提高至在1 nm 下观察样品[54-55],EM 在浸矿微生物- 矿物相互作用的研究中应用较早.D.Mikkelsen 等[56]通过扫描电子电镜(SEM)和透射电子显微镜(TEM)观测极端嗜热微生物Acidianus brier-leyi,Metallosphaera sedula 和Sulfolobus metallicus 与黄铁矿之间的相互作用.随着黄铁矿的分解,沉积结构继续形成,从亚微米的沉淀物到圆片形的结构分布于矿物表面.曾伟民等[57]利用扫描电子显微镜/能谱(SEM/EDX)分析中度嗜热细菌浸出黄铜矿电极,结果表明黄铜矿表面覆盖有EPS 和黄饵铁矶,证明了这些物质是阻碍铜连续浸出的钝化层的主要成分.Hui Liu 等[32]利用SEM 分析了Acidithiobacillus ferrooxi-dans 与黄铁矿相互作用30 d 后的矿渣,结果在矿物表面有圆形的、 方形的和瘦长形的腐蚀坑的存在,这些腐蚀坑的分布正好与不同的晶面相关,并且所有坑的大小都比不上细菌的大小.
3.2 原子力显微镜技术(Atomic force microscopeI AFM)原子力显微镜是研究微生物与矿物之间相互作用的有力工具,它不仅能够获取单细胞在固相表面的吸附等高分辨率的图像,而且可以在纳米距离范围内,测定微生物与矿物之间相互作用力随距离的变化[58-60],具有原子级的分辨率.Jianyu Zhu 等[61]利用A M 探测Acidithiobacillus ferrooxidans,Acidithiobacillus thiooxidans 及Leptospirillum ferrooxidans 分别与黄铜矿之间的相互作用力,结果表明细菌细胞的表面电荷和疏水性质都影响细菌的吸附力,且EPS 缺损时吸附力减小,这说明EPS 对细菌-矿物相互作用是十分重要的. eimin Zeng 等[62]利用A M 观测吸附到矿物表面的中度嗜热微生物Acidithiobacillus caldus快速地产生EPS,并且EPS 一旦产生就很难减少或消除,这样在浸矿后期大量的EPS 介入导致黄饵铁矶生成,阻碍了铜的继续浸出.K. Kinzler 等[3]通过AFM 来观察Acidithiobacillus ferrooxidans Rl,R7,C-52 和SPIII/3 四株菌对黄铁矿的吸附情况,实验数据表明在EPS 中具有更高三价铁离子的菌株展现较好的吸附情况和氧化活性.
3.3 荧光显微镜技术(Epifluorescence microscopyI EFM)荧光显微镜用紫外线使被检测物体发出荧光,它能够对物体的形状及位置进行观察,与原子力显微镜相结合来做定性定量的研究.N. Noël 等[63]靠原子力显微镜和荧光显微镜的DAPI 染色和FISH 探针,来揭示了吸附到黄铁矿样品表面的细菌种类(Acidithiobacillus ferrooxidans,Acidithiobacillus thiooxidans,Acidithiobacillus caldus,Leptospiril- lum ferrooxidans 和Leptospirillum ferriphilum),微生物可以被详细地鉴定至某一特定的种.Leptospiril- lum ferriphilum 引起了聚合,并且提高了细胞吸附到黄铁矿样品表面的量.Acidithiobacillus caldus 单独不能吸附到黄铁矿表面,Leptospirillum ferriphilum 和Acidithiobacillus caldus 昆菌吸附试验,证明Leptospirillum ferriphilum 先吸附到矿物表面才能使Acidithiobacillus caldus 发生吸附,在这种情况下,Leptospirillum ferriphilum 是生物膜形成的关键微生物.Stefanie Mangold 等[64] 利用AFM 和EFM 来研究吸附的Acidithiobacillus ferrooxidans 细菌及EPS 与矿物之间的相互作用.AFM 成像提供了细胞的空间排列和物质从溶液到单细胞之间转换的痕迹.EFM 鉴定了生物膜的组分及其分布状态.AFM 与EFM 相结合有助于我们进一步丰富微生物-矿物界面作用的相关知识.
4.3 激光扫描共聚焦显微镜技术(Confocal laser scanning microscopeICLSM)激光扫描共聚焦显微镜逐点、逐行、逐面的快速扫描成像,经过各种特异性的荧光染色,CLSM 能够排除非焦平面信息以直观反应立体空间分布、无损深层形态结构地观察细胞的形态,及提高分辨率和对比度以定量分析细胞内生化成分等[65-66].Sören Bellen-berg 等[67]利用CLSM 观测Acidithiobacillus ferroox-idans ATCC 23270 的英膜多糖,实验表明细菌与金属硫化物降解产物接触等多方面的影响,诱导了细菌英膜多糖的产生.Cindy-Jade Africa 等[68]结合原子力显微镜、荧光显微镜和激光扫描共聚焦显微镜,来鉴定Metallosphaera hakonensis 分别吸附到黄铜矿和黄铁矿样本表面及细菌在矿物表面形成的生物膜,矿物表面的细菌覆盖率与温度和时间相关,细菌在金属硫化矿的优先吸附和生物膜形成也被观察到.同时原子力显微镜和荧光显微镜的结合,提高了对微生物与矿物位点特异性结合的评估.B. Florian 等[69]利用AFM、 EFM 和CLSM 观测微生物与黄铁矿之间的相互作用,在吸附实验中,矿物表面某些地方细菌成簇的吸附,但是有的地方没有细菌吸附,不同菌种的细菌在矿物表面的分布和空间排布有较大差别,这些实验结果有助于进一步研究细菌与矿物之间的特异性相互作用.
4 结束语综上所述,经典物理化学分析方法是研究浸矿微生物-矿物相互作用基础而重要的研究于段. 从物理化学的角度分析浸矿微生物与矿物的相互作用,考虑两者的静电相互作用、E德华力和在水作用等,反应过程中的自由能和热量变化,但是只通过这些分析方法很难获取浸矿微生物-矿物相互作用的微观信息. 表面成分分析方法和微观表面探测技术,己应用于浸矿微生物和矿物相互作用的机理研究中,如荧光显微镜、X 射线光电子能谱以及X-射线吸收近边结构光谱等技术,以上于段从微观的角度,揭示了浸矿微生物与矿物相互作用前后形貌的变化和相互作用的基团或化学键等信息.经典物理化学分析技术、表面成分分析方法及微观表面探测技术相结合,在浸矿微生物与矿物相互作用研究中使我们更加了解浸矿微生物与矿物相互作用的机理,为进一步提高生物浸出效率和控制酸性矿坑水的污染提供了有效的信息.
| [1] |
Brierley C L. How will biomining be applied in future[J].
Transactions of Nonferrous Metals Society of China, 2008, 18(6): 1302–1310. DOI: 10.1016/S1003-6326(09)60002-9. |
| [2] |
Rawlings D E. Heavy metal mining using microbes[J].
Annual Review of Microbiology, 2002, 56: 65–91. DOI: 10.1146/annurev.micro.56.012302.161052. |
| [3] |
Kinzler K, Gehrke T, Telegdi J, et al. Bioleaching - a result of interfacial processes caused by extracellular polymeric substances (EPS)[J].
Hydrometallurgy, 2003, 71(1/2): 83–88. |
| [4] |
Vera M, Schippers A, Sand W. Progress in bioleaching: fundamentals and mechanisms of bacterial metal sulfide oxidation-part A[J].
Applied Microbiology and Biotechnology, 2013, 97(17): 7529–7541. DOI: 10.1007/s00253-013-4954-2. |
| [5] |
Sampson M I, Phillips C V, Ball A S. Investigation of the attachment of Thiobacillus ferrooxidans to mineral sulfides using scanning electron microscopy analysis[J].
Minerals Engineering, 2000, 13(6): 643–656. DOI: 10.1016/S0892-6875(00)00046-7. |
| [6] |
Devasia P, Natarajan K A, Sathyanarayana D N, et al. Surface chemistry of Thiobacillus ferrooxidans relevant to adhesion on mineral surfaces[J].
Applied and Environmental Microbiology, 1993, 59(12): 4051–4055. |
| [7] |
Gehrke T, Telegdi J, Thierry D, et al. Importance of extracellular polymeric substances from Thiobacillus ferrooxidans for bioleaching[J].
Applied and Environmental Microbiology, 1998, 64(7): 2743–2747. |
| [8] |
Gonzalez A, Bellenberg S, Mamani S, et al. AHL signaling molecules with a large acyl chain enhance biofilm formation on sulfur and metal sulfides by the bioleaching bacterium Acidithiobacillus ferrooxidans[J].
Applied Microbiology and Biotechnology, 2013, 97(8): 3729–3737. DOI: 10.1007/s00253-012-4229-3. |
| [9] |
Ghauri M A, Okibe N, Johnson D B. Attachment of acidophilic bacteria to solid surfaces: The significance of species and strain variations[J].
Hydrometallurgy, 2007, 85. |
| [10] |
Ohmura N, Kitamura K, Saiki H. Selective Adhesion of Thiobacillus ferrooxidans to Pyrite[J].
Applied and Environmental Microbiology, 1993, 59(12): 4044–4050. |
| [11] |
Bayoudh S, Othmane A, Mora L, et al. Assessing bacterial adhesion using DLVO and XDLVO theories and the jet impingement technique[J].
Colloid Surface B: Biointerfaces, 2009, 73(1): 1–9. DOI: 10.1016/j.colsurfb.2009.04.030. |
| [12] |
Hermansson M. The DLVO theory in microbial adhesion[J].
Colloids and Surfaces B: Biointerfaces, 1999, 14(1/2/3/4): 105–119. |
| [13] |
Sharma P K, Rao K H. Adhesion of Paenibacillus polymyxa on chalcopyrite and pyrite: surface thermodynamics and extended DLVO theory[J].
Colloids and Surfaces B: Biointerfaces, 2003, 29(1): 21–38. DOI: 10.1016/S0927-7765(02)00180-7. |
| [14] |
Gu G H, Wang H, Suo J, et al. Interfacial interaction of bio-leaching of pyrite mineral[J].
Journal of Central South University of Technology, 2008, 15(1): 49–53. DOI: 10.1007/s11771-008-0011-1. |
| [15] |
Vilinska A, Rao K H. Surface thermodynamics and extended DLVO theory of Leptospirillum ferrooxidans cells' adhesion on sulfide minerals[J].
Minerals and Metallurgical Processing, 2011, 28(3): 151–158. |
| [16] |
Katsikogianni M, Missirlis Y F. Concise review of mechanisms of bacterial adhesion to biomaterial and of techniques used in estimating bacteria-material interactions[J].
European Cell and Materials, 2004(8): 37–57. |
| [17] |
Farahat M, Hirajima T, Sasaki K. Adhesion of Ferroplasma acidiphilum onto pyrite calculated from the extended DLVO theory using the van Oss-Good-Chaudhury approach[J].
Journal of Colloid and Interface Science, 2010, 349(2): 594–601. DOI: 10.1016/j.jcis.2010.05.091. |
| [18] |
Hameed B H. Equilibrium and kinetics studies of 2,4,6-trichlorophenol adsorption onto activated clay[J].
Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2007, 307(1/2/3): 45–52. |
| [19] |
Ozdemir G, Ceyhan N, Ozturk T, et al. Biosorption of chromium(VI), cadmium(II) and copper(II) by Pantoea sp TEM[J].
Chemical Engineering Journal, 2004, 102(3): 249–253. DOI: 10.1016/j.cej.2004.01.032. |
| [20] |
Xia L X, Shen Z, Vargas T, et al. Attachment of Acidithiobacillus ferrooxidans onto different solid substrates and fitting through Langmuir and Freundlich equations[J].
Biotechnology Letters, 2013, 35(12): 2129–2136. DOI: 10.1007/s10529-013-1316-1. |
| [21] |
Tan S N, Chen M. Early stage adsorption behaviour of Acidithiobacillus ferrooxidans on minerals I: An experimental approach[J].
Hydrometallurgy, 2012, 119: 87–94. |
| [22] |
Fang L C, Cao Y Y, Huang Q Y, et al. Reactions between bacterial exopolymers and goethite: A combined macroscopic and spectroscopic investigation[J].
Water Research, 2012, 46(17): 5613–5620. DOI: 10.1016/j.watres.2012.07.046. |
| [23] |
Fang L C, Huang Q Y, Wei X, et al. Microcalorimetric and potentiometric titration studies on the adsorption of copper by extracellular polymeric substances (EPS), minerals and their composites[J].
Bioresource Technology, 2010, 101(15): 5774–5779. DOI: 10.1016/j.biortech.2010.02.075. |
| [24] |
Rong X M, Huang Q Y, He X M, et al. Interaction of Pseudomonas putida with kaolinite and montmorillonite: A combination study by equilibrium adsorption, ITC, SEM and FTIR[J].
Colloids and Surfaces B: Biointerfaces, 2008, 64(1): 49–55. DOI: 10.1016/j.colsurfb.2008.01.008. |
| [25] |
Rong X M, Huang Q Y, Chen W L. Microcalorimetric investigation on the metabolic activity of Bacillus thuringiensis as influenced by kaolinite, montmorillonite and goethite[J].
Applied Clay Science, 2007, 38(1/2): 97–103. |
| [26] |
Rong X M, Huang Q Y, Jiang D H, et al. Isothermal microcalorimetry: A review of applications in soil and environmental sciences[J].
Pedosphere, 2007, 17(2): 137–145. DOI: 10.1016/S1002-0160(07)60019-8. |
| [27] |
Thore Rohwerder, Axel Schippers, Sand W. Determination of reaction energy values for biological pyrite oxidation by calorimetry[J].
Thermochimica Acta, 1998, 309: 79–85. DOI: 10.1016/S0040-6031(97)00352-3. |
| [28] |
Zhu J Y, Yang P, Li B M, et al. Microcalorimetric studies of interaction between extracellular polymeric substance and sulfide minerals[J].
Transactions of Nonferrous Metals Society of China, 2008, 18(6): 1439–1442. DOI: 10.1016/S1003-6326(09)60022-4. |
| [29] |
Kahle M, Kleber M, Jahn R. Review of XRD-based quantitative analyses of clay minerals in soils: the suitability of mineral intensity factors[J].
Geoderma, 2002, 109(3/4): 191–205. |
| [30] |
Srodon J, Drits V A, McCarty D K, et al. Quantitative X-ray diffraction analysis of clay-bearing rocks from random preparations[J].
Clay Clay Miner, 2001, 49(6): 514–528. DOI: 10.1346/CCMN. |
| [31] |
Xia L X, Liu J S, Xiao L, et al. Single and cooperative bioleaching of sphalerite by two kinds of bacteria - Acidithiobacillus ferriooxidans and Acidithiobacillus thiooxidans[J].
Transactions of Nonferrous Metals Society of China, 2008, 18(1): 190–195. DOI: 10.1016/S1003-6326(08)60034-5. |
| [32] |
Liu H, Gu G H, Xu Y B. Surface properties of pyrite in the course of bioleaching by pure culture of Acidithiobacillus ferrooxidans and a mixed culture of Acidithiobacillus ferrooxidans and Acidithiobacillus thiooxidans[J].
Hydrometallurgy, 2011, 108(1/2): 143–148. |
| [33] |
Dziuba B, Babuchowski A, Nalecz D, et al. Identification of lactic acid bacteria using FTIR spectroscopy and cluster analysis[J].
International Dairy Journal, 2007, 17(3): 183–189. DOI: 10.1016/j.idairyj.2006.02.013. |
| [34] |
Madejova J. FTIR techniques in clay mineral studies[J].
Vibrational Spectroscopy, 2003, 31(1): 1–10. DOI: 10.1016/S0924-2031(02)00065-6. |
| [35] |
Wenning M, Buchl N R, Scherer S. Species and strain identification of lactic acid bacteria using FTIR spectroscopy and artificial neural networks[J].
Journal of Biophotonics, 2010, 3(8/9): 493–505. |
| [36] |
Santhiya D, Subramanian S, Natarajan K A. Surface chemical studies on galena and sphalerite in the presence of thiobacillus thiooxidans with reference to mineral beneficiation[J].
Minerals Engineering, 2000, 13(7): 747–763. DOI: 10.1016/S0892-6875(00)00059-5. |
| [37] |
Diao M, Taran E, Mahler S, et al. Quantifying adhesion of acidophilic bioleaching bacteria to silica and pyrite by atomic force microscopy with a bacterial probe[J].
Colloids and surfaces. B, Biointerfaces, 2013, 115C: 229–236. |
| [38] |
Chen M L, Zhang L, Gu G H, et al. Effects of microorganisms on surface properties of chalcopyrite and bioleaching[J].
Transactions of Nonferrous Metals Society of China, 2008, 18(6): 1421–1426. DOI: 10.1016/S1003-6326(09)60019-4. |
| [39] |
Almarashi J F M, Kapel N, Wilkinson T S, et al. Raman spectroscopy of bacterial species and strains cultivated under reproducible conditions[J].
Spectroscopy-an International Journal, 2012, 27(5/6): 361–365. |
| [40] |
Jarvis R M, Goodacre R. Discrimination of bacteria using surface-enhanced Raman spectroscopy[J].
Analytical Chemistry, 2004, 76(1): 40–47. DOI: 10.1021/ac034689c. |
| [41] |
White S N. Laser Raman spectroscopy as a technique for identification of seafloor hydrothermal and cold seep minerals[J].
Chemical Geology, 2009, 259(3/4): 240–252. |
| [42] |
Lara R H, Valdez-Perez D, Rodriguez A G, et al. Interfacial insights of pyrite colonized by Acidithiobacillus thiooxidans cells under acidic conditions[J].
Hydrometallurgy, 2010, 103(1-4): 35–44. DOI: 10.1016/j.hydromet.2010.02.014. |
| [43] |
Sharma P K, Das A, Rao K H, et al. Surface characterization of Acidithiobacillus ferrooxidans cells grown under different conditions[J].
Hydrometallurgy, 2003, 71(1/2): 285–292. |
| [44] |
Biesinger M C, Hart B R, Polack R, et al. Analysis of mineral surface chemistry in flotation separation using imaging XPS[J].
Minerals Engineering, 2007, 20(2): 152–162. DOI: 10.1016/j.mineng.2006.08.006. |
| [45] |
Dufrene Y F, van der Wal A, Norde W, et al. X-ray photoelectron spectroscopy analysis of whole cells and isolated cell walls of gram-positive bacteria: comparison with biochemical analysis[J].
Journal of Bacteriology, 1997, 179(4): 1023–8. DOI: 10.1128/jb.179.4.1023-1028.1997. |
| [46] |
Kaivosoja E, Virtanen S, Rautemaa R, et al. Spectroscopy in the analysis of bacterial and eukaryotic cell footprints on implant surfaces[J].
European Cell and Materials, 2012, 24: 60–73. DOI: 10.22203/eCM. |
| [47] |
Smart R S, Skinner W M, Gerson A R. XPS of sulphide mineral surfaces: Metal-deficient, polysulphides, defects and elemental sulphur[J].
Surface and Interface Analysis, 1999, 28(1): 101–105. DOI: 10.1002/(ISSN)1096-9918. |
| [48] |
Sandstrom A, Shchukarev A, Paul J. XPS characterisation of chalcopyrite chemically and bio-leached at high and low redox potential[J].
Minerals Engineering, 2005, 18(5): 505–515. DOI: 10.1016/j.mineng.2004.08.004. |
| [49] |
Sasaki K, Takatsugi K, Tuovinen O H. Spectroscopic analysis of the bioleaching of chalcopyrite by Acidithiobacillus caldus[J].
Hydrometallurgy, 2012, 127: 116–120. |
| [50] |
Bovenkamp G L, Zanzen U, Krishna K S, et al. X-Ray Absorption near-edge structure (XANES) spectroscopy study of the interaction of silver ions with staphylococcus aureus, listeria monocytogenes, and escherichia coli[J].
Applied and Environmental Microbiology, 2013, 79(20): 6385–6390. DOI: 10.1128/AEM.01688-13. |
| [51] |
Fleet M E. Xanes spectroscopy of sulfur in earth materials[J].
The Canadian Mineralogist, 2005, 43: 1811–1838. DOI: 10.2113/gscanmin.43.6.1811. |
| [52] |
Galoisy L, Calas G, Arrio M A. High-resolution XANES spectra of iron in minerals and glasses: structural information from the pre-edge region[J].
Chemical Geology, 2001, 174(1/2/3): 307–319. |
| [53] |
He H, Xia J L, Yang Y, et al. Sulfur speciation on the surface of chalcopyrite leached by Acidianus manzaensis[J].
Hydrometallurgy, 2009, 99(1/2): 45–50. |
| [54] |
Grin I, Schwarz H, Linke D. Electron microscopy techniques to study bacterial adhesion[J].
Advances in Experimental Medicine and Biology, 2011, 715: 257–269. DOI: 10.1007/978-94-007-0940-9. |
| [55] |
Pfeffer C, Larsen S, Song J, et al. Filamentous bacteria transport electrons over centimetre distances[J].
Nature, 2012, 491(7423): 218–221. DOI: 10.1038/nature11586. |
| [56] |
Mikkelsen D, Kappler U, Webb R I, et al. Visualisation of pyrite leaching by selected thermophilic archaea: Nature of microorganism-ore interactions during bioleaching[J].
Hydrometallurgy, 2007, 88(1/2/3/4): 143–153. |
| [57] |
Zeng W M, Qiu G Z, Zhou H B, et al. Electrochemical behaviour of massive chalcopyrite electrodes bioleached by moderately thermophilic microorganisms at 48 degrees C[J].
Hydrometallurgy, 2011, 105(3/4): 259–263. |
| [58] |
McGuire M M, Heist C A. In situ atomic force microscopy (AFM) investigations of clay mineral swelling[J].
Abstracts of Papers of the American Chemical Society, 2011: 241. |
| [59] |
Meyer R L, Zhou X F, Tang L N, et al. Immobilisation of living bacteria for AFM imaging under physiological conditions[J].
Ultramicroscopy, 2010, 110(11): 1349–1357. DOI: 10.1016/j.ultramic.2010.06.010. |
| [60] |
Nunez M E, Martin M O, Chan P H, et al. Atomic force microscopy of bacterial communities[J].
Methods in Enzymology, 2005, 397: 256–268. DOI: 10.1016/S0076-6879(05)97015-8. |
| [61] |
Zhu J Y, Li Q, Jiao W F, et al. Adhesion forces between cells of Acidithiobacillus ferrooxidans, Acidithiobacillus thiooxidans or Leptospirillum ferrooxidans and chalcopyrite[J].
Colloids and Surfaces B: Biointerfaces, 2012, 94: 95–100. DOI: 10.1016/j.colsurfb.2012.01.022. |
| [62] |
Zeng W M, Zhou H B, Wan M X, et al. Preservation of Acidithiobacillus caldus: A moderately thermophilic bacterium and the effect on subsequent bioleaching of chalcopyrite[J].
Hydrometallurgy, 2009, 96(4): 333–336. DOI: 10.1016/j.hydromet.2008.11.003. |
| [63] |
Noel N, Florian B, Sand W. AFM & EFM study on attachment of acidophilic leaching organisms[J].
Hydrometallurgy, 2010, 104(3/4): 370–375. |
| [64] |
Mangold S, Harneit K, Rohwerder T, et al. Novel combination of atomic force microscopy and epifluorescence microscopy for visualization of leaching bacteria on pyrite[J].
Applied and Environmental Microbiology, 2008, 74(2): 410–415. DOI: 10.1128/AEM.01812-07. |
| [65] |
de Carvalho F G, Puppin-Rontani R M, Soares L E S, et al. Mineral distribution and CLSM analysis of secondary caries inhibition by fluoride/MDPB-containing adhesive system after cariogenic challenges[J].
Journal of Dentistry, 2009, 37(4): 307–314. DOI: 10.1016/j.jdent.2008.12.006. |
| [66] |
Mogge B, Loferer C, Agerer R, et al. Bacterial community structure and colonization patterns of Fagus sylvatica L-ectomycorrhizospheres as determined by fluorescence in situ hybridization and confocal laser scanning microscopy[J].
Mycorrhiza, 2000, 9(5): 271–278. DOI: 10.1007/PL00009991. |
| [67] |
Bellenberg S, Leon-Morales C F, Sand W, et al. Visualization of capsular polysaccharide induction in Acidithiobacillus ferrooxidans[J].
Hydrometallurgy, 2012, 129: 82–89. |
| [68] |
Africa C J, van Hille R P, Sand W, et al. Investigation and in situ visualisation of interfacial interactions of thermophilic microorganisms with metal-sulphides in a simulated heap environment[J].
Minerals Engineering, 2013, 48: 100–107. DOI: 10.1016/j.mineng.2012.09.011. |
| [69] |
Florian B, Noel N, Thyssen C, et al. Some quantitative data on bacterial attachment to pyrite[J].
Minerals Engineering, 2011, 24(11): 1132–1138. DOI: 10.1016/j.mineng.2011.03.008. |
 2014, Vol. 5
2014, Vol. 5


