| 微波外场对液相合成砂状氧化钇前驱体形貌的影响 |
稀土氧化物可用于熔盐电解制备稀土金属或其铁合金等,但目前熔盐电解采用的稀土氧化物为3~5 μm片状小颗粒,存在流动性差而不便于计算机控制加料以及粉尘飞扬损失大等问题.而砂状稀土氧化物具有比表面积大、颗粒粗、粒度分布集中、耐磨性和流动性好、强度高、活性大和溶解速度快[1-3]等特点,有利于电解过程中氧化物输送、减少飞扬损失以及有利于改善电解过程中的传质,使电解槽运行更加稳定,可获得更高的电流效率和更低的电解电耗等.目前,国内外研究大颗粒砂状氧化铝制备技术较多,而对于稀土氧化物多集中在纳米及超细氧化物制备方法[4-10]的研究,对大粒度砂状稀土氧化物研究报道则极少.此外,微波加热是介质与微波相互作用,使介质分子作高速震动使介质分子间产生摩擦,从而导致介质的温度升高,使物质内外几乎同时加热升温,在介质温度与介质损耗因数呈负相关系时,形成体热源状态物质内外加热均匀一致,能瞬间为物质的沉淀结晶提供所需能量.为此,本课题以氧化钇为例,探索了微波辅助液相合成大颗粒砂状稀土氧化物的可行性.限于篇幅,文本重点探讨微波外场对液相合成砂状氧化钇前驱体形貌的影响.
1 实验 1.1 样品制备将氯化钇和草酸加去离子水配置成一定浓度溶液,取一定量的氯化钇,倒入三口烧瓶中.按需取草酸,倒入恒液漏斗备用.将装有YCl3溶液的三口烧瓶置于微波及超声波协同合成/萃取仪中,打开磁力搅拌,将草酸以2 mL/min滴入YCl3溶液中.反应完后陈化、过滤、洗涤、干燥得前驱体草酸钇,将草酸钇热分解得产品氧化钇.
1.2 分析表征采用Philip-XL30W型扫描电子显微电镜观察前驱体及其热分解粉体形貌以及分散情况,并通过ruler图像处理软件分析估算粉体D50粒径;利用Diamond 6000热重/差热分析(TG-DSC)表征前驱体热分解规律;采用日本理学D/max-rA型转靶全自动X射线衍射仪(Cu靶,入射波长0.154 1 nm)对煅烧产物做XRD晶相结构分析.
2 结果与讨论 2.1 YCl3与H2C2O4的摩尔比对前驱体形貌的影响控制氯化钇浓度0.25 mol/L、草酸浓度1.0 mol/L、反应温度60 ℃、反应时间3 h,采用不同YCl3与H2C2O4摩尔比所得前驱体,如图 1所示.反应体系中YCl3与H2C2O4的理论摩尔比为2:3,但考虑到沉淀反应的充分,本实验采用1:1、1:2和1:4的摩尔比.考察摩尔比对制备Y2O3前驱体形貌的影响.
 |
| 图 1 不同YCl3和H2C2O4摩尔比制备的前驱体SEM像 |
如图 1所示,从颗粒粒径看,YCl3与H2C2O4摩尔比对氧化钇前驱体的影响不大;从颗粒的附聚和团结效果看,YCl3与H2C2O4摩尔比多少对其变化较大.摩尔比为1:1时,如图 1(a)所示,颗粒较小且呈分散的方块状,小颗粒之间没有发生附聚;当YCl3与H2C2O4摩尔比为1:4时,如图 1(c)所示,前驱体单个颗粒的粒径相比较,要比摩尔比为1:1和1:2的颗粒粒径要大,且颗粒看起来明显呈方块状,单个颗粒之间有少许附聚,但与图 1(b)的相比较其效果次之;当YCl3与H2C2O4摩尔比为1:2,如图 1(b)所示,前驱体单个颗粒的粒径大小为1 μm左右,但其附聚效果更好.因此,本实验选择YCl3与H2C2O4的摩尔比1:2.
2.2 YCl3起始浓度对前驱体形貌的影响控制YCl3与H2C2O4摩尔比为1:1,草酸浓度1.0 mol/L,反应温度60 ℃,反应时间3 h,采用不同YCl3浓度分别为:0.5 mol/L,0.8 mol/L,1.0 mol/L,所得前驱体的SEM图如图 2所示.由图 2可知,随着YCl3的浓度增加,前驱体单个晶粒大小和颗粒之间的附聚效果有所变化.如图 2(a)所示,YCl3浓度为0.5 mol/L时,形成的前驱体颗粒较小,但结晶度较好,单个颗粒在一起形成更大的附聚体,且附聚效果较好;如图 2(b)所示,YCl3浓度为0.8 mol/L时,前驱体颗粒粒径有所增大,呈块状形,其附聚效果不好.在YCl3浓度为1.0 mol/L时,前驱体颗粒呈棒状形,其附聚效果也不好.由于料液起始浓度对沉淀结晶过程中晶粒的形核与长大影响较大,当浓度低时形核慢,且形核速度慢于晶核长大速率,晶核周围存在较多的Y3+,使得前驱体附聚效果好;当浓度高时,使单位体积瞬间生成粒子数剧增,则成核速度快于长大速率.粒子在范德华力和表面张力的作用下,剧烈的进行布朗运动增大粒子间相互碰撞的机会,致使粒子长大和附聚现象,而在低浓度下形成的附聚物更符合实验的要求.从前驱体的形貌看,YCl3起始浓度为0.5 mol/L较优.
 |
| 图 2 不同YCl3起始浓度制备的前驱物的SEM像 |
2.3 反应及陈化时间对前驱体形貌和粒度的影响
控制YCl3与H2C2O4摩尔比为1:2,YCl3的浓度为0.5 mol/L,温度为50 ℃,反应及陈化时间为1 h、2 h、3 h、4 h和6 h,所得前驱体测量其粒径,考察反应、陈化时间对制备Y2O3前驱体粒度分布的影响;当溶液中大小晶体同时存在时,由于微小晶体比大晶体溶解度大,溶液对大晶体已经达到饱和,而对微小晶粒尚未达到饱和,因而微小晶体逐渐溶解,溶解到一定程度后,溶液对小晶体为饱和,而对大晶体是过饱和,于是溶液中的构晶离子就在大晶体上沉积;当溶液对大晶体为饱和溶液时,对小晶体又为未饱和,小晶体又继续溶解,这样小晶体将逐渐消失,大晶体不断长大,所以反应时间对制备砂状氧化物影响较大[11].如图 3所示,可以看出,随着反应时间的变化,前驱体粒径变化较大.随着反应时间的延长,前驱体的粒度呈增大的趋势,这是因为随着微波辐射时间的延长,颗粒逐渐长大和附聚.沉淀反应是一个动态过程,布朗运动不断在进行,颗粒的大小也在不断的变化,随着时间的延长,颗粒的变化越来越小,考虑到经济效益,我们选择的最佳微波辐射时间为3 h;此时间要短于水浴加热的陈化时间[12],这是因为微波的内加热,能够瞬间为晶体的形核与长大提供巨大能量,因此能大大缩短陈化时间.
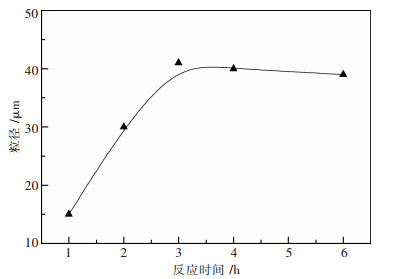 |
| 图 3 前驱体粒径随反应时间的变化图 |
2.4 反应温度对前驱体形貌和粒度的影响
控制YCl3与H2C2O4的摩尔比为1:2,YCl3的浓度为0.5 mol/L,反应时间为3 h,采用温度为:40 ℃和80 ℃进行实验,图 4所示为各反应时间下得前驱物的SEM图.在沉淀反应中,温度是重要的影响因素.温度与过饱和度的关系可知,当溶质含量一定时,溶液过饱和度随温度的增加而降低.温度低时,过饱和度很大,但溶质分子的能量较低,则晶粒的生成速度也很小;随着温度的增大,晶粒的形成速度可以达到最大值,若继续增大温度,一方面会导致过饱和度下降,同时也导致溶液中分子动能增大过快,不利于形成稳定的晶粒,因此晶粒的生长速度下降[12].如图 4所示,在不同温度下颗粒大小有较大的差异.由不同温度下制备的前驱体分析得:当温度为中低温区时,如温度为40 ℃时,颗粒的附聚效果更好,形成的附聚体明显更大;当温度在高温区时,如80 ℃时,颗粒的附聚效果更差,形成的附聚体总体尺寸比中低温的要小,但是附聚体中的单个颗粒比40 ℃要大,因为在80 ℃时,颗粒生长速度快,形成较大的单颗粒,同时分子动能大,不利于形成稳定的团聚体.因此,从前驱体的形貌及能耗考虑,较优的反应温度为40 ℃左右.
 |
| 图 4 不同反应温度制备的前驱物的SEM像 |
2.5 热重/差热分析
图 5为,在微波作用下,以氯化钇为原料、草酸为沉淀剂所制备的氧化钇前驱体的TG-DTG图,取2.631 mg的草酸钇和5.860 mg的Al2O3参比样,在氮气(100 mL/min)气氛中以5 ℃/min的升温速度对样品做热重/差热分析,得到TG-DTG曲线如图 5所示.由图 5可知,由前驱体的微商热重曲线(DTG)知,在110~200 ℃之间有一个失重峰,外延起始温度为110 ℃左右,峰顶温度为160 ℃,这是由于前驱体草酸钇在此温度范围内发生了分解脱水反应失去吸附水和结晶水所引起的.从微商热重曲线(DTG)上看,草酸稀土在430 ℃有一个明显的失重峰,这是由于前驱体草酸盐脱除剩余结晶水和发生分解反应释放出大量的二氧化碳所引起的;从热重曲线(TG)看,400 ℃到650 ℃之间,前驱体失重较为明显,失重率大约为36.0 %.从微商热重曲线(DTG)看,在650 ℃以后无明显的热效应,表明前驱体已分解完全,TG曲线在650 ℃后也变的平坦,并出现失重平台,达到失重平衡,表明草酸钇分解反应结束,前驱体彻底分解为氧化钇.此外,从图 5可知,在500 ℃左右前驱体出现碳酸根热分解高峰,所以热分解温度可以选择500 ℃或500 ℃以上.
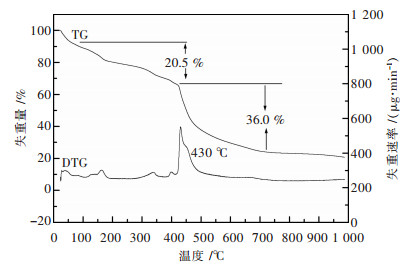 |
| 图 5 草酸钇的TG-DTG图 |
2.6 XRD分析
草酸钇在热分解过程中变化,由文献[13]报道,当温度达200 ℃时,结晶水将脱除从而前驱物由Y2 (C2O4)3·10H2O转变成Y2(C2O4)3 · 2H2O;当温度升高到400 ℃左右时,前驱物中的结晶水已完全脱除,产物结构由Y2 (C2O4) ·2H2O转变为YOOH相.
如图 6所示,为前驱体的热分解产物XRD谱图.结合前驱体的TG-DTG图结果,选择3个热分解温度:500 ℃、700 ℃和900 ℃,热分解时间为2h.可以看出,在500 ℃焙烧2 h已经形成了立方相氧化钇晶相,此时晶粒尺寸细小,X射线衍射峰强度较弱,半峰宽较宽,衍射峰与标准衍射卡(01-083-0927)是一致;继续提高热分解温度,XRD谱图的衍射峰则逐渐变高,半峰宽变窄,表明氧化钇晶粒长大,同时晶格发育趋于完整,缺陷减少,结构趋于稳定.当焙烧温度为900 ℃,其产物的XRD图谱显示出完好的衍射峰且峰形狭窄,此时产物基本转变为立方晶系Y2O3,前驱物中未洗净的杂质离子也已彻底挥发,得到反应完全且高纯度的Y2O3颗粒.随着热分解温度的提高,衍射峰变得尖锐,衍射峰半高宽变小,说明随着热分解温度的提高,Y2O3晶粒尺寸增大,缺陷减少,当热分解温度为900 ℃时,衍射峰已变得非常尖锐,在该温度下晶粒已完成晶化且显著增大;从X衍射分析谱图知,热分解温度为500 ℃时,前驱体已分解为氧化钇,结合TG-DTG图知500 ℃或大于500 ℃都可作为热分解温度.
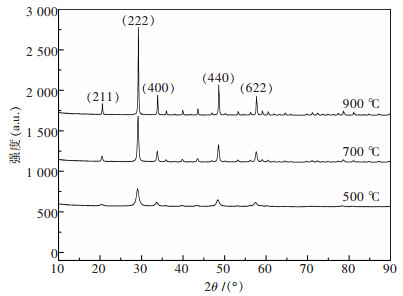 |
| 图 6 不同煅烧温度下样品的XRD图 |
3 结论
(1)在微波外场作用下,以YCl3为原料,草酸为沉淀剂直接液相合成,当H2C2O4与YCl3的摩尔比为2:1、YCl3起始浓度0.5 mol/L、反应时间3 h、反应温度40 ℃和陈化8 h的条件下,可得到砂状氧化钇前驱体,其D50约为40 μm;
(2)前驱物在500 ℃下热分解开始有Y2O3产生,且在900 ℃时,衍射峰已变得非常尖锐,晶粒已完成晶化.
| [1] | 李程文, 周康根, 姜科, 等. 晶种法处理含氟废水与氟化钙沉淀砂状化研究[J]. 环境科学与技术, 2011, 34(5): 157–160. |
| [2] | 吕鲜翠, 唐海红. 氧化铝质量的改善及其对铝电解的影响[J]. 中国有色冶金, 2006, 8(4): 14–17. |
| [3] | 褚丙武, 赵春芳. 铝电解用氧化铝微观结构的研究[J]. 电子显微学报, 2000, 19(4): 567–568. |
| [4] | 张春勇, 周全法, 单万建. 微波辅助法合成大颗粒银[J]. 稀有金属材料与工程, 2012, 41(s2): 76–78. |
| [5] |
Zeng Qing-yun, Chang Qing-qing, Ye Xin-yu. Effect of Microwave with Ultrasonic on the Morphology and Particle Size of (Y, Eu)2O3 Precursor[J].
Advanced Materials Research, 2012, 347-353: 3981–3984. |
| [6] |
Selyunina L A, Mishenina L N, Slizhov Yu G, et al. Effect of citric acid and ethylene glycol on the formation of calcium aluminate via the sol-gel method[J].
Russian Journal of Inorganic Chemistry, 2013, 58(4): 517–522. |
| [7] | 宋英方, 兰新哲, 周军, 等. 表面活性剂对纳米三氧化钼形貌的影响[J]. 稀有金属, 2010, 34(5): 781–783. |
| [8] | 李启厚, 高宇波, 刘志宏, 等. 喷雾热分解法合成BaTiO3超细粉末及其形貌控制[J]. 粉末冶金技术, 2010, 28(4): 292–294. |
| [9] |
XU Dong, SONG Qi, ZHANG Ke, et al. NiO-doped CaCu3Ti4O12 Thin Film by Sol-Gel Method[J].
Journal of Inorganic Materials, 2013, 28(11): 1–5. |
| [10] |
ZHAN Jing, ZHOU Di-fei, ZHANG Chuan-fu. Shape-controlled synthesis of novel precursor for fibrous Ni-Co alloy powders[J].
Transactions of Nonferrous Metals Society of China, 2011, 21(3): 544–551. DOI: 10.1016/S1003-6326(11)60749-8. |
| [11] | 胡艳宏.大颗粒稀土氧化物的制备工艺及流动性研究[D].内蒙古:内蒙古科技大学, 2006. http://cdmd.cnki.com.cn/Article/CDMD-10127-2007169727.htm |
| [12] | 马莹, 李莉娜, 王宝荣, 等. 草酸沉淀法制备大颗粒氧化钇工艺研究[J]. 稀有金属, 2010, 34(6): 950–953. |
| [13] | 王能利, 雷东, 张希艳, 等. 草酸共沉淀法制备Yb3+Y1.88La0.12O3纳米粉体及光谱性[J]. 无机化学学报, 2009, 25(8): 1408–1413. |
 2014, Vol. 5
2014, Vol. 5

