| 土壤重金属污染以及微生物修复技术探讨 |
重金属是指密度4.0 以上约60 种元素或密度在5.0 以上的45 种元素,主要包括铅(Pb)、镉(Cd)、汞(Hg)、铬(Cr)、钡(Ba)、铜(Cu)、银(Ag)、锌(Zn)、镍(Ni)等.砷(As)和硒(Se)虽非严格意义上的重金属,但因其某些性质及生态毒性与重金属相似,故通常列入重金属类进行研究讨论.
随着科技的迅猛发展,重金属在生活、生产中得到广泛应用.然而,对重金属产品的不当处理、处置,已经对人类的生产生活环境造成了严重的污染.而最引起人们关注和担忧的是其危害的隐蔽性、不可逆性和长期性[1].由于环境中的重金属不能被自然降解,因此土壤一旦被重金属污染,就很难彻底消除[2].重金属可以通过空气、水、土壤等途径进入动植物体,并经由食物链放大富集进入人体,损害人体健康[3],重金属在极低浓度下就能破坏人体正常的生理活动,危害程度极大,对生态环境以及人类生存构成了严重的威胁.为此,摸清土壤重金属污染的主要来源及其在土壤中的环境化学特征、转化迁移规律,探索并建立其相应的有效治理技术方法,具有重要的理论和现实意义.
1 重金属污染来源土壤重金属污染主要由采矿、冶炼、电镀、化工、电子、制革等工业产生的含重金属的废弃物进入土壤,以及污灌、农药、化肥、垃圾、粉煤灰和城市污泥的不合理施用引起.传统上可以分为工业来源、农业来源和城市生活来源.
(1)工业来源.工业生产中煤和石油等能源的燃烧所释放的大量含重金属的有害气体和粉尘等,以及其他工业生产环节,如采矿、选矿、矿物加工、冶炼等产生的富含重金属的废气、废水和废渣.
(2)农业来源.农业生产中的重金属污染主要来自农田污水灌溉,以及化肥和杀虫剂的滥用等.
(3)城市生活来源.主要来源于汽车尾气的排放及汽车轮胎磨损所产生的大量含重金属的有害气体和粉尘.
2 土壤重金属污染特征大多数重金属是过渡元素,由于其特有的电子层结构,使得重金属在土壤环境中的化学行为具有以下特点[4]:①重金属具有可变价态,在特定环境条件下,会发生氧化还原反应,重金属的活性和毒性随其价态变化而变化; ②重金属可以与土壤中的一些无机酸反应生成硫化物、碳酸盐、磷酸盐等,同时,也易于在土壤环境中发生水解反应生成氢氧化物.由于生成的化合物在土壤溶液中的溶解度较小,使得重金属在土壤中不易迁移,从而不断累积,造成更为严重的土壤环境问题;③重金属作为中心离子,能够接受多种阴离子,如H-、Cl-、F-等,并且能结合简单分子的独对电子,生成配位络合物,还可与一些大分子有机物,如蛋白质、腐殖质、多糖类等生成螯合物.若形成的络合物和螯合物是可溶性的,则可能渗入地下水或通过其他途径发生迁移,使其污染范围进一步扩大蔓延.
由于重金属具有以上环境化学特性,其在土壤中的行为极其多变.因此,直接导致重金属在土壤环境中的迁移难以准确预测,加大了土壤重金属污染防治的难度.
3 重金属在土壤环境中的行为特征 3.1 土壤中重金属的赋存形态重金属在土壤溶液中,主要以简单离子、有机或无机络离子的形态存在.
土壤中痕量重金属化学形态分布连续提取的方法种类繁多.但以Tessier 五步连续提取法最为经典,受到国内外众多研究学者推崇[5].Tessier 用连续提取法将土壤环境中重金属的赋存形态分为:可交换态、碳酸盐结合态、铁锰氧化物结合态、有机结合态和残渣态[6].尽管Tessier 法对土壤中重金属的形态进行了较详细的划分并在国内外广泛应用,但由于没有统一的分析标准和质量控制的标准物以及各形态间可能会发生窜相,仍存在分析结果可比性较差、数据无法验证对比、再现性不高等问题[7-12].因此,基于该法基础之上又提出了其他连续提取法.例如,BCR 法是1992 年由欧共体标准物质局( European Community Bureau of Reference) 提出的一种三级四步提取法[13],此法再现性显著好于Tessier 法[14].
近年来,大多数研究学者在分析土壤中重金属形态组分时,按浸提剂的不同将土壤环境中重金属的赋存形态分为:水溶态(以去离子水浸提)、交换态(如以MgCl2溶液为浸提剂)、铁锰氧化物结合态(如以NH2H-HCl 为浸提剂)、碳酸盐结合态(如以 NaAc-HAc 为浸提剂)、有机结合态(如以H2O2为浸提剂) 以及残渣态(如以HClO4-HF 消化、1∶1HCl 浸提).各赋存形态重金属的化学活性和生理毒性各异.其中,水溶态和交换态的化学活性和生理毒性最大,各种结合态次之,残渣态最小[15].
3.2 重金属元素在土壤中的迁移转化及其影响因素重金属在土壤中的动态与土壤种类、利用方式、结构以及氧化还原电位等物理化学条件有关,其迁移转化途径主要有[16]:①通过离子交换反应被土壤胶体吸附;②与土壤有机、无机配位体,如羧基、氨基、磷酸基等电子供体形成络合物或螯合物.例如二价重金属离子可与腐殖质发生络合反应,见图 1.也可与碳原子共价结合形成有机金属化合物; ③土壤中的重金属处于溶解与沉淀反应的动态平衡之中,土壤溶度积常数的大小、氧化还原电位Eh、土壤pH 等都会影响其溶解度;④重金属元素多属变价元素,其价态会在氧化还原反应中发生转变,其作用效应亦随之发生相应变化.
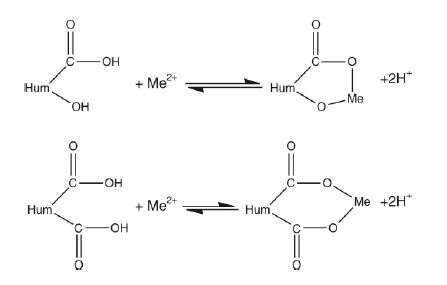 |
| 图 1 土壤二价重金属离子与腐殖质发生络合反应 |
影响重金属在土壤中迁移转化的因素主要包括:①土壤胶体对重金属的吸附作用;②重金属的配合作用;③土壤中重金属的沉淀和溶解作用;④土壤对重金属的氧化还原作用.
4 微生物修复技术 4.1 微生物的特点微生物与动植物相比,有以下5 个显著优点:①个体微小,比表面积大;②繁殖快,代谢能力强;③种类多,分布广;④适应性强;⑤容易培养.造就了其在自然界物质循环、污染土壤修复改良中的独特地位.
4.2 微生物修复重金属污染土壤的技术原理与方法微生物在修复被重金属污染的土壤方面具有独特的作用,其主要作用是降低土壤中重金属的毒性,吸附并累积重金属,以此来净化有毒金属污染或回收有经济价值的金属;与此同时,微生物还可以通过改变根际微环境,从而提高植物对重金属的吸收、挥发或固定率[17-18].
由于微生物修复技术应用成本低,对土壤肥力和代谢活性负面影响小,可以避免因污染物转移而对人类健康和环境产生影响[19],近年来在生态修复技术领域备受关注.利用微生物对土壤中的重金属进行修复是土壤重金属污染修复技术研究的新热点.
微生物主要是通过吸附作用、溶解作用、氧化还原作用以及菌根真菌作用对重金属污染土壤进行修复[20]:①吸附作用是指微生物通过带电荷的细胞表面物质吸附重金属离子,将重金属离子富集在细胞表面或内部.如茁芽短梗霉(Aureobasidium Pullulans)分泌胞外聚合物(EPS)可将Pb2+积累于细胞表面,且随着EPS 分泌增多,细胞表面的Pb2+水平提高4 倍左右[21].②溶解作用是指土壤微生物能够利用土壤中的有效营养和能源,在土壤滤沥过程中通过分泌有机酸络合并溶解土壤中的重金属.Siegel 等报道,真菌可以通过分泌有机酸、氨基酸以及其它代谢产物络合并溶解重金属及含重金属的矿物[22].③氧化还原作用是指微生物氧化还原作用能使某些重金属元素的价态发生转变,从而使其活性和毒性降低.例如,在含高浓度重金属的污泥中,加入适量的硫,部分微生物如嗜酸硫杆菌(Acidithiobacillus)即可把硫氧化成硫酸盐,降低污泥的pH,提高重金属的移动性;又如,绿铜假单胞菌(P.aeruginosa)、大肠埃希菌(E.coli)、变形杆菌(Proteus)等,可使无机或有机化合物中的二价汞离子还原为单质汞.这种转移方式可暂时或永久地将金属从生物接触的环境中清除出去[23].④菌根真菌作用是指菌根真菌能借助有机酸的分泌活化某些重金属离子,并通过离子交换、分泌有机配体等作用间接影响植物对重金属的吸收.Thompson 通过盆栽实验表明,在长期抛荒的土壤中接种VA(Vesicalar-Arbuscular)菌根,可以促进亚麻(Linum usitatissimum)对磷、锌的吸收[24].
4.3 微生物修复技术国内外研究及应用现状目前,利用微生物对重金属污染土壤进行修复的技术开始兴起且发展迅猛.在国内,王瑞兴等[19]对利用微生物矿化固结土壤中的重金属进行了研究,筛选到一种土壤菌-菌株A,并对其进行了深入分析,得到如下结果:①菌株A 在生长繁殖中产生的酶诱导底物分解产生CO32-,使得重金属离子以碳酸盐沉淀的形式矿化固结,从而降低了其溶解度,削弱了重金属在土壤中的迁移能力;②Ca2+与Cd2+共结晶实验显示,重金属离子被菌体细胞膜界面处带负电荷的水可溶有机质(SM)螯合,使菌体周围广域微量重金属离子转变为局部高含量体系,从而在菌体表面成核结晶,晶体按照Ca0.67Cd0.33CO3化学计量形式从液相中沉积,形成CaCO3和CdCO3的共结晶沉积物;同时菌株分泌出制约沉积晶体晶格生长的有机质,沉积晶体普遍为直径1~10 μm 的球形,与化学沉积过程存在显著差异; ③将适当底物添加到被重金属(Cd、 Cu、Pb、Zn 等)污染的土样中并接种菌株A,发现8 d后土壤中有效态的重金属明显减少,去除(固结)率可达50 %~70 %.因此,利用微生物矿化固结土壤中的重金属的技术不仅工艺简单,有较高的实用价值,而且,在建设环境友好型社会下,具有大面积推广使用的可能性.又如,曹德菊[25]利用常规微生物资源(枯草杆菌、酵母菌、大肠杆菌等),对重金属离子Cd2+、 Cu2+进行生物修复试验,其结果表明,在环境中Cu2+、 Cd2+浓度较低的情况下,微生物具有良好的修复性能,去除(固结)率可达25 %~60 %.
在国外,对含有重金属的土壤中土著(Indigenous)降解菌的筛选及其应用有较深入的研究.如L.L.Barton等[26]从受Cr (VI)、Zn2+和Pb2+污染的土壤中分离的菌种P.maltophilia 和Pseu domonas mesophilica,可将亚硒酸盐、硒酸盐和二价铅转化为结构稳定不具毒性的胶态铅和胶态硒.Kuhn[27]用海藻酸钠固定生枝动胶菌,用于含Cd 废液的处理,溶液中Cd2+的去除率可达95.95 %.Butter[28]用细菌作为生物吸附剂处理含 Cd 废水,实验效果较好,具有一定的可行性.
4.4 微生物修复技术的局限性微生物修复技术也具有一定的局限性.首先,微生物存在遗传稳定性差、易发生变异,一般不能将污染物全部去除等问题.其次,微生物对重金属的吸附和累积容量有限,而且须与土著菌株展开生存竞争,最终有可能因难以适应环境(竞争失利)而被淘汰.最后,由于利用微生物对重金属污染土壤进行修复受环境条件的影响显著,因此,为确保应用效果,除了筛选过程,应用前较为繁琐的培植、驯化过程也必不可少,这也在一定程度上制约了微生物修复技术的广泛应用.
5 结束语利用微生物对重金属污染土壤进行修复,具有修复成本低、无二次污染等特点,可在一定程度上带来经济效益和生态效益,是一种较理想的生物修复方法.但是,由于微生物易受环境条件的影响发生变异,再加之其吸附累积容量有限,使得该法在一定程度上受到限制.在这种形势下,应该更着力于技术方法的突破和创新,将其与其他生物修复技术(如植物修复技术)有效的结合起来,打破现行方法的局限性,实现对重金属污染土壤的有效治理.
| [1] | 陈兴兰, 杨成波. 土壤重金属污染 、生态效应及植物修复技术[J]. 农业环境与发展, 2010(3): 59. |
| [2] | 房存金. 土壤中主要重金属污染物的迁移转化及治理[J]. 当代化工, 2010, 39(4): 458. |
| [3] | 陈程, 陈明. 环境重金属污染的危害与修复[J]. 环境保护, 2010, 3(3): 55–56. |
| [4] | 刘春阳, 张宇峰, 腾洁. 土壤中重金属污染的研究进展[J]. 污染防治技术, 2006, 19(4): 42–43. |
| [5] | 陈学诚, 董文庚, 郎志敏, 等. 逐级提取程序应用于土福形态研究的可靠性[J]. 环境科学, 1991, 12(6): 25. |
| [6] |
A. Tessier, P. G. C. Campbell, M. Bisson. Sequential extraction proce- dure for the speciation of particulate trace metals[J].
Analytical Chemistry, 1979, 51(7): 844–850. DOI: 10.1021/ac50043a017. |
| [7] |
J. Usero, M. Gamero, J. Morillo, et al. Comparative study of three se- quential extraction procedures for metals in marine sediments[J].
En- viron Int, 1998, 24(4): 487–496. DOI: 10.1016/S0160-4120(98)00028-2. |
| [8] |
E. Margui, V. Salvado, I. Queralt, et al. Comparison of three-stage sequential extraction and toxicity characteristic leaching tests to e- valuate metal mobility in mining wastes[J].
Anal Chim Acta, 2004(524): 151–159. |
| [9] |
Z. Mester, C. Cremisini, E Ghiara, et al. Comparison of two sequential extraction procedures for metal fractionation in sediment samples[J].
Anal Chim Acta, 1998(359): 133–142. |
| [10] |
Simon W. Poulton, Donald E. Canfield. Development of a sequential extraction procedure for iron, implications for iron partitioning in continentally derived particulates[J].
Chem Geol, 2005, 214: 209–221. DOI: 10.1016/j.chemgeo.2004.09.003. |
| [11] |
Senol Kartal, Zeki Aydin, Serife Tokalioglu. Fractionation of metals in street sediment samples by using the BCR sequential extraction procedures and multivariate statistical elucidation of the data[J].
J Hazard Mater, 2006, 132(1): 80–89. DOI: 10.1016/j.jhazmat.2005.11.091. |
| [12] |
C. M. Davidson, P. C. S. Ferreira, Allen M. Ure. Some sources of vari- ability in application of the three-stage sequential extraction proce- dure recommended by BCR to industrially contaminated soil[J].
Fre- senius J Anal Chem, 1999(363): 446–451. |
| [13] |
Ph.Quevauviller, G. Rauret, B. Griepink. Single and sequential extraction in sediments and soils, Intern[J].
Envir on Anal Chem, 1993, 51: 231–235. DOI: 10.1080/03067319308027629. |
| [14] | 王亚平, 黄毅, 王苏明, 等. 土壤和沉积物中元素的化学形态及顺序提取法[J]. 地质通报, 2005, 24(8): 728–734. |
| [15] | 陶秀成. 环境化学[M]. 北京: 高等教育出版社 , 1999: 109-132. |
| [16] | 杨少之. 环境化学概论[M]. 黑龙江: 黑龙江科学技术出版社 , 1988: 359-360. |
| [17] | 李季, 许艇. 生态工程[M]. 北京: 化学工业出版社 , 2008: 173. |
| [18] | 赵开弘. 环境微生物学[M]. 武汉: 华中科技大学出版社 , 2009: 207. |
| [19] | 李宏, 江澜. 土壤重金属污染的微生物修复研究进展[J]. 贵州农业科学, 2009, 37(7): 72–74. |
| [20] | 王瑞兴, 钱春香, 吴淼, 等. 微生物矿化固结土壤中重金属研究[J]. 功能材料, 2007, 38(9): 15–26. |
| [21] |
J. H. Suh, J. W. Yun, D. S. Kim. Effect of extracellular polymeric substances (EPS) on Pb2+ accumulation by Aure-obasidium pullulans[J].
Bioproc Biosyst Eng, 1999(1): 1–4. |
| [22] | 阎晓明. 重金属污染土壤的微生物修复机理及研究进展[J]. 安徽农业科学, 2002, 30(6): 877–879. |
| [23] | 张景来. 环境生物技术及应用[M]. 北京 : 化学工业出版社 , 2002: 142-147. |
| [24] | 杨耀, 刘二东, 孙英. 土壤重金属污染生物修复技术的研究进展[J]. 内蒙古环境科学, 2009, 21(6): 189–190. |
| [25] | 曹德菊, 程培. 3 种微生物对 Cu Cd 生物吸附效应的研究[J]. 农业环境科学学报, 2004(23): 471–474. |
| [26] | David A. Sabatiji, Robert C. Knox. Transport and Remediation of Subsurface Contaminants[M]. Washington D. C.: American Chemical Society , 1992: 99-107. |
| [27] |
Sabine P. Kuhn, Robert M. Pfister. Adsorption of mixed metals and cadmium by calcium. alginate immobilized Zoogloea ramigera[J].
Applied Microbiology and Biotechnology, 1989, 31(5-6): 613–618. |
| [28] |
T. J. Butter, L. M. Evison, I. C. Hancock, et al. The removal and re- covery of cadmium from dilute aqueous solutions by biosorption and electrolysis at laboratory scale[J].
Water Res, 1998, 32(2): 400–406. DOI: 10.1016/S0043-1354(97)00273-X. |
 2012, Vol. 3
2012, Vol. 3

