| 稀土发光材料的水热法合成及其发光强度 |
近年来,人们已经能够采用高温固相法,溶胶-凝胶法和水热合成法等方法合成出大量的掺稀土离子的发光材料[1],氟化物基质材料掺杂稀土离子后的光功能特性引人瞩目[2], 但是水热法合成的掺铕CaF2系列的发光材料却几乎未见报道.本文用水热法合成出稀土发光材料并探究其发光特性.
1 水热合成法制备稀土发光材料 1.1 CaF2系列的合成首先,将分析纯的Ca(NO3)3·4H2O和NaF按比例分别溶于盛有30 mL的烧杯中,分别放在磁力搅拌器上搅拌30 min,然后将NaF水溶液逐滴滴加到Ca(NO3)3水溶液中,再放在磁力搅拌器上搅拌1 h,最后将混合溶液装于100 mL的水热罐中,将水热罐放在180 ℃下加热24 h,水热完的溶液在室温下自然冷却, 得到的白色沉淀物经离心分离后再用蒸馏水和乙醇按1:1混合的溶液洗涤数次后将洗涤物在80 ℃下干燥6 h得到粉末状样品[3].
类似地可以把SrF2和BaF2合成出来,所需材料如表 1所示.
| 表 1 合成10 mmol物质所需材料 |
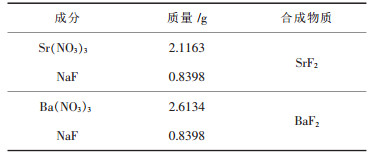 |
| 点击放大 |
对上述合成物质进行XRD检测,如图 1所示.
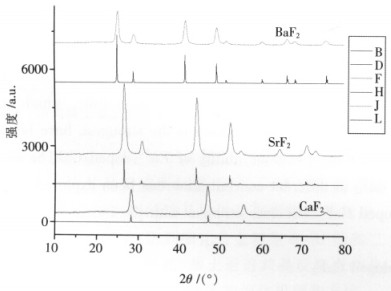 |
| 图 1 CaF2、SrF2和BaF2的XRD图 |
图 1中X轴代表 2θ,θ即衍射角度,Y轴代表衍射强度, 标注名称的为对应物质的标准谱.从图 1可以看出,合成出来的CaF2、SrF2和BaF2的衍射峰与标准谱相当吻合,说明已经准确合成出氟化物基质.
1.2 5 %掺铕CaF2系列的合成 1.2.1 5 %掺铕CaF2的合成下面合成CaF2掺铕的稀土发光材料[4].首先称取2.125 g的Ca(NO3)3·4H2O、0.8398 g的NaF、1.0507 g的柠檬酸.准备2个烧杯,一个盛装20 mL去离子水,另一个盛装30 mL去离子水,将称好的NaF和柠檬酸放入装有20 mL去离子水烧杯中,将Ca(NO3)3·4H2O放入装有30 mL去离子水中,分别将两烧杯放在磁力搅拌器上搅拌30 min,放有NaF的烧杯中可边加入10 mL的0.05 mol/L的Eu(NO3)3·6H2O,为了让生成的纳米颗粒尽可能小,可以将装有NaF的混合液逐滴滴加到装有Ca(NO3)3·4H2O的烧杯中(注意:此时装有Ca(NO3)3·4H2O的烧杯仍在不断搅拌), 滴加完毕后让它继续搅拌1 h,再装入水热罐中,并放在180 ℃的环境下水热24 h,水热完的溶液在室温下自然冷却, 得到的白色沉淀物经离心分离后再用蒸馏水和乙醇按1:1混合的溶液洗涤数次后将洗涤物在80 ℃下干燥6 h得到粉末状样品.测试其XRD如图 2所示.
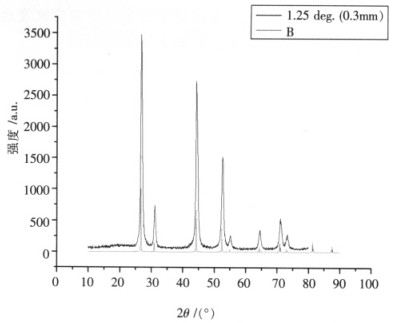 |
| 图 2 Eu:CaF2的XRD |
图 2中黑色曲线B为标准谱, 由图 2可知,合成出来的Eu:CaF2的衍射峰与标准谱也相当吻合.且小角度的衍射峰强度很大而大角度的衍射峰强度很小.各衍射峰衍射强度明显低于标准物的衍射强度.
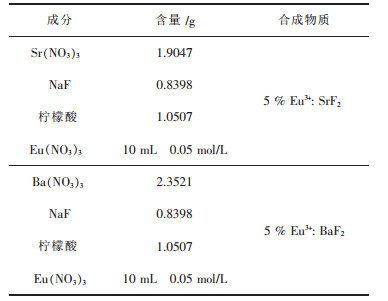
1.2.2 5 %掺铕SrF2和BaF2的合成类似地,合成10 mmol的5 %掺铕SrF2和BaF2所需材料如表 2.
| 表 2 合成10 mmol物质所需材料 |
 |
| 点击放大 |
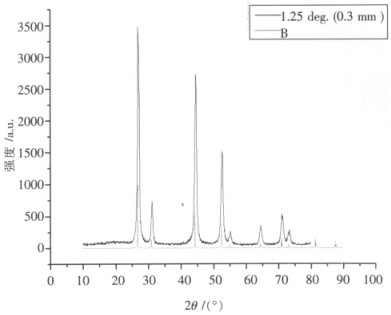 |
| 图 3 Eu:SrF2的XRD |
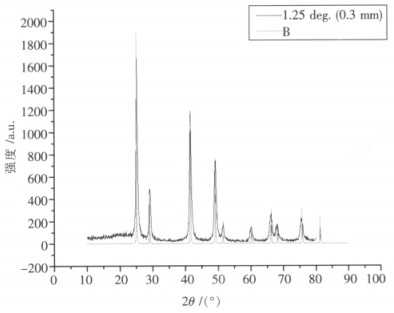 |
| 图 4 Eu:BaF2的XRD |
从图 3、图 4可以看出,合成出来的物质也与标准物吻合,且低角度衍射峰强高角度衍射峰弱.但明显各衍射峰的衍射强度不如标准物的衍射强度.
2 发光性能 2.1 同浓度掺杂CaF2系列的发光强度掺铕CaF2、SrF2和BaF2合成以后, 下面测试同浓度的3种稀土发光材料的发光强度[5-6],如图 5所示.
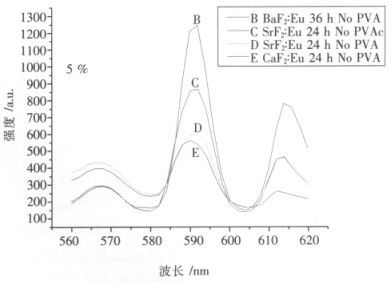 |
| 图 5 掺铕5% CaF2、SrF2和BaF2发光强度对比图 |
图 5中X轴代表波长,Y轴代表发光强度.从图 5可看出,同浓度的掺铕CaF2、SrF2和BaF2中, 掺铕CaF2的发光强度最大.
2.2 不同浓度CaF2发光强度对比下面以掺铕CaF2为例探讨稀土离子在什么浓度时其发光性能最强.类似于前面制备5 %掺铕CaF2的步骤方法,依次制备1 %、10 %、18 %和25 %的掺铕CaF2,并测试它们的发光强度,如图 6所示.
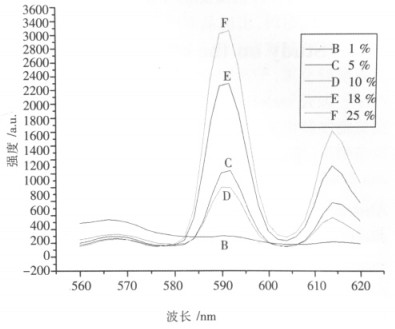 |
| 图 6 不同浓度的Eu:CaF2发光强度对比 |
由图 6可以看出,除了1 %的发光强度有点特别之外,随着掺杂的稀土离子浓度的增加,稀土发光材料的发光性能依次增强.为此,又做了30 %和40 %的掺铕CaF2的制备实验,并测试其发光强度与前面的进行对比,如图 7.
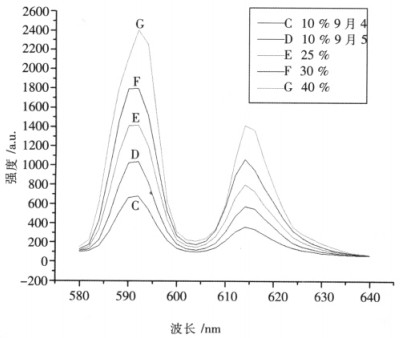 |
| 图 7 不同浓度的Eu:CaF2发光强度对比图 |
从图 7进一步说明了随着掺杂稀土离子浓度的增加,发光强度增加.
3 结论水热合成法作为一种典型的液相方法在制备具有各种可控形貌和结构的无机材料时被证明是有效和简便的[7-8],采用水热合成法成功制备出掺铕CaF2及其系列,实验发现同浓度稀土离子掺杂的CaF2、SrF2和BaF2,掺铕CaF2的发光强度最大.对于掺铕CaF2、SrF2和BaF2的XRD, 都有小角度衍射峰强,大角度衍射峰弱的特点.对不同浓度的掺铕CaF2的发光强度,随掺杂稀土离子浓度的增加,其发光强度增大.
| [1] |
徐学基. 稀土发光材料及其应用的发展[J].
材料导报, 2003, 20(12): 7–10.
|
| [2] |
闫景辉, 李中田, 郭海艳, 等. BaYF5 :Ce3+纳米粒子的制备与光谱性质[J].
应用化学, 2008, 25(2): 254–256.
|
| [3] |
李云鹏, 孙勇, 韦春才, 等.
超微粒子制造与应用技术[M]. 北京: 学苑出版社, 1989: 67-77.
|
| [4] |
LIU Bo, CHEN Yong-hu, SHI Chao-shu, et al. Visible quantum cutting in BaF2 : Gd, eu via downconversion[J].
Journal of Luminescene, 2003, 101: 155–159. DOI: 10.1016/S0022-2313(02)00408-8. |
| [5] |
陈荣, 吴根华, 张启运. 含Ce3+, Tb3+简单氟化物磷光体的荧光特性[J].
光谱学与光谱分析, 1999(1): 104–105.
|
| [6] |
钟盛文, 晏婷婷, 张骞. TiO2增亮氧化铈云母珠光颜料的研究[J].
江西理工大学学报, 2010, 31(1): 26–31.
|
| [7] |
朱国贤, 闫景辉, 莫凤珊, 等. 稀土掺杂氟化镁钾纳米晶的合成及其光谱特性[J].
高等学校化学学报, 2006, 27(3): 401–405.
|
| [8] |
林君, 李春霞. 稀土氟化物纳/微米材料的水热合成、形成机理和发光性质[J].
发光学报, 2011, 32(6): 519–534.
|
 2011, Vol. 2
2011, Vol. 2

